人教版初中化学九年级下册第九单元 溶液 单元测试卷
试卷更新日期:2022-02-07 类型:单元试卷
一、单选题
-
1. 下列物质放入水中能形成溶液的是( )A、蔗糖 B、豆油 C、面粉 D、泥沙2. 下列说法正确的是( )A、水和冰块的共存物是悬浊液 B、凡均一、稳定、透明、澄清的液体一定是溶液 C、溶液都是混合物 D、在泥水里,泥是溶质,水是溶剂3. 向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )
 A、氢氧化钠 B、氯化钠 C、硝酸铵 D、浓硫酸4. 下列洗涤方法中利用了乳化原理的是( )A、用洗洁精洗去餐具上的油污 B、用汽油洗去手上的油污 C、用酒精洗去试管中的碘 D、用稀盐酸清洗装过澄清石灰水的试剂瓶5. 下列关于“10%的硝酸钾溶液”含义的说法中,错误的是( )A、100 g水中溶解了10 g硝酸钾 B、100 g硝酸钾溶液中有10 g硝酸钾 C、将10 g硝酸钾溶于90 g水中所得的溶液 D、将硝酸钾与水按1∶9的质量比配制的溶液6. 甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
A、氢氧化钠 B、氯化钠 C、硝酸铵 D、浓硫酸4. 下列洗涤方法中利用了乳化原理的是( )A、用洗洁精洗去餐具上的油污 B、用汽油洗去手上的油污 C、用酒精洗去试管中的碘 D、用稀盐酸清洗装过澄清石灰水的试剂瓶5. 下列关于“10%的硝酸钾溶液”含义的说法中,错误的是( )A、100 g水中溶解了10 g硝酸钾 B、100 g硝酸钾溶液中有10 g硝酸钾 C、将10 g硝酸钾溶于90 g水中所得的溶液 D、将硝酸钾与水按1∶9的质量比配制的溶液6. 甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )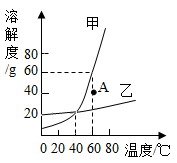 A、甲、乙物质都适用降温结晶法使溶质从溶液中析出 B、60℃时将40g甲物质加入50g水中能得到90g饱和溶液 C、通过降温能使A点甲的不饱和溶液变为饱和溶液 D、分别将甲、乙物质饱和溶液从60℃降至20℃,甲析出晶体较多7. 下列有关氯化钠溶液的说法错误的是( )A、氯化钠溶液是由钠离子、氯离子和水分子组成的各部分组成完全相同的混合物 B、只要水分不蒸发,外界条件不改变,氯化钠就不会从溶液中分离出来 C、氯化钠溶于水,温度不发生改变的原因是溶解过程中没有热量转化 D、一定量的饱和氯化钠溶液,可继续溶解少量的硝酸钾固体8. 20℃时,在各盛有100克水的烧杯中,分别加入10克甲、乙、丙三种纯净物(不含结晶水,不与水反应),充分溶解后,结果如图。下列说法正确的是( )
A、甲、乙物质都适用降温结晶法使溶质从溶液中析出 B、60℃时将40g甲物质加入50g水中能得到90g饱和溶液 C、通过降温能使A点甲的不饱和溶液变为饱和溶液 D、分别将甲、乙物质饱和溶液从60℃降至20℃,甲析出晶体较多7. 下列有关氯化钠溶液的说法错误的是( )A、氯化钠溶液是由钠离子、氯离子和水分子组成的各部分组成完全相同的混合物 B、只要水分不蒸发,外界条件不改变,氯化钠就不会从溶液中分离出来 C、氯化钠溶于水,温度不发生改变的原因是溶解过程中没有热量转化 D、一定量的饱和氯化钠溶液,可继续溶解少量的硝酸钾固体8. 20℃时,在各盛有100克水的烧杯中,分别加入10克甲、乙、丙三种纯净物(不含结晶水,不与水反应),充分溶解后,结果如图。下列说法正确的是( ) A、所得溶液可能都是饱和溶液 B、20℃时,乙溶液的溶质质量最小 C、溶液溶质的质量分数:甲>丙>乙 D、升高温度,溶液溶质的质量分数一定变大9. 在20℃时,小刘同学向100g水中依次加入NaCl固体,充分溶解。实验过程如图所示,下列说法错误的是( )
A、所得溶液可能都是饱和溶液 B、20℃时,乙溶液的溶质质量最小 C、溶液溶质的质量分数:甲>丙>乙 D、升高温度,溶液溶质的质量分数一定变大9. 在20℃时,小刘同学向100g水中依次加入NaCl固体,充分溶解。实验过程如图所示,下列说法错误的是( ) A、20℃时,100g水最多溶解NaCl的质量为36g B、图③中的溶液是饱和溶液 C、图③中溶液的溶质质量为40g D、图③和图④中NaCl溶液的溶质质量分数相等
A、20℃时,100g水最多溶解NaCl的质量为36g B、图③中的溶液是饱和溶液 C、图③中溶液的溶质质量为40g D、图③和图④中NaCl溶液的溶质质量分数相等二、综合题
-
10. 请回答下列问题。(1)、各种洗涤剂广泛进入人们的生活中,下列洗涤所用物质不具有乳化功能的是 。A、用汽油除去衣服上的油污 B、用餐具洗洁精洗餐具上的油污 C、用洗衣液洗衣服 D、用洗发液洗头发(2)、向水中加入后振荡,可以根据产生泡沫多少来鉴别硬水和软水。(3)、硬水对生活的危害很大,生活中经常通过降低水的硬度。11. 水乃生命之源,万物之本,在生产生活中起着重要的作用。(1)、天然水中含有许多杂质,可利用沉降、过滤、吸附和蒸馏等方法进行净化。
①上述净化方法中单一净化程度最高的是。
②活性炭能吸附水中的异味和色素,这属于活性炭的(填“物理”或“化学”) 性质。
③过滤时所需的玻璃仪器有漏斗、烧杯和。
(2)、在盛有水的烧杯中加入一定量的硝酸铵,在形成溶液的过程中,温度会(填“升高”、“降低”或“不变”)。(3)、做铁丝在氧气中燃烧的实验时,在集气瓶底预先放少量水的作用是。(4)、海水淡化可缓解淡水资源匮乏的问题。如图为太阳能海水淡化装置示意图。利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的质量分数(填“变大”、“变小”或“不变”)。 (5)、二氧化氯 (ClO2)是一种消毒剂,能对饮用水消毒,可以有效杀灭病毒。将 Cl2通入 NaClO2溶 液 中可制得 ClO2和 一种 生 活 中常 见 的盐,反 应 的化 学方程式 为 ,其中X的化学式为。12. 根据表中氯化钠和硝酸钾部分溶解度数据分析,回答下列问题。
(5)、二氧化氯 (ClO2)是一种消毒剂,能对饮用水消毒,可以有效杀灭病毒。将 Cl2通入 NaClO2溶 液 中可制得 ClO2和 一种 生 活 中常 见 的盐,反 应 的化 学方程式 为 ,其中X的化学式为。12. 根据表中氯化钠和硝酸钾部分溶解度数据分析,回答下列问题。温度/℃
0
10
20
30
40
50
60
溶解度/g
NaCl
35.7
35.8
36.0
36.3
36.6
37.0
37.3
KNO3
13.3
20.9
31.6
45.8
63.9
85.5
110
(1)、20℃时,氯化钠的溶解度是g。(2)、硝酸钾的溶解度随温度的升高而 , 与硝酸钾相比较,氯化钠的溶解度受温度变化影响(填“较大”或“较小”)。(3)、20℃时,在100g水中加入40g硝酸钾,充分搅拌后,将溶液温度升高到30℃(不考虑水分蒸发),所得溶液是(填“饱和溶液”或“不饱和溶液”)。(4)、海水晒盐利用的结晶方法是 , 氯化钠适用这一方法结晶是因为。13. 如图所示,广口瓶中盛有少量饱和澄清石灰水,小试管和U形管中均有适量水,现向小试管中注入适量氢氧化钠。
请回答:
(1)、可观察到饱和澄清石灰水。(2)、U形管中a、b液面变化情况是______(选填序号)。A、a液面上升,b液面下降 B、a液面下降,b液面上升14. 如图是甲、乙两种物质的溶解度曲线,请回答下列问题。 (1)、 ℃时,甲、乙两种物质的溶解度相等。(2)、将乙的饱和溶液变成不饱和溶液的方法是。(任写一种)(3)、t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,有晶体析出的是 , 此时甲溶液的溶质质量分数(填“大于”、“等于”或“小于”)乙溶液的溶质质量分数。(4)、小明同学用甲物质进行以下实验:
(1)、 ℃时,甲、乙两种物质的溶解度相等。(2)、将乙的饱和溶液变成不饱和溶液的方法是。(任写一种)(3)、t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,有晶体析出的是 , 此时甲溶液的溶质质量分数(填“大于”、“等于”或“小于”)乙溶液的溶质质量分数。(4)、小明同学用甲物质进行以下实验:
①实验过程中,所得溶液溶质质量分数相同的是 (填字母序号)。
②向B中溶液再加入60g甲固体的过程中,发现先固体全部溶解,一段时间后又有部分固体析出。你认为“全部溶解”的原因是。
15. 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答: (1)、25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为g。(2)、要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是。(3)、现有操作步骤:a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是。(填字母序号)(4)、将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数(填“变大”“变小”或“不变”)16. 青海省柴达木盆地的察尔汗盐湖是我国最大的天然内陆成水湖,当地农民通过“冬天捞碱,夏天晒盐”获得大量湖盐。
(1)、25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为g。(2)、要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是。(3)、现有操作步骤:a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是。(填字母序号)(4)、将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数(填“变大”“变小”或“不变”)16. 青海省柴达木盆地的察尔汗盐湖是我国最大的天然内陆成水湖,当地农民通过“冬天捞碱,夏天晒盐”获得大量湖盐。 (1)、“夏天晒盐”中的“盐”溶解度曲线可用如图中来表示。(2)、t1℃时,三种物质的溶解度由小到大关系是。(3)、t2℃时将40g的a放入50g水中充分搅拌,所得溶液质量是。(4)、不改变溶液浓度,将a的不饱和溶液转化为饱和溶液的方法是。(5)、将t2℃时a、b的饱和溶液降温至t1℃时,比较析出溶质的质量大小关系___________。A、a=b B、a>b C、a<b D、无法确定17. 化学实验中经常用到一定溶质质量分数的溶液。请回答:(1)、实验室配制质量分数6的氯化钠溶液50g,准备了下列实验用品。
(1)、“夏天晒盐”中的“盐”溶解度曲线可用如图中来表示。(2)、t1℃时,三种物质的溶解度由小到大关系是。(3)、t2℃时将40g的a放入50g水中充分搅拌,所得溶液质量是。(4)、不改变溶液浓度,将a的不饱和溶液转化为饱和溶液的方法是。(5)、将t2℃时a、b的饱和溶液降温至t1℃时,比较析出溶质的质量大小关系___________。A、a=b B、a>b C、a<b D、无法确定17. 化学实验中经常用到一定溶质质量分数的溶液。请回答:(1)、实验室配制质量分数6的氯化钠溶液50g,准备了下列实验用品。
①配制时,涉及以下实验步骤:A.称量及量取 B.计算 C.溶解 D.装瓶贴标签。
其正确的实验步骤顺序是(填字母)。
②配制过程还缺少的一种玻璃仪器是(填名称)。
③下列各图是某同学量取蒸馏水体积的观察方式,若用图B的观察方式量取蒸馏水的体积,所配制溶液的溶质质量分数会(填“偏大”、“偏小”或“无影响”)。
 (2)、若用质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制200g质量分数为3%的氯化钠溶液。需要6%的氯化钠溶液的体积为mL(计算结果保留至0.1)。
(2)、若用质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制200g质量分数为3%的氯化钠溶液。需要6%的氯化钠溶液的体积为mL(计算结果保留至0.1)。三、计算题
-
18. 制作“叶脉书签”需要100g溶质质量分数为10%的氢氧化钠溶液.请问:(1)、配制时需要氢氧化钠固体的质量是。(2)、若用的20%氢氧化钠溶液和水配制,需要的20%氢氧化钠溶液质量多少克?