人教版初中化学九年级下册第九单元 课题3 溶液的浓度
试卷更新日期:2022-02-07 类型:同步测试
一、单选题
-
1. 对于30%的KNO3溶液,下列说法正确的是( )A、溶液中溶质和溶剂的质量比为3:10 B、每100g水中溶解30gKNO3 C、某种条件下,可转化为悬浊液 D、若再加30g硝酸钾,则变为60%KNO3溶液2. a、b、c三种固体物质的溶解度曲线如图所示。下列说法正确的是( )
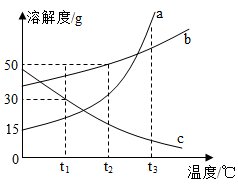 A、t1℃时,a物质的溶解度是30g B、t2℃时,b的饱和溶液中溶质的质量分数为50% C、t3℃时,各取15ga、b、c三种物质分别加入到50g水中充分溶解,能得到饱和溶液的是c D、t3℃时:a、b、c三种物质的饱和溶液均降温到t1℃,三种物质溶质质量分数大小关系为b>c>a3. 室温时,对100mL氯化钠饱和溶液作如下操作,最终甲、乙两烧杯中溶液( )
A、t1℃时,a物质的溶解度是30g B、t2℃时,b的饱和溶液中溶质的质量分数为50% C、t3℃时,各取15ga、b、c三种物质分别加入到50g水中充分溶解,能得到饱和溶液的是c D、t3℃时:a、b、c三种物质的饱和溶液均降温到t1℃,三种物质溶质质量分数大小关系为b>c>a3. 室温时,对100mL氯化钠饱和溶液作如下操作,最终甲、乙两烧杯中溶液( )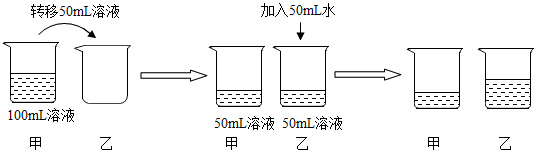 A、溶质质量相同 B、溶质质量分数相同 C、均为不饱和溶液 D、溶剂质量相同4. 下列说法错误的是( )A、用50 g溶质质量分数为10%的NaCl溶液配制溶质质量分数为5%的NaCl溶液需要加水20 g B、100 mL水和100 mL酒精混合后体积小于200 mL,说明分子间有间隔 C、饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液 D、汽油作溶剂可以去除衣物上的油污5. 温度不变,对100mL氯化钠饱和溶液进行如下实验(如图所示):实验一,将烧杯甲中溶液转移出50mL到乙烧杯中,实验二,是把5g水和5g氯化钠分别加入在甲、乙烧杯中、则下列结论错误的是( )
A、溶质质量相同 B、溶质质量分数相同 C、均为不饱和溶液 D、溶剂质量相同4. 下列说法错误的是( )A、用50 g溶质质量分数为10%的NaCl溶液配制溶质质量分数为5%的NaCl溶液需要加水20 g B、100 mL水和100 mL酒精混合后体积小于200 mL,说明分子间有间隔 C、饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液 D、汽油作溶剂可以去除衣物上的油污5. 温度不变,对100mL氯化钠饱和溶液进行如下实验(如图所示):实验一,将烧杯甲中溶液转移出50mL到乙烧杯中,实验二,是把5g水和5g氯化钠分别加入在甲、乙烧杯中、则下列结论错误的是( )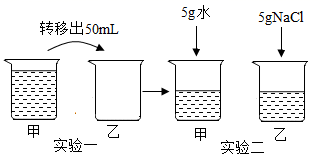 A、实验二后,甲中溶液的溶质质量分数减小 B、实验一后,甲和乙中溶液的溶质质量分数相等 C、实验二后,乙中溶液的溶质质量分数增大 D、实验二后,甲和乙中溶液所含溶质质量相等6. 下列关于a、b数值的比较中,a一定大于b的是( )A、不饱和溶液中溶质质量分数为a%,饱和溶液中溶质的质量分数为b% B、某温度硝酸钾的饱和溶液,溶质质量分数为a%,向该饱和溶液中加入少量氯化钠且完全溶解后的溶液中硝酸钾的的质量分数为b% C、同一饱和溶液中,溶质质量为ag,溶剂为bg D、某物质的溶解度在低温时为ag,高温时为bg
A、实验二后,甲中溶液的溶质质量分数减小 B、实验一后,甲和乙中溶液的溶质质量分数相等 C、实验二后,乙中溶液的溶质质量分数增大 D、实验二后,甲和乙中溶液所含溶质质量相等6. 下列关于a、b数值的比较中,a一定大于b的是( )A、不饱和溶液中溶质质量分数为a%,饱和溶液中溶质的质量分数为b% B、某温度硝酸钾的饱和溶液,溶质质量分数为a%,向该饱和溶液中加入少量氯化钠且完全溶解后的溶液中硝酸钾的的质量分数为b% C、同一饱和溶液中,溶质质量为ag,溶剂为bg D、某物质的溶解度在低温时为ag,高温时为bg二、综合题
-
7. 下列是MgSO4和KCl的溶解度表及溶解度曲线。
温度/℃
20
30
40
50
60
70
80
90
溶解度/g
MgSO4
33.7
38.9
44.5
50.6
54.6
55.8
52.9
52.2
KCl
34.0
37.0
40.0
42.6
45.5
48.3
51.1
54.0
请分析后回答下列问题:
 (1)、代表KCl溶解度曲线的是(填“甲”或“乙”)。(2)、t3℃时,等质量的两种物质饱和溶液,均降温到t1℃,析出晶体质量关系甲乙(填“>”“<”或“无法确定”).(3)、t2℃的范围为____(填字母)。A、30-40 B、40-50 C、70-80 D、80-90(4)、t3℃时MgSO4的饱和溶液降温到t1℃,溶液中溶质的质量分数的变化情况是____(填字母)。A、始终不变 B、先增大后减小 C、先减小后增大 D、先不变后减小 E、先不变后增大8. 甲、乙两种固体物质的溶解度曲线如下图所示。
(1)、代表KCl溶解度曲线的是(填“甲”或“乙”)。(2)、t3℃时,等质量的两种物质饱和溶液,均降温到t1℃,析出晶体质量关系甲乙(填“>”“<”或“无法确定”).(3)、t2℃的范围为____(填字母)。A、30-40 B、40-50 C、70-80 D、80-90(4)、t3℃时MgSO4的饱和溶液降温到t1℃,溶液中溶质的质量分数的变化情况是____(填字母)。A、始终不变 B、先增大后减小 C、先减小后增大 D、先不变后减小 E、先不变后增大8. 甲、乙两种固体物质的溶解度曲线如下图所示。 (1)、t1℃时,甲、乙饱和溶液中溶质的质量分数:甲乙(填“>”“<”或“=”)。(2)、t2℃时,将60g乙物质放入100g水中,所得溶液中,溶质与溶剂的质量比为(填最简整数比)。(3)、现有t2℃时,甲、乙两种物质的饱和溶液各100,将这两种溶液分别降温到t1℃,所得溶液中溶质的质量分数甲乙(填“>”、“<”或“=”)。(4)、小明同学进行了如下图所示的实验:
(1)、t1℃时,甲、乙饱和溶液中溶质的质量分数:甲乙(填“>”“<”或“=”)。(2)、t2℃时,将60g乙物质放入100g水中,所得溶液中,溶质与溶剂的质量比为(填最简整数比)。(3)、现有t2℃时,甲、乙两种物质的饱和溶液各100,将这两种溶液分别降温到t1℃,所得溶液中溶质的质量分数甲乙(填“>”、“<”或“=”)。(4)、小明同学进行了如下图所示的实验:
上述实验过程中所得的溶液,属于不饱和溶液的是(填序号),溶液中溶质的质量分数相同的是(填序号)。
(5)、喝了汽水以后,常常会打嗝。这说明随温度升高气体的溶解度。9. 下面是某同学配制100g质量分数为15%的氯化钠溶液的主要过程。配制上述溶液的主要步骤有:计算、称量、量取、溶解。
(1)、计算:氯化钠固体的质量是g。(2)、本实验是定量实验,选择仪器不恰当或操作不规范都会导致实验结果有不正确。实验时选择量筒规格应为(填“50mL”或“100mL”)。在量取水时俯视量筒读数(其它操作均正确),所得溶液的质量分数15%(填“大于”、“等于”或“小于”),实验过程中玻璃棒的作用是。(3)、若用20%的NaCl溶液100g稀释成质量分数为10%的NaCl溶液,需加水mL。10. 在一定温度下,向100g水中依次加入一定质量的KCl固体,充分溶解,加入KCl固体的质量与所得溶液质量的关系如图所示: (1)、该温度下,实验①所得溶液是溶液(填“饱和”或“不饱和”)。(2)、该温度下,KCl的溶解度为。(3)、实验③所得溶液中溶质的质量分数约是(填选项序号)。A、40% B、37.5% C、28.6%(4)、现有溶质质量分数为10%的KCl的溶液200g,若配制成溶质质量分数为4%的KCl的溶液,问需要加水的质量是g。
(1)、该温度下,实验①所得溶液是溶液(填“饱和”或“不饱和”)。(2)、该温度下,KCl的溶解度为。(3)、实验③所得溶液中溶质的质量分数约是(填选项序号)。A、40% B、37.5% C、28.6%(4)、现有溶质质量分数为10%的KCl的溶液200g,若配制成溶质质量分数为4%的KCl的溶液,问需要加水的质量是g。三、计算题
-
11. 20℃时,将200g10%的氢氧化钠溶液变为20%的氢氧化钠溶液,(1)、若蒸发,需要蒸发掉多少克水?(2)、若加溶质,需要加入多少克氢氧化钠?(请写出计算步骤)12. 现有225克20%的硝酸钠溶液,若在此溶液中;(1)、加入75克硝酸钠晶体完全溶解后,溶液中溶质的质量分数为。(2)、加入5克硝酸钠晶体和170克水后,溶液中溶质的质量分数为。(3)、加入45克硝酸钠晶体再蒸发45克水后(无晶体析出),溶液中溶质的质量分数为。(4)、加入50克20%的硝酸钠溶液后,溶液中溶质的质量分数为。13. 向80g15%的NaNO3溶液中加入28gNaNO3固体后,发现有8 gNaNO3未溶解,则形成的溶液中溶质的质量分数是多少?(写解题过程)14. 某市售过氧乙酸(化学式:C2H4O3),其标签上的部分文字说明如图。请回答:
 (1)、一瓶这种溶液中含过氧乙酸溶质质量为。(2)、0.5%的过氧乙酸溶液可以杀死细菌和新冠病毒。某医院需配制0.5%的过氧乙酸2kg,需要这种过氧乙酸的质量为多少?(请写出计算过程)15. 某浓盐酸瓶上的标签如表所示,则:
(1)、一瓶这种溶液中含过氧乙酸溶质质量为。(2)、0.5%的过氧乙酸溶液可以杀死细菌和新冠病毒。某医院需配制0.5%的过氧乙酸2kg,需要这种过氧乙酸的质量为多少?(请写出计算过程)15. 某浓盐酸瓶上的标签如表所示,则:浓盐酸(HCl)500mL
浓度(质量分数)
36%
密度
1.2g/cm3
(1)、该瓶浓盐酸的质量为克。(2)、取100mL 该浓盐酸与500 mL水均匀混合,所得稀盐酸的质量分数是多少?(结果精确到0.01%)(3)、欲配制100g质量分数为3.6%的稀盐酸,需该浓盐酸质量为多少克?