河南省周口市鹿邑县2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-01-26 类型:期末考试
一、单选题
-
1. 下列诗句中不涉及化学变化的是( )A、千锤万凿出深山 B、化作春泥更护花 C、蜡炬成灰泪始干 D、爆竹声中一岁除2. 下列物质中,硬度最大的是()
A、金刚石 B、石墨 C、焦炭 D、活性炭3. 下列各种“水”中属于纯净物的是( )A、矿泉水 B、自来水 C、湖泊水 D、蒸馏水4. 下列粒子结构示意图中,表示阴离子的是( )A、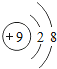 B、
B、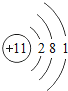 C、
C、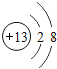 D、
D、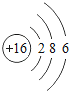 5. 金属不具有的物理通性是( )A、银白色 B、延展性 C、导电性 D、导热性6. 煤燃烧时会放出刺激性气味这是因为煤中含____元素。( )A、碳 B、氢 C、硅 D、硫7. 下列有关实验室制取二氧化碳气体的操作图示正确的是( )A、导管连接
5. 金属不具有的物理通性是( )A、银白色 B、延展性 C、导电性 D、导热性6. 煤燃烧时会放出刺激性气味这是因为煤中含____元素。( )A、碳 B、氢 C、硅 D、硫7. 下列有关实验室制取二氧化碳气体的操作图示正确的是( )A、导管连接 B、胶塞塞紧
B、胶塞塞紧  C、气体验满
C、气体验满 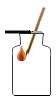 D、气体收集
D、气体收集  8. 下列有关金属及合金的说法错误的是( )A、金属在常温下大多数都是固体 B、铝合金的硬度比铝的硬度小 C、铁制品在潮湿的空气中易生锈 D、钢铁是使用最多的金属材料9. 下列事实的微观解释中,错误的是( )A、墙里开花墙外香——分子在不断的运动 B、干冰升华——分子间间隔增大 C、1滴水中大约有1.67×1021个水分子——分子很小 D、蔗糖放入水中溶解——蔗糖分子分解了10. 为强化安全意识,提升安全素养,某校举行了消防安全知识竞赛。下列做法正确的是( )A、室内起火,打开所有门窗通风 B、电器在使用时着火,立即用水灭火 C、炒菜时油锅着火,立即盖上锅盖 D、高楼住宅发生火灾时,立即乘坐电梯逃生11. 我国北斗卫星导航系统应用了铷原子钟。如图是铷在元素周期表中的信息。下列有关铷的说法正确的是( )
8. 下列有关金属及合金的说法错误的是( )A、金属在常温下大多数都是固体 B、铝合金的硬度比铝的硬度小 C、铁制品在潮湿的空气中易生锈 D、钢铁是使用最多的金属材料9. 下列事实的微观解释中,错误的是( )A、墙里开花墙外香——分子在不断的运动 B、干冰升华——分子间间隔增大 C、1滴水中大约有1.67×1021个水分子——分子很小 D、蔗糖放入水中溶解——蔗糖分子分解了10. 为强化安全意识,提升安全素养,某校举行了消防安全知识竞赛。下列做法正确的是( )A、室内起火,打开所有门窗通风 B、电器在使用时着火,立即用水灭火 C、炒菜时油锅着火,立即盖上锅盖 D、高楼住宅发生火灾时,立即乘坐电梯逃生11. 我国北斗卫星导航系统应用了铷原子钟。如图是铷在元素周期表中的信息。下列有关铷的说法正确的是( ) A、属于非金属元素 B、原子的质量是85.47g C、元素符号为Rb D、原子核内有37个中子12. 火药是我国古代四大发明之一,《天工开物》记载:“凡硫黄配硝而后,火药成声”。其反应的化学方程式为: 。则X的化学式为( )A、O2 B、SO2 C、NO2 D、N213. 中药当归、白芷中富含的紫花前胡醇(化学式为C14H14O4),能增强人体免疫力。下列关于紫花前胡醇叙述错误的是( )A、是一种化合物 B、由三种元素组成 C、在空气中燃烧可能生成CO2 D、C,H,O元素质量比为7:7:214. 已知镁和铝的相对原子质量之比为8:9,若镁和铝分别与足量盐酸反应,生成氢气的质量相等,则参加反应的镁和铝的质量比为( )A、3:2 B、4:3 C、1:1 D、1:2
A、属于非金属元素 B、原子的质量是85.47g C、元素符号为Rb D、原子核内有37个中子12. 火药是我国古代四大发明之一,《天工开物》记载:“凡硫黄配硝而后,火药成声”。其反应的化学方程式为: 。则X的化学式为( )A、O2 B、SO2 C、NO2 D、N213. 中药当归、白芷中富含的紫花前胡醇(化学式为C14H14O4),能增强人体免疫力。下列关于紫花前胡醇叙述错误的是( )A、是一种化合物 B、由三种元素组成 C、在空气中燃烧可能生成CO2 D、C,H,O元素质量比为7:7:214. 已知镁和铝的相对原子质量之比为8:9,若镁和铝分别与足量盐酸反应,生成氢气的质量相等,则参加反应的镁和铝的质量比为( )A、3:2 B、4:3 C、1:1 D、1:2二、填空题
-
15. 根据下列要求用恰当的符号表示:(1)、2个氮原子。(2)、3个硫酸根离子。(3)、地壳中含量最多的金属元素与最多的非金属元素形成的化合物的化学式。16. 如图是电解水的实验示意图,试管a中的气体是。电解水的化学方程式为。
 17. 化学与生活密切相关。回答下列问题:(1)、自来水硬度较大不宜直接饮用。为了降低水的硬度生活中常采用的方法是。(2)、扑灭森林火灾时通常将大火蔓延路线前的一片树木砍掉,其灭火原理是。(3)、为防止铁锅生锈,日常生活中常用的方法是。(写一条)18. 已知 , 现有7gA和24gB2恰好完全反应生成9gD.已知C的相对分子质量为44,则B2的相对分子质量为。19. 如图是某反应的微观示意图。
17. 化学与生活密切相关。回答下列问题:(1)、自来水硬度较大不宜直接饮用。为了降低水的硬度生活中常采用的方法是。(2)、扑灭森林火灾时通常将大火蔓延路线前的一片树木砍掉,其灭火原理是。(3)、为防止铁锅生锈,日常生活中常用的方法是。(写一条)18. 已知 , 现有7gA和24gB2恰好完全反应生成9gD.已知C的相对分子质量为44,则B2的相对分子质量为。19. 如图是某反应的微观示意图。 (1)、写出乙中氮元素的化合价:。(2)、写出该反应的化学方程式:。20. 天然气广泛应用于生产生活,其主要成分是甲烷(CH4)。(1)、天然气属于(填“可再生”或“不可再生")能源。(2)、室温下,充分燃烧1g天然气和1g煤,产生的CO2及热量的对比如图所示。据图分析,与煤相比,用天然气作燃料的优点有哪些?
(1)、写出乙中氮元素的化合价:。(2)、写出该反应的化学方程式:。20. 天然气广泛应用于生产生活,其主要成分是甲烷(CH4)。(1)、天然气属于(填“可再生”或“不可再生")能源。(2)、室温下,充分燃烧1g天然气和1g煤,产生的CO2及热量的对比如图所示。据图分析,与煤相比,用天然气作燃料的优点有哪些? (3)、甲烷和二氧化碳在高温下催化重整(Ni作催化剂)可制得CO和H2.写出该反应的化学方程式。
(3)、甲烷和二氧化碳在高温下催化重整(Ni作催化剂)可制得CO和H2.写出该反应的化学方程式。三、科普阅读题
-
21. 阅读科普短文回答相关问题。
钠元素在自然界中分布很广,储量极为丰富,常以氯化钠、碳酸钠、硫酸钠等物质存在。
19世纪初,英国化学家戴维在实验室中首次制得了金属钠。
钠是一种银白色金属质软。密度为097g·cm-3 , 熔点为97.8℃。金属钠的性质很活泼,能与许多物质发生化学反应。钠暴露在空气中,与氧气反应生成氧化钠(Na2O),钠在空气中燃烧,生成淡黄色的过氧化钠(Na2O2);钠遇水立即发生剧烈反应,生成氢氧化钠和氢气。因此实验室常将钠保存在煤油中。
金属钠的用途广泛。钠和钾形成的合金熔点低,常温下呈液态可用作快中子反应堆的热交换剂。利用钠的强还原性,在一定条件下可以将钛(Ti)、锆(Zr)等稀有金属从其氯化物中置换出来。
工业上通常采用电解熔融氯化钠的方法制取单质钠。
(1)、自然界中钠元素以(填“单质”或“化合物”)形式存在。(2)、钠保存在煤油中是为了防止钠与空气中的反应而变质。(3)、钠钾合金用作快中子反应堆的热交换剂利用钠钾合金良好的(填字母)。a、导电性 b、导热性 c、延展性
(4)、写出高温下钠与四氯化钛反应的化学方程式:。四、综合题
-
22. 木炭、氢气、一氧化碳具有相似的化学性质,如都能燃烧,都能将某些金属从它们的氧化物中还原出来。现有A、B、C 、D、E五种常见的物质,常温下A、E是气态单质,C是液体,D是一种紫红色金属单质,它们之间的转化关系如图所示,反应条件均已略去。
 (1)、E的化学式是。(2)、反应A+B→C+D的化学方程式是。(3)、用А的单质作燃料用很多有优点,请列举一条。23. 地球是我们的家园保护环境人人有责。请回答下列问题:(1)、爱护水资源就要防治水体污染。水体污染产生的原因有哪些?(答一点即可)(2)、大气中二氧化碳的含量不断增多,导致温室效应增强。温室效应增强对人类生产生活造成的危害有哪些?(答一点即可)24. 在实验室中,可以选择下图所示装置来制取气体。
(1)、E的化学式是。(2)、反应A+B→C+D的化学方程式是。(3)、用А的单质作燃料用很多有优点,请列举一条。23. 地球是我们的家园保护环境人人有责。请回答下列问题:(1)、爱护水资源就要防治水体污染。水体污染产生的原因有哪些?(答一点即可)(2)、大气中二氧化碳的含量不断增多,导致温室效应增强。温室效应增强对人类生产生活造成的危害有哪些?(答一点即可)24. 在实验室中,可以选择下图所示装置来制取气体。 (1)、若用A、C装置制取氧气,写出一个反应的化学方程式。(2)、确定B作为气体发生装置应满足的条件是什么?。(3)、若制取某气体时用装置C进行收集,则该气体具有的性质是什么?。25. 如图为探究金属化学性质的两组实验。
(1)、若用A、C装置制取氧气,写出一个反应的化学方程式。(2)、确定B作为气体发生装置应满足的条件是什么?。(3)、若制取某气体时用装置C进行收集,则该气体具有的性质是什么?。25. 如图为探究金属化学性质的两组实验。 (1)、Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,小李同学认为该实验设计不够合理,理由是。(2)、写出实验Ⅱ中E试管内反应的化学方程式:。(3)、实验Ⅱ中金属丝在插入试管前一般要打磨,目的是。(4)、实验Ⅱ中要证明Cu、Fe、Ag的金属活动性顺序,小明认为(填字母序号)是多余的。若实验室只有铜片,小明将铜片分别放入两种化合物溶液中,也通过实验验证了三种金属的活动性顺序,所用的两种化合物溶液可能是溶液和溶液。(5)、将20.0g铜锌合金置于烧杯中,向其中逐渐加入稀硫酸。当加入148.4g稀硫酸时,不再有气体生成此时测得烧杯中混合物的质量为168.0g。请计算:
(1)、Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,小李同学认为该实验设计不够合理,理由是。(2)、写出实验Ⅱ中E试管内反应的化学方程式:。(3)、实验Ⅱ中金属丝在插入试管前一般要打磨,目的是。(4)、实验Ⅱ中要证明Cu、Fe、Ag的金属活动性顺序,小明认为(填字母序号)是多余的。若实验室只有铜片,小明将铜片分别放入两种化合物溶液中,也通过实验验证了三种金属的活动性顺序,所用的两种化合物溶液可能是溶液和溶液。(5)、将20.0g铜锌合金置于烧杯中,向其中逐渐加入稀硫酸。当加入148.4g稀硫酸时,不再有气体生成此时测得烧杯中混合物的质量为168.0g。请计算:①反应中生成气体的质量是g。
②合金中铜的质量分数。(写出计算过程)
-