河北省唐山市迁安市2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-01-26 类型:期末考试
一、单选题
-
1. 《中国诗词大会》弘扬了中国传统文化。下列诗句反映的物质变化主要为化学变化的是( )A、千淘万漉虽辛苦,吹尽狂沙始到金。 B、千锤万凿岀深山,烈火焚烧若等闲 C、花气袭人知骤暖,鹊声穿树喜新晴。 D、无边落木萧萧下,不尽长江滚滚来。2. 规范的实验操作是实验成功的关键。实验操作错误的是( )A、吸取药液
 B、气体发生装置
B、气体发生装置 C、滴加液体
C、滴加液体 D、点酒精灯
D、点酒精灯 3. 下列有关数字“2”的意义的说法,其中正确的是( )A、H2:2个氢原子 B、2:2个三氧化氮离子 C、:氧化汞中汞元素的化合价为+2价 D、2Na:2个钠元素4. 下列物质燃烧的现象,描述正确的是( )A、硫在氧气中燃烧发出淡蓝色火焰,放热,生成有刺激性气味的气体 B、红磷在空气中燃烧产生白雾,放出大量的热 C、木炭在空气中燃烧发出白光,生成二氧化碳气体 D、铁丝在氧气中燃烧火星四射,放热,生成黑色物质5. 关于测定空气中氧气含量的实验,下列说法正确的是( )
3. 下列有关数字“2”的意义的说法,其中正确的是( )A、H2:2个氢原子 B、2:2个三氧化氮离子 C、:氧化汞中汞元素的化合价为+2价 D、2Na:2个钠元素4. 下列物质燃烧的现象,描述正确的是( )A、硫在氧气中燃烧发出淡蓝色火焰,放热,生成有刺激性气味的气体 B、红磷在空气中燃烧产生白雾,放出大量的热 C、木炭在空气中燃烧发出白光,生成二氧化碳气体 D、铁丝在氧气中燃烧火星四射,放热,生成黑色物质5. 关于测定空气中氧气含量的实验,下列说法正确的是( ) A、实验前止水夹没有夹紧 B、将红磷换成木炭进行实验 C、待装置冷却至室温后,再打开止水夹 D、点燃红磷缓慢伸入集气瓶中后,再塞紧瓶塞6. 某学习小组用相同的洁净无锈的铁钉对铁制品锈蚀的条件进行探究,设计的实验如图所示,一周后观察。下列说法错误的是( )
A、实验前止水夹没有夹紧 B、将红磷换成木炭进行实验 C、待装置冷却至室温后,再打开止水夹 D、点燃红磷缓慢伸入集气瓶中后,再塞紧瓶塞6. 某学习小组用相同的洁净无锈的铁钉对铁制品锈蚀的条件进行探究,设计的实验如图所示,一周后观察。下列说法错误的是( ) A、①和②中的铁钉无明显变化,③中的铁钉明显生锈 B、②中加入的蒸馏水要事先煮沸,目的是除去水中溶解的氧气 C、③中铁钉的甲、乙、丙三处,甲处锈蚀最严重 D、探究发现铁生锈的主要条件是铁与空气和水(水蒸气)直接接触7. 如图所示是某化学反应的微观示意图,下列说法正确的是( )
A、①和②中的铁钉无明显变化,③中的铁钉明显生锈 B、②中加入的蒸馏水要事先煮沸,目的是除去水中溶解的氧气 C、③中铁钉的甲、乙、丙三处,甲处锈蚀最严重 D、探究发现铁生锈的主要条件是铁与空气和水(水蒸气)直接接触7. 如图所示是某化学反应的微观示意图,下列说法正确的是( ) A、该反应属于置换反应 B、生成物丁由2个氧原子和1个碳原子构成 C、生成物丙中氢元素和氧元素的质量比为2:1 D、参加反应的甲和乙的分子个数比为2:78. 下列关于水的说法正确的是( )A、用肥皂水不能区别硬水和软水 B、蒸馏后得到的水是纯净物 C、生活污水可以随意排放 D、在河水样品中加入明矾可以除去水中所有杂质9. 下图一是电解水实验装置图,图二是过滤实验装置图,下列有关说法错误的是( )
A、该反应属于置换反应 B、生成物丁由2个氧原子和1个碳原子构成 C、生成物丙中氢元素和氧元素的质量比为2:1 D、参加反应的甲和乙的分子个数比为2:78. 下列关于水的说法正确的是( )A、用肥皂水不能区别硬水和软水 B、蒸馏后得到的水是纯净物 C、生活污水可以随意排放 D、在河水样品中加入明矾可以除去水中所有杂质9. 下图一是电解水实验装置图,图二是过滤实验装置图,下列有关说法错误的是( )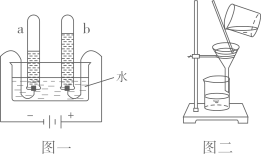 A、图一中a试管内收集的气体是氢气,可以燃烧 B、通过电解水的实验,说明水由氢气和氧气组成 C、图二过滤操作中,玻璃棒的作用是引流 D、图二中漏斗内的液面高于滤纸的边缘会导致滤液浑浊10. 科研人员发现维生素P能封住病毒的侵占途径。已知维生素P的化学式为C27H30O16 , 关于维生素P的叙述中正确的是( )A、维生素P是一种氧化物 B、维生素P是由27个碳原子、30个氢原子和16个氧原子构成 C、维生素P相对分子质量为610g D、将维生素P在足量的氧气中充分燃烧,产物为CO2和H2O11. 下列关于金属材料的说法中,正确的是( )A、生铁和钢是含碳量不同的两种铁合金 B、黄铜片(铜锌合金)比纯铜片硬度小 C、“真金不怕火炼”是指金的熔点高 D、铝制品在空气中耐腐蚀是因为铝不活泼12. 根据如图所示的实验现象,下列判断错误的是( )
A、图一中a试管内收集的气体是氢气,可以燃烧 B、通过电解水的实验,说明水由氢气和氧气组成 C、图二过滤操作中,玻璃棒的作用是引流 D、图二中漏斗内的液面高于滤纸的边缘会导致滤液浑浊10. 科研人员发现维生素P能封住病毒的侵占途径。已知维生素P的化学式为C27H30O16 , 关于维生素P的叙述中正确的是( )A、维生素P是一种氧化物 B、维生素P是由27个碳原子、30个氢原子和16个氧原子构成 C、维生素P相对分子质量为610g D、将维生素P在足量的氧气中充分燃烧,产物为CO2和H2O11. 下列关于金属材料的说法中,正确的是( )A、生铁和钢是含碳量不同的两种铁合金 B、黄铜片(铜锌合金)比纯铜片硬度小 C、“真金不怕火炼”是指金的熔点高 D、铝制品在空气中耐腐蚀是因为铝不活泼12. 根据如图所示的实验现象,下列判断错误的是( )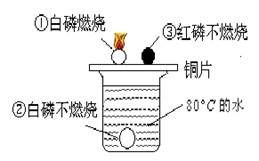 A、①②说明物质燃烧需要氧气 B、①说明白磷的着火点不高于80℃ C、烧杯中的热水只起提高温度的作用 D、①③说明两种可燃物的着火点不同13. 下列物质的用途仅与其物理性质有关的是( )A、用二氧化碳灭火 B、用生石灰作干燥剂 C、铜制作成导线 D、用焦炭冶炼金属14. 孔明灯燃气的火焰温度可达300℃,但纸质灯罩却没被点燃的原因是( )A、纸张不是可燃物,不能燃烧 B、风将热量吹散后灯罩的着火点降低了 C、空气不充足,纸张不会燃烧 D、风将热量吹散使灯罩处温度低于纸的着火点15. 下列生活中的现象,与物质溶解性无关的是( )A、咸菜长期放置在空气中,有一层“白霜” B、揭开啤酒瓶盖,有大量气泡溢出 C、烧开水时,沸腾前有气泡冒出 D、盛石灰水的瓶口有一层白膜16. 有一固体物质(不含结晶水)的溶液甲,在一定温度下,经历如下变化:
A、①②说明物质燃烧需要氧气 B、①说明白磷的着火点不高于80℃ C、烧杯中的热水只起提高温度的作用 D、①③说明两种可燃物的着火点不同13. 下列物质的用途仅与其物理性质有关的是( )A、用二氧化碳灭火 B、用生石灰作干燥剂 C、铜制作成导线 D、用焦炭冶炼金属14. 孔明灯燃气的火焰温度可达300℃,但纸质灯罩却没被点燃的原因是( )A、纸张不是可燃物,不能燃烧 B、风将热量吹散后灯罩的着火点降低了 C、空气不充足,纸张不会燃烧 D、风将热量吹散使灯罩处温度低于纸的着火点15. 下列生活中的现象,与物质溶解性无关的是( )A、咸菜长期放置在空气中,有一层“白霜” B、揭开啤酒瓶盖,有大量气泡溢出 C、烧开水时,沸腾前有气泡冒出 D、盛石灰水的瓶口有一层白膜16. 有一固体物质(不含结晶水)的溶液甲,在一定温度下,经历如下变化:
据此判断下列结论中正确的是( )
A、该温度下,固体物质的溶解度是30g B、溶液乙和溶液丙的溶质质量分数可能相等 C、溶液乙一定是不饱和溶液 D、溶液丙再蒸发10g水,析出晶体的质量一定大于3g17. 下列四个实验中只需完成三个就可以证明Fe、Cu 、Ag三种金属的活动性顺序,其中不必进行的是( )A、将铁片放入稀盐酸 B、将铜片放入盐酸 C、将铁片放入硝酸银溶液 D、将铜片放入硝酸银溶液18. 将一定质量的铁粉加入到Mg(NO3)2、AgNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣。向滤液中加入稀盐酸,无明显现象。下列叙述正确的是( )A、滤液中一定含有Mg2+和Fe3+ B、滤液中含有Mg2+和Ag+ C、滤渣中一定含有Ag D、滤渣中可能含有Mg19. 如图,室温下,盛水的烧杯内放置两支分别盛有等质量KNO3溶液和饱和石灰水的试管甲和乙,向烧杯内的水中加入NH4NO3固体后,甲中未观察到明显现象。下列说法正确的是( ) A、乙中溶液一定变浑浊 B、甲中溶液一定变成饱和溶液 C、乙中溶液溶质的质量分数一定变小 D、甲、乙中溶液质量一定相等20. 现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( )
A、乙中溶液一定变浑浊 B、甲中溶液一定变成饱和溶液 C、乙中溶液溶质的质量分数一定变小 D、甲、乙中溶液质量一定相等20. 现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( )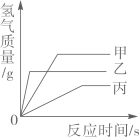 A、完全反应所需时间:丙>甲>乙 B、生成氢气的质量:甲>乙>丙 C、相对原子质量:乙>丙>甲 D、消耗硫酸的质量:甲>乙>丙
A、完全反应所需时间:丙>甲>乙 B、生成氢气的质量:甲>乙>丙 C、相对原子质量:乙>丙>甲 D、消耗硫酸的质量:甲>乙>丙二、填空题
-
21. 当前,新冠肺炎肆虐全球。面对来势汹汹的疫情,习近平总书记亲自指挥、亲自布置,提出坚定信心、同舟共济、科学防治、精准施策的总要求。疾控专家强调要做好个人防护措施,如出门戴口罩、保持社交距离、勤洗手、多通风、定期消毒等,人们在出门前、回家后可使用75%的乙醇溶液等消毒液对手部、衣物进行消毒。在使用75%乙醇进行消毒过程中,室内禁止大面积喷洒式消毒方式,要防止空气中浓度超过3%而发生火灾,如果喷洒浓度达到3%,衣服静电就可能引起燃爆。请回答下列问题:(1)、乙醇俗称酒精,请写出乙醇燃烧的化学方程式。(2)、在汽油中加入适量的乙醇作为汽车燃料,除了适当的节省石油资源,还有一个优点:。(3)、乙醇可以通过高梁、玉米和薯类等发酵、蒸馏而得到,属于可再生资源。我们现在更多的在使用不可再生能源,如:。(写一个即可)22. 水与溶液在生产生活中有广泛的用途。请结合所学知识回答下列问题:
“十·一”期间,小明一家去白羊峪长城旅游。
(1)、小明带去“自热米饭”的加热原理是饭盒夹层中的水与生石灰反应放出大量的热,该反应的化学方程式为。(2)、回家后,小明发现衣物上有油污,于是他用洗洁精清洗衣服上的油污,是因为洗洁精具有作用。23. 如图是不含结晶水的甲、乙、丙三种固体物质的溶解度曲线,看图并回答下列问题。 (1)、M点表示的含义是。(2)、t2℃时,将20g甲物质加入到50g水中,充分溶解后所得溶液的质量是g。(3)、t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温至t2℃,所得溶液中溶质质量分数由大到小的顺序是。(4)、若甲物质中混有少量乙物质,最好采用的方法提纯甲。
(1)、M点表示的含义是。(2)、t2℃时,将20g甲物质加入到50g水中,充分溶解后所得溶液的质量是g。(3)、t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温至t2℃,所得溶液中溶质质量分数由大到小的顺序是。(4)、若甲物质中混有少量乙物质,最好采用的方法提纯甲。三、综合题
-
24. 炼铁的原理是利用一氧化碳与氧化铁的反应,实验装置如图所示。
 (1)、实验开始先通入一氧化碳,再加热氧化铁,目的是:。(2)、从实验中可以观察到,玻璃管里的粉末 , 试管里澄清石灰水。(3)、玻璃管中反应的化学方程式为。25. 下图是配制50g质量分数为4%的NaCl溶液的过程示意图。请回答下列问题:
(1)、实验开始先通入一氧化碳,再加热氧化铁,目的是:。(2)、从实验中可以观察到,玻璃管里的粉末 , 试管里澄清石灰水。(3)、玻璃管中反应的化学方程式为。25. 下图是配制50g质量分数为4%的NaCl溶液的过程示意图。请回答下列问题: (1)、量水用到的仪器有:。(2)、若按照上述图示操作(假定再无其他不正确),则所配制溶液的质量分数(选填“大于”、“小于”或“等于”)4%。(3)、若将图中的不正确更正后重新配制溶液,测得溶液的质量分数大于4%。请你分析可能的原因(写一条):。26. 实验室常用如图的一些装置制备气体,请回答下列问题。
(1)、量水用到的仪器有:。(2)、若按照上述图示操作(假定再无其他不正确),则所配制溶液的质量分数(选填“大于”、“小于”或“等于”)4%。(3)、若将图中的不正确更正后重新配制溶液,测得溶液的质量分数大于4%。请你分析可能的原因(写一条):。26. 实验室常用如图的一些装置制备气体,请回答下列问题。 (1)、写出实验室用氯酸钾制O2的化学方程式:;如要收集比较纯净的氧气,则选用的收集装置是。(填序号)(2)、实验室检验二氧化碳是否收集满的方法是:。(3)、已知氯气(Cl2)是黄绿色、密度比空气大的气体,可溶于水,不易溶于饱和食盐水。实验室通常用浓盐酸和二氧化锰反应加热制取氯气。
(1)、写出实验室用氯酸钾制O2的化学方程式:;如要收集比较纯净的氧气,则选用的收集装置是。(填序号)(2)、实验室检验二氧化碳是否收集满的方法是:。(3)、已知氯气(Cl2)是黄绿色、密度比空气大的气体,可溶于水,不易溶于饱和食盐水。实验室通常用浓盐酸和二氧化锰反应加热制取氯气。①实验室制取氯气的发生装置是(填序号)选用此装置的依据:。
②若用G收集氯气,气体应从端进(填字母编号):若F的集气瓶内先装满饱和食盐水,收集氯气时应从端进(填字母编号)。
27. A、B、C、D、E、F、G是初中常见的七种不同物质,其中A、D均为黑色粉末,C的溶液为蓝色,F物质在空气中不能燃烧,只有在气体E中能剧烈燃烧,“一”表示两种物质可以发生反应,“→表示两种物质可以相互转化,请回答下列问题: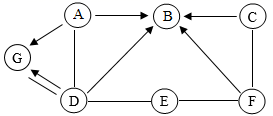 (1)、写出下列物质的化学式:A;F。(2)、写出D与G反应的化学方程式。(3)、写出C与F发生化学反应的基本类型。28. 在探究质量守恒定律的实验时,同学们将洁净的铁钉放入盛有硫酸铜溶液的烧杯中,并将烧杯放于天平左盘,调节天平使之平衡。(1)、观察到铁钉表面变为红色,反应的化学方程式为 , 反应一段时间后,发现天平指针向右偏转。细心的同学发现,铁钉表面同时有气泡冒出,同学们对此现象在老师指导下进行了如下探究:
(1)、写出下列物质的化学式:A;F。(2)、写出D与G反应的化学方程式。(3)、写出C与F发生化学反应的基本类型。28. 在探究质量守恒定律的实验时,同学们将洁净的铁钉放入盛有硫酸铜溶液的烧杯中,并将烧杯放于天平左盘,调节天平使之平衡。(1)、观察到铁钉表面变为红色,反应的化学方程式为 , 反应一段时间后,发现天平指针向右偏转。细心的同学发现,铁钉表面同时有气泡冒出,同学们对此现象在老师指导下进行了如下探究:探究产生的气泡成分是什么?
(2)、(查阅资料)二氧化硫具有漂白性,会使品红溶液褪色,浓硫酸具有吸水干燥气体的作用。
(提出猜想)A:氧气B:二氧化硫C:二氧化碳D:氢气
经讨论,同学们一致认为C同学的猜想是不合理的,理由是。
(3)、(进行实验)利用如图所示的装置分别进行实验反应一段时间后,A同学将带火星的木条放在a处,观察到: , 则她的猜想不正确。
(4)、B同学将产生的气体通入品红溶液中,观察到 , 则她的猜想也不正确。(5)、D同学将图I中的a端导管与图Ⅱ中的端导管相连。反应一段时间后,点燃从图Ⅱ另一端导管出来的气体,通过对现象的分析,得出他的猜想正确。(得出结论)铁与硫酸铜溶液反应时产生的气体为氢气。
四、计算题
-
29. 我国第一艘国产航母的许多电子元件使用了黄铜(假设合金中仅含铜,锌),兴趣小组同学向盛有30g黄铜样品的烧杯中逐渐加入稀硫酸,生成氢的质量与加入稀硫酸的质量关系如图所示,计算:
 (1)、充分反应后生成氢气的质量为g。(2)、硫酸溶液中溶质的质量分数。30. 某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数,先将10g样品放入烧杯中,再把100g稀盐酸分5次加入该样品中(该实验条件下,杂质不与酸反应,也不溶解于水,忽略稀盐酸挥发),得实验数据如表格。
(1)、充分反应后生成氢气的质量为g。(2)、硫酸溶液中溶质的质量分数。30. 某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数,先将10g样品放入烧杯中,再把100g稀盐酸分5次加入该样品中(该实验条件下,杂质不与酸反应,也不溶解于水,忽略稀盐酸挥发),得实验数据如表格。稀盐酸的质量
充分反应后剩余固体的质量
第一次加入20g
8g
第二次加入20g
6g
第三次加入20g
4g
第四次加入20g
2g
第五次加入20g
2g
(1)、10g石灰石样品中碳酸钙的质量分数是。(2)、求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)