河北省唐山市滦州市2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-01-26 类型:期末考试
一、单选题
-
1. 下列现象不涉及化学变化的是( )A、蜡烛燃烧 B、酒精挥发 C、高炉炼铁 D、电解水2. 下列图示实验操作中,正确的是( )A、点燃酒精灯
 B、闻气体气味
B、闻气体气味 C、读取液体体积
C、读取液体体积 D、稀释浓硫酸
D、稀释浓硫酸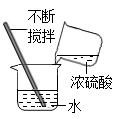 3. 下列符号中,既能表示一种单质的化学式,还能表示一种元素和该元素的 一个原子的是:( )A、O B、H2 C、2N D、C4. 下列化学用语与含义相符的是( )A、2H2O:两个水分子 B、Mg2+:镁元素在化合物中是+2价 C、2N:两个氮元素 D、O2:2个氧原子5. 某两种物质在一定条件下能发生化学反应,其反应的微观示意图如下,则下列说法中错误的是(说明:一种小球代表一种元素的原子)( )
3. 下列符号中,既能表示一种单质的化学式,还能表示一种元素和该元素的 一个原子的是:( )A、O B、H2 C、2N D、C4. 下列化学用语与含义相符的是( )A、2H2O:两个水分子 B、Mg2+:镁元素在化合物中是+2价 C、2N:两个氮元素 D、O2:2个氧原子5. 某两种物质在一定条件下能发生化学反应,其反应的微观示意图如下,则下列说法中错误的是(说明:一种小球代表一种元素的原子)( ) A、乙物质含有两种元素 B、该反应属于置换反应 C、图中两种反应物的质量比为2:3 D、反应的本质是原子进行了重新组合6. 下列说法正确的是()A、铁是地壳中含量最多的金属元素 B、铁制品在潮湿的空气中容易生锈 C、多数合金的熔点高于它的成分金属 D、铝制品在空气中耐腐蚀是因为铝不活泼7. 下列化学方程式书写正确的是( )A、 B、 C、 D、8. 花生油、盐、面酱、醋是厨房中常用的调味品,将它们分别与足量水充分混合后,形成的混合物属于溶液的是( )
A、乙物质含有两种元素 B、该反应属于置换反应 C、图中两种反应物的质量比为2:3 D、反应的本质是原子进行了重新组合6. 下列说法正确的是()A、铁是地壳中含量最多的金属元素 B、铁制品在潮湿的空气中容易生锈 C、多数合金的熔点高于它的成分金属 D、铝制品在空气中耐腐蚀是因为铝不活泼7. 下列化学方程式书写正确的是( )A、 B、 C、 D、8. 花生油、盐、面酱、醋是厨房中常用的调味品,将它们分别与足量水充分混合后,形成的混合物属于溶液的是( )①花生油 ②食盐 ③面酱 ④白醋
A、①③ B、②③ C、①④ D、②④9. 下列溶液,能使无色酚酞变红的是( )A、硫酸 B、盐水 C、苹果醋 D、石灰水10. 如图所示已平衡的天平两端放着两个分别盛有浓盐酸和浓硫酸的敞口烧杯,过一段时间后,天平会( ) A、左端下沉 B、右端下沉 C、仍平衡 D、无法判断11. 中国著名的制碱专家侯德榜发明了“联合制碱法”。侯德榜为纯碱、氮肥工业技术的发展作出了杰出的贡献。纯碱(化学式为Na2CO3)属于( )A、氧化物 B、酸 C、碱 D、盐12. 人被蚊虫叮咬之后,皮肤红肿疼痛,这是因为被注入了一种叫做蚁酸的物质。此时为减轻疼痛,可涂抹的物质是( )A、食盐水 B、肥皂水 C、橘子汁 D、米醋13. 下列使用pH试纸的方法正确的是()A、将溶液倒在pH试纸上测定溶液的pH B、将pH试纸伸入溶液中测定溶液的pH C、测定前必须先用蒸馏水润湿pH试纸 D、用胶头滴管滴1小滴待测液到pH试纸上测定溶液的pH。14. 下列说法正确的是( )A、100g水溶解了30g某物质,则该物质的溶解度为30g B、饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 C、温度相同条件下,同一种物质的饱和溶液比不饱和溶液溶质的质量分数大 D、20℃,某物质的溶解度为20克,此时它的饱和溶液的溶质在整个溶液中的质量分数是20%15. 下列图象与所属实验现象相符的是( )A、
A、左端下沉 B、右端下沉 C、仍平衡 D、无法判断11. 中国著名的制碱专家侯德榜发明了“联合制碱法”。侯德榜为纯碱、氮肥工业技术的发展作出了杰出的贡献。纯碱(化学式为Na2CO3)属于( )A、氧化物 B、酸 C、碱 D、盐12. 人被蚊虫叮咬之后,皮肤红肿疼痛,这是因为被注入了一种叫做蚁酸的物质。此时为减轻疼痛,可涂抹的物质是( )A、食盐水 B、肥皂水 C、橘子汁 D、米醋13. 下列使用pH试纸的方法正确的是()A、将溶液倒在pH试纸上测定溶液的pH B、将pH试纸伸入溶液中测定溶液的pH C、测定前必须先用蒸馏水润湿pH试纸 D、用胶头滴管滴1小滴待测液到pH试纸上测定溶液的pH。14. 下列说法正确的是( )A、100g水溶解了30g某物质,则该物质的溶解度为30g B、饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 C、温度相同条件下,同一种物质的饱和溶液比不饱和溶液溶质的质量分数大 D、20℃,某物质的溶解度为20克,此时它的饱和溶液的溶质在整个溶液中的质量分数是20%15. 下列图象与所属实验现象相符的是( )A、 稀释NaOH溶液
B、
稀释NaOH溶液
B、 镁在空气中燃烧
C、
镁在空气中燃烧
C、 铁加入稀盐酸中
D、
铁加入稀盐酸中
D、 氧气的溶解度
氧气的溶解度
二、填空题
-
16. 写出下列物质的化学式:(1)、俗名为火碱、烧碱、苛性钠的碱。(2)、胃液里含有的一种酸。(3)、常用于作建筑材料的一种碱。(4)、常用于汽车电瓶的一种酸。(5)、日常生活中焙制糕点所用发酵粉主要成分之一的一种盐。17. 化学就在我们身边,与我们的生活息息相关。请回答下列生活中的化学问题。(1)、医疗急救时需要氧气,是因为氧气能。(2)、用墨书写或绘制的字画能够保存很长时间不变色的原因是。(3)、生活中可用来检验是硬水还是软水,要降低水的硬度,在生活中可采取的简便可行的方法是。(4)、通常用活性炭除去冰箱中的异味,这是因为活性炭具有性。18. 将一根锃亮的铁丝放入蓝色的硫酸铜溶液中,过一会儿,会发现铁丝表面出现 , 溶液由蓝色逐渐变为色,写出发生反应的化学方程式。由此判断,铁的金属活动性比铜。19. 鉴别稀硫酸、石灰水和烧碱溶液:用三支试管分别取适量的三种溶液,然后分别滴加紫色的石蕊试液,试管中溶液变红的是;然后向剩余的两支试管中分别滴加适量的碳酸钠溶液,出现现象的是石灰水,写出该反应的化学方程式。20. 在高锰酸钾、硫酸铜、纯碱、氯化钠、小苏打中,用于腌制食品的是 , 用来配制波尔多液的是 , 可用作洗涤剂的是21. 如图所示是氧原子的结构示意图和氧元素在元素周期表中的相关信息,由此可知,氧原子核内有个质子,氧的相对原子质量是。氧原子的最外层电子数是 , 氧与其他物质发生化学反应时容易电子(选填“得到”或“失去”)。
 22. 人体中化学元素含量的多少会直接影响人体健康,如果缺元素会引起贫血;如果缺元素儿童易得佝偻病:如果缺元素容易引起甲状腺肿大。23. 小明同学在化学实验室制作“叶脉书签”,需要50g质量分数为10%的氢氧化钠溶液。请回答下列问题:(1)、若用氢氧化钠固体配制,需用称取氢氧化钠g。用量取mL的水,读数时若俯视,会使溶质质量分数。(填偏大、偏小、不变)(已知ρ水=1g/cm3)。(2)、若用25%的氢氧化钠溶液配制,需25%的氢氧化钠溶液g,水g。24. 如表是氯化钠和硝酸钾在不同温度下的溶解度,运用溶解度表与溶解度曲线回答下列问题:
22. 人体中化学元素含量的多少会直接影响人体健康,如果缺元素会引起贫血;如果缺元素儿童易得佝偻病:如果缺元素容易引起甲状腺肿大。23. 小明同学在化学实验室制作“叶脉书签”,需要50g质量分数为10%的氢氧化钠溶液。请回答下列问题:(1)、若用氢氧化钠固体配制,需用称取氢氧化钠g。用量取mL的水,读数时若俯视,会使溶质质量分数。(填偏大、偏小、不变)(已知ρ水=1g/cm3)。(2)、若用25%的氢氧化钠溶液配制,需25%的氢氧化钠溶液g,水g。24. 如表是氯化钠和硝酸钾在不同温度下的溶解度,运用溶解度表与溶解度曲线回答下列问题: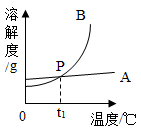
温度/℃
10
30
50
60
溶解度/g
氯化钠
35.8
36.3
37.0
37.3
硝酸钾
20.9
45.8
85.5
110
(1)、图中能表示氯化钠的溶解度曲线是(选填“A”或“B”),P点表示的含义是。(2)、据表格可知,氯化钠和硝酸钾两物质溶解度相等的温度范围在℃之间。(3)、60℃时,100g水中加入90g硝酸钾,充分溶解,所得溶液是(填“饱和”或“不饱和”)溶液。将该溶液降温到10℃时,析出晶体的质量为g。(4)、60℃时,用等质量的氯化钠、硝酸钾分别配制两种饱和溶液,测得其质量依次为m1g和m2g,则m1m2(填或“>”、“<”“=”)。25. 如图所示是粗盐提纯的实验。 (1)、实验的操作顺序应为。(填字母序号)(2)、图B中仪器a的名称是;溶解过程玻璃棒的作用及达到的目的是;过滤过程玻璃棒的作用是;蒸发操作中玻璃棒的作用及达到的目的是 , 当出现时停止加热利用余热将滤液蒸干:蒸发操作结束后,用将固体转移到纸片上。26. “对比实验”是科学探究常用的方法,根据下列实验回答问题。
(1)、实验的操作顺序应为。(填字母序号)(2)、图B中仪器a的名称是;溶解过程玻璃棒的作用及达到的目的是;过滤过程玻璃棒的作用是;蒸发操作中玻璃棒的作用及达到的目的是 , 当出现时停止加热利用余热将滤液蒸干:蒸发操作结束后,用将固体转移到纸片上。26. “对比实验”是科学探究常用的方法,根据下列实验回答问题。 (1)、实验1中,将大小相同的滤纸片和乒乓球碎片放在薄铜片的两侧,加热铜片的中部,观察到乒乓球碎片比滤纸片先燃烧,通过此现象说明燃烧的条件之一是____。A、可燃物 B、与氧气接触 C、温度达到着火点(2)、实验2中,把干燥的紫色石蕊纸花和湿润的紫色石落纸花分别放入两瓶干燥的二氧化碳气体中,观察到干燥的紫色石蕊纸花不变色,湿润的紫色石蕊纸花变红,通过此现象说明CO2与水发生了反应且生成物具有性。(3)、实验3是探究铁生锈条件的实验,会出现明显现象的是(填序号,下同)。欲得出“铁生锈需要与氧气接触”的实验结论,需要对比两次实验。
(1)、实验1中,将大小相同的滤纸片和乒乓球碎片放在薄铜片的两侧,加热铜片的中部,观察到乒乓球碎片比滤纸片先燃烧,通过此现象说明燃烧的条件之一是____。A、可燃物 B、与氧气接触 C、温度达到着火点(2)、实验2中,把干燥的紫色石蕊纸花和湿润的紫色石落纸花分别放入两瓶干燥的二氧化碳气体中,观察到干燥的紫色石蕊纸花不变色,湿润的紫色石蕊纸花变红,通过此现象说明CO2与水发生了反应且生成物具有性。(3)、实验3是探究铁生锈条件的实验,会出现明显现象的是(填序号,下同)。欲得出“铁生锈需要与氧气接触”的实验结论,需要对比两次实验。三、综合题
-
27. A是常见金属单质,B、C是非金属单质,且C是密度最小的气体,甲是磁铁矿的主要成分,乙是无色液体,它们之间有如下图所示的转化关系(部分产物和反应条件未标明)
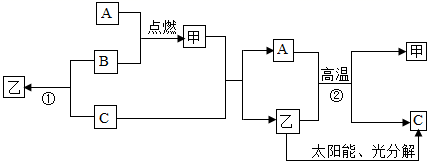 (1)、甲、乙的化学式为:甲 , 乙;(2)、写出反应②的化学方程式;(3)、写出反应①的化学方程式 , 该反应的基本类型是。28. 小刚在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末,小刚叫来小军和小红,共同探究这种白色粉末的成分。他们有依据所学的化学知识,对这种白色粉末的成分作了如下猜想:
(1)、甲、乙的化学式为:甲 , 乙;(2)、写出反应②的化学方程式;(3)、写出反应①的化学方程式 , 该反应的基本类型是。28. 小刚在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末,小刚叫来小军和小红,共同探究这种白色粉末的成分。他们有依据所学的化学知识,对这种白色粉末的成分作了如下猜想:a.可能是NaOH
b.可能是 ▲
c.可能是NaOH与Na2CO3的混合物为了验证猜想,他们分别做了下面的实验。
(1)、猜想b。(2)、小刚取少量白色粉末,滴加稀盐酸,有气体生成,由此小刚认为白色粉末是Na2CO3 , 请判断小刚所得结论是否合理? , 理由是。(3)、小军取少量白色粉未溶于水,向所得溶液中滴加酚酞试液。溶液变成红色,由此小军认为白色粉末是NaOH,请判断小军所得结论是否合理?。理由是。(4)、小红取少量白色粉末溶于水,向所得溶液中滴加BaCl2溶液,有白色沉淀产生。由此判断白色粉末中含有。此反应的化学方程式为;小红继续向溶液中滴加BaCl2溶液至不再产生沉淀,过滤,然后向滤液中滴加酚酞试液。若滤液变红,说明猜想正确;若滤液不变色,说明猜想正确。四、计算题
-
29. 鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,取12.5g干燥的鸡蛋壳,捣碎,放在烧杯中,然后向其中滴加某浓度的稀盐酸,滴加过程中产生气体质量与所加稀盐酸质量的关系如图所示(鸡蛋壳中除CaCO3外的其他成分都不溶于水,也不与稀盐酸反应)。试计算:
 (1)、产生CO2的质量为 g;(2)、该鸡蛋壳中CaCO3的质量分数。
(1)、产生CO2的质量为 g;(2)、该鸡蛋壳中CaCO3的质量分数。