浙教版科学八下2.7元素符号表示的量同步练习
试卷更新日期:2022-01-24 类型:同步测试
一、单选题
-
1. 如图是测定相对原子质量的示意图,推断A原子的相对原子质量约为( )
 A、6 B、12 C、14 D、162. 2020年12月17日,嫦娥五号返回器携带月壤样品回到地球。月壤中蕴含He-3,它被认为是解决未来能源问题的重要物质之一。He-3原子核内有2个质子和1个中子。地球上的氦元素主要以He-4(信息如图所示)形式存在。下列说法不正确的是( )
A、6 B、12 C、14 D、162. 2020年12月17日,嫦娥五号返回器携带月壤样品回到地球。月壤中蕴含He-3,它被认为是解决未来能源问题的重要物质之一。He-3原子核内有2个质子和1个中子。地球上的氦元素主要以He-4(信息如图所示)形式存在。下列说法不正确的是( ) A、 He-3、He-4属于同种元素 B、 He-3、He-4互为同位素 C、 He-3和He-4的相对原子质量相同 D、 He-3原子和He-4原子的电子数相同3. 2020年2月4日,中国工程院院士李兰娟的研究团队发现:达芦那韦(化学式:C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列说法错误的是( )A、 达芦那韦由五种元素组成 B、达芦那韦由分子构成 C、一个达芦那韦分子由75个原子构成 D、达芦那韦中C,H两种元素的质量比为27:374. 化合物A和B均由元素X、Y组成,X元素化合价均为正价,在A中X的质量分数为40%,在B中X的质量分数为50%,已知A中X、Y原子个数比为1:3,则B的化学式为( )A、Y2X B、Y3X C、XY2 D、XY35. 石石是主要含KNO3的天然矿物,历史上《本草经集注》中对硝石有记载:“强烧之紫青烟起……云是真硝石也”。下列有关KNO3的叙述正确的是( )A、是一种混合物 B、由三种元素构成 C、可能发生化合反应 D、氮元素的质量分数约为13.9%6. 2019年诺贝尔化学奖用于表彰锂离子电池的研发。这种质量轻、可充电、功能强大的电池现在被广泛应用于手机、笔记本电脑和电动汽车等各种产品。碳酸二甲酯(C3H6O3)是锂电池电解液的一种成分,下列关于碳酸二甲酯说法错误的是( )A、由C,H,O三种元素组成 B、相对分子质量是90克 C、氧元素的质量分数最大 D、分子中C,H,O三种原子的个数比为1:2:17. 已知R元素的相对原子质量为64,在其氧化物中的质量分数为80%,则该氧化物中R元素的化合价为( )A、+1 B、+2 C、+3 D、+48. 连花清瘟胶囊具有清瘟解毒,宣肺泄热的功效。其成分中含有一种名为绿原酸的物质,下列有关绿原酸(C16H18O9)的说法正确的是( )A、绿原酸是由3种元素组成的化合物 B、绿原酸的相对分子质量是354g C、绿原酸中氢元素的质量分数最大 D、绿原酸由16个碳原子、18个氢原子和9个氧原子构成9. PLA是一种新型可降解塑料,以乳酸(C3H6O3)为主要原料聚合而成,下列有关乳酸的说法错误的是( )A、乳酸是由碳、氢、氧三种元素组成 B、乳酸中含有12个原子 C、乳酸的相对分子质量是90 D、乳酸中氧元素的质量分数最大10. 《我不是药神》是一部关于白血病和印度药的电影作品。药品“甲磺酸伊马替尼片”用于治疗慢性髓性白血病和恶性胃肠道间质肿瘤,原理是融合基因,使BCR-ABL蛋白得不到磷酸,不能活化,就发不出指令,细胞的增殖态势便会得到抑制。甲磺酸伊马替尼的化学式为C29H31N7O·CH4SO3 , 关于甲磺酸伊马替尼的说法正确的是( )A、甲磺酸伊马替尼是由八种元素组成的化合物 B、甲磺酸伊马替尼由77个原子构成 C、甲磺酸伊马替尼中碳、氢、氧元素的质量比为30∶35∶4 D、甲磺酸伊马替尼的相对分子质量是58911. 现有一种由FeSO4和Fe2(SO4)3组成的固体混合物,已知该混合物中硫元素的质量分数为23%,则该混合物中铁元素的质量分数为( )A、31% B、40% C、30% D、46%12. 瑞德西韦一度被认为是治疗新冠肺炎较为有效的药物,其主要成分的化学式是C27H35N6O8P,对此分析可得出的信息是( )A、相对分子质量为602g B、1个C27H35N6O8P分子中有35个氢原子 C、该分子由五种元素组成 D、该物质中氢元素的质量分数最大13. 2020年初出现了罕见的新型冠状病毒疫情,过氧乙酸(分子模型如图)能有效杀灭病毒。下列关于过氧乙酸的说法中正确的是( )
A、 He-3、He-4属于同种元素 B、 He-3、He-4互为同位素 C、 He-3和He-4的相对原子质量相同 D、 He-3原子和He-4原子的电子数相同3. 2020年2月4日,中国工程院院士李兰娟的研究团队发现:达芦那韦(化学式:C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列说法错误的是( )A、 达芦那韦由五种元素组成 B、达芦那韦由分子构成 C、一个达芦那韦分子由75个原子构成 D、达芦那韦中C,H两种元素的质量比为27:374. 化合物A和B均由元素X、Y组成,X元素化合价均为正价,在A中X的质量分数为40%,在B中X的质量分数为50%,已知A中X、Y原子个数比为1:3,则B的化学式为( )A、Y2X B、Y3X C、XY2 D、XY35. 石石是主要含KNO3的天然矿物,历史上《本草经集注》中对硝石有记载:“强烧之紫青烟起……云是真硝石也”。下列有关KNO3的叙述正确的是( )A、是一种混合物 B、由三种元素构成 C、可能发生化合反应 D、氮元素的质量分数约为13.9%6. 2019年诺贝尔化学奖用于表彰锂离子电池的研发。这种质量轻、可充电、功能强大的电池现在被广泛应用于手机、笔记本电脑和电动汽车等各种产品。碳酸二甲酯(C3H6O3)是锂电池电解液的一种成分,下列关于碳酸二甲酯说法错误的是( )A、由C,H,O三种元素组成 B、相对分子质量是90克 C、氧元素的质量分数最大 D、分子中C,H,O三种原子的个数比为1:2:17. 已知R元素的相对原子质量为64,在其氧化物中的质量分数为80%,则该氧化物中R元素的化合价为( )A、+1 B、+2 C、+3 D、+48. 连花清瘟胶囊具有清瘟解毒,宣肺泄热的功效。其成分中含有一种名为绿原酸的物质,下列有关绿原酸(C16H18O9)的说法正确的是( )A、绿原酸是由3种元素组成的化合物 B、绿原酸的相对分子质量是354g C、绿原酸中氢元素的质量分数最大 D、绿原酸由16个碳原子、18个氢原子和9个氧原子构成9. PLA是一种新型可降解塑料,以乳酸(C3H6O3)为主要原料聚合而成,下列有关乳酸的说法错误的是( )A、乳酸是由碳、氢、氧三种元素组成 B、乳酸中含有12个原子 C、乳酸的相对分子质量是90 D、乳酸中氧元素的质量分数最大10. 《我不是药神》是一部关于白血病和印度药的电影作品。药品“甲磺酸伊马替尼片”用于治疗慢性髓性白血病和恶性胃肠道间质肿瘤,原理是融合基因,使BCR-ABL蛋白得不到磷酸,不能活化,就发不出指令,细胞的增殖态势便会得到抑制。甲磺酸伊马替尼的化学式为C29H31N7O·CH4SO3 , 关于甲磺酸伊马替尼的说法正确的是( )A、甲磺酸伊马替尼是由八种元素组成的化合物 B、甲磺酸伊马替尼由77个原子构成 C、甲磺酸伊马替尼中碳、氢、氧元素的质量比为30∶35∶4 D、甲磺酸伊马替尼的相对分子质量是58911. 现有一种由FeSO4和Fe2(SO4)3组成的固体混合物,已知该混合物中硫元素的质量分数为23%,则该混合物中铁元素的质量分数为( )A、31% B、40% C、30% D、46%12. 瑞德西韦一度被认为是治疗新冠肺炎较为有效的药物,其主要成分的化学式是C27H35N6O8P,对此分析可得出的信息是( )A、相对分子质量为602g B、1个C27H35N6O8P分子中有35个氢原子 C、该分子由五种元素组成 D、该物质中氢元素的质量分数最大13. 2020年初出现了罕见的新型冠状病毒疫情,过氧乙酸(分子模型如图)能有效杀灭病毒。下列关于过氧乙酸的说法中正确的是( )
 A、 过氧乙酸的分子式为CH3COOH B、过氧乙酸是由碳、氢、氧三种原子构成 C、过氧乙酸的相对分子质量是76 D、过氧乙酸中碳元素的质量分数最大14. 2013年5月,国内外各大媒体曝光;山东潍坊霞山区生姜种植户,在种植内销的生姜时使用了一种叫“神农丹”的剧毒农药.“神农丹”所含物质的化学式为C7H14N2O2S,下列关于该物质的说法,不正确的是( )A、该物质由五种元素组成 B、该物质的一个分子中含碳、氢原子的个数比为1:2 C、该物质燃烧时可能会产生形成酸雨的物质 D、该物质中硫元素质量分数最小15. 由Na2SO4和CaSO4组成的混合物中,测知氧元素的质量分数为46%.若再计算混合物中的下列各项:①硫元素的质量分数 ②钠元素的质量分数 ③CaSO4的质量分数 ④Na2SO4和CaSO4的质量比 ⑤CaSO4的质量,以下判断正确的是( )A、都能确定 B、都不能确定 C、只有①能确定 D、只有⑤不能确定16. 地震过后,防疫部门常用到一种高效安全灭菌消毒剂,该消毒剂可表示为RO2 , 主要用于饮用水消毒。实验测得该氧化物中R与O的质量比为71:64,则RO2的化学式为( )A、CO2 B、NO2 C、SO2 D、ClO217. 同等条件下,新型生物冰袋的保温时间是普通冰袋保温时间的6倍,卫生无毒,广泛应用于疫苗、血液、低温食品等需要冷冻冷藏货物的保存与配送,其主要材料是羧甲基纤维素钠(又称CMC) ,分子式为C8H11O7Na。下列关于CMC的说法正确的是( )
A、 过氧乙酸的分子式为CH3COOH B、过氧乙酸是由碳、氢、氧三种原子构成 C、过氧乙酸的相对分子质量是76 D、过氧乙酸中碳元素的质量分数最大14. 2013年5月,国内外各大媒体曝光;山东潍坊霞山区生姜种植户,在种植内销的生姜时使用了一种叫“神农丹”的剧毒农药.“神农丹”所含物质的化学式为C7H14N2O2S,下列关于该物质的说法,不正确的是( )A、该物质由五种元素组成 B、该物质的一个分子中含碳、氢原子的个数比为1:2 C、该物质燃烧时可能会产生形成酸雨的物质 D、该物质中硫元素质量分数最小15. 由Na2SO4和CaSO4组成的混合物中,测知氧元素的质量分数为46%.若再计算混合物中的下列各项:①硫元素的质量分数 ②钠元素的质量分数 ③CaSO4的质量分数 ④Na2SO4和CaSO4的质量比 ⑤CaSO4的质量,以下判断正确的是( )A、都能确定 B、都不能确定 C、只有①能确定 D、只有⑤不能确定16. 地震过后,防疫部门常用到一种高效安全灭菌消毒剂,该消毒剂可表示为RO2 , 主要用于饮用水消毒。实验测得该氧化物中R与O的质量比为71:64,则RO2的化学式为( )A、CO2 B、NO2 C、SO2 D、ClO217. 同等条件下,新型生物冰袋的保温时间是普通冰袋保温时间的6倍,卫生无毒,广泛应用于疫苗、血液、低温食品等需要冷冻冷藏货物的保存与配送,其主要材料是羧甲基纤维素钠(又称CMC) ,分子式为C8H11O7Na。下列关于CMC的说法正确的是( ) A、该物质全部由非金属元素组成 B、该分子的相对分子质量是242克 C、碳、氢、氧和钠元素的个数比为8:11:7:1 D、该物质中氧元素的质量分数最大约46.3%18. 燃放烟花爆竹时,产生一种具有刺激性气味的气体,会造成大气污染。这种气体由两种元素组成且两种元素的质量分数相等,它是( )A、H2S B、SO2 C、NO2 D、CO19. 由碳、氧两种元素组成的气体中,碳与氧的质量比为3:5,则该气体可能是( )A、只由CO组成的纯净物 B、由CO和CO2共同组成的混合物 C、只由CO2组成的纯净物 D、由CO2和O2共同组成的混合物20. 已知FeSO4、Fe2(SO4)3混合物中铁元素的质量分数为a%,则硫元素的质量分数为( )A、1-a% B、 C、 D、无法计算
A、该物质全部由非金属元素组成 B、该分子的相对分子质量是242克 C、碳、氢、氧和钠元素的个数比为8:11:7:1 D、该物质中氧元素的质量分数最大约46.3%18. 燃放烟花爆竹时,产生一种具有刺激性气味的气体,会造成大气污染。这种气体由两种元素组成且两种元素的质量分数相等,它是( )A、H2S B、SO2 C、NO2 D、CO19. 由碳、氧两种元素组成的气体中,碳与氧的质量比为3:5,则该气体可能是( )A、只由CO组成的纯净物 B、由CO和CO2共同组成的混合物 C、只由CO2组成的纯净物 D、由CO2和O2共同组成的混合物20. 已知FeSO4、Fe2(SO4)3混合物中铁元素的质量分数为a%,则硫元素的质量分数为( )A、1-a% B、 C、 D、无法计算二、填空题
-
21. 每年5、6月是蓝莓丰收的时节,蓝莓中含有丰富的花青素,具有活化视网膜的作用,已知花青素的化学式为C15H11O6。请回答下列问题:
 (1)、花青素的相对分子质量为。(2)、57.4克花青素中含有氧元素质量克。22. 食物的煎炸过程中会产生一种有害物质——丙烯醛,化学式为 C2H3CHO,请计算:(1)、丙烯醛中的 C、H、O 元素的质量比是。(2)、112 克丙烯醛中碳元素的质量为克。23. “神州”“嫦娥”系列飞船,圆了中华民族的千年飞天梦。请从科学的视角对我国宇宙飞船的相关信息进行思考,并回答下列问题:人类探索太空的其中一个目的是开发新的核聚变能源,已知某种核原料的原子核含有1个质子和2个中子,则(填字母)。
(1)、花青素的相对分子质量为。(2)、57.4克花青素中含有氧元素质量克。22. 食物的煎炸过程中会产生一种有害物质——丙烯醛,化学式为 C2H3CHO,请计算:(1)、丙烯醛中的 C、H、O 元素的质量比是。(2)、112 克丙烯醛中碳元素的质量为克。23. “神州”“嫦娥”系列飞船,圆了中华民族的千年飞天梦。请从科学的视角对我国宇宙飞船的相关信息进行思考,并回答下列问题:人类探索太空的其中一个目的是开发新的核聚变能源,已知某种核原料的原子核含有1个质子和2个中子,则(填字母)。A.该原子是一种氢原子 B.该元素是金属元素
C.该原子核外有3个电子 D.该原子核带3个单位的正电荷
该核原料的相对原子质量为;若该原子形成的离子带一个单位的正电荷,请写出其离子符号:。
24. 如图为某牙膏的部分标签,活性成分单氟磷酸钠的化学式为Na2PO3F(相对分子质量为144),请回答下列问题。 (1)、人体中氟元素属于(填“微量”或“常量”)元素。(2)、Na2PO3F中金属元素与氧元素的质量比为。(3)、若牙膏中其他成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为g。(结果保留小数点后一位)25. 回答下列问题。(1)、下表是元素周期表的一部分,请回答有关问题:
(1)、人体中氟元素属于(填“微量”或“常量”)元素。(2)、Na2PO3F中金属元素与氧元素的质量比为。(3)、若牙膏中其他成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为g。(结果保留小数点后一位)25. 回答下列问题。(1)、下表是元素周期表的一部分,请回答有关问题: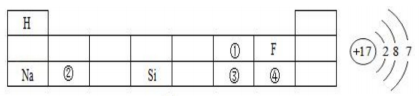
右图表示左表中(填表中序号)的原子结构示意图;得电子后形成的离子符号为;①处元素和②处元素形成常见化合物的化学式为;
(2)、X、Y两种元素的相对原子质量之比为7∶2,X与Y形成的化合物中,X、Y两种元素的质量之比为21∶8,则该化合物的化学式可表示为。若X、Y两种元素的相对原子质量之比为2∶1,由这两种元素形成的化合物中,X、Y的质量之比为2∶3,其中X的化合价为+a。则在该化合物中Y的化合价为。26. 在K2R2O7中(R代表某元素)含钾元素26.5%,氧元素38.1%,推算出R的相对原子质量是;甲、乙两种化合物都只含有X、Y两种元素.甲、乙两种化合物中X元素的质量分数分别为30.4%和25.9%.若已知甲的化学式为XY2 , 则乙的化学式为 。27.(1)、X、Y两种元素组成的化合物甲和乙,甲的化学式为X2Y3 , 其中Y元素的质量分数为50%,乙中X元素的质量分数为60%,则乙的化学式为;(2)、元素X的原子失去1个电子,元素Y的原子得到2个电子后,所形成的离子所带电子数均与氖原子相同,由X、Y两元素的离子形成的化合物的相对分子质量为;(3)、相同质量的H2O2和D2O(D即2H)中氢元素的质量比为。(4)、某样品可能由铁、氧化亚铁、氧化铁和四氧化三铁中的一种或几种组成,现测得该样品中铁元素与氧元素的质量比是21:8;若该样品由两种物质混合而成,则一定不含;若该样品由三种物质混合而成,则一定含有。28. 赤铁矿的主要成分为Fe2O3 , 可用于冶炼铁.某赤铁矿,其中Fe2O3的质量分数为64%,该赤铁矿中铁元素的质量分数是(保留到小数点后面一位)。若以杂质含量为42%的磁铁矿(主要成分四氧化三铁,杂质不含铁元素)为原料代替该赤铁矿炼铁,若要得到相同质量的铁,则磁铁矿与赤铁矿的质量比为。参考答案:44.8%;16:15
29. 甲烷是天然气的主要成分,可作为燃料使用。用 表示碳原子,
表示碳原子,  表示氢原子,甲烷分子可表示为
表示氢原子,甲烷分子可表示为  ,则甲烷的化学式为 , 每个甲烷分子由个原子构成。甲烷分子中碳原子与氢原子的个数比是;甲烷中碳元素的化合价为。
,则甲烷的化学式为 , 每个甲烷分子由个原子构成。甲烷分子中碳原子与氢原子的个数比是;甲烷中碳元素的化合价为。 三、实验探究题
-
30. 只含铜和氧两种元素的固体样品18g,测得铜元素的质量为16g。已知铜的氧化物有CuO和Cu2O。请通过分析或计算回答下列问题:(1)、该样品的组成情况有。(写出所有可能的组成);(2)、若固体样品由两种物质组成,则质量偏少的那种物质在样品中的质量分数为。(用分数表示)31. 常用塑化剂的学名“邻苯二甲酸二辛酯”,化学式为C24H38O4 , 它是一种无色透明的液体,有特殊气味,不溶于水,溶于大多数有机溶剂,有毒。常用作各种塑料制品的工业添加剂,不可食用。可是不法商人为了牟取暴利竟然其将添加到多种饮料、果冻、果酱和方便面等食品中。若长期食用含塑化剂的食品可能对生殖系统、免疫系统造成危害,大量摄入还可能致癌。
请分析上述信息,回答下列问题:
(1)、根据常用塑化剂的化学式计算:①相对分子质量;
②氧元素的质量分数为(计算结果精确到0.1%)。
(2)、下列做法,可以使我们远离塑化剂的是。①少喝各种饮料,日常饮水以白开水为主
②经常吃方便面、面包等速食食品以适应我们快节奏的生活
③尽量少用塑料制品直接接触热的、含油脂的食物
④呼吁政府完善食品安全监督检验机制,严惩不法黑心业者
(3)、写出该塑化剂的两条物理性质:、。32. 小林去超市买盐时发现超市供应的食盐除普通碘盐外,还有无碘竹盐、低钠盐和健康平衡盐等,售货员告诉他是为了满足不同人群的需要。现有两种品牌的食盐A和B,主要成分的含量见表:(注:两种食盐仅NaCl中含有钠元素;35.1g/100g表示每100g食盐中含钠元素质量为35.1g)食盐种类
食盐A
食盐B
主要成分的含量
(以钠元素质量计)35.1g/100g
(以NaCl质量计)93.0g/100g
(1)、加碘盐是通过加入KIO3的方法制成的,KIO3中碘元素的化合价为。(2)、NaCl中钠元素质量分数以39%计,请比较食盐A、B中NaCl含量高低,其中含量较高的是(填食盐种类)。33. 小林同学收集了一些微粒的资料,请你和他一起根据表格数据回答下列问题。微粒名称
质子数
中子数
电子数
带电性
A
14
14
14
不带电
B
26
30
24
带2个单位正电荷
C
14
14
16
D
14
16
14
不带电
(1)、表格中属于互为同位素的是。(2)、根据表格信息写出微粒C的符号。(3)、比较C与D两种微粒,其中质量较大的是。34. 阅读下列材料,并回答问题:美国科学家鲁宾和卡门利用同位素标记法对光合作用进行了探究。他们用氧18同位素分别标记水和二氧化碳中的氧元素,使它们分别成为含氧18的水(氧的相对原子量为18)和含氧18的二氧化碳。未标记的为原子量是16的氧原子,然后他们分两组进行实验,两组实验所用的植物、光照及其他条件都相同,实验结果如下表所示:
水
二氧化碳
生成的氧气
第一组
H2O
C18O2
O2
第二组
H218O
CO2
18O2
注:H218O---氧18水,C18O2---氧18二氧化碳,18O2---氧18氧气
(1)、该实验所探究的问题是:光合作用释放的中的元素究竟是来自水还是二氧化碳?(2)、该实验得出的结论是:。(3)、H218O这种水它的相对分子量是。四、解答题
-
35. 若冶炼200吨含杂质的质量分数为2%的生铁,需要含氧化铁的质量分数为80%的赤铁矿石多少吨?