浙教版科学八下2.5 表示元素的符号同步练习
试卷更新日期:2022-01-24 类型:同步测试
一、单选题
-
1. 铈是一种稀士元素,在元素周期表中铈元素的某些信息如图所示。下列有关铈的说法不正确的是( )
 A、元素符号为Ce B、属于金属元素 C、相对原子质量140.1g D、原子核内质子数为582. 2020年6月23日我国北斗导航组网最后一颗卫星成功发射,开启北斗导航的全新时代。北斗导航卫星系统采用铷原子钟,提供精确时间,如图是铷元素在元素周期表中的相关信息。下列说法中正确的是( )
A、元素符号为Ce B、属于金属元素 C、相对原子质量140.1g D、原子核内质子数为582. 2020年6月23日我国北斗导航组网最后一颗卫星成功发射,开启北斗导航的全新时代。北斗导航卫星系统采用铷原子钟,提供精确时间,如图是铷元素在元素周期表中的相关信息。下列说法中正确的是( ) A、 铷的中子数为37 B、铷的元素符号为Rb C、铷属于非金属元素 D、铷的相对原子质量为85.47g3. 科学家用锌原子加速轰击铋原子,合成出了第113号元素鉨,如图是鉨在元素周期表中的部分信息,下列有关说法不正确的是( )
A、 铷的中子数为37 B、铷的元素符号为Rb C、铷属于非金属元素 D、铷的相对原子质量为85.47g3. 科学家用锌原子加速轰击铋原子,合成出了第113号元素鉨,如图是鉨在元素周期表中的部分信息,下列有关说法不正确的是( ) A、鉨属于金属元素 B、Nh可表示鉨这种物质 C、每个鉨原子中有284个电子 D、鉨和铜的本质区别是质子数不同4. 下列符号能同时表示一种元素,又能表示一个原子,还能表示一种单质的是( )A、H B、Fe C、CO2 D、O25. 下列符号既可表示一个原子,又可表示一种元素,还能表示一种物质的是( )A、N B、Mg C、O2 D、H6. 下列元素名称与元素符号书写都正确的是( )A、锌Zn B、硅SI C、氯cl D、贡Hg7. 国际通用的元素符号是用1个或2个拉丁文字母表示的,其中第一个字母大写,第二个字母小写。镍元素的拉丁文名称为Niccolum,则镍的元素符号为( )A、Ni B、NI C、n D、Na8. 如图是元素周期表中的一格,从该图中获取的相关信息中错误的是( )
A、鉨属于金属元素 B、Nh可表示鉨这种物质 C、每个鉨原子中有284个电子 D、鉨和铜的本质区别是质子数不同4. 下列符号能同时表示一种元素,又能表示一个原子,还能表示一种单质的是( )A、H B、Fe C、CO2 D、O25. 下列符号既可表示一个原子,又可表示一种元素,还能表示一种物质的是( )A、N B、Mg C、O2 D、H6. 下列元素名称与元素符号书写都正确的是( )A、锌Zn B、硅SI C、氯cl D、贡Hg7. 国际通用的元素符号是用1个或2个拉丁文字母表示的,其中第一个字母大写,第二个字母小写。镍元素的拉丁文名称为Niccolum,则镍的元素符号为( )A、Ni B、NI C、n D、Na8. 如图是元素周期表中的一格,从该图中获取的相关信息中错误的是( ) A、该元素的名称是镁 B、该元素的原子核外电子数是12 C、该元素的原子序数是12 D、该元素的一个原子的实际质量是24.31g9. 如图是元素周期表的一部分。下列说法正确的是( )
A、该元素的名称是镁 B、该元素的原子核外电子数是12 C、该元素的原子序数是12 D、该元素的一个原子的实际质量是24.31g9. 如图是元素周期表的一部分。下列说法正确的是( ) A、硼为金属元素 B、碳的原子序数是12.01 C、铝是地壳中含量最高的元素 D、三种原子中质量最大的是铝10. 如图为元素周期表的一部分,A~E代表五种不同元素。下列说法不正确的是( )
A、硼为金属元素 B、碳的原子序数是12.01 C、铝是地壳中含量最高的元素 D、三种原子中质量最大的是铝10. 如图为元素周期表的一部分,A~E代表五种不同元素。下列说法不正确的是( ) A、原子序数:C>B B、核内质子数:A=E C、B,C同周期 D、A,D同族11. 法国里昂的科学家发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似。有关该粒子的说法不正确的是( )A、不显电性 B、相当于一个氦(He)原子的质量 C、失去一个中子后也不显电性 D、在周期表中与氢元素占同一位置12. 2019年诺贝尔化学奖授予给了三位科学家,以表彰他们在发明锂电池过程中做出的贡献。锂的元素符号是( )A、 La B、Li C、Al D、Be13. 如图是科学家最新发现的第四个磁性元素钌的相关信息,则钌原子的核外电子数为( )
A、原子序数:C>B B、核内质子数:A=E C、B,C同周期 D、A,D同族11. 法国里昂的科学家发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似。有关该粒子的说法不正确的是( )A、不显电性 B、相当于一个氦(He)原子的质量 C、失去一个中子后也不显电性 D、在周期表中与氢元素占同一位置12. 2019年诺贝尔化学奖授予给了三位科学家,以表彰他们在发明锂电池过程中做出的贡献。锂的元素符号是( )A、 La B、Li C、Al D、Be13. 如图是科学家最新发现的第四个磁性元素钌的相关信息,则钌原子的核外电子数为( ) A、44 B、57 C、101 D、14514. 元素周期表是学习和研究科学的重要工具.右表是元素周期表的一部分,A﹣F代表六种不同短周期元素。下列说法不正确的是( )
A、44 B、57 C、101 D、14514. 元素周期表是学习和研究科学的重要工具.右表是元素周期表的一部分,A﹣F代表六种不同短周期元素。下列说法不正确的是( ) A、A,B同周期 B、A,D同族 C、原子核中质子数D>B D、D,F化学性质相似15. 下图是门捷列夫1869年研究元素周期规律时的一页手稿照片,照片中的数据如右图。根据右图中的数据,你认为当时门捷列夫将元素依次排列的依据是( )
A、A,B同周期 B、A,D同族 C、原子核中质子数D>B D、D,F化学性质相似15. 下图是门捷列夫1869年研究元素周期规律时的一页手稿照片,照片中的数据如右图。根据右图中的数据,你认为当时门捷列夫将元素依次排列的依据是( )
 A、字母顺序 B、质子数由大到小 C、相对原子质量由大到小 D、化合价由大到小16. 如图为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是( )
A、字母顺序 B、质子数由大到小 C、相对原子质量由大到小 D、化合价由大到小16. 如图为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是( ) A、原子序数:Z<Y B、核外电子数:X=Y C、Y和Z处于同一周期 D、X和Y核外电子层数相同
A、原子序数:Z<Y B、核外电子数:X=Y C、Y和Z处于同一周期 D、X和Y核外电子层数相同二、填空题
-
17. 元素周期表是学习科学的重要工具。下表是元素周期表的一部分,请回答下列问题
 (1)、不同种元素之间最本质的区别是( )不同。A、相对原子质量 B、质子数 C、中子数(2)、第3号元素属于(填“金属”或“非金属”)元素。(3)、第8号元素和第13号元素组成化合物的化学式为 。18. 如表是元素周期表的一部分,请回答下列问题
(1)、不同种元素之间最本质的区别是( )不同。A、相对原子质量 B、质子数 C、中子数(2)、第3号元素属于(填“金属”或“非金属”)元素。(3)、第8号元素和第13号元素组成化合物的化学式为 。18. 如表是元素周期表的一部分,请回答下列问题 (1)、周期表中的①②③代表三种不同的元素,③是元素(填名称),属于非金属的是 , 属于同一周期的元素是(填序号)。(2)、氕、氘、氚都属于表中的氢元素,原因是其原子的相同,但不同。(3)、最近,科学家用大量高速钙原子轰击锫原子,形成了核电核数为117的元素的原子,该原子的核外电子数是 。19. 元素周期表是学习科学的重要工具。下表是元素周期表的一部分,请回答下列问题:
(1)、周期表中的①②③代表三种不同的元素,③是元素(填名称),属于非金属的是 , 属于同一周期的元素是(填序号)。(2)、氕、氘、氚都属于表中的氢元素,原因是其原子的相同,但不同。(3)、最近,科学家用大量高速钙原子轰击锫原子,形成了核电核数为117的元素的原子,该原子的核外电子数是 。19. 元素周期表是学习科学的重要工具。下表是元素周期表的一部分,请回答下列问题: (1)、第3号元素属于(填“金属”或“非金属”)元素,它在化学反应中容易(填“得到”或“失去”)电子;(2)、第13号元素和第17号元素组成化合物的化学式是;(3)、每一周期结尾的是稀有气体元素,它们的化学性质(填“活泼”或“稳定”);(4)、一个2H216O分子所含的中子数为(元素符号左上角的数字代表该原子中质子数和中子数之和)20. 元素周期律是学习和研究化学的重要工具。
(1)、第3号元素属于(填“金属”或“非金属”)元素,它在化学反应中容易(填“得到”或“失去”)电子;(2)、第13号元素和第17号元素组成化合物的化学式是;(3)、每一周期结尾的是稀有气体元素,它们的化学性质(填“活泼”或“稳定”);(4)、一个2H216O分子所含的中子数为(元素符号左上角的数字代表该原子中质子数和中子数之和)20. 元素周期律是学习和研究化学的重要工具。下表是元素周期表的部分信息:
1H
氢2He
氦3Li
锂4Be
铍5B
硼6C
碳7N
氮8O
氧9F
氟10Ne
氖11Na
钠12Mg
镁13A1
铝14Si
硅15P
磷16S
硫X 18Ar
氩19K
钾20Ca
钙认真分析信息,回答:
(1)、地壳中含量最多的元素是(填符号)。(2)、分析上表规律,可推知,表中X =(填序号);元素名称是 。(3)、写出与金属钠化学性质相似物质有:。(4)、写出一个由1、8号两种元素组成的化合物的名称。21. 根据所给的元素名称填写元素符号①镁 ②铝 ③锂 ④氧 ⑤钙
⑥氩 ⑦氟 ⑧碳 ⑨氯 ⑩磷
22. 核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列问题。(注圆圈表示原子核,圈内数字表示核内带电微粒数目,弧线上数字表示电子数) (1)、2017年5月9日,中国科学院等单位联合发布了115号元素的中文名为“镆”。此元素原子的核电荷数为 , 核外电子数为。(2)、在第三周期中,随着原子序数的递增,元素原子核外电子数目的变化规律是。(3)、利用上表中给出的元素,写出含有氢元素的常见单质、化合物的化学式各一个:单质;化合物。(4)、钠和氯元素构成的化合物是由构成的。23. 空气中含量最多的元素为 , 地壳中含量最多的元素为 , 地核中含量最多的元素为 , 太阳中含量最多的元素为 , 海水中含量最多的元素为;人体中含量最多的元素为。(均填元素符号)24. 如图是元素周期表的一部分,请回答相关问题:
(1)、2017年5月9日,中国科学院等单位联合发布了115号元素的中文名为“镆”。此元素原子的核电荷数为 , 核外电子数为。(2)、在第三周期中,随着原子序数的递增,元素原子核外电子数目的变化规律是。(3)、利用上表中给出的元素,写出含有氢元素的常见单质、化合物的化学式各一个:单质;化合物。(4)、钠和氯元素构成的化合物是由构成的。23. 空气中含量最多的元素为 , 地壳中含量最多的元素为 , 地核中含量最多的元素为 , 太阳中含量最多的元素为 , 海水中含量最多的元素为;人体中含量最多的元素为。(均填元素符号)24. 如图是元素周期表的一部分,请回答相关问题:第一周期
1H
2He
第二周期
3Li
4Be
5B
9F
10Ne
第三周期
11Na
12Mg
13Al
17Cl
18Ar
(1)、氟元素与氯元素位于同一纵行的原因是相同,它们在化学反应中都是容易(填“得到”或“失去”)电子。(2)、M2-与Ne核外电子数相同,则M元素名称为元素。25. 元素周期表是学习和研究科学的重要工具,下列是元素周期表的一部分。结合表中信息,回答下列问题。族
周期
ⅣA
VA
ⅥA
ⅦA
2
6碳
12.01
7氦
14.01
8氧
16.00
9氟
19.00
3
14硅
28.09
15磷
30.96
16硫
32.06
17氯
35.45
(1)、表中不同元素间最本质区别是不同。(2)、同一周期元素原子的核电荷数变化规律是 。26. 元素周期表是我们学习和研究科学的重要工具,请根据如图所示部分周期表回答问题。 (1)、每一周期结尾的是稀有气体元素,它们的化学性质(填“活泼”或“稳定”);(2)、根据周期表的元素排列规律,锂与钠、碳与硅的化学性质相似,则氟与化学性质相似。27. 化学元素组成万物。人们很早就意识到物质都是由几种亘古不变的基本成分——“元素"组成的。
(1)、每一周期结尾的是稀有气体元素,它们的化学性质(填“活泼”或“稳定”);(2)、根据周期表的元素排列规律,锂与钠、碳与硅的化学性质相似,则氟与化学性质相似。27. 化学元素组成万物。人们很早就意识到物质都是由几种亘古不变的基本成分——“元素"组成的。 (1)、古人曾认为水是组成物质的元素之一。在你学过的知识中能说明“水不是元素“的实验事实是。(2)、现代化学对“元素"做了科学定义,图甲是两个微粒的结构模型示意图,小科认为这两个微粒不属于同种元素,你认为他的依据是。(3)、1869年,俄国化学家门捷列夫在前人研究的基础上制作出第一张元素周期表,图乙是元素周期表的部分内容,表中空白格处元素原子的质子数为 。28. 2019年是“国际化学元素周期表年”,以纪念俄国化学家门捷列夫在1869年发明第一张元素周期表150周年。门捷列夫将当时已知的63种元素依据相对原子质量大小并以表的形式排列,将相似化学性质的元素放在同一列中,制成了元素周期表的雏形。(1)、钔的质子数为101,中子数为157,相对原子质量为258,则其核外电子数为。(2)、在1869年之前,许多化学家就对当时已知的元素进行排列。但国际上公认把发明元素周期律的桂冠戴在了门捷列夫的头上,你推测可能的原因是 。A、门捷列夫按照相对原子质量排列元素,这也是现在元素周期表元素排列的标准 B、门捷列夫以“相似化学性质的元素放同一列”原则修正一些元素的相对原子质量 C、门捷列夫发明的元素周期表完全是他的独创,并不需要吸收别人的研究成果 D、门捷列夫非常准确地预言了当时还没有发现的新元素,并最终获得证实 E、门捷列夫当时在科学界威望极高,他的发明成果更能让人信服
(1)、古人曾认为水是组成物质的元素之一。在你学过的知识中能说明“水不是元素“的实验事实是。(2)、现代化学对“元素"做了科学定义,图甲是两个微粒的结构模型示意图,小科认为这两个微粒不属于同种元素,你认为他的依据是。(3)、1869年,俄国化学家门捷列夫在前人研究的基础上制作出第一张元素周期表,图乙是元素周期表的部分内容,表中空白格处元素原子的质子数为 。28. 2019年是“国际化学元素周期表年”,以纪念俄国化学家门捷列夫在1869年发明第一张元素周期表150周年。门捷列夫将当时已知的63种元素依据相对原子质量大小并以表的形式排列,将相似化学性质的元素放在同一列中,制成了元素周期表的雏形。(1)、钔的质子数为101,中子数为157,相对原子质量为258,则其核外电子数为。(2)、在1869年之前,许多化学家就对当时已知的元素进行排列。但国际上公认把发明元素周期律的桂冠戴在了门捷列夫的头上,你推测可能的原因是 。A、门捷列夫按照相对原子质量排列元素,这也是现在元素周期表元素排列的标准 B、门捷列夫以“相似化学性质的元素放同一列”原则修正一些元素的相对原子质量 C、门捷列夫发明的元素周期表完全是他的独创,并不需要吸收别人的研究成果 D、门捷列夫非常准确地预言了当时还没有发现的新元素,并最终获得证实 E、门捷列夫当时在科学界威望极高,他的发明成果更能让人信服三、实验探究题
-
29. 如图是1~18号元素原子最外层电子数与原子核电荷数的关系图。试回答:
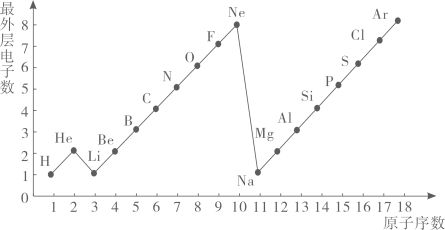 (1)、一个Mg2+核外共有个电子;Cl﹣的最外层电子数和原子的最外层电子数相同。(2)、通过对该图的分析,你能发现哪些规律?请写出其中一个:。
(1)、一个Mg2+核外共有个电子;Cl﹣的最外层电子数和原子的最外层电子数相同。(2)、通过对该图的分析,你能发现哪些规律?请写出其中一个:。四、解答题
-
30. 下图为元素周期表的一部分,请按要求填空:
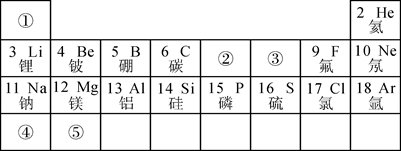 (1)、表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的相同。(2)、表中9号和17号元素最外层电子数相同,都易(填“得到”或“失去”)电子,则钠元素和氟元素组成的化合物的化学式为。(3)、请在表中①~⑤五种元素里选出三种元素组成一种常见的化合物,其化学式为。31. 元素周期律是学习和研究化学的重要工具。下表是元素周期表的部分信息:
(1)、表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的相同。(2)、表中9号和17号元素最外层电子数相同,都易(填“得到”或“失去”)电子,则钠元素和氟元素组成的化合物的化学式为。(3)、请在表中①~⑤五种元素里选出三种元素组成一种常见的化合物,其化学式为。31. 元素周期律是学习和研究化学的重要工具。下表是元素周期表的部分信息:1 H
氢

2 He
氦
3 Li
锂
4 Be
铍
……
5 B
硼
6 C
碳
7 N
氮
8 O
氧
10 Ne
氖
11 Na
钠
12 Mg
镁
13 Al
铝
X Si
硅
15 P
磷
16 S
硫
17 Cl
氯
18 Ar
氩
19 K
钾
20 Ca
……
认真分析信息,回答:
(1)、原子序数为6的碳元素的核外电子数为 ;(2)、分析上表规律,可推知,表中X =。(3)、同一族元素特征是相似。32. 1932年,美国化学大师Linus Pauling提出电负性(用希腊字母x表示)的概念,用来确定化合物中原子某种能力的相对大小。Linus Pauling假定F的电负性为4,井通过热化学方法建立了其它元素的电负性。LhlusPauhg建立的有关元素的电负性如下:H:2.1
Li:1.0
Be:1.5
B:2.0
C:2.5
N:3.0
O:3.5
F:4.0
Na:0.9
Mg:1.2
A1:1.5
Si:1.8
P:2.1
S:2.5
Cl:3.0
K:0.8
Ca:1. 0
Ga:1.6
Ge:1.8
As:2.0
Se:2.4
Br:2.8
Rb:0.8
Sr:1.0
In:1.7
Sn:1.8
Sb:1.9
Te:x
I:2.5
Cs:0.7
Ba:0.9
Tl:1.8
Pb:1.9
Bi:1.9
Po:2.0
At:2.2
Fr:0.7
Ra:0.9
回答下列问题:
(1)、写出元素电负性在上表中同一横行和同一纵行中的递变规律:.(2)、预测Te元素x的取值范围.(3)、观察上表可得出如下结论:一般情况下,金属元素的电负性越小,它的金属活动性就越(选填“强”或“弱”),该元素的原子 (选填“失电子”或“得电 子”)的能力越大。(4)、大量事实表明,当两种元素的x值相差大于或等于1.7时,形成的化合物一般是离子化合物。根据此经验规律,AlCl3物质(选填“是”或“不是”)离子化合物。
-