河北省秦皇岛市2021-2022学年九年级上学期期末模拟化学试题
试卷更新日期:2022-01-19 类型:期末考试
一、单选题
-
1. 下列变化都与CO2有关,其中与其他变化不同的是( )A、干冰用于人工降雨 B、植物光合作用 C、动植物呼吸 D、用CO2制汽水2. 关于化学“之最”的说法,错误的是( )A、地壳中含量最多的金属元素是铝 B、金刚石是天然存在最硬的物质 C、真金不怕火炼,说明金的熔点最高 D、常见金属中导电性最好的是银3. 下列关于水的叙述正确的是( )A、水体有一定的自净能力,因此工业污水可以直接排放 B、活性炭具有吸附性,能除去溶解在水中的所有杂质 C、氢气在空气中燃烧生成水,说明水是由氢、氧两种元素组成的 D、地球上水资源丰富,有71%面积被水覆盖,淡水资源也十分丰富,不用节约用水4. 对下列事实的微观解释错误的是( )A、化学反应前后质量守恒的原因是原子的种类、数目、质量在反应前后不改变 B、水银温度计的工作原理是分子之间有间隔,能随温度改变 C、一滴水有1.67×1021个水分子,说明水分子的体积和质量都很小 D、冰的密度比水的密度小,说明水有反常膨胀现象5. 下列关于燃烧和灭火的描述正确的是( )A、木材着火可用水浇灭,因为水能降低木材的着火点 B、图书、档案、精密仪表等失火应使用干粉灭火器,而不能使用泡沫灭火器 C、蜡烛用嘴一吹就会熄灭,是因为人呼出的气体中含有二氧化碳 D、一般可燃物燃烧要与氧气接触,并且温度达到可燃物的着火点6. 乙醇的化学式为C2H5OH,下列关于乙醇的说法,正确的是( )A、乙醇分子是由两个碳原子、六个氢原子、一个氧原子构成的 B、把乙醇按一定比例添加到汽油中得到的乙醇汽油是混合物 C、乙醇中碳、氢、氧三种元素的质量比是2:6:1 D、乙醇可以用粮食、薯类等发酵制取,是不可再生能源7. 甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列说法正确的是( )
 A、丁一定是化合物 B、该反应是置换反应 C、丙一定是该反应的催化剂 D、反应前后甲和乙变化的质量比为9:88. 如图所示是某化学反应的微观结构示意图,下列说法错误的是( )
A、丁一定是化合物 B、该反应是置换反应 C、丙一定是该反应的催化剂 D、反应前后甲和乙变化的质量比为9:88. 如图所示是某化学反应的微观结构示意图,下列说法错误的是( ) A、该反应的生成物是混合物 B、参加反应的一种物质的化学式为C2H4 C、参加反应的两种物质的分子个数比为1:1 D、生成物中碳、氢、氧原子个数比为2:6:19. 下列实验不能达到实验目的的是( )
A、该反应的生成物是混合物 B、参加反应的一种物质的化学式为C2H4 C、参加反应的两种物质的分子个数比为1:1 D、生成物中碳、氢、氧原子个数比为2:6:19. 下列实验不能达到实验目的的是( )实验
方法
A
鉴别水和双氧水
二氧化锰粉末
B
鉴别氧气和氮气
燃着的木条
C
除去二氧化碳中的一氧化碳
在空气中点燃
D
硬水和蒸馏水
滴加肥皂水,搅拌,观察产生泡沫的情况
A、A B、B C、C D、D10. 对比实验是实验探究的重要方法,下列对比实验设计能实现相应实验目的的是( )
 A、探究温度对分子运动的影响 B、探究可燃物燃烧条件 C、探究二氧化锰对过氧化氢分解的催化作用 D、探究空气与呼出气体中氧气含量不同11. 两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是( )
A、探究温度对分子运动的影响 B、探究可燃物燃烧条件 C、探究二氧化锰对过氧化氢分解的催化作用 D、探究空气与呼出气体中氧气含量不同11. 两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是( )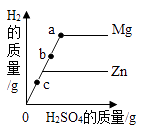 A、该图反映出镁比锌的金属活动性强 B、a点时,两个烧杯中的酸都恰好完全反应 C、b点时,两个烧杯中产生氢气的质量相等 D、c点时,两个烧杯中都有金属剩余12. 取一定量的Mg放入到Cu(NO3)2溶液中充分反应后过滤,得到固体和滤液,下列说法错误的是( )A、固体中只有铜时,滤液可能呈蓝色 B、固体中一定有铜,滤液中一定有Cu(NO3)2 C、固体中有Mg和Cu时,滤液一定呈无色 D、固体中只有铜时,滤液中可能没有Cu(NO3)213. 下列关于“10%的硝酸钾溶液”含义的说法中,错误的是( )A、100 g水中溶解了10 g硝酸钾 B、100 g硝酸钾溶液中有10 g硝酸钾 C、将10 g硝酸钾溶于90 g水中所得的溶液 D、将硝酸钾与水按1∶9的质量比配制的溶液14. 甲、乙两种固体(不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A、该图反映出镁比锌的金属活动性强 B、a点时,两个烧杯中的酸都恰好完全反应 C、b点时,两个烧杯中产生氢气的质量相等 D、c点时,两个烧杯中都有金属剩余12. 取一定量的Mg放入到Cu(NO3)2溶液中充分反应后过滤,得到固体和滤液,下列说法错误的是( )A、固体中只有铜时,滤液可能呈蓝色 B、固体中一定有铜,滤液中一定有Cu(NO3)2 C、固体中有Mg和Cu时,滤液一定呈无色 D、固体中只有铜时,滤液中可能没有Cu(NO3)213. 下列关于“10%的硝酸钾溶液”含义的说法中,错误的是( )A、100 g水中溶解了10 g硝酸钾 B、100 g硝酸钾溶液中有10 g硝酸钾 C、将10 g硝酸钾溶于90 g水中所得的溶液 D、将硝酸钾与水按1∶9的质量比配制的溶液14. 甲、乙两种固体(不含结晶水)的溶解度曲线如图所示。下列说法正确的是( ) A、乙中含有少量甲时,可用降温结晶法提纯乙 B、t2℃时的甲、乙饱和溶液分别降温到t1℃时,析出晶体的质量甲大于乙 C、t2℃时,将50g甲加入50g水中,可得到100g溶液 D、t1℃时,甲、乙饱和溶液溶质的质量分数相等
A、乙中含有少量甲时,可用降温结晶法提纯乙 B、t2℃时的甲、乙饱和溶液分别降温到t1℃时,析出晶体的质量甲大于乙 C、t2℃时,将50g甲加入50g水中,可得到100g溶液 D、t1℃时,甲、乙饱和溶液溶质的质量分数相等二、填空题
-
15. 化学与我们的生产、生活息息相关。(1)、衣:用洗洁精去除衣服上的油污是利用了洗洁精的作用。(2)、食:使用天然气烹煮食物时,发现火焰发红的原因可能是。(3)、住:利用活性炭的性除去新装修房间的异味。(4)、行:车用燃料汽油通常是将石油加热炼制得到的,石油属于(填“可再生”或“不可再生”)资源。(5)、用:焊接金属时常用氮气作保护气,因为其化学性质。16. 根据表中氯化钠和硝酸钾部分溶解度数据分析,回答下列问题。
温度/℃
0
10
20
30
40
50
60
溶解度/g
NaCl
35.7
35.8
36.0
36.3
36.6
37.0
37.3
KNO3
13.3
20.9
31.6
45.8
63.9
85.5
110
(1)、20℃时,氯化钠的溶解度是g。(2)、硝酸钾的溶解度随温度的升高而 , 与硝酸钾相比较,氯化钠的溶解度受温度变化影响(填“较大”或“较小”)。(3)、20℃时,在100g水中加入40g硝酸钾,充分搅拌后,将溶液温度升高到30℃(不考虑水分蒸发),所得溶液是(填“饱和溶液”或“不饱和溶液”)。(4)、海水晒盐利用的结晶方法是 , 氯化钠适用这一方法结晶是因为。17. 下面是某同学配制100g质量分数为15%的氯化钠溶液的主要过程。配制上述溶液的主要步骤有:计算、称量、量取、溶解。
(1)、计算:氯化钠固体的质量是g。(2)、本实验是定量实验,选择仪器不恰当或操作不规范都会导致实验结果有不正确。实验时选择量筒规格应为(填“50mL”或“100mL”)。在量取水时俯视量筒读数(其它操作均正确),所得溶液的质量分数15%(填“大于”、“等于”或“小于”),实验过程中玻璃棒的作用是。(3)、若用20%的NaCl溶液100g稀释成质量分数为10%的NaCl溶液,需加水mL。18. 某同学用如图装置,进行有关碳及其氧化物的实验(图中夹持已略去),在完成气密性检査后加入药品,并已在装置中充满二氧化碳。 (1)、填写表格中的空白内容:
(1)、填写表格中的空白内容:实验步骤
实验现象
实验分析
①缓缓通入CO2 , 点燃A处酒精喷灯,加热一段时间
木炭粉减少,D中有气泡产生,澄清石灰水且D装置中的液体进入到E装置。
硬质玻璃管中A处发生反应的化学方程式为:
②点燃B处酒精喷灯,加热一段时间
B处玻璃管内
以上实验说明具有还原性
③停止通入二氧化碳,熄灭A、B两处的火焰
C中有D中液体进入
C装置的作用是:
(2)、有同学认为该装罝需要添加尾气处理装置,你认为是否需要并说明理由:。(3)、写出D处集气瓶内发生反应的化学反应方程式。三、综合题
-
19. A~G是初中化学常见的物质。已知A为黑色固体单质,B为红棕色粉末,G为紫红色固体单质,它们的转化关系如图所示。回答下列问题:
 (1)、写出化学式:B。(2)、物质G的用途。(3)、反应III的基本反应类型是。(4)、反应II的化学方程式为。
(1)、写出化学式:B。(2)、物质G的用途。(3)、反应III的基本反应类型是。(4)、反应II的化学方程式为。四、计算题
-
20. 鸡蛋壳的主要成分是碳酸钙,为了测定某鸡蛋壳中碳酸钙的含量,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入足量的稀盐酸90g,充分反应后,称得烧杯中物质的总质量为97.8g。(假设鸡蛋壳中的其他物质不与盐酸反应)(1)、产生二氧化碳气体g。(2)、计算10g该鸡蛋壳中碳酸钙的质量分数,要求写出完整的解题步骤。
-