广东省广州市天河区2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-01-19 类型:期末考试
一、单选题
-
1. 广东有许多优秀的民间制作工艺,下列工艺制作过程涉及化学变化的是( )




A.雕刻精微玲珑的增城核雕
B.剪裁出精美生动的佛山剪纸
C.酿制香醇的梅州客家娘酒
D.缝制精美的潮州刺绣扇子
A、A B、B C、C D、D2. 硒是人体必需的微量元素,严重缺硒可能诱发皮肤病和癌症。如图为元素周期表中硒元素的信息及其原子结构示意图。下列说法错误的是( )
 A、硒的质子数为34 B、硒属于非金属元素 C、硒的相对原子质量为78.96 D、X=83. 在生产、生活和实验中经常用到水。如图甲为活性炭净水器示意图,如图乙是制取蒸馏水简易装置图,下列说法正确的是( )
A、硒的质子数为34 B、硒属于非金属元素 C、硒的相对原子质量为78.96 D、X=83. 在生产、生活和实验中经常用到水。如图甲为活性炭净水器示意图,如图乙是制取蒸馏水简易装置图,下列说法正确的是( )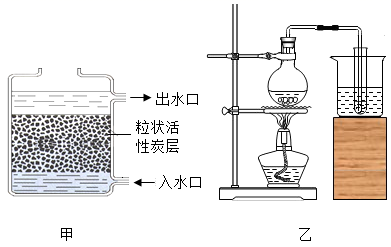 A、图甲中活性炭的作用是杀菌消毒 B、图甲中水流下进上出是为了提高水的净化效果 C、图乙中烧杯内水的作用是密封 D、图乙经过蒸馏后的水仍然是硬水4. 下列关于数字“2”的意义说法错误的是( )A、H2CO3表示含有氢分子 B、 表示1个硫酸根离子带2个单位的负电荷 C、2N表示2个氮原子 D、 表示氯化钙中钙元素的化合价为+25. 下列实验现象的描述正确的是( )A、红磷在空气中燃烧产生大量白色烟雾 B、硫在氧气中燃烧产生微弱的淡蓝色火焰 C、铁丝在氧气中剧烈燃烧,火星四射,产生黑色固体 D、木炭在氧气中剧烈燃烧,发出白光,生成二氧化碳气体6. 电解水实验如图,下列说法正确的是( )
A、图甲中活性炭的作用是杀菌消毒 B、图甲中水流下进上出是为了提高水的净化效果 C、图乙中烧杯内水的作用是密封 D、图乙经过蒸馏后的水仍然是硬水4. 下列关于数字“2”的意义说法错误的是( )A、H2CO3表示含有氢分子 B、 表示1个硫酸根离子带2个单位的负电荷 C、2N表示2个氮原子 D、 表示氯化钙中钙元素的化合价为+25. 下列实验现象的描述正确的是( )A、红磷在空气中燃烧产生大量白色烟雾 B、硫在氧气中燃烧产生微弱的淡蓝色火焰 C、铁丝在氧气中剧烈燃烧,火星四射,产生黑色固体 D、木炭在氧气中剧烈燃烧,发出白光,生成二氧化碳气体6. 电解水实验如图,下列说法正确的是( ) A、试管1连接的电源正极一端 B、试管2中得到的气体为O2 C、产生氢气与氧气的质量比为2:1 D、该实验可说明水由氢气和氧气组成7. 在预防新冠病毒过程中,人们常用过氧乙酸(C2H4O3)进行消毒。下列说法正确的是( )A、过氧乙酸由9个原子构成 B、过氧乙酸中C,H,O三种元素的质量比为2:4:3 C、过氧乙酸属于氧化物 D、过氧乙酸中碳元素的质量分数为8. 物质的性质决定其用途。下列物质的性质与用途对应关系错误的是( )A、干冰升华吸热,可用于人工降雨 B、一氧化碳具有氧化性,可用于冶炼金属 C、金刚石硬度大,可用于裁玻璃 D、氮气化学性质不活泼,可用作食品防腐的保护气9. 分类是一种重要的化学学习方法。下列物质分类完全正确的是( )A、CO、NO2、SO2——空气污染物 B、HgO、C60、K2MnO4——化合物 C、不锈钢、焊锡、金——合金 D、海水、稀有气体、氧化铝——混合物10. 科学认识燃烧,增强安全意识。下列说法错误的是( )A、在容易引起森林着火的地方设置隔离带,利用的原理是移除可燃物 B、搬运取用易燃、易爆物时要轻拿轻放,不能砸摔和撞击 C、酒精灯使用后需用灯帽盖灭,利用的原理是隔绝氧气 D、堆放杂物的纸箱着火用水浇灭,降低了可燃物的着火点11. 下列方案不能达到实验目的的是( )
A、试管1连接的电源正极一端 B、试管2中得到的气体为O2 C、产生氢气与氧气的质量比为2:1 D、该实验可说明水由氢气和氧气组成7. 在预防新冠病毒过程中,人们常用过氧乙酸(C2H4O3)进行消毒。下列说法正确的是( )A、过氧乙酸由9个原子构成 B、过氧乙酸中C,H,O三种元素的质量比为2:4:3 C、过氧乙酸属于氧化物 D、过氧乙酸中碳元素的质量分数为8. 物质的性质决定其用途。下列物质的性质与用途对应关系错误的是( )A、干冰升华吸热,可用于人工降雨 B、一氧化碳具有氧化性,可用于冶炼金属 C、金刚石硬度大,可用于裁玻璃 D、氮气化学性质不活泼,可用作食品防腐的保护气9. 分类是一种重要的化学学习方法。下列物质分类完全正确的是( )A、CO、NO2、SO2——空气污染物 B、HgO、C60、K2MnO4——化合物 C、不锈钢、焊锡、金——合金 D、海水、稀有气体、氧化铝——混合物10. 科学认识燃烧,增强安全意识。下列说法错误的是( )A、在容易引起森林着火的地方设置隔离带,利用的原理是移除可燃物 B、搬运取用易燃、易爆物时要轻拿轻放,不能砸摔和撞击 C、酒精灯使用后需用灯帽盖灭,利用的原理是隔绝氧气 D、堆放杂物的纸箱着火用水浇灭,降低了可燃物的着火点11. 下列方案不能达到实验目的的是( )



A.测定空气中氧气含量
B.探究铁钉生锈需要氧气
C.探究分子在不断运动
D.检查装置的气密性
A、A B、B C、C D、D12. 常见金属M与硝酸银溶液反应的化学方程式为 。有关该反应的说法错误的是( )A、该反应是置换反应 B、金属活动性M>Ag C、M可能是铝 D、M表面有固体析出13. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、分子可以构成物质,所以物质都由分子构成 B、燃烧过程中伴随着发光放热,所以有发光放热现象的变化都是燃烧 C、催化剂在化学反应前后质量不变,所以反应前后质量不变的物质都是催化剂 D、单质只含一种元素,所以只含一种元素的纯净物都是单质14. 除去下列物质中混有的杂质,选用的试剂和操作方法均正确的是( )选项
物质
杂质
选用的试剂和操作方法
A
CO2
CO
点燃
B
CaCO3
CaO
高温煅烧
C
N2
O2
通过灼热的铜粉
D
Fe2O3
C
隔绝空气加强热
A、A B、B C、C D、D二、填空题
-
15. “宏观辨识与微观探析”是化学学科的核心素养之一、甲烷燃烧时发生化学反应的微观示意图如下所示。
 (1)、写出该反应的化学方程式:。(2)、将图B的微观粒子示意图补充完整。(3)、甲烷中含有碳元素和氢元素,碳元素与氢元素的本质区别为。(4)、甲烷的实验室制取原理为 ,其中X的化学式为。(5)、天然气的主要成分为甲烷,液化天然气是天然气经压缩、冷却至1615℃后变成的液体。从微观角度解释此过程发生变化的是。
(1)、写出该反应的化学方程式:。(2)、将图B的微观粒子示意图补充完整。(3)、甲烷中含有碳元素和氢元素,碳元素与氢元素的本质区别为。(4)、甲烷的实验室制取原理为 ,其中X的化学式为。(5)、天然气的主要成分为甲烷,液化天然气是天然气经压缩、冷却至1615℃后变成的液体。从微观角度解释此过程发生变化的是。三、科普阅读题
-
16. 阅读下面的短文并回答问题。
为应对CO2等温室气体引起的气候变化问题,世界各国以全球协约的方式减排温室气体,我国提出争取2030年前达到碳达峰,2060年实现碳中和的目标。现阶段我国的能源结构以化石燃料为主,其燃烧释放出大量的CO2.通过植树造林、海洋封存、矿石碳化和綜合利用等途径可降低大气中CO2浓度。
矿石碳化:利用矿石中的氧化镁或氧化钙等,在一定条件下与CO2反应,生成碳酸镁或碳酸钙等,但过程缓慢。
综合利用:工业上可以将CO2转化成甲醇(CH3OH)等资源,CO2和氢气在一定条件下生成甲醇和一种常见的液体氧化物。一定条件下,该反应在有、无分子筛膜时甲醇的产率随温度的变化如图所示。
 (1)、化石燃料包括煤、、天然气。(2)、CO2可以封存在海洋里,但会引起海水酸化,体现出二氧化碳的性质是。(3)、写出利用CO2合成甲醇的化学方程式: , 参加反应的CO2与氢气的质量比为。(4)、由上图可知,为提高甲醇的产率,合成甲醇应选择的最佳条件为。(5)、下列说法正确的是___________(填字母)。A、碳达峰、碳中和中的“碳”指的是碳单质 B、大气中CO2过多会导致温室效应,也会造成酸雨 C、植树造林是利用植物的光合作用吸收CO2 , 光合作用属于物理变化 D、推广使用太阳能、风能等新能源代替化石燃料,可以减少CO2的排放 E、矿石碳化过程中,可能发生反应
(1)、化石燃料包括煤、、天然气。(2)、CO2可以封存在海洋里,但会引起海水酸化,体现出二氧化碳的性质是。(3)、写出利用CO2合成甲醇的化学方程式: , 参加反应的CO2与氢气的质量比为。(4)、由上图可知,为提高甲醇的产率,合成甲醇应选择的最佳条件为。(5)、下列说法正确的是___________(填字母)。A、碳达峰、碳中和中的“碳”指的是碳单质 B、大气中CO2过多会导致温室效应,也会造成酸雨 C、植树造林是利用植物的光合作用吸收CO2 , 光合作用属于物理变化 D、推广使用太阳能、风能等新能源代替化石燃料,可以减少CO2的排放 E、矿石碳化过程中,可能发生反应四、综合题
-
17. 金属的回收利用是保护金属资源的有效途径。某学校化学兴趣小组打算从混有金属镁、铁、铜的废弃粉末中分离、提取出化工原料MgSO4和有关金属,实验过程如下:
 (1)、金属A为(填化学式)。(2)、操作a的名称是;在该过程中需要使用玻璃棒,其作用是。(3)、写出步骤②所涉及的化学方程式: , 进行该操作时,需要通风并远离火源,其原因是。(4)、步骤②中除了加入稀硫酸外,还可选用另一种试剂是(填化学式)溶液。(5)、根据图中数据,计算理论上蒸发可得到MgSO4固体的质量为g(不考虑实验过程中的损耗)。18. 如图是实验室中常见的气体发生和收集装置。请回答下列问题:
(1)、金属A为(填化学式)。(2)、操作a的名称是;在该过程中需要使用玻璃棒,其作用是。(3)、写出步骤②所涉及的化学方程式: , 进行该操作时,需要通风并远离火源,其原因是。(4)、步骤②中除了加入稀硫酸外,还可选用另一种试剂是(填化学式)溶液。(5)、根据图中数据,计算理论上蒸发可得到MgSO4固体的质量为g(不考虑实验过程中的损耗)。18. 如图是实验室中常见的气体发生和收集装置。请回答下列问题: (1)、仪器b的名称是。(2)、实验室用氯酸钾制取并收集一瓶较纯净的氧气,反应的化学方程式为 , 应选用的装置组合是(从装置A-F中选,填字母)。若收集完成后,测得氧气纯度明显偏低,原因可能是(填编号)。
(1)、仪器b的名称是。(2)、实验室用氯酸钾制取并收集一瓶较纯净的氧气,反应的化学方程式为 , 应选用的装置组合是(从装置A-F中选,填字母)。若收集完成后,测得氧气纯度明显偏低,原因可能是(填编号)。①加热前没有进行预热
②收集前,集气瓶中未注满水
③未见气泡连续均匀地冒出时就开始收集
④收集后,集气瓶中仍有少量水
(3)、2021年10月30日,我国在国际上首次实现从一氧化碳到蛋白质的合成。实验室常用甲酸(HCOOH)溶液混合催化剂浓硫酸加热,分解获得一氧化碳和水,选用的发生装置为 , 若用F装置排水法收集CO,气体应从端通入。19. 某小组同学调查了市面上几种家用清洁剂的功能和有效成分,结果如下表。清洁剂
洁厕灵
彩漂液
漂白水
功能
清除污垢,除异味
漂洗衣物,使色彩鲜艳
漂除衣物污渍
有效成分
HCl
H2O2
NaClO
(1)、若不慎将“洁厕灵”滴到大理石地面上,出现的现象是。(2)、“洁厕灵”与“漂白水”不能混用。二者若混合其有效成分之间能发生化学反应,产生氯化钠、水和有毒的氯气(Cl2),化学方程式为。(3)、该小组同学在实验室对“彩漂液”有效成分H2O2的漂白性进行探究,将红色布条分别浸泡在4种溶液中,现象如下表。已知:10%表示H2O2溶液的浓度,该溶液中过氧化氢和水的质量比为10:90.
实验Ⅰ
实验Ⅱ
实验Ⅲ
实验Ⅳ




20分钟后布条无明显变化
20分钟后布条颜色稍变浅
20分钟后布条颜色明显变浅
1分钟后布条红色褪去
①通过以上4个实验发现影响H2O2溶液漂白性的因素除NaOH溶液外,还有。
②通过对比实验Ⅲ、Ⅳ,得出的结论是。
③欲进一步探究NaOH溶液的用量对H2O2溶液的漂白性的影响,可补充实验:将红色布条浸泡到℃25mL10%H2O2溶液+5滴NaOH溶液中,观察实验现象。
20. 某同学在博物馆看到一些铜制文物上有绿色的锈迹后,对绿色锈迹产生了探究兴趣。该同学查阅资料得知:Ⅰ、绿色锈迹是碱式碳酸铜(Cu2(OH)2CO3),受热易分解。
Ⅱ、无水硫酸铜为白色粉末,遇水变蓝。
Ⅲ、碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠和水。
Ⅳ、氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中。
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成。为了进一步确定碱式碳酸铜受热分解的产物,进行了如下猜想与探究:
(1)、该黑色固体可能是①碳粉;②氧化铜:③。请帮助该同学完成下述实验方案设计与记录。
实验操作
现象
实验结论
将少量黑色固体放入试管中,加入 , 充分振荡
猜想②正确
(2)、对于“加热碱式碳酸铜,试管壁上有无色液滴生成”的现象,该同学猜想无色液滴可能是水,根据反应前后元素守恒,猜想分解产物还有CO2 , 并选择如下图所示装置进行探究。
①实验步骤:
步骤一:连接A和B,打开活塞,通入一段时间的空气。
步骤二:关闭活塞,依次连接装置A→B→→(填“C”、“D”)。
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
②当观察到 , 可以得出碱式碳酸铜受热分解生成了H2O,根据装置C的实验现象可以得出碱式碳酸铜受热分解生成了CO2 , 请写出C中反应的化学方程。
③上述装置A中碱石灰的作用是。
-
-