甘肃省定西市2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-01-19 类型:期末考试
一、单选题
-
1. 下列变化属于化学变化的是( )A、胆矾研碎 B、红磷燃烧 C、品红在水中扩散 D、水的蒸发2. 空气中氮气约占空气体积的( )A、78% B、21% C、0.94% D、0.03%3. 下列图标属于节水图标的是( )A、
 B、
B、 C、
C、 D、
D、 4. 下列物质属于空气污染指数项目的是( )A、二氧化碳 B、稀有气体 C、氧气 D、一氧化碳5. 下列物质属于纯净物的是( )A、果汁 B、冰水混合物 C、酱油 D、天然气6. 下列粒子结构示意图中,表示阴离子的是( )A、
4. 下列物质属于空气污染指数项目的是( )A、二氧化碳 B、稀有气体 C、氧气 D、一氧化碳5. 下列物质属于纯净物的是( )A、果汁 B、冰水混合物 C、酱油 D、天然气6. 下列粒子结构示意图中,表示阴离子的是( )A、 B、
B、 C、
C、 D、
D、 7. 下列有关液体的实验操作正确的是( )A、量取4.5mL的液体
7. 下列有关液体的实验操作正确的是( )A、量取4.5mL的液体 B、加热液体
B、加热液体  C、滴加液体
C、滴加液体  D、取用液体
D、取用液体  8. 宏观与微观的结合是化学学科特有的思维方式。下列对宏观事实的微观解释错误的是( )A、十月桂花飘香——分子是不断运动的 B、氧气和液氧都能支持燃烧——同种分子的化学性质相同 C、液态水受热变成水蒸气,体积膨胀——升高温度,分子之间间隔变大 D、变瘪的乒乓球放入热水中能鼓起来——分子的个数增多9. 下列实验现象的描述正确的是( )A、二氧化碳通入紫色石蕊溶液中,溶液变红,再加热,溶液变为无色 B、红磷在空气中燃烧,产生大量的白烟 C、铁在空气中燃烧,火星四射,生成黑色固体 D、镁条在空气中燃烧产生耀眼的白光,生成白色固体氧化镁10. 水在化学实验中的作用不可忽视。下图实验中水的作用解释错误的是( )A、
8. 宏观与微观的结合是化学学科特有的思维方式。下列对宏观事实的微观解释错误的是( )A、十月桂花飘香——分子是不断运动的 B、氧气和液氧都能支持燃烧——同种分子的化学性质相同 C、液态水受热变成水蒸气,体积膨胀——升高温度,分子之间间隔变大 D、变瘪的乒乓球放入热水中能鼓起来——分子的个数增多9. 下列实验现象的描述正确的是( )A、二氧化碳通入紫色石蕊溶液中,溶液变红,再加热,溶液变为无色 B、红磷在空气中燃烧,产生大量的白烟 C、铁在空气中燃烧,火星四射,生成黑色固体 D、镁条在空气中燃烧产生耀眼的白光,生成白色固体氧化镁10. 水在化学实验中的作用不可忽视。下图实验中水的作用解释错误的是( )A、 实验Ⅰ中量筒中的水:只是防止红磷燃烧的产物污染空气
B、
实验Ⅰ中量筒中的水:只是防止红磷燃烧的产物污染空气
B、 实验Ⅱ中集气瓶中的水:防止集气瓶炸裂
C、
实验Ⅱ中集气瓶中的水:防止集气瓶炸裂
C、 实验Ⅲ中烧杯中的水:作为反应物
D、
实验Ⅲ中烧杯中的水:作为反应物
D、 实验Ⅳ中烧杯中的水:提供热量和隔绝氧气
实验Ⅳ中烧杯中的水:提供热量和隔绝氧气
二、填空题
-
11. 用化学用语填空。(1)、铁:。(2)、两个氧气分子:。(3)、氧化铜中铜元素的化合价为+2:。(4)、3个碳酸根离子:。12. 城市中的生活用水是经自来水厂净化处理过的,但仍不建议直接饮用。因为中间经过管道、水箱等多个环节,容易被微生物、细菌、重金属等污染,所以自来水一定要处理后才能饮用。(1)、我国生活饮用水卫生标准规定,饮用水(包括自来水)中含有铁、锰、铜、锌、钙等多种矿物质。这里的“铁、锰、铜、锌、钙等”是指(填“分子”、“原子”或“元素”)。(2)、自来水厂净水的主要流程如图:

①物质的性质决定物质的用途,上述过程中吸附池内起吸附作用的物质A的名称为。
②杀菌消毒时加入的液氯(Cl2)与水反应生成氯化氢和次氯酸(HClO),写出该反应的化学方程式:;HClO中氢元素和氧元素的质量比为。
(3)、要鉴别自来水是软水还是硬水,我们可向自来水样品中加入适量的进行搅拌。(4)、生活中,常采用的方法降低水的硬度。13. 随着经济的发展,能源和环境成为人们日益关注的问题。(1)、煤、、天然气是生活中经常使用的化石燃料,其中天然气是较清洁的燃料,天然气属于(填“可再生”或“不可再生”)能源。(2)、燃煤发电时将煤块粉碎,其目的是。(3)、将CO2转化为化工原料乙烯(C2H4)的微观过程如图所示:
①请写出上述反应的化学方程式:。
②依据微观反应的示意图可得到的信息:。
(4)、化石燃料的燃烧产生大量的二氧化碳会引起温室效应,为减缓大气中二氧化碳含量的增加,下列措施可行的是(填字母)。a.植树造林,开发和利用太阳能、水能、风能等新能源
b.禁止使用煤、石油、天然气等化石燃料
三、综合题
-
14. A~H都是初中化学中的常见物质,它们之间的转化关系如图所示。A是天然气的主要成分,E是一种常见的食品干燥剂,D和G的组成元素相同。请回答:
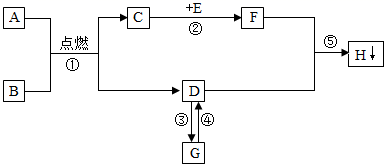 (1)、在反应②的过程中(填“放出”或“吸收”)热量。(2)、反应③(“一定”或“不一定”)属于化合反应。(3)、A物质的化学式为 , 在生活中常用作。(4)、写出反应⑤的化学方程式为;反应④是G与Fe2O3反应得到D,在反应中利用了G的性。15. 实验室制取气体的各种装置图如图所示。据图回答下列问题。
(1)、在反应②的过程中(填“放出”或“吸收”)热量。(2)、反应③(“一定”或“不一定”)属于化合反应。(3)、A物质的化学式为 , 在生活中常用作。(4)、写出反应⑤的化学方程式为;反应④是G与Fe2O3反应得到D,在反应中利用了G的性。15. 实验室制取气体的各种装置图如图所示。据图回答下列问题。 (1)、图中标号为a的仪器名称是。(2)、实验室利用氯酸钾和二氧化锰的混合物制取氧气,应选用的发生装置是(填字母);用装置D收集氧气时,验满的方法是。(3)、实验室制取二氧化碳的化学方程式是;发生装置选取C而不用B的原因可能是。(4)、实验室常用浓氨水和氢氧化钠固体在常温下制取氨气,氨气的密度小于空气的密度,且氨气易溶于水。制取氨气的发生装置可以选择图中的 , 收集装置可选择图中。某同学用图中G装置收集氨气,应该从(填“m”或“n”)端通入。16. 化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣。(1)、(提出问题)甲烷燃烧后生成哪些物质?
(1)、图中标号为a的仪器名称是。(2)、实验室利用氯酸钾和二氧化锰的混合物制取氧气,应选用的发生装置是(填字母);用装置D收集氧气时,验满的方法是。(3)、实验室制取二氧化碳的化学方程式是;发生装置选取C而不用B的原因可能是。(4)、实验室常用浓氨水和氢氧化钠固体在常温下制取氨气,氨气的密度小于空气的密度,且氨气易溶于水。制取氨气的发生装置可以选择图中的 , 收集装置可选择图中。某同学用图中G装置收集氨气,应该从(填“m”或“n”)端通入。16. 化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣。(1)、(提出问题)甲烷燃烧后生成哪些物质?(查阅资料)含碳元素的物质完全燃烧生成CO2 , 不完全燃烧生成CO;无水CuSO4遇水变蓝。
(猜想与假设)甲:CO2、H2O;乙:CO、H2O;丙:NH3、CO2、H2O;丁:CO2、CO、H2O。
你认为同学的猜想是错误的,理由是。
(2)、(实验探究)为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过如图所示装置:
A、B装置的顺序能否颠倒? (填“能”或“否”)。
(3)、实验中用纯净O2而不用空气的原因是。(4)、实验中观察到A中 , B、D中澄清石灰水变浑浊,C中黑色粉末变成红色,由此推断丁同学猜想成立(5)、请写出C中黑色粉末变成红色的化学方程式:。(6)、(反思与交流)为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是。
四、计算题
-
17. 已知碳酸钙在高温下可分解生成氧化钙和二氧化碳,反应的化学方程式为 ,同学们从山上采集到一种石灰石(主要成分为碳酸钙),他们取50g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量与反应时间的关系如下表:
反应时间/s
t0
t1
t2
t3
t4
t5
反应后固体的质量/g
50
46
41
36.2
34.6
34.6
请回答下列问题:
(1)、当石灰石完全反应后,生成CO2的质量为g。(2)、碳酸钙中钙元素的质量分数为。(3)、求该石灰石中含CaCO3的质量分数。(写出计算过程)