湖南省邵阳市绥宁县2021-2022学年九年级上学期第二次月考化学试题
试卷更新日期:2022-01-07 类型:月考试卷
一、单选题
-
1. 下列成语中不涉及化学变化的是( )A、星火燎原 B、披荆斩棘 C、死灰复燃 D、百炼成钢2. 正确规范的操作是实验成功和人身安全的重要保证。下列实验操作正确的是( )A、量取液体
 B、点燃酒精灯
B、点燃酒精灯 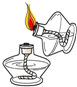 C、加热液体
C、加热液体 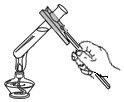 D、倾倒液体
D、倾倒液体 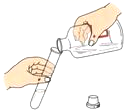 3. “化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xi)”,如今把这种“矽”元素命名为 ( )A、硒 B、硅 C、铝 D、锡4. “改善环境质量,推动绿色发展”是当前环保工作的重点。下列做法不符合这一要求的是( )A、建立污水处理厂,处理城市生活污水 B、提倡公交出行,减少城市雾霾 C、燃放烟花爆竹,增加节日气氛 D、拆除水上娱乐设施,恢复湿地生态5. 有关空气的叙述中,正确的是( )A、空气中的氧气具有可燃性,可用作火箭燃料 B、化工厂废气及汽车尾气,不会造成空气污染 C、稀有气体有广泛的用途,可制成多种用途的电光源 D、空气中的氮气与氧气体积比约为5:16. 下列不属于空气质量指数(简称AQI)中污染物监测范畴的是( )A、CO B、CO2 C、SO2 D、PM2.57. 下列有关水的说法错误的是( )A、日常生活中的饮用水是硬水还是软水,可用肥皂水鉴别 B、生活污水、工业污水等污水经处理达标后才可排放 C、沉淀、过滤、吸附、蒸馏等净化水的方式中,其中蒸馏的净化程度最高 D、自来水是干净、卫生的纯净物8. 下列物质按照混合物、氧化物、单质顺序排列的是( )A、空气、二氧化锰、氧气 B、海水、氯酸钾、氢气 C、氧化铁、锰酸钾、水 D、硫酸铜、高锰酸钾、二氧化碳9. 亚硝酸钠是一种工业用盐它有毒、有咸味,外形与食盐相似。人若误食会引起中毒,危害人体健康。亚硝酸钠(NaNO2)中氮元素的化合价是( )A、+2 B、+3 C、+4 D、+510. 下列化学反应方程式书写正确的是( )A、 B、 C、 D、11. 科研人员制备了一种纳米催化剂,二氧化碳和水在其表面发生反应的微观示意图如图,下列说法正确的是( )
3. “化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xi)”,如今把这种“矽”元素命名为 ( )A、硒 B、硅 C、铝 D、锡4. “改善环境质量,推动绿色发展”是当前环保工作的重点。下列做法不符合这一要求的是( )A、建立污水处理厂,处理城市生活污水 B、提倡公交出行,减少城市雾霾 C、燃放烟花爆竹,增加节日气氛 D、拆除水上娱乐设施,恢复湿地生态5. 有关空气的叙述中,正确的是( )A、空气中的氧气具有可燃性,可用作火箭燃料 B、化工厂废气及汽车尾气,不会造成空气污染 C、稀有气体有广泛的用途,可制成多种用途的电光源 D、空气中的氮气与氧气体积比约为5:16. 下列不属于空气质量指数(简称AQI)中污染物监测范畴的是( )A、CO B、CO2 C、SO2 D、PM2.57. 下列有关水的说法错误的是( )A、日常生活中的饮用水是硬水还是软水,可用肥皂水鉴别 B、生活污水、工业污水等污水经处理达标后才可排放 C、沉淀、过滤、吸附、蒸馏等净化水的方式中,其中蒸馏的净化程度最高 D、自来水是干净、卫生的纯净物8. 下列物质按照混合物、氧化物、单质顺序排列的是( )A、空气、二氧化锰、氧气 B、海水、氯酸钾、氢气 C、氧化铁、锰酸钾、水 D、硫酸铜、高锰酸钾、二氧化碳9. 亚硝酸钠是一种工业用盐它有毒、有咸味,外形与食盐相似。人若误食会引起中毒,危害人体健康。亚硝酸钠(NaNO2)中氮元素的化合价是( )A、+2 B、+3 C、+4 D、+510. 下列化学反应方程式书写正确的是( )A、 B、 C、 D、11. 科研人员制备了一种纳米催化剂,二氧化碳和水在其表面发生反应的微观示意图如图,下列说法正确的是( )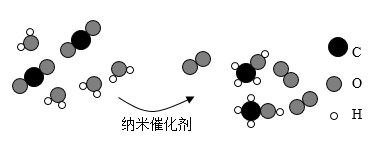 A、两种反应物的分子个数比为1:1 B、生成物
A、两种反应物的分子个数比为1:1 B、生成物 的化学式是CH4O
C、催化剂的化学性质在反应前后发生变化
D、原子的种类和数目在反应前后都发生变化
12. 建立宏观和微观之间的联系是化学学科特有的思维方式。下列关于宏观事实的微观解释错误的是( )A、氢气球在高空膨胀——分子体积变大 B、品红在静置的水中会扩散——分子在不停地运动 C、水和过氧化氢性质不同——不同分子的性质不同 D、水蒸发由液态变成气态——分子间的间隔变大13. 对下列化学用语中“2”的说法正确的是:( )
的化学式是CH4O
C、催化剂的化学性质在反应前后发生变化
D、原子的种类和数目在反应前后都发生变化
12. 建立宏观和微观之间的联系是化学学科特有的思维方式。下列关于宏观事实的微观解释错误的是( )A、氢气球在高空膨胀——分子体积变大 B、品红在静置的水中会扩散——分子在不停地运动 C、水和过氧化氢性质不同——不同分子的性质不同 D、水蒸发由液态变成气态——分子间的间隔变大13. 对下列化学用语中“2”的说法正确的是:( )①2O3;②2N;③N2;④
A、表示分子中原子个数的是③ B、表示离子所带电荷数的是④ C、表示原子个数的是① D、表示分子个数的是②14. 2021年3月,三星堆遗址出士了黄金面具残片,结合如图,下列说法正确的是( )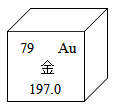 A、金的元素符号是AU B、金原子的质子数是79 C、金原子的核外电子数是118 D、金的相对原子质量是197.0g15. 维生素C(C6H8O6)主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。下列关于维生素C的说法中错误的是( )A、维生素C由碳、氢、氧三种元素组成 B、维生素C中氢元素的质量分数约是4.5% C、维生素C中含氢分子和氧分子的个数比是4:3 D、维生素C中C,H,O三种元素的质量比是9:1:1216. 在测定锌、铟等元素的相对原子质量方面做出卓越献的中国科学家是( )A、杨振宁 B、屠呦呦 C、侯德榜 D、张青莲17. 下列鉴别物质所用的方法或试剂中,错误的是( )A、水和白醋——闻气味 B、氧气和氮气——带火星的木条 C、氯酸钾和氯化钾——观察颜色 D、一氧化碳和二氧化碳——灼热的氧化铜18. 化学知识中有许多的“一定”和“不一定”,下列有关说法正确的是( )A、原子的最外层电子数相等,则元素化学性质一定相似 B、同种元素组成的物质一定是单质 C、10g甲和15g乙两物质恰好完全反应,生成物的总质量不一定为25g D、化合反应不一定是氧化反应19. 如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球。下列能准确描述实验现象的是( )
A、金的元素符号是AU B、金原子的质子数是79 C、金原子的核外电子数是118 D、金的相对原子质量是197.0g15. 维生素C(C6H8O6)主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。下列关于维生素C的说法中错误的是( )A、维生素C由碳、氢、氧三种元素组成 B、维生素C中氢元素的质量分数约是4.5% C、维生素C中含氢分子和氧分子的个数比是4:3 D、维生素C中C,H,O三种元素的质量比是9:1:1216. 在测定锌、铟等元素的相对原子质量方面做出卓越献的中国科学家是( )A、杨振宁 B、屠呦呦 C、侯德榜 D、张青莲17. 下列鉴别物质所用的方法或试剂中,错误的是( )A、水和白醋——闻气味 B、氧气和氮气——带火星的木条 C、氯酸钾和氯化钾——观察颜色 D、一氧化碳和二氧化碳——灼热的氧化铜18. 化学知识中有许多的“一定”和“不一定”,下列有关说法正确的是( )A、原子的最外层电子数相等,则元素化学性质一定相似 B、同种元素组成的物质一定是单质 C、10g甲和15g乙两物质恰好完全反应,生成物的总质量不一定为25g D、化合反应不一定是氧化反应19. 如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球。下列能准确描述实验现象的是( )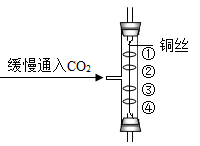 A、④比①先红,②、③不变红 B、①比④先红,②、③不变红 C、④变红,①②③不变红 D、①变红,②③④不变红20. 化学是以实验为基础的学科,下列有关实验现象的描述正确的是( )A、电解水实验中正极与负极产生的气体体积之比为8:1 B、硫在氧气中燃烧,发出明亮的蓝紫色火焰,生成无色无味的气体 C、铁丝伸入氧气中,剧烈燃烧,火星四射,生成黑色固体 D、二氧化碳通入紫色石蕊溶液,溶液变红21. 下列有关碳和碳的化合物说法中,错误的是( )A、金刚石、石墨物理性质有很大差异的原因是碳原子排列方式不同 B、CO2不能燃烧也不支持燃烧可用于灭火 C、碳在氧气中燃烧一定生成二氧化碳 D、自然界消耗CO2的主要途径是植物的光合作用22. 下列用化学方程式表示的除杂(括号内为杂质)方法正确的是( )A、CO(C): B、CO2(CO): C、N2(O2): D、KCl(KClO3):23. 将一定量的丙醇(C3H8O)和氧气置于一个密封的容器中引燃,测得反应前后各物质的质量如表。下列说法错误的是( )
A、④比①先红,②、③不变红 B、①比④先红,②、③不变红 C、④变红,①②③不变红 D、①变红,②③④不变红20. 化学是以实验为基础的学科,下列有关实验现象的描述正确的是( )A、电解水实验中正极与负极产生的气体体积之比为8:1 B、硫在氧气中燃烧,发出明亮的蓝紫色火焰,生成无色无味的气体 C、铁丝伸入氧气中,剧烈燃烧,火星四射,生成黑色固体 D、二氧化碳通入紫色石蕊溶液,溶液变红21. 下列有关碳和碳的化合物说法中,错误的是( )A、金刚石、石墨物理性质有很大差异的原因是碳原子排列方式不同 B、CO2不能燃烧也不支持燃烧可用于灭火 C、碳在氧气中燃烧一定生成二氧化碳 D、自然界消耗CO2的主要途径是植物的光合作用22. 下列用化学方程式表示的除杂(括号内为杂质)方法正确的是( )A、CO(C): B、CO2(CO): C、N2(O2): D、KCl(KClO3):23. 将一定量的丙醇(C3H8O)和氧气置于一个密封的容器中引燃,测得反应前后各物质的质量如表。下列说法错误的是( )物质
丙醇
氧气
水
二氧化碳
X
反应前质量/g
6.0
14.8
0
0.4
0
反应后质量/g
0
2
7.2
9.2
a
A、表中a的值为2.8 B、参加反应的氧气和生成二氧化碳的质量比为16:11 C、X中一定含碳元素、氧元素 D、该反应属于分解反应24. 工业上用氮气合成氨气(NH3),用氨气生产硝酸,相关反应如下:① ②
③ ④
下列说法错误的是( )
A、反应①③属于化合反应 B、反应②中X的化学式为N2 C、反应④中氮元素的化合价既有升高又有降低 D、NO和NO2可以相互转化25. 已知FeSO4、Fe2(SO4)3混合物中铁元素的质量分数为a%,则硫元素的质量分数为( )A、1﹣a% B、 C、 D、无法计算二、填空题
-
26. 请用化学用语填空。(1)、人体中含量最多的物质;(2)、3个锌原子;(3)、氢氧根离子;(4)、标出氧化亚铁中铁元素的化合价。27. 现有下列物质:①金刚石②蔗糖③石墨④干冰,请选择合适物质的序号填空。(1)、铅笔芯的主要成分;(2)、可用作玻璃刀的是;(3)、常用作甜味剂的是;(4)、可用于人工降雨的是。28. 如图为某化学反应的微观示意图。请回答:
 (1)、右方框图中的物质属于(填“纯净物”或“混合物”)。(2)、此反应的化学方程式为 , 基本反应类型为。29. 观察下列粒子结构示意图和元素周期表(部分)。
(1)、右方框图中的物质属于(填“纯净物”或“混合物”)。(2)、此反应的化学方程式为 , 基本反应类型为。29. 观察下列粒子结构示意图和元素周期表(部分)。 (1)、图甲中,具有相对稳定结构的原子是(填元素符号)。(2)、图甲中,属于金属阳离子的是(填离子符号)。(3)、图乙中,X的值为。(4)、C和D两种元素形成化合物的化学式是。
(1)、图甲中,具有相对稳定结构的原子是(填元素符号)。(2)、图甲中,属于金属阳离子的是(填离子符号)。(3)、图乙中,X的值为。(4)、C和D两种元素形成化合物的化学式是。三、综合题
-
30. A-F分别是氢气、氧气、碳、一氧化碳、二氧化碳、氧化铜等六种物质中的一种,它们之间的相互关系如图所示实线相连的两种物质可以相互反应,虚线相连的两种物质不能相互反应),其中B是一种黑色固体。请回答下列问题:
 (1)、若A是最清洁的能源,则A的化学式为。(2)、写出F的一种用途。(3)、C和D反应的化学方程式为。31. 请根据下列各图中有关信息,回答下列问题:
(1)、若A是最清洁的能源,则A的化学式为。(2)、写出F的一种用途。(3)、C和D反应的化学方程式为。31. 请根据下列各图中有关信息,回答下列问题: (1)、仪器b的名称。(2)、若用装置A制取氧气,要收集到较纯净的氧气,其收集装置应选;待收集完毕后先 , 再。某同学用收集好的氧气做铁丝燃烧实验时发现集气瓶炸裂,原因可能是。(3)、实验制取CO2的化学方程式为 , C装置的突出优点是;若用G装置收集CO2气体,气体应从端(填“c”或“d”)进入。32. 下图为碳还原氧化铜的实验装置图。老师指出反应物不同的质量比可能会影响生成物的种类,在学习时,可以从定性观察和定量分析两个角度来判断生成物。请你跟随老师的思路,探究碳还原氧化铜生成的气体。(所有反应均充分进行)
(1)、仪器b的名称。(2)、若用装置A制取氧气,要收集到较纯净的氧气,其收集装置应选;待收集完毕后先 , 再。某同学用收集好的氧气做铁丝燃烧实验时发现集气瓶炸裂,原因可能是。(3)、实验制取CO2的化学方程式为 , C装置的突出优点是;若用G装置收集CO2气体,气体应从端(填“c”或“d”)进入。32. 下图为碳还原氧化铜的实验装置图。老师指出反应物不同的质量比可能会影响生成物的种类,在学习时,可以从定性观察和定量分析两个角度来判断生成物。请你跟随老师的思路,探究碳还原氧化铜生成的气体。(所有反应均充分进行)(提出问题)碳还原氧化铜生成的气体是什么?
(作出猜想)猜想①:CO猜想②:CO2 猜想③:CO2和CO
(实验设计)装置图如下:
 (1)、方案一:从定性观察角度判断:
(1)、方案一:从定性观察角度判断:实验时,A中出现的现象。
(2)、若猜想①成立,B、D处会出现的现象是(填序号)。a.B中变浑浊,D处能点燃
b.B中变浑浊,D处不能点燃
c.B中无明显实验现象,D处能点燃
d.B中无明显实验现象,D处不能点燃
(3)、方案二:从定量计算角度判断:测定表格中的四个数据:
反应前的质量
反应后的质量
A(试管+固体)
m1
m2
B+C(广口瓶+溶液)
m3
m4
若猜想②成立,则m4-m3m1-m2(选填“>”、“<”或“=”),此时A中发生反应的化学方程式为。
(4)、若猜想③成立,且8gCuO全部参与反应,则生成的气体混合物的质量取值范围是。四、计算题
-
33. 胆矾(CuCO4·5H2O,相对分子质量为250)广泛应用于生产生活中。(将25.0g胆矾放在坩埚内加热,固体质量与成分随温度变化的曲线如图。)
 (1)、加热至℃时,CuSO4开始分解。(2)、加热至1000℃时,CuO开始分解,生成Cu2O与一种能使带火星的木条复燃的气体,该气体为。CuO完全分解时产生该气体的质量为g。(3)、根据胆矾分解的化学方程式 ,计算“上图”中x的值(写出计算过程)。(4)、下列物质均可作为炼铜的原料。理论上,冶炼等质量的下列物质得到铜最多的是_______(填字母序号)。A、CuSO4·5H2O B、CuSO4 C、CuO D、Cu2O
(1)、加热至℃时,CuSO4开始分解。(2)、加热至1000℃时,CuO开始分解,生成Cu2O与一种能使带火星的木条复燃的气体,该气体为。CuO完全分解时产生该气体的质量为g。(3)、根据胆矾分解的化学方程式 ,计算“上图”中x的值(写出计算过程)。(4)、下列物质均可作为炼铜的原料。理论上,冶炼等质量的下列物质得到铜最多的是_______(填字母序号)。A、CuSO4·5H2O B、CuSO4 C、CuO D、Cu2O