人教(新课标)高中化学一轮复习:专题4氧化还原反应
试卷更新日期:2022-01-05 类型:一轮复习
一、单选题
-
1. 日本大地震引发的福岛第一核电站核泄漏事故,造成放射性物质和向外界泄漏。下列相关说法正确的是( )A、每个原子中有82个质子 B、CsOH的碱性比NaOH弱 C、KIO3是碘的最高价氧化物的水化物的盐 D、I¯比F¯还原性强2. 为阿伏加德罗常数的值。下列有关叙述正确的是( )A、的硫酸溶液中含的数目为 B、含有的质子数和中子数均为 C、通入适量水中,转移的电子数为 D、标准状况下,含有的共价键数为3. 一种提纯白磷样品(含惰性杂质)的工艺流程如图所示。下列说法错误的是 ( )
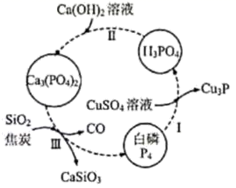 A、过程Ⅰ中,白磷既做氧化剂又做还原剂 B、过程Ⅱ中,发生复分解反应 C、过程Ⅲ中,反应的化学方程式为: D、理论上,通过本提纯工艺不会产生白磷损失4. 2021年5月29日,顺德企业研发的世界首台航天微波炉随着“天舟二号”进入太空。其中芯片全为中国制造,制作芯片的刻蚀液为硝酸与氢氟酸的混合液,工艺涉及的反应为:。下列说法错误的是( )A、该反应中,还原产物只有 B、标况下,生成时,转移电子的物质的量为 C、氧化性: D、制作芯片的单质硅具有半导体性能5. 下图是铜及部分含铜粒子的价荷图。下列推断不合理的是( )
A、过程Ⅰ中,白磷既做氧化剂又做还原剂 B、过程Ⅱ中,发生复分解反应 C、过程Ⅲ中,反应的化学方程式为: D、理论上,通过本提纯工艺不会产生白磷损失4. 2021年5月29日,顺德企业研发的世界首台航天微波炉随着“天舟二号”进入太空。其中芯片全为中国制造,制作芯片的刻蚀液为硝酸与氢氟酸的混合液,工艺涉及的反应为:。下列说法错误的是( )A、该反应中,还原产物只有 B、标况下,生成时,转移电子的物质的量为 C、氧化性: D、制作芯片的单质硅具有半导体性能5. 下图是铜及部分含铜粒子的价荷图。下列推断不合理的是( ) A、在酸性环境中,变成需要加氧化剂 B、转化成需要加碱 C、如果将高铜酸根离子()填入坐标,应该填在的位置 D、在酸性环境中,可以歧化成和6. 下列说法正确的是( )A、因为具有漂白性,所以它能使酸性高锰酸钾溶液褪色 B、气体通入溶液能产生白色沉淀 C、热稳定性: D、硫和氯气分别与铁反应后,铁元素的价态相同7. MnO2催化某反应的一种催化机理如图所示。已知:HCHO中氢元素化合价+1,氧元素化合价−2,下列叙述正确的是( )
A、在酸性环境中,变成需要加氧化剂 B、转化成需要加碱 C、如果将高铜酸根离子()填入坐标,应该填在的位置 D、在酸性环境中,可以歧化成和6. 下列说法正确的是( )A、因为具有漂白性,所以它能使酸性高锰酸钾溶液褪色 B、气体通入溶液能产生白色沉淀 C、热稳定性: D、硫和氯气分别与铁反应后,铁元素的价态相同7. MnO2催化某反应的一种催化机理如图所示。已知:HCHO中氢元素化合价+1,氧元素化合价−2,下列叙述正确的是( )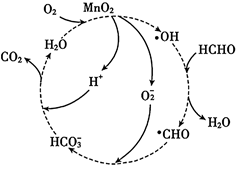 A、使用MnO2催化时,该反应的∆H会发生变化 B、催化过程中,所发生的反应均为氧化还原反应 C、1molHCHO参与反应时转移4mol电子 D、 为中间产物之一,该微粒与Na2O2中所含阴离子相同8. 下列氧化还原反应中,表示电子转移的方向和数目正确的是( )A、
A、使用MnO2催化时,该反应的∆H会发生变化 B、催化过程中,所发生的反应均为氧化还原反应 C、1molHCHO参与反应时转移4mol电子 D、 为中间产物之一,该微粒与Na2O2中所含阴离子相同8. 下列氧化还原反应中,表示电子转移的方向和数目正确的是( )A、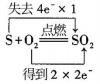 B、
B、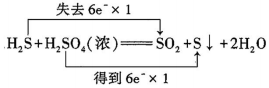 C、
C、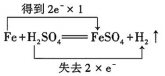 D、
D、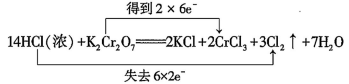 9. 已知下列实验事实:
9. 已知下列实验事实:①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液。
②向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7
③将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是( )
A、化合物KCrO2中Cr元素为+3价 B、实验①中Cr2O3没有发生氧化还原反应 C、实验②证明H2O2既有氧化性又有还原性 D、实验③证明氧化性:Cr2O72->I210. 二氧化硫可以与硫化氢发生归中反应:SO2+2H2S=2H2O+3S;硫单质有多种组成形式,如 。下列有关说法中正确的是( ) A、还原性SO2>H2S B、O-H键的键能大于S-H键的键能,所以沸点:H2O>H2S C、S4、S6、S8形成的晶体均为共价晶体 D、SO2、H2S与H2O分子的空间构型均为V形11. 下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )A、Fe+CuSO4=FeSO4+Cu B、3CO+Fe2O3 2Fe+3CO2 C、AgNO3+NaCl=AgCl↓+NaNO3 D、2KMnO4 K2MnO4+MnO2+O2↑12. 实现下列物质之间的转化,必须加入氧化剂才能实现的是( )A、Cl2→Clˉ B、Fe2+→Fe3+ C、HClO→O2 D、CuO→Cu13. 食盐中的碘以碘酸钾(KIO3)形式存在,可根据反应: +5I-+6H+=3I2+3H2O验证食盐中存在 。根据上述反应,下列说法错误的是( )A、 作氧化剂,发生还原反应 B、I2既是氧化产物又是还原产物 C、该条件下氧化性: >I2 D、被氧化的I原子和被还原的I原子个数比1:5
。下列有关说法中正确的是( ) A、还原性SO2>H2S B、O-H键的键能大于S-H键的键能,所以沸点:H2O>H2S C、S4、S6、S8形成的晶体均为共价晶体 D、SO2、H2S与H2O分子的空间构型均为V形11. 下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )A、Fe+CuSO4=FeSO4+Cu B、3CO+Fe2O3 2Fe+3CO2 C、AgNO3+NaCl=AgCl↓+NaNO3 D、2KMnO4 K2MnO4+MnO2+O2↑12. 实现下列物质之间的转化,必须加入氧化剂才能实现的是( )A、Cl2→Clˉ B、Fe2+→Fe3+ C、HClO→O2 D、CuO→Cu13. 食盐中的碘以碘酸钾(KIO3)形式存在,可根据反应: +5I-+6H+=3I2+3H2O验证食盐中存在 。根据上述反应,下列说法错误的是( )A、 作氧化剂,发生还原反应 B、I2既是氧化产物又是还原产物 C、该条件下氧化性: >I2 D、被氧化的I原子和被还原的I原子个数比1:5二、多选题
-
14. 实验室中利用固体KMnO4进行如图实验,下列说法错误的是( )
 A、G与H均为氧化产物 B、实验中KMnO4只作氧化剂 C、Mn元素至少参与了3个氧化还原反应 D、G与H的物质的量之和可能为0.25mol15. 利用间接成对电化学合成间氨基苯甲酸的工作原理如图所示。下列说法错误的是( )
A、G与H均为氧化产物 B、实验中KMnO4只作氧化剂 C、Mn元素至少参与了3个氧化还原反应 D、G与H的物质的量之和可能为0.25mol15. 利用间接成对电化学合成间氨基苯甲酸的工作原理如图所示。下列说法错误的是( )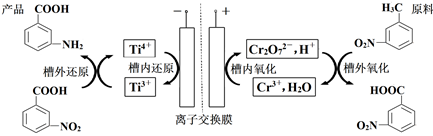 A、阳极的电极反应式为:2Cr3++7H2O-6e-=Cr2O +14H+ B、阳极槽外氧化反应为:
A、阳极的电极反应式为:2Cr3++7H2O-6e-=Cr2O +14H+ B、阳极槽外氧化反应为: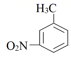 +Cr2O +8H+→
+Cr2O +8H+→ 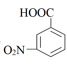 +2Cr3++5H2O
C、通电时阳极区pH增大
D、当电路中转移1mole-时,理论上可得到1mol间氨基苯甲酸
16. 利用含钴废料(主要成分为Co3O4 , 还含有少量的铝箔、LiCoO2等杂质)制备碳酸钴的工艺流程如图:
+2Cr3++5H2O
C、通电时阳极区pH增大
D、当电路中转移1mole-时,理论上可得到1mol间氨基苯甲酸
16. 利用含钴废料(主要成分为Co3O4 , 还含有少量的铝箔、LiCoO2等杂质)制备碳酸钴的工艺流程如图: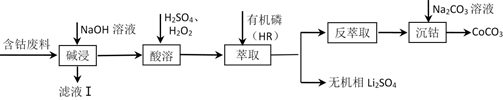
已知:萃取Co2+的反应原理:Co2++2HR(有机磷) CoR2+2H+。下列说法错误的是( )
A、“滤液Ⅰ”中溶质的主要成分是Na[Al(OH)4] B、“酸溶”中H2O2的作用是将Co2+氧化为Co3+ C、“反萃取”中可加入H2SO4分离出Co2+ D、“沉钴”时增大Na2CO3溶液的浓度或滴加速率,能够提高产品的纯度17. 某同学研究浓硝酸与 溶液的反应,进行如下实验: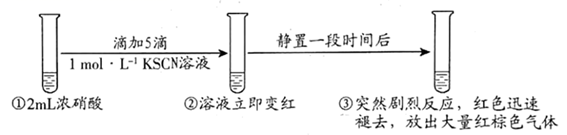
已知: 能被氧化为黄色的 可聚合为红色的 。
下列分析错误的是( )
A、②中溶液变红,是由于生成了 B、取少量③中的溶液加入 溶液,产生白色沉淀,证明最终有 生成 C、分析①②知,硝酸氧化 的速率大于 聚合为 ,的速率 D、向溶有 的浓硝酸中加几滴 溶液,溶液先变红后迅速褪色并产生大量红棕色气体,证明 催化浓硝酸氧化 ,的反应18. 如图是PdCl2、CuCl2催化下的烯烃的氧化反应,L是配体或溶剂。下列说法正确的是( )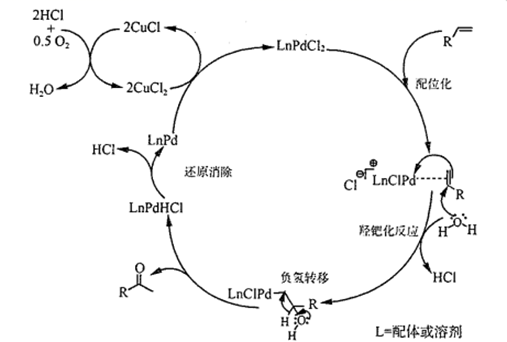 A、加入CuCl2之后再通入O2 , 目的是使催化剂再生 B、该过程原子利用率100%,且原料、催化剂、溶剂和试剂产物均无毒无害 C、过程中元素Pd、Cu、O和C等元素发生过化合价变化 D、
A、加入CuCl2之后再通入O2 , 目的是使催化剂再生 B、该过程原子利用率100%,且原料、催化剂、溶剂和试剂产物均无毒无害 C、过程中元素Pd、Cu、O和C等元素发生过化合价变化 D、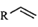 和
和 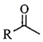 (二者R相同)中的 键数目相等
(二者R相同)中的 键数目相等
三、填空题
-
19. 物质分类与转化是学习化学的基石,如图为氯及其化合物的“价—类”二维图,请正确回答下列问题。
 (1)、填写二维图缺失的类别 A和化学式 B。(2)、某同学利用以下试剂研究 HCl 性质,进行了如下预测:
(1)、填写二维图缺失的类别 A和化学式 B。(2)、某同学利用以下试剂研究 HCl 性质,进行了如下预测:a.Na2CO3
b.Fe
c.NaOH
d.KMnO4
从物质类别上看,HCl 属于酸,可能与 HCl 反应的有(填字母);
(3)、关于盐酸与 NaClO 反应,同学们有不同意见,甲同学认为发生反应:NaClO+HCl=NaCl+HClO,该反应属于反应类型(填四大基本反应类型);乙同学认为发生氧化还原反应,写出反应方程式;该反应从化合价角度体现了盐酸具有性。20. ClO2是广泛使用的漂白剂、消毒剂。某工厂生产 ClO2和 NaClO2的反应原理为:2NaClO3+Na2SO3+H 2 SO 4 =Na2SO 4 +2ClO2↑+H2O(1)、NaClO 3 中氯元素的化合价;该反应的还原剂为;(2)、用单线桥法标出上述化学方程式的电子转移情况;(3)、若生成标准状况下ClO211.2L,则反应转移的电子数为;(4)、ClO2 是市场上一种比较理想的饮用水消毒剂,在消毒时自身均被还原为 Cl- ,则 ClO2 的消毒效率(以单位质量得到的电子数表示)是 (结果用最简分数表示)四、综合题
-
21. 主要用作颜料、釉料及磁性材料,利用一种钴矿石(主要成分为 , 含少量、及铝、镁、钙等金属元素的氧化物)制取的工艺流程如图所示。

部分阳离子以氢氧化物形式沉淀时溶液
沉淀物
完全沉淀的
3.7
9.6
9.2
5.2
回答下列问题:
(1)、“溶浸”过程中,可以加快反应速率和提高原料利用率的方法是(写出一种即可),加入的作用是。(2)、“氧化”过程中金属离子与反应的离子方程式为 , 由此推测还原性:Fe2+Co2+(填“”或“”)。(3)、滤渣2的主要成分为(写化学式),检验铁元素的离子已被完全沉淀的实验操作及现象;取少量待测液于试管中,。(4)、已知某温度下 , 。该温度下,“沉淀除杂”时加入足量的溶液可将、沉淀除去,若所得滤液中 , 则滤液中为(保留2位有效数字)。(5)、在空气中充分煅烧,除得到产品外还产生了 , 则反应中与的化学计量数之比为。22. 从高铝粉煤灰(主要成分为、、、、等)中回收金属、并制备电池正极材料的工艺流程如下图所示:
已知:①与同主族,其化学性质相似。
②随着温度升高,在水溶液中的溶解度减小:
温度/
0
20
40
60
80
100
溶解度/
1.54
1.33
1.17
1.01
0.85
0.72
③本工艺流程中,不同金属离子形成氢氧化物沉淀的范围如表格所示:
金属离子
形成氢氧化物沉淀的范围
3.3~10.6
2.9~9.4
回答下列问题:
(1)、“滤渣1”的成分除了之外还含有。(2)、已知“酸浸”后铁元素以铁配离子()的形式存在,写出在该过程中的离子方程式。(3)、“调”步骤中的范围应为 , “滤液2”中镓元素的存在形式为。(4)、工业上通过电解法利用“物质”制备 , 反应的化学方程式为。(5)、“”中的元素化合价为 , 在“电池级”转化为“”的反应中,氧化剂与还原剂物质的量之比为。23. 某探究小组利用该反应,用浓度为0.1000mol/L酸性KMnO4标准溶液滴定未知浓度的草酸(H2C2O4).记录数据如下:滴定次数
待测溶液体积/mL
标准溶液体积/mL
滴定前刻度
滴定后刻度
1
20.00
1.50
23.70
2
20.00
1.02
21.03
3
20.00
2.00
21.99
(1)、写出滴定过程中发生反应的离子方程式为 .(2)、 如图是某次滴定时的滴定管中的液面,其读数为mL。 (3)、KMnO4(H+)溶液应装入(填“酸式”、“碱式”)滴定管中。(4)、判断已达滴定终点的现象是:;(5)、实验测得草酸溶液的浓度为;(6)、下列操作会引起实验结果偏高的是_____________.A、滴定管用水洗净后直接注入KMnO4溶液 B、滴定前盛放H2C2O4溶液的锥形瓶用蒸馏水洗净后没有干燥 C、滴定管内在滴定前有气泡,滴定后气泡消失 D、读取KMnO4溶液体积时,滴定前平视,滴定结束后俯视读数24. 回答下列问题。(1)、如图,某温度(t℃)时水的图像如下,a点离子积KW= , 在该温度下,pH=7的溶液显性(填“酸”“碱”或“中”);在该温度下,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2= ,
如图是某次滴定时的滴定管中的液面,其读数为mL。 (3)、KMnO4(H+)溶液应装入(填“酸式”、“碱式”)滴定管中。(4)、判断已达滴定终点的现象是:;(5)、实验测得草酸溶液的浓度为;(6)、下列操作会引起实验结果偏高的是_____________.A、滴定管用水洗净后直接注入KMnO4溶液 B、滴定前盛放H2C2O4溶液的锥形瓶用蒸馏水洗净后没有干燥 C、滴定管内在滴定前有气泡,滴定后气泡消失 D、读取KMnO4溶液体积时,滴定前平视,滴定结束后俯视读数24. 回答下列问题。(1)、如图,某温度(t℃)时水的图像如下,a点离子积KW= , 在该温度下,pH=7的溶液显性(填“酸”“碱”或“中”);在该温度下,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2= ,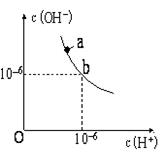 (2)、25℃时,向0.1mol·L-1氨水中加入少量NH4Cl固体,当固体溶解后,测得溶液pH会。(填“增大”、“减小”或“不变”)(3)、25℃时,等浓度的NH3·H2O溶液和NH4Cl溶液等体积混合,pH>7,则混合溶液中各种离子浓度大小关系为。(4)、+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72−还原成Cr3+ , 反应的离子方程式为。
(2)、25℃时,向0.1mol·L-1氨水中加入少量NH4Cl固体,当固体溶解后,测得溶液pH会。(填“增大”、“减小”或“不变”)(3)、25℃时,等浓度的NH3·H2O溶液和NH4Cl溶液等体积混合,pH>7,则混合溶液中各种离子浓度大小关系为。(4)、+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72−还原成Cr3+ , 反应的离子方程式为。五、实验探究题
-
25. 亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,沸点为-5.5℃,遇水和潮气分解。
回答下列问题:
(1)、NO与Cl2在通常条件下可反应得到NOCl。某实验小组用浓盐酸与MnO2反应制Cl2 , Cu和稀HNO3制NO。①制取NO的离子方程式为
②选用下列部分装置预制备一瓶干燥纯净的氯气,各玻璃导管接口连接顺序为(气流方向从左至右)。
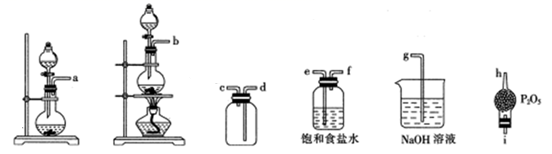 (2)、文献中记录的一种利用浓盐酸和NaNO2浓溶液反应制取NOCl的原理及装置如下所示:
(2)、文献中记录的一种利用浓盐酸和NaNO2浓溶液反应制取NOCl的原理及装置如下所示:反应原理:NaNO2+2HCl=NOCl↑+NaCl+H2O。制取装置图:

①仪器X的名称为 , 用它代替分液漏斗的优点是
②装置C的U形管中观察到的现象是 , 装置D的作用是
(3)、取少量产品NOCl滴入盛有水的试管中,液面上方有白雾且产生无色气体,该气体在试管口变为红棕色,NOCl与水反应的化学方程式为26. 高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水的处理剂,制备流程如图所示: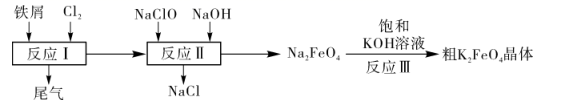
某化学兴趣小组模拟上述流程,在实验室中探究制备K2FeO4的方法,回答下列问题:
查阅资料:K2FeO4具有强氧化性,在酸性或中性溶液中易快速产生O2 , 在碱性溶液中较稳定。
(1)、反应Ⅲ中能够得到高铁酸钾的原因是。(2)、若实验室用高锰酸钾与浓盐酸制取少量氯气,则反应的最佳装置应选用图中的(填标号),反应的离子方程式为。a.
 b.
b. 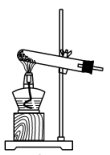
c.
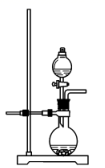 d.
d. 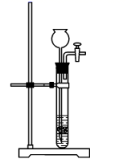 (3)、制备K2FeO4的实验装置如图。装置中仪器乙的名称为 , 实验时应先打开活塞K2的原因是 , 为了提高氯气的利用率,可采取的措施是。
(3)、制备K2FeO4的实验装置如图。装置中仪器乙的名称为 , 实验时应先打开活塞K2的原因是 , 为了提高氯气的利用率,可采取的措施是。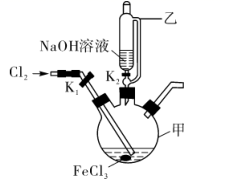 (4)、验证酸性条件下氧化性 >Cl2的实验方案为:取少量K2FeO4固体于试管中,(实验中须使用的试剂和用品有:浓盐酸,NaOH溶液、淀粉KI试纸、棉花)。(5)、根据K2FeO4的制备实验得出:氧化性Cl2> ,和第(4)小题实验表明的Cl2和 的氧化性强弱关系相反,原因是。
(4)、验证酸性条件下氧化性 >Cl2的实验方案为:取少量K2FeO4固体于试管中,(实验中须使用的试剂和用品有:浓盐酸,NaOH溶液、淀粉KI试纸、棉花)。(5)、根据K2FeO4的制备实验得出:氧化性Cl2> ,和第(4)小题实验表明的Cl2和 的氧化性强弱关系相反,原因是。