人教【新课标】高中化学一轮复习:专题8
试卷更新日期:2021-12-27 类型:一轮复习
一、单选题
-
1. 短周期元素R、X、Y、Z、M原子序数依次递增,最外层电子数:3Z+M=X+Y,其中元素R、X、Y、M形成的化合物(结构式)具有如图所示转化关系。下列说法正确的是( )
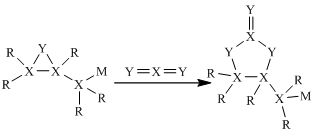 A、原子半径:M>Z>Y B、简单气态氢化物的沸点:Y>X C、X的最高价氧化物对应水化物为强酸 D、Z分别与R、X、Y、M形成的化合物中均只含离子键2. 短周期主族元素W、X、Y、Z原子序数依次增大,W与Y同主族,X与Z同主族。其中X、Y、Z构成的某种物质结构如图所示。下列叙述正确的是( )
A、原子半径:M>Z>Y B、简单气态氢化物的沸点:Y>X C、X的最高价氧化物对应水化物为强酸 D、Z分别与R、X、Y、M形成的化合物中均只含离子键2. 短周期主族元素W、X、Y、Z原子序数依次增大,W与Y同主族,X与Z同主族。其中X、Y、Z构成的某种物质结构如图所示。下列叙述正确的是( )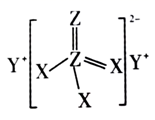 A、简单氢化物的沸点:Z>X B、简单离子半径:Z>Y>X>W C、W与X形成的化合物一定是共价化合物 D、Y和Z形成的最简单化合物水溶液显碱性3. 已知X、Y、Z、W、R是三个短周期的主族元素。Y和W同主族,Z被誉为“国防金属”,W的最外层电子数是其内层电子总数的一半,Z与R原子序数之和为29.则下列说法正确的是( )A、X与Y、Z、W。R均可形成共价化合物 B、Y与R形成的化合物水解后产生有刺激性气味的气体 C、简单离子半径:R>Z>Y D、Z与R形成的化合物溶于水后不存在4. 2020年12月17日,嫦娥五号探测器携带着珍贵的月球“土特产”——月壤成功返回,研究表明月壤包含微细的矿物颗粒、岩石碎屑和玻璃质微粒等,主要由氧、硅、铝、铁、镁钙、钠、钾、钛等元素构成。下列相关化学用语正确的是( )A、 和 是氧的两种不同的同素异形体 B、 核外有m个电子、n个中子,X原子符号为 C、钾原子的原子结构示意图为:
A、简单氢化物的沸点:Z>X B、简单离子半径:Z>Y>X>W C、W与X形成的化合物一定是共价化合物 D、Y和Z形成的最简单化合物水溶液显碱性3. 已知X、Y、Z、W、R是三个短周期的主族元素。Y和W同主族,Z被誉为“国防金属”,W的最外层电子数是其内层电子总数的一半,Z与R原子序数之和为29.则下列说法正确的是( )A、X与Y、Z、W。R均可形成共价化合物 B、Y与R形成的化合物水解后产生有刺激性气味的气体 C、简单离子半径:R>Z>Y D、Z与R形成的化合物溶于水后不存在4. 2020年12月17日,嫦娥五号探测器携带着珍贵的月球“土特产”——月壤成功返回,研究表明月壤包含微细的矿物颗粒、岩石碎屑和玻璃质微粒等,主要由氧、硅、铝、铁、镁钙、钠、钾、钛等元素构成。下列相关化学用语正确的是( )A、 和 是氧的两种不同的同素异形体 B、 核外有m个电子、n个中子,X原子符号为 C、钾原子的原子结构示意图为: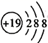 D、一种月壤辉长岩成分为 ,用氧化物的形式表示其组成为
5. 短周期元素 、 、 、 的原子序数依次增大, 、 、 原子的最外层电子数之和为11, 与 同族, 最外层电子数等于 次外层电子数, 的单质晶体是应用最广泛的半导体材料。下列叙述错误的是( )A、非金属性: B、简单氢化物的沸点: C、化合物 中含有共价键 D、 的单质可与 的氧化物发生置换反应6. X、Y、Z、W是原子序数依次增大的短周期主族元素。X的原子核内只有一个质子,液态ZX3常用作制冷剂,Y原子L层比W原子M层多1个电子,W的单质在常温下能被浓硫酸钝化。下列说法正确的是( )A、最简单氢化物沸点:Z>Y B、X、Y形成的化合物中只含有极性键 C、最高正价:W>Z>Y>X D、最高价氧化物对应水化物的酸性:Y>Z7. NA为阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,体积均为1.12L的HCl和HF中所含分子数都为0.05NA B、2.0gD216O和14ND3的混合物中含有的电子数为NA C、标准状况下,22.4LNO与11.2LO2混合后所得气体含分子数为NA D、23gC2H6O分子中含有碳氢键的数目一定为3NA8. 下列有关放射性核素 的说法中,错误的是( )A、 原子核外电子数为15 B、 原子的质量数为15 C、 可能用于同位素示踪 D、 和 的化学性质基本相同9. W、M、X、Y、Z为原子序数依次增大的短周期元素。已知五种元素原子序数依次相差2,W、Z同主族,M、X、Y、Z同周期,W的简单气态氢化物的稳定性大于Z的简单气态氢化物的稳定性。下列说法错误的是( )A、M、X、Y、Z、W的原子半径依次减小 B、W的氢化物的水溶液酸性比Z的氢化物的水溶液酸性强 C、M、X、Z的最高价氧化物对应的水化物能两两发生反应 D、W与M形成的化合物中只含离子键10. 有X、Y、Z、W、Q五种原子序数依次递增的短周期主族元素,其中X、W同主族且W的原子序数为X的两倍,Y为金属元素,Z离子在同周期内离子半径最小。下列说法中,正确的是( )A、元素X和Q的某些单质或化合物可作为工业生产上的脱色剂、消毒剂等 B、由于X元素的氢化物分子间存在氢键,所以X元素的氢化物比W元素的氢化物更稳定且沸点更高 C、工业生产Z,常通过电解熔融的 ,因 的熔点较低,能耗低 D、Z元素的最高价氧化物对应的水化物会与Q元素的最高价氧化物对应的水化物反应,也会与Y元素的最高价氧化物水化物反应11. 研究小组在探究卤素离子与硝酸银的反应时,进行了以下实验。
D、一种月壤辉长岩成分为 ,用氧化物的形式表示其组成为
5. 短周期元素 、 、 、 的原子序数依次增大, 、 、 原子的最外层电子数之和为11, 与 同族, 最外层电子数等于 次外层电子数, 的单质晶体是应用最广泛的半导体材料。下列叙述错误的是( )A、非金属性: B、简单氢化物的沸点: C、化合物 中含有共价键 D、 的单质可与 的氧化物发生置换反应6. X、Y、Z、W是原子序数依次增大的短周期主族元素。X的原子核内只有一个质子,液态ZX3常用作制冷剂,Y原子L层比W原子M层多1个电子,W的单质在常温下能被浓硫酸钝化。下列说法正确的是( )A、最简单氢化物沸点:Z>Y B、X、Y形成的化合物中只含有极性键 C、最高正价:W>Z>Y>X D、最高价氧化物对应水化物的酸性:Y>Z7. NA为阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,体积均为1.12L的HCl和HF中所含分子数都为0.05NA B、2.0gD216O和14ND3的混合物中含有的电子数为NA C、标准状况下,22.4LNO与11.2LO2混合后所得气体含分子数为NA D、23gC2H6O分子中含有碳氢键的数目一定为3NA8. 下列有关放射性核素 的说法中,错误的是( )A、 原子核外电子数为15 B、 原子的质量数为15 C、 可能用于同位素示踪 D、 和 的化学性质基本相同9. W、M、X、Y、Z为原子序数依次增大的短周期元素。已知五种元素原子序数依次相差2,W、Z同主族,M、X、Y、Z同周期,W的简单气态氢化物的稳定性大于Z的简单气态氢化物的稳定性。下列说法错误的是( )A、M、X、Y、Z、W的原子半径依次减小 B、W的氢化物的水溶液酸性比Z的氢化物的水溶液酸性强 C、M、X、Z的最高价氧化物对应的水化物能两两发生反应 D、W与M形成的化合物中只含离子键10. 有X、Y、Z、W、Q五种原子序数依次递增的短周期主族元素,其中X、W同主族且W的原子序数为X的两倍,Y为金属元素,Z离子在同周期内离子半径最小。下列说法中,正确的是( )A、元素X和Q的某些单质或化合物可作为工业生产上的脱色剂、消毒剂等 B、由于X元素的氢化物分子间存在氢键,所以X元素的氢化物比W元素的氢化物更稳定且沸点更高 C、工业生产Z,常通过电解熔融的 ,因 的熔点较低,能耗低 D、Z元素的最高价氧化物对应的水化物会与Q元素的最高价氧化物对应的水化物反应,也会与Y元素的最高价氧化物水化物反应11. 研究小组在探究卤素离子与硝酸银的反应时,进行了以下实验。编号
操作
试剂
现象
1
①KCl溶液②稀硝酸酸化的 溶液
产生白色沉淀
2
①KCl溶液②浓硝酸酸化的 溶液
产生白色沉淀
3
①KI溶液 ②稀硝酸酸化的 溶液
产生黄色沉淀
4
①KI溶液 ②浓硝酸酸化的 溶液
产生褐色的浊液
下列说法错误的是( )
A、实验1和2说明,硝酸浓度不影响 的检验 B、实验1和3说明,卤素离子的检验可使用稀硝酸酸化的 溶液 C、对比实验2和4,说明异常现象的产生与卤素离子种类有关 D、由上述实验推测, 的检验不能使用浓硝酸酸化的 溶液12. 科学家致力于将大气中过多的 转化为有益于人类的物质,下图是一种可以从空气中捕获 直接转化为甲醇的方法。下列说法正确的是。( )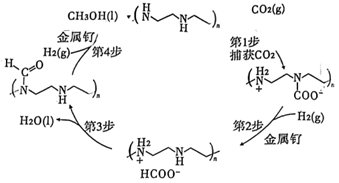 A、从空气中每捕获 ,转移的电子数为 B、第1步反应的原子利用率为100% C、第4步反应中有极性键和非极性键的断裂和生成 D、该历程以金属钌、
A、从空气中每捕获 ,转移的电子数为 B、第1步反应的原子利用率为100% C、第4步反应中有极性键和非极性键的断裂和生成 D、该历程以金属钌、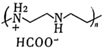 作催化剂
13. 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示,其中W原子的质子数是其M层电子数的三倍,下列说法正确的是( )
作催化剂
13. 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示,其中W原子的质子数是其M层电子数的三倍,下列说法正确的是( )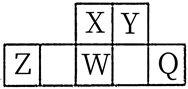 A、工业上常通过电解Z的熔融氯化物的方法制取Z的单质 B、简单离子半径:Q>Z>X>Y C、氢化物的沸点:Y>X>W D、X与Y可形成5种以上的化合物14. P4具有正四面体结构,它在Cl2中燃烧可生成PCl5和PCl3两种产物,经测定在PCl5中P-Cl与PCl3中的P-Cl键能是不同的。PCl5中P—Cl键的键能为ckJ·mol-1 , PCl3中P-Cl键的键能为1.2ckJ·mol-1。已知:P4(g)+6Cl2(g)=4PCl3(g)ΔH=akJ·mol-1 , P4(g)+10Cl2(g)=4PCl5(g)ΔH=bkJ·mol-1 , 下列叙述正确的是( )A、PCl5分子中原子最外层均满足8电子结构 B、可求Cl2(g)+PCl3(g)=PCl5(s)的反应热ΔH C、Cl-Cl键的键能为 kJ·mol-1 D、P-P键的键能为 kJ·mol-115. W、X、Y、Z为原子序数依次增大的四种短周期元素。W与X可形成一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;Z原子最外层的电子数与W的电子总数相同。下列叙述错误的是( )A、四种元素的原子半径大小顺序为: B、元素X、Y形成的简单离子具有相同的电子层结构 C、X与Y两种元素组成的化合物中一定不含非极性共价键 D、由X、Y和Z三种元素组成的化合物的水溶液可能呈中性16. 有机化合物M的结构简式如右图所示,其组成元素X、Y、Z、W、Q为原子序数依次增大的短周期元素。只有Y、Z、W为同周期相邻元素,Z的原子序数与Q的最外层电子数相同。下列说法正确的是( )
A、工业上常通过电解Z的熔融氯化物的方法制取Z的单质 B、简单离子半径:Q>Z>X>Y C、氢化物的沸点:Y>X>W D、X与Y可形成5种以上的化合物14. P4具有正四面体结构,它在Cl2中燃烧可生成PCl5和PCl3两种产物,经测定在PCl5中P-Cl与PCl3中的P-Cl键能是不同的。PCl5中P—Cl键的键能为ckJ·mol-1 , PCl3中P-Cl键的键能为1.2ckJ·mol-1。已知:P4(g)+6Cl2(g)=4PCl3(g)ΔH=akJ·mol-1 , P4(g)+10Cl2(g)=4PCl5(g)ΔH=bkJ·mol-1 , 下列叙述正确的是( )A、PCl5分子中原子最外层均满足8电子结构 B、可求Cl2(g)+PCl3(g)=PCl5(s)的反应热ΔH C、Cl-Cl键的键能为 kJ·mol-1 D、P-P键的键能为 kJ·mol-115. W、X、Y、Z为原子序数依次增大的四种短周期元素。W与X可形成一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;Z原子最外层的电子数与W的电子总数相同。下列叙述错误的是( )A、四种元素的原子半径大小顺序为: B、元素X、Y形成的简单离子具有相同的电子层结构 C、X与Y两种元素组成的化合物中一定不含非极性共价键 D、由X、Y和Z三种元素组成的化合物的水溶液可能呈中性16. 有机化合物M的结构简式如右图所示,其组成元素X、Y、Z、W、Q为原子序数依次增大的短周期元素。只有Y、Z、W为同周期相邻元素,Z的原子序数与Q的最外层电子数相同。下列说法正确的是( )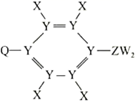 A、简单氢化物的沸点由高到低顺序为 B、含氧酸的酸性强弱顺序为 C、元素第一电离能由小到大的顺序为 D、元素X、Z、W形成的离子化合物中含有正四面体结构17. 阿伏加德罗常数的值为NA。下列说法正确的是( )A、2.0 g重水(D2O)中含NA个中子 B、0.3 mol甲基所含电子数为2.1NA C、60 g乙酸与足量乙醇发生酯化反应,充分反应后断裂的C-O键数目为NA D、标准状况下,11.2 L NH3含有的质子数为0.5NA
A、简单氢化物的沸点由高到低顺序为 B、含氧酸的酸性强弱顺序为 C、元素第一电离能由小到大的顺序为 D、元素X、Z、W形成的离子化合物中含有正四面体结构17. 阿伏加德罗常数的值为NA。下列说法正确的是( )A、2.0 g重水(D2O)中含NA个中子 B、0.3 mol甲基所含电子数为2.1NA C、60 g乙酸与足量乙醇发生酯化反应,充分反应后断裂的C-O键数目为NA D、标准状况下,11.2 L NH3含有的质子数为0.5NA二、多选题
-
18. 短周期主族元素 、 、 、 的原子序数依次增大, 的阴离子与锂离子具有相同的电子层结构, 的一种核素常用于考古断代, 原子的最外层电子数是内层电子数的3倍, 、 、 原子的最外层电子数总和等于 的原子序数。下列推断错误的是( )A、原子半径: B、化合物 中既含离子键又含共价键 C、最简单气态氢化物的稳定性: D、由上述四种元素组成的化合物的水溶液不可能呈碱性19. 下列操作能达到实验目的的是( )
选项
目的
操作
A
除去Cu粉中混有的CuO
加入稀硝酸,过滤、洗涤、干燥
B
探究温度对Fe3+水解程度的影响
向25 mL冷水和沸水中分别滴入5滴饱和FeCl3溶液,比较溶液颜色
C
证明甲苯中的甲基能够活化苯环
分别取甲苯和苯与酸性KMnO4溶液反应,观察酸性KMnO4溶液的褪色情况
D
证明非金属性:Cl>S
向Na2S溶液中滴加新制氯水,观察实验现象
A、A B、B C、C D、D20. 短周期元素X、Y、Z、R的原子序数依次增大,离子化合物YR可用于调味和食品保存,X、Y、Z三种元素组成的两种化合物A、B的性质如图,X的基态原子中s能级与p能级上的电子数相等。下列说法正确的是( )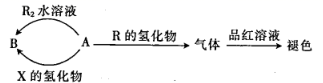 A、X与Z形成的三原子分子为直线形分子 B、简单离子半径:Y<R<Z C、X、Z、R的氢化物的分子间均能形成氢键 D、X、Y、Z、R中,Y的第一电离能最小21. 短周期主族元素X、Y、Z、W原子序数依次增大,X与Z可以形成两种常见液态化合物,W的原子半径在矩周期主族元素中最大,由Y、Z、W三种元素形成的化合物A的结构如图所示。下列叙述错误的是( )
A、X与Z形成的三原子分子为直线形分子 B、简单离子半径:Y<R<Z C、X、Z、R的氢化物的分子间均能形成氢键 D、X、Y、Z、R中,Y的第一电离能最小21. 短周期主族元素X、Y、Z、W原子序数依次增大,X与Z可以形成两种常见液态化合物,W的原子半径在矩周期主族元素中最大,由Y、Z、W三种元素形成的化合物A的结构如图所示。下列叙述错误的是( )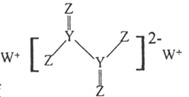 A、Y的氢化物沸点一定低于Z的氢化物 B、X与Z可能形成由极性键与非极性键构成的极性分子 C、化合物 可以与乙二醇在一定条件下发生缩聚反应 D、0.1 化合物A与足量酸性高锰酸钾溶液完全反应转移电子数是0.122. 利用如图所示装置进行实验,能达到相应实验目的的是( )
A、Y的氢化物沸点一定低于Z的氢化物 B、X与Z可能形成由极性键与非极性键构成的极性分子 C、化合物 可以与乙二醇在一定条件下发生缩聚反应 D、0.1 化合物A与足量酸性高锰酸钾溶液完全反应转移电子数是0.122. 利用如图所示装置进行实验,能达到相应实验目的的是( )选项
①
②
③
实验目的

A
浓
蔗糖
品红溶液
检验是否有 生成
B
稀
某盐溶液
澄清石灰水
检验盐溶液中是否含有 或
C
浓盐酸
溶液
比较非金属性:Cl与S
D
浓
浓盐酸
悬浊液
比较 与
A、A B、B C、C D、D三、填空题
-
23. 下列物质中:①MgCl2②金刚石③NaCl④H2O⑤Na2O2⑥O2⑦H2SO4⑧CO2⑨NH4Cl⑩Ne。只含离子键的是 , 只含共价键的是 , 既含离子键又含共价键的是 , 不存在化学键的是 , 属于离子化合物的是 , 属于共价化合物的是。24. 有下列七种物质:A、干冰 B、氧化镁 C、氯化铵 D、固态碘 E、烧碱 F、冰 G、过氧化钾(1)、熔化时需要破坏共价键和离子键的是(填序号,下同);(2)、既有离子键又有共价键的是;(3)、只含有极性键的是;(4)、含非极性键的是。25. 下列五种物质中 ①Ne ②H2O ③NH3 ④KOH ⑤Na2O(填写序号):只存在共价键的是 ,只存在离子键的是 ,既存在共价键又存在离子键的是 ,不存在化学键的是。26. 下表是中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题。

IA
0
1
①
II A
IIIA
IV A
VA
VIA
VIIA
2
②
③
Ne
3
④
⑤
Al
S
⑥
(1)、⑥表示的元素是;(2)、②的原子结构示意图是;(3)、由①和③两种元素组成的化合物的化学式是;(4)、④和⑤两种元素的金属性强弱顺序是④⑤(填“<”或“>”)。四、实验探究题
-
27.(1)、I.请回答下列问题:
常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图。1 mol 硼酸(H3BO3)晶体中含有 mol 氢键。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:。
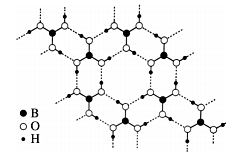 (2)、比较酸性的相对强弱:H2SO4HClO4 (填“>”“=”或“<”),已知能发生反应:H2SO4(浓)+NaClO4 HClO4+NaHSO4 , 说明该反应能发生的理由。(3)、Ⅱ.氮化铝(AlN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理欲在实验室制备氮化铝。查阅资料:①实验室用饱和NaNO2溶液与NH4Cl溶液共热制N2:NaNO2+NH4Cl NaCl+N2↑+2H2O;②工业制氮化铝:Al2O3+3C+N2 2AlN+3CO,氮化铝在高温下能水解。
(2)、比较酸性的相对强弱:H2SO4HClO4 (填“>”“=”或“<”),已知能发生反应:H2SO4(浓)+NaClO4 HClO4+NaHSO4 , 说明该反应能发生的理由。(3)、Ⅱ.氮化铝(AlN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理欲在实验室制备氮化铝。查阅资料:①实验室用饱和NaNO2溶液与NH4Cl溶液共热制N2:NaNO2+NH4Cl NaCl+N2↑+2H2O;②工业制氮化铝:Al2O3+3C+N2 2AlN+3CO,氮化铝在高温下能水解。氮化铝的制备
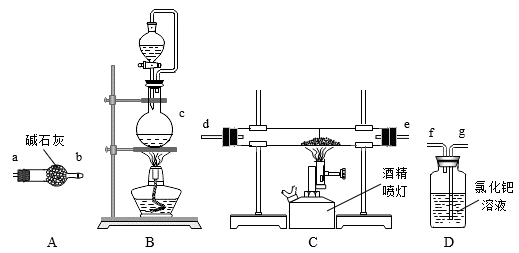
①实验中使用的装置如上图所示,请按照氮气流方向将各仪器接口连接:c→。 (根据实验需要,上述装置可使用多次)
②D装置内氯化钯溶液的作用可能是。
(4)、AlN粉末会缓慢发生水解反应,粒径为100 nm的AlN粉末水解时溶液pH的变化如下图所示。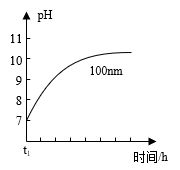
①AlN粉末水解的化学方程式是。
②相同条件下,请在图中画出粒径为40 nm的AlN粉末水解的变化曲线。
28. 某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。(1)、浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中存在盐酸和MnO2。①反应的离子方程式是。
②电极反应式:
i还原反应:MnO2+2e-+4H+=Mn2++2H2O
ii氧化反应:。
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱.
ii随c(Cl-)降低,。
④补充实验证实了③中的分析。
实验操作
试剂
产物
I
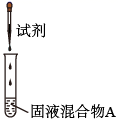
较浓H2SO4
有Cl2
II
a
有Cl2
III
a+b
无Cl2
a是 , b是。
(2)、利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)由大到小的顺序是 , 从原子结构角度说明理由。(3)、根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是。(4)、Ag分别与1mol·L1的盐酸、氢溴酸、氢碘酸混合,Ag只与氢碘酸发生置换反应,试解释原因:。(5)、总结:物质氧化性和还原性变化的一般规律是。29. 研究发现,NO在心脑血管调节、免疫调节等方面有着十分重要的作用,但NO无法直接作为药物使用。科学家发现NO 有着与NO相似的功效,可以用作药物。某研究小组对亚硝酸盐转化为NO的反应进行了研究。(1)、NO中N元素的化合价呈现正价,用原子结构解释原因为。(2)、为研究NO 的转化,甲同学完成了如下实验:实验方案
实验现象

i.溶液先变黄色,迅速变为棕色
ii.将棕色溶液加热,颜色变浅,冷却
资料:FeSO4+NO⇌Fe(NO)SO4(棕色)△H<0
在冷却后的溶液中滴加(填“试剂和现象”),说明有Fe3+生成。从而证明Fe2+可以还原NO 。
(3)、乙同学认为甲同学的实验方案不严谨,其理由是。并进一步利用下列实验装置进行实验,以验证甲同学的实验结论是正确的。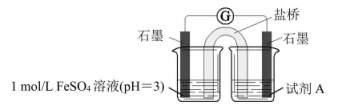
①右侧烧杯中试剂A是。
②实验证据是。
(4)、写出NaNO2溶液与FeSO4溶液反应的离子方程式。(5)、解释“棕色溶液加热,颜色变浅”的原因是。(6)、研究表明,亚硝酸盐能够被人体内含Fe2+等的还原性酶还原为NO,NO的生物学作用揭示着无机分子在医学领域中的重要作用,它与血红素铁具有很高的亲合力,以取代O2的位置。因此,亚硝酸盐作为药物使用时,必须严格控制剂量。若服用过量,可能会产生的影响是。五、综合题
-
30. 某工厂的工业废水中含有大量的 FeSO4 和 CuSO4 ,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收 FeSO4 和金属 Cu 。请根据以下流程图,回答相关问题:
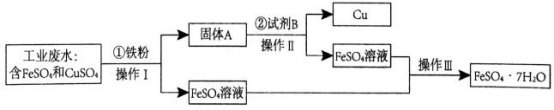 (1)、操作Ⅰ和操作Ⅱ的方法是。(2)、为了将 CuSO4 完全转化,步骤①加入的铁粉应(选填“过量”或“少量”) ,其对应的化学方程式为。(3)、固体 A 的成分是铁和(填名称)。(4)、操作Ⅱ加入试剂 B 的稀溶液,B 的化学式为 , 该物质在该反应中作剂(选填“氧化”或“还原”)。(5)、取 1~2mLFeSO4 溶液于试管中,滴加几滴 NaOH 溶液,生成的白色沉淀迅速变为灰绿色,最 后变成红褐色,写出该反应中沉淀转化对应的化学反应方程式。
(1)、操作Ⅰ和操作Ⅱ的方法是。(2)、为了将 CuSO4 完全转化,步骤①加入的铁粉应(选填“过量”或“少量”) ,其对应的化学方程式为。(3)、固体 A 的成分是铁和(填名称)。(4)、操作Ⅱ加入试剂 B 的稀溶液,B 的化学式为 , 该物质在该反应中作剂(选填“氧化”或“还原”)。(5)、取 1~2mLFeSO4 溶液于试管中,滴加几滴 NaOH 溶液,生成的白色沉淀迅速变为灰绿色,最 后变成红褐色,写出该反应中沉淀转化对应的化学反应方程式。