人教【新课标】高中化学一轮复习:专题6常见的非金属元素
试卷更新日期:2021-12-27 类型:一轮复习
一、单选题
-
1. 为检验溶液里的某种离子,进行下列实验,其中结论正确的是( )A、溶液中加 AgNO3 溶液有白色沉淀生成,再加入稀盐酸沉淀不溶解,溶液一定含 Cl- B、先滴加 KSCN 溶液不显红色,再滴加氯水后显红色证明某溶液中含有 Fe2- C、某溶液进行焰色反应为黄色,则该溶液一定含有 Na+ ,一定没有K+ D、溶液中加入稀 HCl,产生使澄清石灰水变浑浊的无色气体,则溶液中一定含 CO32-2. 每天用“84”消毒液(NaClO溶液)可用于消毒,下列说法正确的是( )A、NaClO溶液的消毒原理是生成Cl2 B、NaClO暴露在空气中变质形成HClO C、NaClO溶液漂白原理与活性炭相同 D、“84”消毒液可与“洁厕灵” (HCl)共同使用3. 元素化合物在实验中具有广泛的应用。下列实验中,实验现象与结论不匹配的是( )
实验操作
实验现象
结论
A
将Cl2通入水中制成溶液,向该溶液中加入KMnO4溶液
KMnO4溶液褪色
Cl2具有氧化性
B
将一小块钠投到水中
钠浮在水面上
钠的密度比水小
C
在空气中点燃纯净的H2 , 然后把导管缓慢伸入盛满Cl2的集气瓶中
纯净的H2在Cl2中安静地燃烧,发出苍白色火焰
燃烧不一定需要O2
D
用红色激光笔照射纳米金的水溶液(纳米金指金的微小颗粒)
看到一条光亮的通路
纳米金的水溶液是一种胶体
A、A B、B C、C D、D4. 化学材料的使用对人类生活质量的提高和科技的发展有重要作用,下列说法正确的是( )A、生铁的含碳量为0.03%~2% B、“天和”核心舱电推进系统中的霍尔推力器腔体,使用的氮化硼陶瓷基复合材料属于无机非金属材料 C、T-碳是一种新型三维碳结构晶体,与C60互为同位素 D、“北斗三号”导航卫星使用的太阳能电池材料-砷化镓属于金属材料5. 如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让潮湿的氯气经过甲瓶后,通入乙瓶,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种气体,布条褪色。甲瓶中所盛的试剂不可能是( ) A、浓H2SO4 B、浓NaOH溶液 C、饱和NaCl溶液 D、石灰乳6. 下列既能由金属和氯气直接制取,又能由金属和盐酸直接制取的是( )A、FeCl2 B、NaCl C、FeCl3 D、CuCl27. 下列实验现象与新制氯水中的某些成分(括号内物质)没有关系的是( )A、新制氯水显淡黄绿色(Cl2) B、将NaHCO3固体加入新制氯水中,有无色气泡产生(HClO) C、向新制氯水中滴加石蕊溶液,溶液先变红后褪色(H+、HClO) D、滴加AgNO3溶液有白色沉淀产生(Cl-)8. 下列说法错误的是( )A、O2和O3互为同素异形体 B、KBr→Br2需加入还原剂才能实现 C、钠的焰色试验是物理变化 D、ClO2可用于自来水消毒9. 2021年7月25日,“泉州:宋元中国的世界海洋商贸中心”正式列入《世界遗产名录》。古代丝绸、茶叶、瓷器、铜铁器等从泉州运往世界各地。下列说法错误的是( )A、可用灼烧的方法鉴别丝绸和化学纤维制品 B、泡茶时茶香四溢,体现了分子是运动的 C、烧制陶瓷的过程中不涉及化学变化 D、从赤铁矿冶炼铁的过程中一定有氧化还原反应发生10. “84”消毒液(NaClO溶液)可用于消毒,下列说法正确的是( )A、可用pH试纸测定该消毒液的pH B、NaClO暴露在空气中变质形成HClO C、NaClO溶液漂白原理与活性炭相同 D、“84”消毒液与“洁厕灵"(HCl)混用,效果更佳.11. 下列关于氯气、液氯、新制氯水和久置氯水的叙述正确的是( )A、久置的氯水相当于盐酸 B、液氯和新制氯水均是混合物 C、常温下,氯水和液氯均可用钢罐存放 D、氯气有强氧化性、氯水无氧化性12. 10月16日,搭载神舟十三号载人飞船的长征二号F遥十三运载火箭,在酒泉卫星发射中心点火升空。长征系列运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法错误的是( )A、煤油和液氢都是可再生能源 B、火箭燃料燃烧时,化学能转化为热能 C、运载火箭主体结构件框所用高精尖铝合金材料具有质量轻、强度高等优点 D、液氢属于纯净物,煤油属于混合物13. 关于合成氨工业的说法错误的是( )A、合成氨工业采用循环操作,主要是为了提高氮气和氢气的利用率 B、工业上一般选择400-500℃的主要原因是让铁触媒的活性大,反应速率快 C、从合成氨的原理出发,增大压强既有利于加快速率又有利于平衡右移,但压强增大设备成本大幅度提升,所以实际工业中往往采用常压 D、为了防止催化剂“中毒”,原料气需要经过净化14. 部分含硫物质中的硫元素的价态及该物质的类别关系如图所示。下列说法错误的是( )
A、浓H2SO4 B、浓NaOH溶液 C、饱和NaCl溶液 D、石灰乳6. 下列既能由金属和氯气直接制取,又能由金属和盐酸直接制取的是( )A、FeCl2 B、NaCl C、FeCl3 D、CuCl27. 下列实验现象与新制氯水中的某些成分(括号内物质)没有关系的是( )A、新制氯水显淡黄绿色(Cl2) B、将NaHCO3固体加入新制氯水中,有无色气泡产生(HClO) C、向新制氯水中滴加石蕊溶液,溶液先变红后褪色(H+、HClO) D、滴加AgNO3溶液有白色沉淀产生(Cl-)8. 下列说法错误的是( )A、O2和O3互为同素异形体 B、KBr→Br2需加入还原剂才能实现 C、钠的焰色试验是物理变化 D、ClO2可用于自来水消毒9. 2021年7月25日,“泉州:宋元中国的世界海洋商贸中心”正式列入《世界遗产名录》。古代丝绸、茶叶、瓷器、铜铁器等从泉州运往世界各地。下列说法错误的是( )A、可用灼烧的方法鉴别丝绸和化学纤维制品 B、泡茶时茶香四溢,体现了分子是运动的 C、烧制陶瓷的过程中不涉及化学变化 D、从赤铁矿冶炼铁的过程中一定有氧化还原反应发生10. “84”消毒液(NaClO溶液)可用于消毒,下列说法正确的是( )A、可用pH试纸测定该消毒液的pH B、NaClO暴露在空气中变质形成HClO C、NaClO溶液漂白原理与活性炭相同 D、“84”消毒液与“洁厕灵"(HCl)混用,效果更佳.11. 下列关于氯气、液氯、新制氯水和久置氯水的叙述正确的是( )A、久置的氯水相当于盐酸 B、液氯和新制氯水均是混合物 C、常温下,氯水和液氯均可用钢罐存放 D、氯气有强氧化性、氯水无氧化性12. 10月16日,搭载神舟十三号载人飞船的长征二号F遥十三运载火箭,在酒泉卫星发射中心点火升空。长征系列运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法错误的是( )A、煤油和液氢都是可再生能源 B、火箭燃料燃烧时,化学能转化为热能 C、运载火箭主体结构件框所用高精尖铝合金材料具有质量轻、强度高等优点 D、液氢属于纯净物,煤油属于混合物13. 关于合成氨工业的说法错误的是( )A、合成氨工业采用循环操作,主要是为了提高氮气和氢气的利用率 B、工业上一般选择400-500℃的主要原因是让铁触媒的活性大,反应速率快 C、从合成氨的原理出发,增大压强既有利于加快速率又有利于平衡右移,但压强增大设备成本大幅度提升,所以实际工业中往往采用常压 D、为了防止催化剂“中毒”,原料气需要经过净化14. 部分含硫物质中的硫元素的价态及该物质的类别关系如图所示。下列说法错误的是( ) A、 微溶于酒精,易溶于 B、向 的溶液中通入 ,可产生淡黄色沉淀 C、滴加 溶液,即可鉴别 、 两种溶液 D、在一定条件下,可实现 的转化15. 2020年12月17日,嫦娥五号探测器携带着珍贵的月球“土特产”——月壤成功返回,研究表明月壤包含微细的矿物颗粒、岩石碎屑和玻璃质微粒等,主要由氧、硅、铝、铁、镁钙、钠、钾、钛等元素构成。下列相关化学用语正确的是( )A、 和 是氧的两种不同的同素异形体 B、 核外有m个电子、n个中子,X原子符号为 C、钾原子的原子结构示意图为:
A、 微溶于酒精,易溶于 B、向 的溶液中通入 ,可产生淡黄色沉淀 C、滴加 溶液,即可鉴别 、 两种溶液 D、在一定条件下,可实现 的转化15. 2020年12月17日,嫦娥五号探测器携带着珍贵的月球“土特产”——月壤成功返回,研究表明月壤包含微细的矿物颗粒、岩石碎屑和玻璃质微粒等,主要由氧、硅、铝、铁、镁钙、钠、钾、钛等元素构成。下列相关化学用语正确的是( )A、 和 是氧的两种不同的同素异形体 B、 核外有m个电子、n个中子,X原子符号为 C、钾原子的原子结构示意图为: D、一种月壤辉长岩成分为 ,用氧化物的形式表示其组成为
16. 利用如图装置进行Cl2制备及其化学性质的探究。下列说法错误的是( )
D、一种月壤辉长岩成分为 ,用氧化物的形式表示其组成为
16. 利用如图装置进行Cl2制备及其化学性质的探究。下列说法错误的是( ) A、拉动a或b的活塞,可检查装置气密性 B、c中反应的氧化产物与还原产物的质量比为6:1 C、c中产生Cl2后,d褪色的原因是次氯酸具有漂白性 D、性质实验结束后,加入b中溶液除去多余的Cl2 , 溶液由红色变为无色17. 下列反应的离子方程式书写正确的是( )A、金属铝溶于氢氧化钠溶液:Al+2OH =AlO+H2 B、用氢氧化钠溶液吸收少量二氧化碳:OH + CO2 =HCO3 C、向饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液: Ca2+ + HCO+ OH= CaCO3 +H2O D、向硫酸铁酸性溶液中通入足量硫化氢: 2Fe3++S2-=2Fe2++S18. 甲、乙、丙三种不同的物质中均含有同一种元素,反应④为置换反应,往乙溶液中滴加KSCN 溶液,乙溶液变为红色。它们之间的转化关系如图所示(部分反应物及生成物已略去)。下列说法 错误的是( )
A、拉动a或b的活塞,可检查装置气密性 B、c中反应的氧化产物与还原产物的质量比为6:1 C、c中产生Cl2后,d褪色的原因是次氯酸具有漂白性 D、性质实验结束后,加入b中溶液除去多余的Cl2 , 溶液由红色变为无色17. 下列反应的离子方程式书写正确的是( )A、金属铝溶于氢氧化钠溶液:Al+2OH =AlO+H2 B、用氢氧化钠溶液吸收少量二氧化碳:OH + CO2 =HCO3 C、向饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液: Ca2+ + HCO+ OH= CaCO3 +H2O D、向硫酸铁酸性溶液中通入足量硫化氢: 2Fe3++S2-=2Fe2++S18. 甲、乙、丙三种不同的物质中均含有同一种元素,反应④为置换反应,往乙溶液中滴加KSCN 溶液,乙溶液变为红色。它们之间的转化关系如图所示(部分反应物及生成物已略去)。下列说法 错误的是( ) A、反应① 、②可能为化合反应 B、反应④的另一反应物可以为某种盐的水溶液 C、甲为金属单质,也可能为非金属单质 D、若甲为金属单质,甲、乙、丙中的相同元素化合价不同
A、反应① 、②可能为化合反应 B、反应④的另一反应物可以为某种盐的水溶液 C、甲为金属单质,也可能为非金属单质 D、若甲为金属单质,甲、乙、丙中的相同元素化合价不同二、多选题
-
19. 实现氨按照一定方向转化一直是科学领域研究的重要课题,如图为 分子在催化剂的作用下发生的一系列转化示意图:

下列叙述正确的是( )
A、改变两个反应使用的催化剂,其转化率不变 B、两个反应的原子利用率均为100% C、合成氨反应 ,降低温度将缩短反应达到平衡的时间 D、催化剂 表面反应生成NO时有电子转移20. 某同学研究浓硝酸与 溶液的反应,进行如下实验: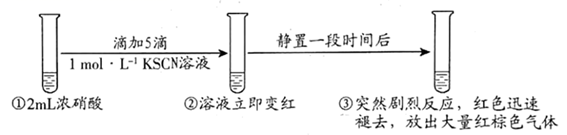
已知: 能被氧化为黄色的 可聚合为红色的 。
下列分析错误的是( )
A、②中溶液变红,是由于生成了 B、取少量③中的溶液加入 溶液,产生白色沉淀,证明最终有 生成 C、分析①②知,硝酸氧化 的速率大于 聚合为 ,的速率 D、向溶有 的浓硝酸中加几滴 溶液,溶液先变红后迅速褪色并产生大量红棕色气体,证明 催化浓硝酸氧化 ,的反应21. 某溶液中只可能含有 中的几种离子,各离子浓度均为 。某同学进行了如图实验: 下列说法错误的是( )A、无法确定原溶液中是否含有 B、原溶液中肯定存在的离子为 C、沉淀A为 ,沉淀C为 D、滤液X中大量存在的阳离子有 和22. 下列有关实验操作对应的现象﹑解释或结论都正确的是( )
下列说法错误的是( )A、无法确定原溶液中是否含有 B、原溶液中肯定存在的离子为 C、沉淀A为 ,沉淀C为 D、滤液X中大量存在的阳离子有 和22. 下列有关实验操作对应的现象﹑解释或结论都正确的是( )选项
实验操作
现象
解释或结论
A
向酸性 溶液中通入
溶液紫色褪去
具有还原性
B
将常温下用冷的浓硝酸处理过的铝片插入硫酸铜溶液中
铝片表面无明显现象
用硝酸处理后,铝的金属性减弱
C
向试管中加入5mL10% 溶液,然后滴加5滴5%NaOH溶液,再向所得悬浊液中滴加葡萄糖溶液,加热煮沸
试管内产生砖红色沉淀
葡萄糖分子中含有醛基
D
向新制氯水中加入足量碳酸钙固体,然后用玻璃棒蘸取溶液于pH试纸上
氯水颜色变浅,pH试纸颜色褪去
加入碳酸钙后,氯水中的HCl被消耗,平衡 向右移动,HClO浓度增大,且HClO具有漂白性
A、A B、B C、C D、D23. 某科研小组为了探究久置空气中某浓度氢氧化钠溶液(250mL)的组分,往溶液中滴入2mol·L-1的稀盐酸,反应中生成CO2的物质的量随加入稀盐酸的体积如图所示,下列说法正确的是( ) A、当V1>100时,NaOH溶液未完全变质 B、a点存在c(Na+)+c(H+)=2c(CO )+c(HCO )+c(OH-) C、氢氧化钠溶液未变质前c(NaOH)=1.6mol·L-1 D、O~b点溶液中存在两种溶质
A、当V1>100时,NaOH溶液未完全变质 B、a点存在c(Na+)+c(H+)=2c(CO )+c(HCO )+c(OH-) C、氢氧化钠溶液未变质前c(NaOH)=1.6mol·L-1 D、O~b点溶液中存在两种溶质三、填空题
-
24. 某化学兴趣小组设计了如图装置,该装置能制取 Cl2 , 并进行相关性质实验,且可利用装置A 储存多余的氯气。
 (1)、A 中发生反应的化学方程式为。(2)、储气瓶 b 可以收集氯气,则 B 内盛放的试剂是;装置 E 中球形干燥管的作用是。(3)、在装置 D 中能看到的实验现象是;此现象可推断氧化性:Cl2I2(填“>”或“<”)(4)、装置 C 中 Fe 2+ 被 Cl2氧化为 Fe 3+ ,反应的离子方程式为。25. 某化学兴趣小组设计以下装置来验证Cl2的性质。
(1)、A 中发生反应的化学方程式为。(2)、储气瓶 b 可以收集氯气,则 B 内盛放的试剂是;装置 E 中球形干燥管的作用是。(3)、在装置 D 中能看到的实验现象是;此现象可推断氧化性:Cl2I2(填“>”或“<”)(4)、装置 C 中 Fe 2+ 被 Cl2氧化为 Fe 3+ ,反应的离子方程式为。25. 某化学兴趣小组设计以下装置来验证Cl2的性质。
①装置A中的现象是 , 出现此现象的原因是(用化学方程式和文字解答)。
②装置B的作用是。
③装置C与装置D中的现象是否相同(填“是”或“否” ),根据装置C和D中的现象可以得到的结论是。
④装置E的作用是吸收尾, E中发生反应的化学方程式为。
26.(1)、亚磷酸(H3PO3)为二元弱酸。H3PO3中P元素的化合价为 , 其在元素周期表的位置是 , H3PO3与过量NaOH溶液反应的离子方程式为。(2)、三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
①在图示的转化中,被还原的元素是 , X的化学式为。
②SCR技术可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的量之比为2:1时,写出发生反应的化学方程式:。
四、实验探究题
-
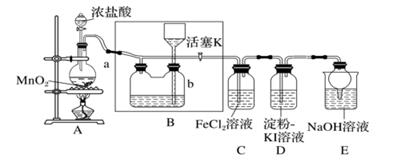
27. 实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:
 (1)、A中盛有浓盐酸,B中盛有MnO2 , 写出反应的离子方程式:。(2)、E中为红色干布条,F中为红色湿布条,可观察到的现象是。对比E和F中现象的差异可得出的结论及解释是。(3)、试管C和D中试剂各为。(4)、装置G处发生反应的离子方程式为。(5)、用离子方程式表示试剂X的作用:。(6)、家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
(1)、A中盛有浓盐酸,B中盛有MnO2 , 写出反应的离子方程式:。(2)、E中为红色干布条,F中为红色湿布条,可观察到的现象是。对比E和F中现象的差异可得出的结论及解释是。(3)、试管C和D中试剂各为。(4)、装置G处发生反应的离子方程式为。(5)、用离子方程式表示试剂X的作用:。(6)、家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。注意事项:
1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。
2.密封保存,请勿与洁厕灵同时使用。
3.保质期为一年
“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:。
28. 鱼浮灵主要成分为过碳酸钠(2Na2CO3•3H2O2)是水产养殖的速效增氧剂信息:①过碳酸钠具有Na2CO3和H2O2的双重性质,50℃开始分解
②2Na2CO3(aq)+3H2O2(aq)=2Na2CO3•3H2O2(aq)△H<0
③过碳酸钠在异丙醇中的溶解度较低
实验室用Na2CO3与稳定剂的混合液和H2O2化合制备过碳酸钠,制备装置如图。
 (1)、冷凝管中冷凝水的进口是(填“a”或“b”),恒压滴液漏斗中盛装的药品是。(2)、实验测定反应温度对产物的影响如表所示,根据表中数据可以得知最佳的反应温度为15—20℃,请说明选择该温度的理由是。
(1)、冷凝管中冷凝水的进口是(填“a”或“b”),恒压滴液漏斗中盛装的药品是。(2)、实验测定反应温度对产物的影响如表所示,根据表中数据可以得知最佳的反应温度为15—20℃,请说明选择该温度的理由是。t/℃
活性氧百分含量/%
产率/%
5~10
13.94
85.49
10~15
14.02
85.78
15~20
15.05
88.38
20~25
14.46
83.01
(3)、反应结束后,停止搅拌,( ),( ),( ),( ),干燥得到产品,从下列选项中选出合理的操作(操作不能重复使用)并排序。a.蒸发溶剂至100℃,冷却结晶
b.蒸发至大量晶体析出,用余热蒸干
c.加入异丙醇
d.用异丙醇溶液洗涤
e.用饱和碳酸钠溶液洗涤
f.抽滤
g.加入氯化钠晶体
h.静置
(4)、过碳酸钠成分的测定:①取适量过氧碳酸钠样品,用蒸馏水溶解后转移至250mL容量瓶中,定容,摇匀
②用移液管移取25.00mL于锥形瓶中,加入2-3滴甲基橙,用0.2000mol•L-1硫酸标准溶液滴定至终点。重复操作2-3次,记录数据。
③用移液管移取12.50mL于锥形瓶中,加入足量稀硫酸,用0.0200mol•L-1KMnO4标准溶液滴定至终点。重复操作2-3次,记录数据。
经计算发现过氧碳酸钠中碳酸钠与双氧水的比例大于2:3,引起上述结果可能的原因有___。
A、干燥产品时采用了加热烘干的方式 B、上述步骤②操作过程中,滴定完成后,俯视滴定管 C、上述步骤③滴定操作前润洗了滴定管和锥形瓶 D、上述步骤③滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡(5)、某小组在常温下进行H2O2在不同pH下,相同时间内溶解氧含量测定的实验,数据记录如表:试剂
H2O2
H2O2+NaCl
H2O2+Na2CO3
H2O2+NaOH
H2O2+NaOH
pH
6.01
5.97
8.14
8.15
9.26
溶解氧
6.44
6.48
9.11
9.12
10.97
结合以上数据分析“鱼浮灵”溶于水后在水产养殖中速效增氧的原理是。
五、综合题
-
29. 人类的生活离不开化学反应,在关注反应物质变化的同时也要关注能量变化。(1)、Ⅰ.金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,氧气充足时燃烧生成二氧化碳,反应中放出的热量如图所示。

在通常状况下,(填“金刚石”或“石墨”)更稳定;石墨的燃烧热ΔH为
(2)、若12 g金刚石在24 g氧气中燃烧,生成气体36 g,则该过程放出的热量为。(3)、已知:N2、O2分子中化学键的键能分别是946 mol·L-1、497 mol·L-1 , N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ·mol-1 , 综合上述有关信息请写出CO和NO反应生成两种无毒气体的热化学方程式:(4)、Ⅱ.Cl、C、Si在工业生产、生活中有重要应用用液氯消毒自来水会产生微量有机氯代物,危害人体健康,可使用二氧化氯(ClO2)代替液氯工业上以黄铁矿(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯。已知黄铁矿中的硫元素( 价)被氧化成SO42- , 制备二氧化氯的离子方程式为。
(5)、下列关于C、Si元素及化合物的说法中正确的是A、碳纳米材料包括:富勒烯、碳纳米管、石墨烯、炭黑 B、云母、沙土、宝石的主要成分为二氧化硅 C、工业制水泥、玻璃的主要原料中都有碳酸钙 D、实验室中氢氟酸能用玻璃瓶盛装但不能用玻璃塞 E、氮化硅熔点高,硬度大,电绝缘性好可用于制作坩埚、耐高温轴承、制作切削刀具30. 疫情期间,某项目化学学习小组开展了对84消毒液使用安全性的研究。查找资料可知:①84消毒液有效成分为NaClO。含氯消毒剂中HCO的消毒效果远高于ClO- , 而ClO-的稳定性要高于HClO。
②HClO的K=2.0×10-8;H2CO3的K1=4.3×10-7 , K2=5.6×10-11。
请回答下列问题:
(1)、在84消毒液中滴加几滴酚酞试液,可观察到的现象是。(2)、通常购买的84消毒液pH在12左右,目的是增强消毒液的稳定性,试从平衡的角度分析原因。(3)、84消毒液必须避光密封保存,目的是防止与空气中的二氧化碳反应而变质,试写出该反应的离子方程式:。(4)、为了研究消毒效果,同学们测定了84消毒液中Cl2、HClO和ClO-三种微粒的物质的量分数随pH变化的关系,如图所示。
根据图示同学们认为在使用84消毒液时应调节pH在4~6范围内,试说明原因。
(5)、84消毒液还可作为水处理剂除去水中的杂质离子。例如过量次氯酸钠可使酸性废水中 完全转化为N2 , 请写出相应的离子反应方程式:。若处理废水产生了0.448LN2(标准状况),则需消耗有效氯为5%的84消毒液的质量为g。(“有效氯”指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力,常以百分数表示)