陕西省西安市蓝田县2020-2021学年高一下学期期末质量监测化学试题
试卷更新日期:2021-12-27 类型:期末考试
一、单选题
-
1. 化学与生产、生活息息相关。下列说法错误的是( )A、废旧电池不能填埋、不能焚烧,必须单独收集和处理 B、塑料在自然条件下不易分解,会造成“白色污染” C、催化合成甲酸: , 符合绿色化学的“原子经济”理念 D、石油的分馏、裂化、裂解均属于化学变化2. 下列含有非极性键的化合物是( )A、 B、 C、 D、3. 工业上不宜用电解法制备的金属是( )A、Na B、Mg C、Al D、Fe4. 下列化学用语错误的是( )A、苯的比例模型:
 B、丙烷的球棍模型:
B、丙烷的球棍模型: C、中子数为20的的核素:
D、次氯酸的结构式:
5. 下列有关颜色变化的说法错误的是( )A、葡萄糖溶液中加入新制的氢氧化铜,加热至沸腾,观察到砖红色沉淀 B、将苯加入酸性高锰酸钾溶液中,溶液紫色褪去 C、向乙酸中加入紫色石蕊试液,溶液变红 D、在鸡蛋清溶液中加入浓 , 微热后会生成黄色物质6. 如图所示,为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法错误的是( )
C、中子数为20的的核素:
D、次氯酸的结构式:
5. 下列有关颜色变化的说法错误的是( )A、葡萄糖溶液中加入新制的氢氧化铜,加热至沸腾,观察到砖红色沉淀 B、将苯加入酸性高锰酸钾溶液中,溶液紫色褪去 C、向乙酸中加入紫色石蕊试液,溶液变红 D、在鸡蛋清溶液中加入浓 , 微热后会生成黄色物质6. 如图所示,为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法错误的是( ) A、过程①将太阳能转换成化学能 B、电能属于一次能源 C、能量利用率:燃料电池比直接燃烧高 D、过程②将化学能转换为电能7. 下列说法正确的是( )A、油脂在酸性条件下水解可制得肥皂 B、淀粉与纤维素的分子式均为 , 互为同分异构体 C、可用灼烧的方法来鉴别蚕丝和棉麻织物 D、乙酸分子中含有羧基,乙酸的酸性比碳酸弱8. 把A、B、C三种金属浸人稀硫酸中,用导线两两相连可以组成各种原电池。若A、B相连,A上有气泡逸出;B、C相连,C的质量减少。则A、B、C三种金属的活动性顺序是( )A、B>A>C B、A>B>C C、C>B>A D、C>A>B9. 下列关于碱金属元素的单质及其化合物说法错误的是( )A、锂与水反应不如钠与水反应剧烈 B、在氧气中燃烧生成 C、熔、沸点: D、碱性:氢氧化铯>氢氧化钠10. 下列有关化学反应的说法正确的是( )A、把食物放入冰箱内,可减缓食物腐败的速率 B、铝粉与需要在高温下反应,所以该反应是吸热反应 C、蜡烛燃烧过程中,只有化学能转化为热能的能量变化 D、品红溶液中通入褪色,加热后又恢复红色属于可逆反应11. 根据(g)与(g)发生反应生成(g)过程中的能量变化示意图,下列说法正确的是( )
A、过程①将太阳能转换成化学能 B、电能属于一次能源 C、能量利用率:燃料电池比直接燃烧高 D、过程②将化学能转换为电能7. 下列说法正确的是( )A、油脂在酸性条件下水解可制得肥皂 B、淀粉与纤维素的分子式均为 , 互为同分异构体 C、可用灼烧的方法来鉴别蚕丝和棉麻织物 D、乙酸分子中含有羧基,乙酸的酸性比碳酸弱8. 把A、B、C三种金属浸人稀硫酸中,用导线两两相连可以组成各种原电池。若A、B相连,A上有气泡逸出;B、C相连,C的质量减少。则A、B、C三种金属的活动性顺序是( )A、B>A>C B、A>B>C C、C>B>A D、C>A>B9. 下列关于碱金属元素的单质及其化合物说法错误的是( )A、锂与水反应不如钠与水反应剧烈 B、在氧气中燃烧生成 C、熔、沸点: D、碱性:氢氧化铯>氢氧化钠10. 下列有关化学反应的说法正确的是( )A、把食物放入冰箱内,可减缓食物腐败的速率 B、铝粉与需要在高温下反应,所以该反应是吸热反应 C、蜡烛燃烧过程中,只有化学能转化为热能的能量变化 D、品红溶液中通入褪色,加热后又恢复红色属于可逆反应11. 根据(g)与(g)发生反应生成(g)过程中的能量变化示意图,下列说法正确的是( ) A、(g)和(g)的总能量大于(g)的总能量 B、通常情况下,该反应发生的条件是加热或光照 C、过程Ⅰ与Ⅱ放出能量 D、过程Ⅲ吸收能量12. 下列有关装置的说法正确的是( )
A、(g)和(g)的总能量大于(g)的总能量 B、通常情况下,该反应发生的条件是加热或光照 C、过程Ⅰ与Ⅱ放出能量 D、过程Ⅲ吸收能量12. 下列有关装置的说法正确的是( )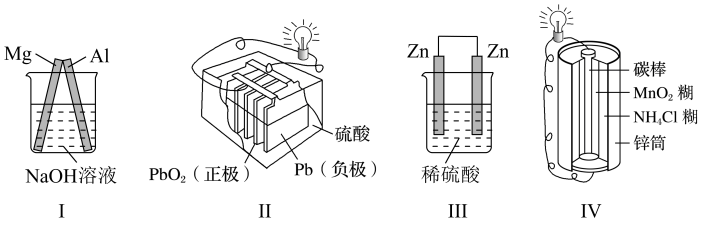 A、装置Ⅰ中为原电池的负极 B、装置Ⅱ为一次电池 C、装置Ⅲ可构成原电池 D、装置Ⅳ工作时,电子由锌通过导线流向碳棒13. 某烷烃的相对分子质量为114,则该烷烃的同分异构体中,主链有5个碳原子的结构有( )A、3种 B、4种 C、5种 D、6种14. 下列除杂方案错误的是( )
A、装置Ⅰ中为原电池的负极 B、装置Ⅱ为一次电池 C、装置Ⅲ可构成原电池 D、装置Ⅳ工作时,电子由锌通过导线流向碳棒13. 某烷烃的相对分子质量为114,则该烷烃的同分异构体中,主链有5个碳原子的结构有( )A、3种 B、4种 C、5种 D、6种14. 下列除杂方案错误的是( )选项
被提纯的物质
杂质
除杂试剂
除杂方法
A
苯
乙酸
溶液
分液
B
乙烷
乙烯
酸性溶液
洗气
C
乙烯
溶液
洗气
D
乙醇
水
蒸馏
A、A B、B C、C D、D15. W、X、Y和Z为原子序数依次增大的四种短周期主族元素。W与X可生成一种红棕色有刺激性气味的气体,Y的周期数是族序数的3倍,Z原子最外层电子数与W的电子总数相同。下列叙述正确的是( )A、原子半径: B、Y与X形成的化合物都只含有离子键 C、四种元素的简单离子具有相同的电子层结构 D、Z的氧化物对应的水化物均为强酸16. 下列与乙醇相关实验的说法错误的是( ) A、实验①中,在铜丝的中间部分加热,片刻后开始有节奏地鼓入空气,可观察到铜丝中间部分出现黑红交替的现象 B、实验②中增加烧瓶上方的导管长度,可减少原料的损失 C、实验②中若用和发生酯化反应,则乙酸乙酯中不含 D、实验③中,乙醇和金属钠的反应并不剧烈,钠粒逐渐变小,产生的气体具有可燃性
A、实验①中,在铜丝的中间部分加热,片刻后开始有节奏地鼓入空气,可观察到铜丝中间部分出现黑红交替的现象 B、实验②中增加烧瓶上方的导管长度,可减少原料的损失 C、实验②中若用和发生酯化反应,则乙酸乙酯中不含 D、实验③中,乙醇和金属钠的反应并不剧烈,钠粒逐渐变小,产生的气体具有可燃性二、综合题
-
17. 是工业制硫酸的主要反应之一,研究该反应的速率和限度有着重要的现实意义。
 (1)、反应过程的能量变化如图所示,该反应为(填“放热”或“吸热”)反应。(2)、一定条件下,在2L的密闭容器中加入(g)、(g)和(g)发生上述反应,在末达到平衡,测得。
(1)、反应过程的能量变化如图所示,该反应为(填“放热”或“吸热”)反应。(2)、一定条件下,在2L的密闭容器中加入(g)、(g)和(g)发生上述反应,在末达到平衡,测得。①内的平均反应速率。
②末。
③若其他条件不变,将容器的容积扩大至3L,该化学反应速率将(填“增大”、“不变”或“减小”)。
④恒温恒容下,能说明该反应达到化学平衡状态的是(填字母)。
a. b. c.混合气体的压强不再变化 d.不再变化 e.单位时间内生成的同时生成
18. 按要求回答下列问题:(1)、Ⅰ.某同学依据反应设计的原电池如图所示。
负极上发生的电极反应为。
(2)、溶液中流向(填“”或“”)电极。(3)、当反应进行一段时间后取出电极材料,测得某一电极增重了5.4g,则反应中转移的电子数目是。(4)、Ⅱ.海带中含有非富的确元素,某化学研究性学习小组用如图流程从海带中提取碘:
步骤①灼烧海带时,除需要三脚架、泥三角、酒精灯外,还需要用到的实验仪器是____(填字母)。
A、烧杯 B、蒸发皿 C、坩埚 D、干燥器:(5)、步骤③、⑥的实验操作名称分别是、。步骤⑤中,除选择用苯来提取碘,还可选择的试剂是(填字母)。A.酒精 B.醋酸 C.四氯化碳
19. 乙烯和苯是来自石油和煤的两种重要化工原料。(1)、乙烯在一定条件下与水反应可以生成乙醇,写出该反应的化学方程式 , 反应类型为。(2)、聚乙烯塑料常用于制作食品包装袋,写出聚乙烯的结构简式。(3)、有关苯的转化关系如图所示,请回答下列问题:
①反应Ⅰ、Ⅱ、Ⅲ、Ⅳ中属于取代反应的是(填序号)。
②反应Ⅰ的化学方程式为。若将苯倒入盛有溴水的试管中,振荡后静置,现象是。
③反应Ⅲ中有机产物的结构简式为:。
④反应Ⅳ中苯能与反应生成环己烷。
20. 如图是部分短周期主族元素的原子序数与其最高或最低化合价的关系图(用原子序数代表所对应的元素),已知a为元素周期表中相对原子质量最小的元素,请回答下列问题: (1)、b在元素周期表中的位置是;元素e和g组成的化合物的电子式为。(2)、d、f、g、h四种元素的简单离子半径由大到小的顺序为(用离子符号表示)。
(1)、b在元素周期表中的位置是;元素e和g组成的化合物的电子式为。(2)、d、f、g、h四种元素的简单离子半径由大到小的顺序为(用离子符号表示)。