2022届中考科学第一轮专题复习:元素符号与化学式
试卷更新日期:2021-12-01 类型:一轮复习
一、单选题
-
1. 下列各物质的俗称和化学式表示的是同一种物质的是( )A、消石灰 CaO B、纯碱 NaOH C、石灰石 CaCO3 D、生石灰 Ca(OH)22. 我国古代将炉甘石( )、赤铜( )和木炭混合加热至800℃,得到一种外形似金子的锌铜合金(俗称黄铜)。下列说法正确的是( )A、 铜的化合价为+2价 B、黄铜熔点比铜与锌的熔点都低 C、该变化过程中有化合反应 D、通过观察颜色可鉴别金子与黄铜3. 下列选项中,物质的名称、俗名、化学式不完全一致的是( )A、碳酸钠—纯碱— B、亚硝酸钠—食盐— C、氢氧化钙—消石灰— D、氢氧化钠—烧碱—4. 近年来有人提出了利用处理后的海水(主要成分是氯化钠溶液)吸收含二氧化硫的废气 ,该方法的流程如图所示。下列说法正确的是( )
 A、反应中硫元素的化合价发生变化 B、图中反应①属于分解反应 C、反应③中,反应前后分子数目没有变化 D、反应④中的反应物是两种酸5. 归纳法是学习化学的重要方法之一,下列图示正确的是( )A、化学反应分类
A、反应中硫元素的化合价发生变化 B、图中反应①属于分解反应 C、反应③中,反应前后分子数目没有变化 D、反应④中的反应物是两种酸5. 归纳法是学习化学的重要方法之一,下列图示正确的是( )A、化学反应分类 B、金属的化学性质
B、金属的化学性质  C、地壳中元素含量
C、地壳中元素含量  D、物质分类
D、物质分类  6. 如图是一种防霾新产品——鼻用空气净化器,它的填充物是硅胶(SiO2•nH2O),对PM2.5吸收率高达99%,下列说法正确的是( )
6. 如图是一种防霾新产品——鼻用空气净化器,它的填充物是硅胶(SiO2•nH2O),对PM2.5吸收率高达99%,下列说法正确的是( ) A、从组成元素种类分析,SiO2•nH2O是混合物 B、SiO2•nH2O中Si的化合价为+2价 C、该净化器不宜用碱性洗涤剂清洗 D、硅胶由一个硅原子,2n个氢原子,(2+n)个氧原子构成7. 洛阳师范学院开发了一种用于吸附处理有毒物质的新型多孔材料,特别是对铬酸钠(Na2CrO4)的处理效果最好,铬酸钠中的铬(Cr)元素是水污染控制的一项重要指标。下列相关叙述正确的是( )A、Cr的单质是一种金属 B、Cr有毒,若回收是毫无意义的 C、Na2CrO4中的Cr的化合价是-6价 D、Na2CrO4是氧化物8. 氢氧化铯是一种可溶性碱,其化学式为CsOH,则下列叙述中正确的是( )A、CsOH 溶液的pH小于7 B、CsOH 和CuO能发生化学反应 C、CsOH 溶液能使酚酞试液变蓝 D、CsOH 中Cs元素化合价为+1价9. 据报道,中小学生喜欢使用的涂改液中,含有许多挥发性的有害物质,长期使用易引起慢性中毒而头晕、头痛,二氯甲烷就是其中的一种,下列关于二氯甲烷(CH2Cl2)组成的叙述中,正确的是( )A、二氯甲烷是由碳、氢气和氯气组成的 B、二氯甲烷是由碳、氢和氯三种元素组成的 C、二氯甲烷是由一个碳原子、一个氢分子和一个氯分子组成的 D、二氯甲烷是由一个碳原子、两个氢原子和两个氯原子组成的10. 将 Fe3O4、Fe2O3、CuO的固体混合粉末mg,在加热条件下用足量CO还原得到金属混合物2.32g,将生成的CO2气体用足量澄清石灰水吸收后,产生5.00g白色沉淀,则m的数值为( )A、5.32 B、3.12 C、3.59 D、2.3711. 在化学王国里,数字被赋予了丰富的内涵.对下列化学用语中数字“2”的说法正确的是( )
A、从组成元素种类分析,SiO2•nH2O是混合物 B、SiO2•nH2O中Si的化合价为+2价 C、该净化器不宜用碱性洗涤剂清洗 D、硅胶由一个硅原子,2n个氢原子,(2+n)个氧原子构成7. 洛阳师范学院开发了一种用于吸附处理有毒物质的新型多孔材料,特别是对铬酸钠(Na2CrO4)的处理效果最好,铬酸钠中的铬(Cr)元素是水污染控制的一项重要指标。下列相关叙述正确的是( )A、Cr的单质是一种金属 B、Cr有毒,若回收是毫无意义的 C、Na2CrO4中的Cr的化合价是-6价 D、Na2CrO4是氧化物8. 氢氧化铯是一种可溶性碱,其化学式为CsOH,则下列叙述中正确的是( )A、CsOH 溶液的pH小于7 B、CsOH 和CuO能发生化学反应 C、CsOH 溶液能使酚酞试液变蓝 D、CsOH 中Cs元素化合价为+1价9. 据报道,中小学生喜欢使用的涂改液中,含有许多挥发性的有害物质,长期使用易引起慢性中毒而头晕、头痛,二氯甲烷就是其中的一种,下列关于二氯甲烷(CH2Cl2)组成的叙述中,正确的是( )A、二氯甲烷是由碳、氢气和氯气组成的 B、二氯甲烷是由碳、氢和氯三种元素组成的 C、二氯甲烷是由一个碳原子、一个氢分子和一个氯分子组成的 D、二氯甲烷是由一个碳原子、两个氢原子和两个氯原子组成的10. 将 Fe3O4、Fe2O3、CuO的固体混合粉末mg,在加热条件下用足量CO还原得到金属混合物2.32g,将生成的CO2气体用足量澄清石灰水吸收后,产生5.00g白色沉淀,则m的数值为( )A、5.32 B、3.12 C、3.59 D、2.3711. 在化学王国里,数字被赋予了丰富的内涵.对下列化学用语中数字“2”的说法正确的是( )①2H ②2NH3 ③SO2 ④ ⑤Mg2+ ⑥2OHˉ ⑦H2O.
A、表示离子个数的是⑤⑥ B、表示离子所带电荷数的是④⑤ C、表示分子中原子个数的是③⑦ D、表示分子个数的是①②12. 高铼酸钠(NaReO4)是稀有金属铼(Re)的重要来源之一。高铼酸钠中铼元素的化合价是( )A、+1 B、+7 C、-1 D、-713. 下列物质的名称、俗名与化学式完全正确的是( )A、氯化钠 食盐 NaCl2 B、碳酸氢钠 纯碱 NaHCO3 C、氢氧化钙 熟石灰 CaO D、氢氧化钠 火碱 NaOH14. 市场上销售的一种食用盐——竹盐,其中富含钙、镁、锌、硒、铁等。这里的钙、镁、锌、硒、铁是指( )A、分子 B、原子 C、元素 D、单质15. 下列推理不正确的是 ( )①燃烧过程中伴随着发光放热,所以有发光放热现象的变化一定是燃烧
②分子可以构成物质,所以物质一定由分子构成的
③单质只含一种元素,所以含一种元素的物质一定是单质
④物理变化没有新物质生成,所以没有新物质生成的变化一定是物理变化
⑤同种元素质子数相同,所以质子数相同的粒子一定是同种元素
A、③ ⑤ B、① ② ⑤ C、① ③ ④ D、① ② ③ ⑤16. 维生素B12是人体不可或缺的物质,其中所含的元素钴,也能促使血红蛋白的合成及红细胞数目的增加。已知钴是第27号元素,常见化合价为+2和+3。以下关于这种元素认识正确的是( )A、钴元素属于非金属元素 B、符号Co同时可以表示一氧化碳 C、一个Co3+中含有24个电子 D、用放大镜能观察到元素钴促进红细胞增加的过程17. 工业上可以用甲烷制合成气,如图所示是反应的微观示意图。下列说法不正确的是( ) A、图中甲为甲烷,化学式为CH4 B、乙和丙都属于氧化物
A、图中甲为甲烷,化学式为CH4 B、乙和丙都属于氧化物
C、参加反应的甲和乙的质量比是5:3 D、生成的丙和丁的分子个数比为1:318. 诺贝尔化学奖的成果之一是对CO催化过程的研究,即一氧化碳在铂催化剂作用下的反应,这一过程可以表示为:① CO COad , ② O2
COad , ② O2  2Oad , ③ COad + Oad→CO2(式中标有ad的表示吸附在金属铂表面的原子或分子),下列说法错误的是( ) A、经过过程①②③后,铂的质量和化学性质都不变 B、经过这个化学变化,碳元素的化合价发生改变 C、一氧化碳在铂催化剂作用下发生的这个反应属于化合反应 D、一氧化碳在铂催化剂作用下的反应原理可应用于汽车尾气处理,但会造成酸雨危害19. 下列关于“2”的含义的解释中,正确的是( )A、NO2 中的“2”表示1个二氧化氮分子中含有2个氧元素 B、H2SO4中的化学式中的2表示一个氢分子中的两个氢原子 C、H2O中的“2”表示一个水分子中含有二个氢原子 D、Cu2+中的“2+”表示铜原子的化合价为+2价
2Oad , ③ COad + Oad→CO2(式中标有ad的表示吸附在金属铂表面的原子或分子),下列说法错误的是( ) A、经过过程①②③后,铂的质量和化学性质都不变 B、经过这个化学变化,碳元素的化合价发生改变 C、一氧化碳在铂催化剂作用下发生的这个反应属于化合反应 D、一氧化碳在铂催化剂作用下的反应原理可应用于汽车尾气处理,但会造成酸雨危害19. 下列关于“2”的含义的解释中,正确的是( )A、NO2 中的“2”表示1个二氧化氮分子中含有2个氧元素 B、H2SO4中的化学式中的2表示一个氢分子中的两个氢原子 C、H2O中的“2”表示一个水分子中含有二个氢原子 D、Cu2+中的“2+”表示铜原子的化合价为+2价二、填空题
-
20. 有下列几种物质:盐酸、硫酸、食盐、苛性钠、纯碱、熟石灰;请选择合适的物质填空(均填化学式)。(1)、少量存在于胃液中帮助消化的是。(2)、常用于降低土壤酸性的是。(3)、在日常生活中用做调味剂的是。(4)、做馒头时用于除去面团发酵生成的酸的是。21. 从N、O、H、Na四种元素中,选择适当的元素,按要求写出下列各物质的化学式:(各举一例)(1)、金属氧化物(2)、酸(3)、碱(4)、盐22. 一款名为“史莱姆”的水晶泥玩具,其主要成分是普通胶水、硼砂晶体和水。查阅资料知道:
①硼砂晶体(Na2B4O7·10H2O)是一种易溶于水的白色固体,可用作清洁剂、杀虫剂。
②人体若摄入过多的硼,会引发多脏器的蓄积性中毒。
(1)、硼砂晶体(Na2B4O7·10H2O)中硼(B)元素的化合价为。(2)、请至少写出一条关于硼砂晶体的物理性质。23. 如图所示是1-18号元素中某些元素的部分化合价,回答下列问题。1 H
2He
3Li
4Be
5B
6C
7N
8O
9F
10Ne
11Na
+1
12Mg
+2
13Al
+3
14 Si
+4 -4
15P
16S
+6 -2
17Cl
18Ar
(1)、3号元素属于(选填“金属元素”或“非金属元素”)。(2)、13号元素与8号元素组成的化合物为(填化学式)。24. 燃煤发电厂利用反应2SO2+2CaCO3+X=2CaSO4+2CO2来减少SO2的排放,其中X的化学式为 , 其中化合价发生变化的元素有(填元素符号)。25. 现有Na、O、S、H四种元素中,请选用其中一种或几种元素写出符合下列要求的化学式(各写一个)(1)、盐;(2)、酸;(3)、碱。26. 新冠肺炎疫情的蔓延,使得市场上84消毒液等消毒剂非常紧缺。84消毒液的主要成分是次氯酸钠,工业上可用如下反应制取:2NaOH+Cl2=NaCl+NaClO+H2O。回答:(1)、反应物氯气属于(填物质类别)。(2)、NaClO中Cl的化合价是。(3)、NaClO是由 Na+和ClO-构成的,具有消毒作用的主要成分是离子。27. 有6种物质能按下列顺序排列:①CO②H2O③NH3④X⑤C2H4⑥P2O5根据它们的组成和排列的规律,X可能是(填选项字母) ,解释你选择的理由:。A.CH3OH B.CH4 C.Fe2O3 D.SO3
28. 请用化学用语表示(1)、镁离子的化学式(2)、正二价的铜元素(3)、保持氯化钠化学性质的微粒(4)、符号“2Fe”中数字2的含义29. A是地壳中含量最高的金属元素,B元素的一种气体单质支持人类呼吸,C元素的原子核外只有两个电子。请写出相应的化学式:A和B组成的化合物 , C元素组成的气体单质 , 相对分子质量最小的氧化物是。三、解答题
-
30. 隔夜菜是否能吃,主要在于烧熟后的隔夜菜中亚硝酸盐含量的变化是否符合食品安全要求。蔬菜中的硝酸盐来自生长过程中所施氮肥。空气中的微生物(如硝酸盐还原菌)进入到蔬菜中,会产生一种还原酶,使蔬菜中的部分硝酸盐还原成亚硝酸盐。烧熟后的菜在食用和保存阶段都会有一些细菌进入;做熟的蔬菜更适合细菌生长。某研究小组对烧熟的菜中亚硝酸盐含量做了测试,数据如下表:(盖有保鲜膜的菜肴在4℃的冰箱中放置不同时间的亚硝酸盐含量,单位:mg/kg)
莱肴
半小时
6小时
18小时
24小时
炒青菜
0.6861
0.7982
4.3333
5.3624
韭菜炒蛋
1.8153
1.9249
2.8390
5.6306
红烧肉
2.4956
4.2558
4.3668
5.5188
红烧鳃鱼
/
2.0948
3.2300
7.2397
将一份红烧鲫鱼样本(不盖保鲜膜)在常温下放置4小时,测定其亚硝酸盐含量为8.9483mg/g。
请根据以上材料,回答下列问题:
(1)、亚硝酸盐中含有NO2- , 其中氮元素的化合价是价。(2)、根据上述的实验数据,菜中的亚硝酸盐含量变化的共同规律是:(3)、要使烧熟后的隔夜菜中亚硝酸盐含量尽可能低,保存的条件应该是。(4)、炒菜过程中温度一般在100℃以上,你认为从生菜炒到熟菜过程中亚硝酸盐含量是否会持续增加?为什么?。31. 治疗新冠患者用到的中医药“金银花”,成效明显。中医药中“金银花”的有效成分“绿原酸”具有抗菌杀毒的作用,其分子式为C16HXO9。已知绿原酸的相对分子质量为354,请你计算:(1)、C16HXO9中X=.(2)、“绿原酸”中碳元素和氧元素的质量比(3)、“绿原酸”中氧元素的质量分数是(计算结果精确到0.1%)32. 2019年6月21日,杭州市开始在全市范围稳步推进垃圾分类管理,将生活垃圾分为如图所示的四类。 (1)、以下四种物品中属于垃圾分类中可回收物的是A、破碗瓷片 B、过期药物 C、废旧报纸 D、枯枝落叶(2)、易腐垃圾经过处理会产生沼气,沼气可以燃烧发电。沼气的主要成分是甲烷(CH4),请写出甲烷燃烧的化学方程式。(3)、沼气发电时,能量转化形式是转化为电能。(4)、废电池属于“有害垃圾”,主要是因为废电池里含有大量的汞、镉、锰、铅等重金属(选填“元素"或“单质”)。(5)、“可回收物”中也包含铝制易拉罐,对铝制易拉罐的回收一般分四步:破碎、脱漆、打包、熔炼。将易拉罐熔炼成铝块的过程,铝发生的物态变化是。33. 建造“南昌舰”的特种钢材需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe2O3)中的含铁量,进行实验;取20g赤铁矿石样品,逐渐加入稀盐酸,充分反应。实验相关数据如图所示(假设杂质不溶于水,也不与酸反应)。
(1)、以下四种物品中属于垃圾分类中可回收物的是A、破碗瓷片 B、过期药物 C、废旧报纸 D、枯枝落叶(2)、易腐垃圾经过处理会产生沼气,沼气可以燃烧发电。沼气的主要成分是甲烷(CH4),请写出甲烷燃烧的化学方程式。(3)、沼气发电时,能量转化形式是转化为电能。(4)、废电池属于“有害垃圾”,主要是因为废电池里含有大量的汞、镉、锰、铅等重金属(选填“元素"或“单质”)。(5)、“可回收物”中也包含铝制易拉罐,对铝制易拉罐的回收一般分四步:破碎、脱漆、打包、熔炼。将易拉罐熔炼成铝块的过程,铝发生的物态变化是。33. 建造“南昌舰”的特种钢材需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe2O3)中的含铁量,进行实验;取20g赤铁矿石样品,逐渐加入稀盐酸,充分反应。实验相关数据如图所示(假设杂质不溶于水,也不与酸反应)。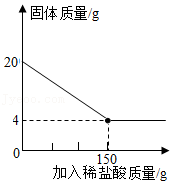 (1)、20g赤铁矿石样品中氧化铁的质量为g;(2)、该样品中铁元素的质量分数为 , 由此判断出该赤铁矿石(填“属于”或“不属于”)富铁矿石。(3)、若赤铁矿中氧化铁的质量分数为80%(其他成分不含铁),600t这样的赤铁矿可以炼出含杂质为4%的生铁多少吨?34. “青团”是宁波的一种传统食物。在“青团”制作过程中,需要往糯米粉中添加艾草(或艾草汁)。艾草含有侧柏莲酮芳香油()C10H10O,侧柏莲酮芳香油是一种淡黄色液体,具有香脂香气,所以“青团”具有独特风味。(1)、侧柏莲酮芳香油由种元素组成。(2)、7.3g侧柏莲桐芳香油中碳元素的质量为g。(3)、侧柏莲桐芳香油在氧气中完全燃烧的产物是。
(1)、20g赤铁矿石样品中氧化铁的质量为g;(2)、该样品中铁元素的质量分数为 , 由此判断出该赤铁矿石(填“属于”或“不属于”)富铁矿石。(3)、若赤铁矿中氧化铁的质量分数为80%(其他成分不含铁),600t这样的赤铁矿可以炼出含杂质为4%的生铁多少吨?34. “青团”是宁波的一种传统食物。在“青团”制作过程中,需要往糯米粉中添加艾草(或艾草汁)。艾草含有侧柏莲酮芳香油()C10H10O,侧柏莲酮芳香油是一种淡黄色液体,具有香脂香气,所以“青团”具有独特风味。(1)、侧柏莲酮芳香油由种元素组成。(2)、7.3g侧柏莲桐芳香油中碳元素的质量为g。(3)、侧柏莲桐芳香油在氧气中完全燃烧的产物是。四、实验探究题
-
35. 2020年1月25日总建筑面积为3.39万平方米的火神山医院正式开工,火神山医院在建造过程中用到了HDPE膜。老师告诉同学们HDPE膜具有极好的抗冲击性和防潮性,听完老师的描述后,同学们对HDPE膜的组成元素产生了浓厚的兴趣,进行了如下探究:
【提出问题】HDPE膜由什么元素组成?
【査阅资料】①HDPE膜能够燃烧,燃烧生成水和碳的氧化物:
②碱石灰主要成分是氢氧化钠固体和氧化钙固体
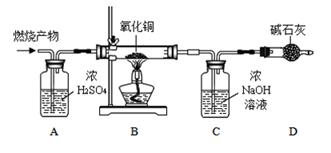
【实验探究】如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在一定质量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D(装置中每步反应均进行完全)。
装置质量
A装置总质量
装置总质量
实验前
100.0g
100.0g
实验后
105.4g
113.2g
【实验现象及分析】
(1)、装置D中碱石灰的作用是。(2)、实验现象:观察到装置B中黑色粉末变成红色,证明燃烧产物中有。(3)、【数据处理】见上图【实验结论】HDPE膜仅有C和H两者中元素组成,理由是(用数据分析):。
(4)、【反思拓展】实验中的4.2 g HDPE膜样品燃烧消耗的氧气质量为m,则m的取值范围为。36. 下图装置是用燃烧法来确定有机物组成的常用装置,这种方法是在电炉加热时用纯氧气氧化硬质玻璃管内样品,根据氧化产物的质量确定有机物的组成(在装置中C里的氧化铜是确保有机物中的碳元素完全转化为二氧化碳).请回答有关问题: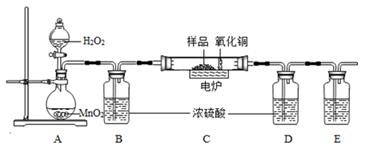 (1)、写出A装置中发生反应的化学方程式 .(2)、若去掉B装置会对元素的测定结果有影响。(3)、若准确称取1.12克样品(样品只含C、H、O三种元素中的两种或三种).经充分燃烧,D装置增重1.44克,E装置增重3.52克,则该有机物样品中所含的元素为 .37. 科学兴趣小组利用如图装置对FeSO4·nH2O晶体中的结晶水的含量进行测定(铁架台等己省略)。已知:①FeSO4和FeSO4·nH2O加热时易被空气氧化;②FeSO4·nH2O FeSO4+nH2O。实验步骤如下:
(1)、写出A装置中发生反应的化学方程式 .(2)、若去掉B装置会对元素的测定结果有影响。(3)、若准确称取1.12克样品(样品只含C、H、O三种元素中的两种或三种).经充分燃烧,D装置增重1.44克,E装置增重3.52克,则该有机物样品中所含的元素为 .37. 科学兴趣小组利用如图装置对FeSO4·nH2O晶体中的结晶水的含量进行测定(铁架台等己省略)。已知:①FeSO4和FeSO4·nH2O加热时易被空气氧化;②FeSO4·nH2O FeSO4+nH2O。实验步骤如下:
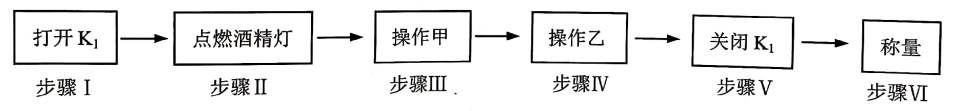
请回答:
(1)、步骤Ⅰ打开K1导入二氧化碳气体,排尽装置中的空气,其目的是 。(2)、步骤Ⅳ中的操作乙是通二氧化碳直至C装置冷却至室温,则操作甲指的是。(3)、有同学建议,为加快产生CO2的速率,可将A中装置中盐酸浓度增大、石灰石磨成粉状。制取气体时反应速度是否越快越好?其理由是。(4)、步骤Ⅵ称量,若晶体FeSO4·nH2O质量为m,反应前后C装置质量减少了m1 , D装置质量增加了m2 , 则此晶体中的结晶水的百分含量为。(用字母表示)
38. 在宏观、微观和符号之间建立联系是化学学科的特点.甲、乙、丙、丁表示四种物质,它们的部分化学式和微观示意图分别列于下表:物质
甲
乙
丙
丁
图例:
 ﹣﹣氢原子
﹣﹣氢原子 ﹣﹣碳原子
﹣﹣碳原子 ﹣﹣氧原子
﹣﹣氧原子化学式
?
C
H2O
H2
微观
示意图



?
(1)、请写出甲物质的化学式 , 画出丁物质的微观示意图 .(2)、能保持丙物质化学性质的微粒是(填“分子”或“原子”),四种物质中属于氧化物的有(填“甲、乙、丙、丁”).39. 通过对已学知识的对比和归纳,我们往往可以得出一些十分有趣的规律,这些规律可以帮助我们掌握学习科学的方法.请仔细阅读下表中的内容,并回答相应的问题:常见的几种离子
H+ Na+ Mg2+ OH﹣ Cl﹣ SO42﹣
对应元素及原子团
在化合物中的化合价
、 、 、O 、 、S
所能形成化合物的化学式
酸
碱
盐
HCl、H2SO4
NaOH、Mg(OH)2
MgCl2、Na2SO4
(1)、由前两行内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的数相等.(2)、由后两行内容对照可得出的规律是:通过元素或原子团的可以确定相应化合物的化学式.(3)、利用表中所给内容,请你写出硫酸钠的化学式 .(4)、根据硫酸亚铁的化学式FeSO4 , 可推出该物质所含阳离子的符号为 .