四川省绵阳市江油市2021-2022学年九年级上学期期中化学试题
试卷更新日期:2021-12-01 类型:期中考试
一、单选题
-
1. 下列成语涉及化学变化的是( )A、死灰复燃 B、香气四溢 C、木已成舟 D、水乳交融2. 下列为一些物质的自我介绍,其中介绍自己化学性质的是( )A、我是紫红色固体 B、我在自然界中硬度最大 C、我在常温下是气体 D、我会生锈3. 2021年9月21日,中国国家领导人以视频方式出席第七十六届联合国大会一般性辩论,并向世界宣布:中国将大力支持发展中国家能源绿色低碳发展,不再新建境外煤电项目。如果煤燃烧后大量尾气直接排放到空气中,会造成空气污染,下列物质中不会造成空气污染的是( )A、NO2 B、CO2 C、SO2 D、可吸入颗粒物4. 下列物质的用途主要由物理性质决定的是( )A、氧气用于医疗急救 B、氦可用于制造低温环境 C、氮气用于制硝酸、氮肥 D、酒精可用作燃料5. 汤姆森发现电子,卢瑟福积极探索原子内部结构,门捷列夫列出了第一张元素周期表,徐寿为大量化学元素创造汉语名称……许许多多科学家为理论化学研究做出了巨大贡献,推开了物质的微观世界之门。下列有关说法错误的是( )A、固态水的分子在不停地运动 B、氯化钠是由Na+和Cl-构成的化合物 C、氧原子结构示意图为
 D、甲烷(CH4)中碳、氢元素的质量比为3:1
6. 下列说法正确的是( )A、带电的微粒一定是离子 B、原子核是由质子和电子构成 C、不同种元素的根本区别是核内质子数不同 D、质子数相同的两种粒子属于同种元素7. 以下是某化学学习小组在“人吸入的空气和呼出的气体中有什么不同”的探究活动中提出的一些说法,其中错误的是( )A、要选择规格、大小完全相同的集气瓶进行对比实验 B、实验中呼出的气体含二氧化碳的现象是:呼出的气体能使澄清石灰水变浑浊 C、实验中呼出的气体含水蒸气的现象是:呼出的气体在冷而干燥的玻璃片上结下水珠 D、实验中呼出的气体含氧气的现象是:呼出的气体能使木条燃烧更旺8. 实验操作考试中,小红同学抽到“实验室制取氧气”,以下是她的部分实验操作,其中有错误的一项是( )A、装二氧化锰
D、甲烷(CH4)中碳、氢元素的质量比为3:1
6. 下列说法正确的是( )A、带电的微粒一定是离子 B、原子核是由质子和电子构成 C、不同种元素的根本区别是核内质子数不同 D、质子数相同的两种粒子属于同种元素7. 以下是某化学学习小组在“人吸入的空气和呼出的气体中有什么不同”的探究活动中提出的一些说法,其中错误的是( )A、要选择规格、大小完全相同的集气瓶进行对比实验 B、实验中呼出的气体含二氧化碳的现象是:呼出的气体能使澄清石灰水变浑浊 C、实验中呼出的气体含水蒸气的现象是:呼出的气体在冷而干燥的玻璃片上结下水珠 D、实验中呼出的气体含氧气的现象是:呼出的气体能使木条燃烧更旺8. 实验操作考试中,小红同学抽到“实验室制取氧气”,以下是她的部分实验操作,其中有错误的一项是( )A、装二氧化锰 B、加5%的过氧化氢溶液
B、加5%的过氧化氢溶液  C、制取并收集O2
C、制取并收集O2  D、检验是否收集满
D、检验是否收集满  9. 掌握化学用语是学好化学的关键。下列化学符号中数字“2”表示的意义不相符的是( )A、CO2——二氧化碳分子中含有2个氧元素 B、Mg2+——1个镁离子带两个单位正电荷 C、2Cu——2个铜原子 D、 ——氧化亚铁中铁元素的化合价为+2价10. 装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏,下列装置中,不能检查气密性的是( )A、
9. 掌握化学用语是学好化学的关键。下列化学符号中数字“2”表示的意义不相符的是( )A、CO2——二氧化碳分子中含有2个氧元素 B、Mg2+——1个镁离子带两个单位正电荷 C、2Cu——2个铜原子 D、 ——氧化亚铁中铁元素的化合价为+2价10. 装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏,下列装置中,不能检查气密性的是( )A、 B、
B、 C、
C、 D、
D、 11. 用氯酸钾和二氧化锰的混合物加热制取氧气时,有关二氧化锰说法正确的是( )A、能增加氧气的产量 B、不加二氧化锰,加热氯酸钾不能产生氧气 C、加快产生氧气的速率,氧气的产量不变 D、加快产生氧气的速率,增加氧气的产量12. 2018年2月9日,冬奥会在韩国平昌如期举行,俄罗斯运动员受兴奋剂风波影响,诸多名将未能参加。乙基雌烯醇C20H32O是禁止运动员服用的兴奋剂之一、下列说法正确的是( )A、乙基雌烯醇是混合物 B、乙基雌烯醇的相对分子质量是288g C、乙基雌烯醇中碳、氢、氧元素的个数比为20:32:1 D、一个乙基雌烯醇分子由20个碳原子、32个氢原子和一个氧原子构成13. 空气是一种重要的资源,下列有关空气说法正确的是( )A、空气中氧气的质量分数为21% B、空气中各成分所占的比例是永恒不变的 C、空气是由多种物质组成的混合物 D、空气质量级别数目越大,空气的质量越好14. 保持氧气化学性质的最小粒子是( )A、氧分子 B、氧原子 C、氧离子 D、氧气15. 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆代表纯净物,下列选项正确的是( )
11. 用氯酸钾和二氧化锰的混合物加热制取氧气时,有关二氧化锰说法正确的是( )A、能增加氧气的产量 B、不加二氧化锰,加热氯酸钾不能产生氧气 C、加快产生氧气的速率,氧气的产量不变 D、加快产生氧气的速率,增加氧气的产量12. 2018年2月9日,冬奥会在韩国平昌如期举行,俄罗斯运动员受兴奋剂风波影响,诸多名将未能参加。乙基雌烯醇C20H32O是禁止运动员服用的兴奋剂之一、下列说法正确的是( )A、乙基雌烯醇是混合物 B、乙基雌烯醇的相对分子质量是288g C、乙基雌烯醇中碳、氢、氧元素的个数比为20:32:1 D、一个乙基雌烯醇分子由20个碳原子、32个氢原子和一个氧原子构成13. 空气是一种重要的资源,下列有关空气说法正确的是( )A、空气中氧气的质量分数为21% B、空气中各成分所占的比例是永恒不变的 C、空气是由多种物质组成的混合物 D、空气质量级别数目越大,空气的质量越好14. 保持氧气化学性质的最小粒子是( )A、氧分子 B、氧原子 C、氧离子 D、氧气15. 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆代表纯净物,下列选项正确的是( ) A、①单质③氧化物 B、②化合物④氧化物 C、①单质③化合物 D、②含氧化合物④氧化物16. 如图是某密闭容器中物质变化过程的微观示意图。下列说法正确的是()
A、①单质③氧化物 B、②化合物④氧化物 C、①单质③化合物 D、②含氧化合物④氧化物16. 如图是某密闭容器中物质变化过程的微观示意图。下列说法正确的是() A、上述变化Ⅰ、Ⅱ和Ⅲ中,属于化学变化的是Ⅱ和Ⅲ B、A、B、C中表示混合物的是A C、该变化中一定不变的微粒是碳原子和氧分子 D、该反应的文字表达式为碳 氧气 二氧化碳17. 下列关于分子、原子的说法正确的是( )A、分子可分而原子不可分 B、分子间有间隔而原子间没有间隔 C、分子的质量一定比原子质量大 D、分子、原子都可以直接构成物质18. 下列说法中正确的是( )A、红磷在氧气中能燃烧,在空气中不能燃烧 B、硫在氧气中燃烧后生成有刺激性气味的气体 C、镁条在氧气中燃烧时,火星四射,生成黑色固体 D、木炭伸入盛有氧气的集气瓶中剧烈燃烧,发出白光19. 某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如下图所示,下列关于该过程的说法正确的是( )
A、上述变化Ⅰ、Ⅱ和Ⅲ中,属于化学变化的是Ⅱ和Ⅲ B、A、B、C中表示混合物的是A C、该变化中一定不变的微粒是碳原子和氧分子 D、该反应的文字表达式为碳 氧气 二氧化碳17. 下列关于分子、原子的说法正确的是( )A、分子可分而原子不可分 B、分子间有间隔而原子间没有间隔 C、分子的质量一定比原子质量大 D、分子、原子都可以直接构成物质18. 下列说法中正确的是( )A、红磷在氧气中能燃烧,在空气中不能燃烧 B、硫在氧气中燃烧后生成有刺激性气味的气体 C、镁条在氧气中燃烧时,火星四射,生成黑色固体 D、木炭伸入盛有氧气的集气瓶中剧烈燃烧,发出白光19. 某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如下图所示,下列关于该过程的说法正确的是( )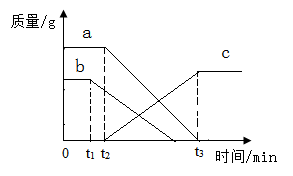 A、c代表氧气 B、t2时刻,O2开始产生 C、t1时刻,KMnO4开始分解 D、起催化作用物质的质量一直保持不变20. 实验室使用一定质量的高锰酸钾加热分解制氧气,各物理量随加热时间变化的图象正确的是( )A、
A、c代表氧气 B、t2时刻,O2开始产生 C、t1时刻,KMnO4开始分解 D、起催化作用物质的质量一直保持不变20. 实验室使用一定质量的高锰酸钾加热分解制氧气,各物理量随加热时间变化的图象正确的是( )A、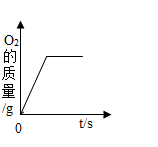 B、
B、 C、
C、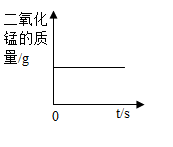 D、
D、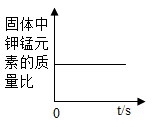
二、填空题
-
21. 用化学用语符号填空:(1)、相对分子质量最小的氧化物;(2)、地壳中含量最多的金属元素,非金属元素和空气中含量最多的元素组成的化合物是;(3)、氖气;(4)、化学符号的含义:5 ;(5)、构成金属铁的微粒;(6)、标出二氧化碳中碳元素的化合价:。22. 美国两位科学家利用碘元素,借助放射学进行了“G蛋白偶联受体”研究,揭开了“细胞如何感知周围环境”之谜,获得了2012年诺贝尔化学奖。如图一是碘元素在元素周期表中的部分信息及碘原子的结构示意图。请回答:
 (1)、由上图可知碘元素属于(填“金属”或“非金属”)元素,位于元素周期表第周期,碘元素的相对原子质量是 , 碘元素的质子数;(2)、根据图二中的信息可知,碘原子在化学反应中易(填“得”或“失”)电子而形成碘离子,碘离子属于(填“阴”或“失”)离子,其符号是。(3)、图三中微粒与碘元素化学性质相似的是 , 属于稳定结构的是(填字母)。
(1)、由上图可知碘元素属于(填“金属”或“非金属”)元素,位于元素周期表第周期,碘元素的相对原子质量是 , 碘元素的质子数;(2)、根据图二中的信息可知,碘原子在化学反应中易(填“得”或“失”)电子而形成碘离子,碘离子属于(填“阴”或“失”)离子,其符号是。(3)、图三中微粒与碘元素化学性质相似的是 , 属于稳定结构的是(填字母)。三、综合题
-
23. 天然水净化为自来水的主要流程如下:
 (1)、下列说法错误的是___________(填字母)。A、过滤池可以除去难溶性杂质 B、活性炭吸附池可以除去水中的色素和臭味 C、清水池中一定是软水 D、投药消毒发生的是化学变化(2)、自然界中的水多含杂质。含有较多可溶性钙、镁化合物的水称为硬水,鉴别硬水和软水的方法是加入。(3)、絮凝剂可用于净水,自来水厂净水过程中所加的絮凝剂成分是 , 是因为它溶于水生成的胶状物可以悬浮于水中的杂质。(4)、日常生活中,当水的硬度大并且担心病菌过多时,可以采取的方法降低水的硬度并杀灭病菌。每一滴水都来之不易,列举一条生活中具体可行的节水措施。24. 甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素完全相同的化合物,丙是单质;甲为液体,在一定条件下可分解生成乙和丙。它们之间有如图所示的转化关系。
(1)、下列说法错误的是___________(填字母)。A、过滤池可以除去难溶性杂质 B、活性炭吸附池可以除去水中的色素和臭味 C、清水池中一定是软水 D、投药消毒发生的是化学变化(2)、自然界中的水多含杂质。含有较多可溶性钙、镁化合物的水称为硬水,鉴别硬水和软水的方法是加入。(3)、絮凝剂可用于净水,自来水厂净水过程中所加的絮凝剂成分是 , 是因为它溶于水生成的胶状物可以悬浮于水中的杂质。(4)、日常生活中,当水的硬度大并且担心病菌过多时,可以采取的方法降低水的硬度并杀灭病菌。每一滴水都来之不易,列举一条生活中具体可行的节水措施。24. 甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素完全相同的化合物,丙是单质;甲为液体,在一定条件下可分解生成乙和丙。它们之间有如图所示的转化关系。 (1)、写出物质的化学式:甲 ;乙 。(2)、从微观的角度解释甲、乙性质有差异的原因是 。(3)、A是一种黑色固体粉末,能加快甲的分解速度,但反应前后其质量和化学性质没有发生变化,则A的化学式可能是 ,在该反应中作 。(4)、反应③的文字表达式是: ,其基本反应类型属于 。从反应③可以推测丁物质具有的一种化学性质是: 。丁是未来能源领域中的新型高能燃料,从环保的角度看,其突出的优点是 。25. 用下图所示实验装置测定空气中氧气含量。
(1)、写出物质的化学式:甲 ;乙 。(2)、从微观的角度解释甲、乙性质有差异的原因是 。(3)、A是一种黑色固体粉末,能加快甲的分解速度,但反应前后其质量和化学性质没有发生变化,则A的化学式可能是 ,在该反应中作 。(4)、反应③的文字表达式是: ,其基本反应类型属于 。从反应③可以推测丁物质具有的一种化学性质是: 。丁是未来能源领域中的新型高能燃料,从环保的角度看,其突出的优点是 。25. 用下图所示实验装置测定空气中氧气含量。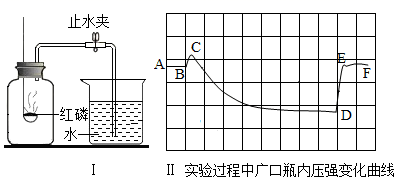 (1)、图Ⅰ中,发生反应的文字表达式为。(2)、图Ⅱ中,BC段压强升高的原因是。(3)、实验前广口瓶内空气体积为V,烧杯中水的体积为V1 , 实验后烧杯中剩余水的体积为V2.空气中氧气体积分数的表达式为(用V、V1、V2以表示)。26. 请结合下列常用实验装置,回答有关问题。
(1)、图Ⅰ中,发生反应的文字表达式为。(2)、图Ⅱ中,BC段压强升高的原因是。(3)、实验前广口瓶内空气体积为V,烧杯中水的体积为V1 , 实验后烧杯中剩余水的体积为V2.空气中氧气体积分数的表达式为(用V、V1、V2以表示)。26. 请结合下列常用实验装置,回答有关问题。
 (1)、写出图中标有序号仪器的名称:①。(2)、若用高锰酸钾制取氧气,应选用的发生装置是(填字母),在加入药品前,应首先 , 发生反应的方程式或文字表达式为。(3)、若要用过氧化氢溶液和二氧化锰制取干燥的氧气,发生反应的方程式或文字表达式为 ,为了使反应随时发生或停止,可选择的发生收集装置是(填字母,从“A-F”中选),检验氧气是否集满的方法是。(4)、二氧化氮是一种红棕色的有毒气体,密度比空气大,易溶于水,若用装置G收集二氧化氮,你认为气体应从(填“a”或“b”)端进入。27. 某研究小组用如图所示装置,探究能否用镁条代替红磷测定空气中氧气含量。实验前,小组成员提出了不同的猜想。
(1)、写出图中标有序号仪器的名称:①。(2)、若用高锰酸钾制取氧气,应选用的发生装置是(填字母),在加入药品前,应首先 , 发生反应的方程式或文字表达式为。(3)、若要用过氧化氢溶液和二氧化锰制取干燥的氧气,发生反应的方程式或文字表达式为 ,为了使反应随时发生或停止,可选择的发生收集装置是(填字母,从“A-F”中选),检验氧气是否集满的方法是。(4)、二氧化氮是一种红棕色的有毒气体,密度比空气大,易溶于水,若用装置G收集二氧化氮,你认为气体应从(填“a”或“b”)端进入。27. 某研究小组用如图所示装置,探究能否用镁条代替红磷测定空气中氧气含量。实验前,小组成员提出了不同的猜想。
(猜想与假设)
猜想1:可以代替,因为镁条与氧气反应后不会产生气体
猜想2:不能代替,查阅资料知金属镁很活泼,可能会与空气中的氮气反应
(进行实验)
步骤
实验操作
实验现象
Ⅰ
组装好装置后,打开止水夹,手捂集气瓶,一段时间后,松开手
烧杯中导管口有气泡冒出,松手后,烧杯中导管末端有一段液柱
Ⅱ
关闭止水夹,点燃镁条,迅速伸入集气瓶中,塞好塞子
镁条燃烧,放出大量热,发出耀眼白光,生成大量白烟,剩余固体为白色带状物
Ⅲ
冷却至室温,打开止水夹
烧杯中水从导管进入集气瓶中,体积约为集气瓶体积的2/5
(解释与结论)
(1)、Mg与氧气反应的化学方程式为 。(2)、步骤Ⅰ说明装置的气密性 。(3)、步骤Ⅱ中,关闭止水夹的目的是 。(4)、推测猜想2成立的现象证据是 。(5)、(反思与评价)该小组认为,即使步骤Ⅲ中水的体积恰好占集气瓶体积的1/5,也不能说明猜想1成立,理由是 。
(6)、小组中同学对镁条与瓶中气体的反应提出了进一步的猜想:甲同学认为镁条先与O2反应,乙同学认为镁条先与N2反应。为进一步检验他们的猜想,可以进行的实验操作是:取少量镁条,点燃后迅速放入盛有空气的集气瓶中,待镁条熄灭后, 。四、计算题
-
28. 缺钙能导致儿童发育不良或佝偻病。小明同学从食物中摄入钙元素的量不足,每天需要服用2片某种钙片。该钙片标签的部分内容如图所示(假设钙片中只有碳酸钙含有钙元素),请计算:
 (1)、碳酸钙中各元素的质量比;(2)、碳酸钙中钙元素的质量分数;(3)、小明同学每天从钙片中摄入钙元素的质量;(4)、若小明改用喝牛奶(每100mL牛奶中含钙≥0.10g)来补充钙,每天至少需要喝多少毫升牛奶?
(1)、碳酸钙中各元素的质量比;(2)、碳酸钙中钙元素的质量分数;(3)、小明同学每天从钙片中摄入钙元素的质量;(4)、若小明改用喝牛奶(每100mL牛奶中含钙≥0.10g)来补充钙,每天至少需要喝多少毫升牛奶?