山东省青岛市市北区2021-2022学年九年级上学期期中联考化学试题
试卷更新日期:2021-12-01 类型:期中考试
一、单选题
-
1. 下列变化中,不属于化学变化的是( )A、水结成冰 B、食物腐烂 C、蜡烛燃烧 D、铁生锈2. 下列基本实验操作错误的一项是( )A、过滤
 B、量筒读数
B、量筒读数  C、检查装置气密性
C、检查装置气密性  D、用滴管滴加液体
D、用滴管滴加液体  3. 空气是一种宝贵的自然资源。下列有关空气的说法中,错误的是( )A、工业上可以利用分离液态空气法制氧气 B、空气中氧气的体积分数约为21% C、氮气的化学性质不活泼,充入食品包装袋中可延长食品保质期 D、尽早实现“碳中和”(碳排放量与吸收量相等)有利于缓解温室效应,说明二氧化碳属于空气污染物4. 建立宏观与微观的联系是化学学科特有的思维方式。下列对于宏观现象的微观解释中,错误的是( )A、一卉能熏一室香,是因为分子不断运动 B、水结成冰,是因为水分子停止了运动 C、水和过氧化氢具有不同的化学性质,是因为它们的分子构成不同 D、20mL水与20mL酒精混合后体积小于40mL,是因为分子之间有间隔5. 下列实验现象描述正确的是( )A、木炭在氧气中燃烧,生成有刺激性气味的气体 B、蜡烛在空气中燃烧,生成水和二氧化碳 C、红磷在空气中燃烧,产生大量白雾 D、铁丝在氧气中燃烧,火星四射,生成黑色固体6. 下图是表示气体分子微粒的示意图图中“O”和“●”分别表示两种不同质子数的原子那么其中表示化合物的是( )A、
3. 空气是一种宝贵的自然资源。下列有关空气的说法中,错误的是( )A、工业上可以利用分离液态空气法制氧气 B、空气中氧气的体积分数约为21% C、氮气的化学性质不活泼,充入食品包装袋中可延长食品保质期 D、尽早实现“碳中和”(碳排放量与吸收量相等)有利于缓解温室效应,说明二氧化碳属于空气污染物4. 建立宏观与微观的联系是化学学科特有的思维方式。下列对于宏观现象的微观解释中,错误的是( )A、一卉能熏一室香,是因为分子不断运动 B、水结成冰,是因为水分子停止了运动 C、水和过氧化氢具有不同的化学性质,是因为它们的分子构成不同 D、20mL水与20mL酒精混合后体积小于40mL,是因为分子之间有间隔5. 下列实验现象描述正确的是( )A、木炭在氧气中燃烧,生成有刺激性气味的气体 B、蜡烛在空气中燃烧,生成水和二氧化碳 C、红磷在空气中燃烧,产生大量白雾 D、铁丝在氧气中燃烧,火星四射,生成黑色固体6. 下图是表示气体分子微粒的示意图图中“O”和“●”分别表示两种不同质子数的原子那么其中表示化合物的是( )A、 B、
B、 C、
C、 D、
D、 7. 下列化学用语书写正确的是( )A、2个氮原子:N2 B、一个一氧化碳分子:Co C、水中氧元素的化合价为−2价: D、一个氧离子:O2-8. 氨催化氧化是制硝酸的主要反应之一、该反应前后分子种类变化的微观示意图如下,下列说法错误的是( )
7. 下列化学用语书写正确的是( )A、2个氮原子:N2 B、一个一氧化碳分子:Co C、水中氧元素的化合价为−2价: D、一个氧离子:O2-8. 氨催化氧化是制硝酸的主要反应之一、该反应前后分子种类变化的微观示意图如下,下列说法错误的是( ) A、甲分子中氮、氢原子个数比为1:3 B、反应前后各元素的化合价不变 C、上图所示4种物质中,含氧元素的化合物有2种 D、反应前后原子的种类肯定不会发生变化9. 2020年,全世界范围内爆发了新型冠状病毒感染导致的肺炎,某科研团队发布消息洛匹那韦(化学式为C37H48N4O5)能对病毒有抑制效果,下列对于该物质的说法错误的是( )A、洛匹那韦分子由碳、氢、氮、氧四种元素组成 B、一个洛匹那韦分子含有37个碳原子、48个氢原子、4个氮原子和5个氧原子 C、洛匹那韦中碳元素质量分数最大 D、洛匹那韦属于化合物10. 水是我们日常生活必不可少的物质,下列有关水的说法正确的是( )A、用过滤的方法可以使硬水软化 B、用活性炭吸附水中的色素和异味是化学变化 C、可用肥皂水区分硬水与软水 D、电解水生成氢气和氧气,说明水是由氢气和氧气组成11. 20℃时,在各盛有100克水的烧杯中,分别加入10克甲、乙、丙三种纯净物(不含结晶水,不与水反应),充分溶解后,结果如图。下列说法正确的是( )
A、甲分子中氮、氢原子个数比为1:3 B、反应前后各元素的化合价不变 C、上图所示4种物质中,含氧元素的化合物有2种 D、反应前后原子的种类肯定不会发生变化9. 2020年,全世界范围内爆发了新型冠状病毒感染导致的肺炎,某科研团队发布消息洛匹那韦(化学式为C37H48N4O5)能对病毒有抑制效果,下列对于该物质的说法错误的是( )A、洛匹那韦分子由碳、氢、氮、氧四种元素组成 B、一个洛匹那韦分子含有37个碳原子、48个氢原子、4个氮原子和5个氧原子 C、洛匹那韦中碳元素质量分数最大 D、洛匹那韦属于化合物10. 水是我们日常生活必不可少的物质,下列有关水的说法正确的是( )A、用过滤的方法可以使硬水软化 B、用活性炭吸附水中的色素和异味是化学变化 C、可用肥皂水区分硬水与软水 D、电解水生成氢气和氧气,说明水是由氢气和氧气组成11. 20℃时,在各盛有100克水的烧杯中,分别加入10克甲、乙、丙三种纯净物(不含结晶水,不与水反应),充分溶解后,结果如图。下列说法正确的是( ) A、所得溶液可能都是饱和溶液 B、20℃时,乙溶液的溶质质量最小 C、溶液溶质的质量分数:甲>丙>乙 D、升高温度,溶液溶质的质量分数一定变大12. 下列关于溶液的说法中,正确的是( )A、溶液都是均一、稳定的纯净物 B、饱和溶液的浓度一定大于不饱和溶液的浓度 C、形成溶液的溶质只能是固体 D、配制一定溶质质量分数的溶液需要经过计算、称量(量取)、溶解13. 中科院的全超导的“人造太阳”——托克马克核聚变试验装置的调试运行成功,使我在该领域的研究处于世界前列。氘和氚是核聚变的原料(氘、氚原子核内都只有1个质子,但分别含有1个中子、2个中子),聚变发生后,氘、氚原子核转变为氦原子核(氦原子核内含2个质子)。根据以上叙述,下列说法正确的是( )A、氘原子不带电,氚原子带电 B、氘原子和氦原子的质子数相同 C、氘原子和氚原子的质子数相同 D、氘原子和氚原子的相对原子质量相同14. 近年来,我国的航空航天技术迅速发展,建立了多个太空空间实验站。空间站中的氧气源自电解水,所得的H2和CO2反应生成了H2O和 CH4 , 该反应的微观示意图如下,下列说法错误的是( )
A、所得溶液可能都是饱和溶液 B、20℃时,乙溶液的溶质质量最小 C、溶液溶质的质量分数:甲>丙>乙 D、升高温度,溶液溶质的质量分数一定变大12. 下列关于溶液的说法中,正确的是( )A、溶液都是均一、稳定的纯净物 B、饱和溶液的浓度一定大于不饱和溶液的浓度 C、形成溶液的溶质只能是固体 D、配制一定溶质质量分数的溶液需要经过计算、称量(量取)、溶解13. 中科院的全超导的“人造太阳”——托克马克核聚变试验装置的调试运行成功,使我在该领域的研究处于世界前列。氘和氚是核聚变的原料(氘、氚原子核内都只有1个质子,但分别含有1个中子、2个中子),聚变发生后,氘、氚原子核转变为氦原子核(氦原子核内含2个质子)。根据以上叙述,下列说法正确的是( )A、氘原子不带电,氚原子带电 B、氘原子和氦原子的质子数相同 C、氘原子和氚原子的质子数相同 D、氘原子和氚原子的相对原子质量相同14. 近年来,我国的航空航天技术迅速发展,建立了多个太空空间实验站。空间站中的氧气源自电解水,所得的H2和CO2反应生成了H2O和 CH4 , 该反应的微观示意图如下,下列说法错误的是( ) A、反应前后分子种类没变 B、反应前后原子种类没变 C、反应中分子可分 D、原子可以构成分子15. 向氯化钠饱和溶液中,逐渐加入氯化钠固体(不考虑溶解时的热量变化),边加边搅拌。下列图形中变化关系正确的是( )A、
A、反应前后分子种类没变 B、反应前后原子种类没变 C、反应中分子可分 D、原子可以构成分子15. 向氯化钠饱和溶液中,逐渐加入氯化钠固体(不考虑溶解时的热量变化),边加边搅拌。下列图形中变化关系正确的是( )A、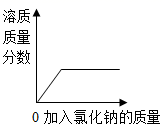 B、
B、 C、
C、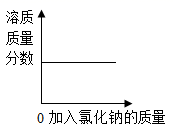 D、
D、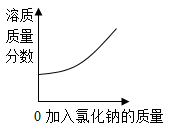 16. 镓是一种奇妙的金属,放在手心马上熔化,犹如荷叶上的水珠流来流去。结合如图信息判断下列说法错误的是( )
16. 镓是一种奇妙的金属,放在手心马上熔化,犹如荷叶上的水珠流来流去。结合如图信息判断下列说法错误的是( ) A、图中X=3 B、金属镓的熔点很低 C、镓元素的原子发生化学变化时易失电子 D、镓元素在周期表中与氮元素是同一族17. 推理和归纳是化学学习和研究中常用的思维方法。下列推理中,正确的是( )A、离子是带电的原子或原子团,所以带电的粒子一定是离子 B、单质是由一种元素组成的,则由一种元素组成的物质一定是单质 C、点燃可燃性气体前要验纯,所以点燃氢气前一定要验纯 D、化学变化通常伴随着发光、发热现象,所以有发光发热现象的变化一定是化学变化18. 用如图所示装置制取气体,需满足的条件是( )
A、图中X=3 B、金属镓的熔点很低 C、镓元素的原子发生化学变化时易失电子 D、镓元素在周期表中与氮元素是同一族17. 推理和归纳是化学学习和研究中常用的思维方法。下列推理中,正确的是( )A、离子是带电的原子或原子团,所以带电的粒子一定是离子 B、单质是由一种元素组成的,则由一种元素组成的物质一定是单质 C、点燃可燃性气体前要验纯,所以点燃氢气前一定要验纯 D、化学变化通常伴随着发光、发热现象,所以有发光发热现象的变化一定是化学变化18. 用如图所示装置制取气体,需满足的条件是( )
①反应物是固体;②反应需加热:③制得的气体不易溶于水;④制得的气体密度比空气大;⑤制得的气体能与空气中氧气反应。
A、①②③④⑤ B、①② C、②④⑤ D、①②③19. 下列图像不能正确反映对应变化关系的是( )
 A、用红磷燃烧法测定空气中氧气的含量 B、将水通电一段时间 C、用向上排空气法收集氧气时集气瓶内氧气的质量 D、完全相同的甲、乙两份过氧化氢溶液,甲中加入适量的二氧化锰20. 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆代表纯净物,则在下列选项中,能符合题意指出①、②、③、④所属物质类别的是( )
A、用红磷燃烧法测定空气中氧气的含量 B、将水通电一段时间 C、用向上排空气法收集氧气时集气瓶内氧气的质量 D、完全相同的甲、乙两份过氧化氢溶液,甲中加入适量的二氧化锰20. 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆代表纯净物,则在下列选项中,能符合题意指出①、②、③、④所属物质类别的是( ) A、②为含氧化合物、④为氧化物 B、①为单质、③为氧化物 C、④为单质、③为化合物 D、②为化合物、④为氧化物
A、②为含氧化合物、④为氧化物 B、①为单质、③为氧化物 C、④为单质、③为化合物 D、②为化合物、④为氧化物二、多选题
-
21. 如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀.如表中液体X和固体Y的组合,正确的是( )

A
B
C
D
X
双氧水
水
水
水
Y
二氧化锰
氯化钠
氢氧化钠
硝酸铵
A、A B、B C、C D、D22. 建立宏观与微观之间的联系是化学学科特有的思维方式。下列对宏观事实的微观解释错误的是( )A、50mL酒精与50mL水混合后总体积小于100mL,是因为分子变小了 B、分离液态空气法可以制得氧气,说明分子可以再分 C、电解水生成氢气和氧气,是因为分子在化学变化中可以再分 D、冰和干冰的化学性质不同,是因为构成它们的分子不同三、填空题
-
23. 化学物质及其变化与人类生产、生活密切相关请填写下列空格:(1)、用化学符号表示:
①空气中含量最多的气体。
②保持金属镁化学性质的最小微粒。
③三个氢氧根离子。
④氯化钙中钙元素的化合价为+2价。
(2)、用化学方程式表示镁粉制作照明弹燃烧的原理:。(3)、小华经常用洗洁精洗刷碗筷上的油污,是利用了洗洁精的作用。(4)、2020年10月13日,在“粵澳呼吸道病原体新药联合研究中心”第四次理事会上中国工程院院士钟南山透露,复方板蓝根对新冠病毒有体外抑制药效。已知板蓝根的某有效成分化学式为C15HxO5(相对分子质量为270),请你计算:①C15HxO5中x=。
②C15HxO5中碳元素和氧元素的质量比为。
③克该板蓝根中含有1.6克氧元素。
24. 如图中的①、②是元素周期表中的部分信息,A、B、C、D是四种粒子的结构示意图。
请你回答:
(1)、元素周期表中不同元素间最本质的区别是不同。(2)、D是一种元素的原子,则x=。(3)、A是氟的原子结构示意图,可知氟气的化学性质(填“活泼”或“稳定”)。(4)、A,B,C,D属于同种元素的粒子是(填粒子符号)25. 下图是初中教材中关于氧气的几个实验,请回答下列问题。 (1)、实验一中,反应的化学方程式为;水的作用是。(2)、实验二中,检验生成物用到的药品为。(3)、实验三中,选择红磷需考虑的因素有 (填序号)。A、可以在空气中消耗氧气 B、除氧气外不与空气中其他成分反应 C、生成物不是气体 D、与氧气反应有明显的实验现象(4)、从反应角度分析,三个反应的相同点是 (填序号)。A、都放出热量 B、产物常温下都是固体 C、都是氧化反应26. 将80gM物质加入50g水中,充分溶解,测得溶液的质量随温度的变化曲线如图所示,按要求填空。
(1)、实验一中,反应的化学方程式为;水的作用是。(2)、实验二中,检验生成物用到的药品为。(3)、实验三中,选择红磷需考虑的因素有 (填序号)。A、可以在空气中消耗氧气 B、除氧气外不与空气中其他成分反应 C、生成物不是气体 D、与氧气反应有明显的实验现象(4)、从反应角度分析,三个反应的相同点是 (填序号)。A、都放出热量 B、产物常温下都是固体 C、都是氧化反应26. 将80gM物质加入50g水中,充分溶解,测得溶液的质量随温度的变化曲线如图所示,按要求填空。 (1)、A点时,该溶液的溶质质量分数为 。(2)、向B点对应的溶液中加入70g的水,所得溶液的溶质的质量分数是 。(3)、C点所对应的溶液是 (填“饱和“不饱和”)。
(1)、A点时,该溶液的溶质质量分数为 。(2)、向B点对应的溶液中加入70g的水,所得溶液的溶质的质量分数是 。(3)、C点所对应的溶液是 (填“饱和“不饱和”)。四、综合题
-
27. 如图所示,甲、乙是常用的净化水的过程图或装置图。

请根据图回答:
(1)、图甲是自来水的净化过程。①硬水中含有较多的钙离子、镁离子,长期饮用硬水对人体健康不利,生活中常用鉴别硬水和软水,常用的方法降低水的硬度。
②消毒剂高铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化。高铁酸钠中铁元素的化合价为;
(2)、图乙是一个自制的简易净水器。A、B两层需要放置细沙或活性炭,根据净化材料特性,A层放置的材料最好是(选“细沙”或“活性炭”)。(3)、节约用水是每个公民的义务,下列用水方式不应提倡的是(填字母序号)。A 间断地流水洗衣
B 用喷灌、滴灌的方法浇灌
C 园林用淘米水浇花
D 桶装水没用完就倒掉
28. 根据下列实验装置图,回答问题: (1)、写出如图所示装置中标有序号的仪器名称:① , ②。(2)、实验室用过氧化氢溶液和二氧化锰混合制取氧气,所选用的发生装置是(选填装置序号,下同),组装好仪器后,应先 , 再添加药品,请写出该反应的化学方程式 , 现准备收集一瓶氧气供细铁丝燃烧的实验用,选择装置收集氧气便于直接做这个实验。(3)、甲烷是一种无色无味,难溶于水。密度比空气小的气体,实验室常用加热无水醋酸钠和碱石灰的固体混合物制取甲烷时,发生装置应选 , 收集装置应选用。29. 下图是小梅配制100g溶质质量分数为12%的NaCl溶液的实验操作示意图:
(1)、写出如图所示装置中标有序号的仪器名称:① , ②。(2)、实验室用过氧化氢溶液和二氧化锰混合制取氧气,所选用的发生装置是(选填装置序号,下同),组装好仪器后,应先 , 再添加药品,请写出该反应的化学方程式 , 现准备收集一瓶氧气供细铁丝燃烧的实验用,选择装置收集氧气便于直接做这个实验。(3)、甲烷是一种无色无味,难溶于水。密度比空气小的气体,实验室常用加热无水醋酸钠和碱石灰的固体混合物制取甲烷时,发生装置应选 , 收集装置应选用。29. 下图是小梅配制100g溶质质量分数为12%的NaCl溶液的实验操作示意图: (1)、上图中的玻璃仪器分别是广口瓶、量筒、烧杯和。(2)、指出图中的一处不正确操作。(3)、配制时应选择mL(10mL或50mL或100mL)的量筒量取所需要的水。(4)、用上述图示的序号表示配制溶液的操作顺序。(5)、若在量取水时俯视凹液面最低处,其它操作正确,则所得溶液的溶质质量分数为12%(填>或<或=)。30. 空气是一种重要资源(1)、如图1所示装置可测定空气中氧气的含量,用注射器抽取30mL空气,硬质玻璃管的体积为50mL,在硬质玻璃管中放入过量的铜粉,在右侧导管口套上瘪的气球,点燃酒精灯,反复推拉注射器,待反应结束后,冷却值室温.
(1)、上图中的玻璃仪器分别是广口瓶、量筒、烧杯和。(2)、指出图中的一处不正确操作。(3)、配制时应选择mL(10mL或50mL或100mL)的量筒量取所需要的水。(4)、用上述图示的序号表示配制溶液的操作顺序。(5)、若在量取水时俯视凹液面最低处,其它操作正确,则所得溶液的溶质质量分数为12%(填>或<或=)。30. 空气是一种重要资源(1)、如图1所示装置可测定空气中氧气的含量,用注射器抽取30mL空气,硬质玻璃管的体积为50mL,在硬质玻璃管中放入过量的铜粉,在右侧导管口套上瘪的气球,点燃酒精灯,反复推拉注射器,待反应结束后,冷却值室温.
①实验时,铜粉过量的目的是。
②冷却后,理论上注射器内剩余气体的体积约为mL。
(2)、利用空气制取氮肥(尿素)的流程如图2所示:
①I中参加反应的单质甲为 , 请你写出Ⅲ中反应的化学方程式(煤的主要成分是碳)。
②已知常压下,氮气沸点-196℃,氧气沸点-183℃,若将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是。