山东省东营市广饶县2021-2022学年九年级上学期化学期中考试试卷
试卷更新日期:2021-11-18 类型:期中考试
一、单选题
-
1. 厨房是家庭中的小小实验室,厨房中有①面粉②豆油③纯碱④料酒⑤味精⑥胡椒面⑦面酱⑧食醋⑨食盐⑩白砂糖等,把它们分别放入适量水中,充分搅拌能够得到溶液的是( )A、①③⑤⑥⑧⑨⑩ B、③④⑤⑧⑨⑩ C、②③⑦⑧⑨⑩ D、③④⑥⑧⑨⑩2. 推理是一种重要的化学思维方法,以下推理合理的是( )A、酸溶液的pH小于7,故pH小于7的溶液一定是酸溶液 B、溶液是均一、稳定的,所以均一、稳定的物质一定是溶液 C、洗涤剂去油污是利用了乳化作用,则汽油去油污也是利用了乳化作用 D、中和反应一定有盐和水生成,但是有盐和水生成的反应不一定是中和反应3. 《天工开物》中对“海水盐”有如下描述:“凡煎盐锅古谓之“牢盆”,……其下列灶燃薪,多者十二三眼,少者七八眼,共煎此盘,……火燃釜底,滚沸延及成盐。”文中没有涉及到的操作是( )A、加热 B、结晶 C、蒸发 D、过滤4. 根据如图原理,海水加压一段时间后,剩余海水中不变的是( )
 A、溶质质量 B、溶液组成 C、溶液质量 D、溶剂质量5. 下列叙述错误的是( )A、利用光照和风力使水分蒸发得到食盐 B、海水晒盐得到食盐后的母液可用于提取多种化工原料 C、海水淡化只能得到淡水,剩余物质不再有利用价值 D、'海水中溶有二氧化碳,可供海水中的绿色植物进行光合作用6. 正确规范的操作是实验成功和人身安全的重要保证。( )A、测定溶液pH
A、溶质质量 B、溶液组成 C、溶液质量 D、溶剂质量5. 下列叙述错误的是( )A、利用光照和风力使水分蒸发得到食盐 B、海水晒盐得到食盐后的母液可用于提取多种化工原料 C、海水淡化只能得到淡水,剩余物质不再有利用价值 D、'海水中溶有二氧化碳,可供海水中的绿色植物进行光合作用6. 正确规范的操作是实验成功和人身安全的重要保证。( )A、测定溶液pH B、配制溶液
B、配制溶液  C、称量固体
C、称量固体  D、稀释浓硫酸
D、稀释浓硫酸  7. 食醋里通常含有3%-5%的醋酸(CH3COOH),食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。下列不能作为醋酸属于酸的证据的是( )A、产生的气体是二氧化碳 B、食醋可以去除金属制品上的的少量锈迹 C、加水稀释食醋,溶液pH变大 D、不宜用铝容器盛装食醋8. 下列关于海洋开发利用的说法中正确的是( )A、海水“晒盐”获得是纯净物氯化钠 B、海底的可燃冰大量燃烧后,不会造成温室效应 C、海洋是个巨人的水资源库,如何获取廉价的淡水对缓解淡水危机意义重大 D、可以从海水中直接提取纯碱9. 下列图象不能正确反映其对应的实验操作的是( )A、
7. 食醋里通常含有3%-5%的醋酸(CH3COOH),食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。下列不能作为醋酸属于酸的证据的是( )A、产生的气体是二氧化碳 B、食醋可以去除金属制品上的的少量锈迹 C、加水稀释食醋,溶液pH变大 D、不宜用铝容器盛装食醋8. 下列关于海洋开发利用的说法中正确的是( )A、海水“晒盐”获得是纯净物氯化钠 B、海底的可燃冰大量燃烧后,不会造成温室效应 C、海洋是个巨人的水资源库,如何获取廉价的淡水对缓解淡水危机意义重大 D、可以从海水中直接提取纯碱9. 下列图象不能正确反映其对应的实验操作的是( )A、 A图:向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
B、
A图:向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
B、 B图:向一定量氢氧化钠和碳酸钠的混合溶液中加入过量的石灰水
C、
B图:向一定量氢氧化钠和碳酸钠的混合溶液中加入过量的石灰水
C、 C图:向含有一定量硫酸的硫酸钠溶液中滴加氯化钡溶液
D、
C图:向含有一定量硫酸的硫酸钠溶液中滴加氯化钡溶液
D、 D图:向部分变质的NaOH溶液中滴加过量稀盐酸
10. 如图为甲、乙、丙三种物质的溶解度曲线。下列说法正确的是( )
D图:向部分变质的NaOH溶液中滴加过量稀盐酸
10. 如图为甲、乙、丙三种物质的溶解度曲线。下列说法正确的是( ) A、t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等 B、将甲、乙、丙的饱和溶液从t2℃降到t1℃,析出晶体质量最大的是甲 C、将甲的饱和溶液由t1℃升温至t2℃,溶质质量分数变大 D、t2℃时,等质量的甲乙丙三种物质分别溶于水得到饱和溶液,甲需要的水质量最大11. 除去下列物质中的杂质,选用的方法和试剂正确的是( )
A、t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等 B、将甲、乙、丙的饱和溶液从t2℃降到t1℃,析出晶体质量最大的是甲 C、将甲的饱和溶液由t1℃升温至t2℃,溶质质量分数变大 D、t2℃时,等质量的甲乙丙三种物质分别溶于水得到饱和溶液,甲需要的水质量最大11. 除去下列物质中的杂质,选用的方法和试剂正确的是( )选项
物质
杂质
除去杂质所用的试剂和方法
A
碳酸钠粉末
碳酸钙粉末
加足量水过滤、蒸发
B
二氧化碳
氯化氢
通过氢氧化钠溶液、洗气
C
铁
氧化铁
加足量盐酸、过滤
D
氯化铁溶液
盐酸
加足量铁粉、过滤
A、A B、B C、C D、D12. 石蕊、硫酸、氢氧化钙、碳酸钠是常见的四种物质,它们的溶液之间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述正确的是( ) A、石蕊溶液变为红色 B、无明显现象 C、有无色气泡产生 D、石蕊呈紫色
A、石蕊溶液变为红色 B、无明显现象 C、有无色气泡产生 D、石蕊呈紫色二、填空题
-
13. 酸、碱、盐之间的反应与人们日常生活有着密切的关系。(1)、食醋能作酸味的调味剂,是因为其主要成分醋酸(化学式为CH3OOH)在水溶液中能解离出CH3COO-和(填离子符号)。(2)、胃液分泌过多会引起胃病。服用含有氢氧化铝的药物可缓解病痛,其治疗的化学原理为(用化学方程式表示)。(3)、某同学不小心被黄蜂了(黄蜂毒液呈碱性),为了减轻疼痛可以涂抹下列物质中的(填字母)。
A食醋(pH=3) B浓硫酸 C食盐水(pH=7) D苏打或肥皂水(pH=9~10)
(4)、酿酒厂生产白酒时,常加入适量稀硫酸来控制酸度,发酵完成后进行蒸馏,即可得到白酒,盐酸的价格比硫酸低,同样能控制酸度,请说明控制酸度不用盐酸的原因。14. 图1是三种常见物质的溶解度曲线。请回答以下问题。
 (1)、由图1可知,同质量的三种物质的饱和溶液由50℃降温到10℃时,析出晶体质量最多的物质是(填名称)。(2)、图1所示三种物质中溶解度随温度升高而减小的物质(填名称)。(3)、若硝酸钾固体中混有少量氯化钠、提纯硝酸钾的方法是(选填“降温结晶”“蒸发结晶”)。(4)、现有40℃时等质量的硝酸钾、氯化钠的饱和溶液,加热蒸发等质量的水后恢复至40℃,剩余溶液的质量关系大小为硝酸钾的氯化钠的(选填“>”、“=”或“<”)。(5)、若a、b、c分別代表上述三种物质,图2是在室温下,烧杯中a物质的溶液、试管①中b物质的溶液和试管②中c物质的溶液的状态。当从室温升至60℃时,发现烧杯中a物质没有明显变化,试管①中b物质全部溶解,试管②中有c物质析出,写出a、b、c三种物质的化学式:a , b , c。(6)、20℃时,欲测定Ca(OH)2溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH(填“偏大”、“偏小”或“不受影响”)。15. 构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
(1)、由图1可知,同质量的三种物质的饱和溶液由50℃降温到10℃时,析出晶体质量最多的物质是(填名称)。(2)、图1所示三种物质中溶解度随温度升高而减小的物质(填名称)。(3)、若硝酸钾固体中混有少量氯化钠、提纯硝酸钾的方法是(选填“降温结晶”“蒸发结晶”)。(4)、现有40℃时等质量的硝酸钾、氯化钠的饱和溶液,加热蒸发等质量的水后恢复至40℃,剩余溶液的质量关系大小为硝酸钾的氯化钠的(选填“>”、“=”或“<”)。(5)、若a、b、c分別代表上述三种物质,图2是在室温下,烧杯中a物质的溶液、试管①中b物质的溶液和试管②中c物质的溶液的状态。当从室温升至60℃时,发现烧杯中a物质没有明显变化,试管①中b物质全部溶解,试管②中有c物质析出,写出a、b、c三种物质的化学式:a , b , c。(6)、20℃时,欲测定Ca(OH)2溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH(填“偏大”、“偏小”或“不受影响”)。15. 构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题: (1)、为了验证性质①,李华将紫色石蕊试液滴加到稀盐酸中,溶液变成色。(2)、李华将一枚生锈的铁钉放入足量的稀盐酸中,他首先观察到的现象是 , 过一会儿,他又观察到。发生以上反应现象的化学方程式分别为、。李华的这个实验体现了性质(填序号,下同),其中性质在工业上可用于除铁锈。(3)、假设编号③反应的盐是AgNO3 , 则编号③对应的化学方程式是。(4)、物质组成和结构决定其性质。从微观进入宏观,探索物质变化规律。
(1)、为了验证性质①,李华将紫色石蕊试液滴加到稀盐酸中,溶液变成色。(2)、李华将一枚生锈的铁钉放入足量的稀盐酸中,他首先观察到的现象是 , 过一会儿,他又观察到。发生以上反应现象的化学方程式分别为、。李华的这个实验体现了性质(填序号,下同),其中性质在工业上可用于除铁锈。(3)、假设编号③反应的盐是AgNO3 , 则编号③对应的化学方程式是。(4)、物质组成和结构决定其性质。从微观进入宏观,探索物质变化规律。例如:稀盐酸不能与氯化钡溶液反应,而稀硫酸则能与之反应生成白色沉淀,写出化学方程式:。体现了不同的酸也具有各自的特性,原因是。
(5)、通过分析组成和结构,可以预测物质的某些性质。根据如图硫酸氢钠溶液的微观图示,分析推断NaHSO4的性质,其中正确的是 A、其水溶液能使紫色石蕊试液变蓝 B、其水溶液能与金属镁粉反应 C、其水溶液能与碳酸钠反应 D、其水溶液能与硝酸钡溶液反应
A、其水溶液能使紫色石蕊试液变蓝 B、其水溶液能与金属镁粉反应 C、其水溶液能与碳酸钠反应 D、其水溶液能与硝酸钡溶液反应三、综合题
-
16. 海水中有大量可以利用的化学资源, 例如氯化镁、氯化钠、溴化钾等。综合利用海水制备金属镁的流程如图所示:
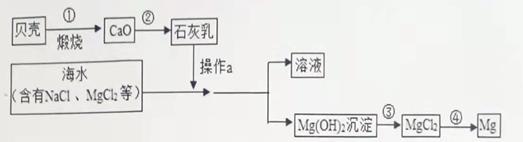 (1)、从海水中获得食盐用到的方法是 , 提取氯化镁不用该方法的原因是。(2)、请写出其中任意三个反应的化学方程式,要求所属反应基本类型不能有重复。;;。17. 学习化学开启了我们认识物质之旅。某实验小组的同学对氢氧化钠的性质及应用进行了如下的探究。(1)、(探究一)溶解过程中的能量变化。如图所示,同学们设计了不同的实验方案进行探究:
(1)、从海水中获得食盐用到的方法是 , 提取氯化镁不用该方法的原因是。(2)、请写出其中任意三个反应的化学方程式,要求所属反应基本类型不能有重复。;;。17. 学习化学开启了我们认识物质之旅。某实验小组的同学对氢氧化钠的性质及应用进行了如下的探究。(1)、(探究一)溶解过程中的能量变化。如图所示,同学们设计了不同的实验方案进行探究:
实验一中的硝酸铵溶解后,溶液温度(填“升高”、“降低”或“不变”)。
(2)、实验二所加试剂及用量如图,将分液漏斗中的水全部加入试管后,立即关闭分液漏斗的活塞,此时观察到U形管的液面左低右高,由此得出“氢氧化钠溶于水时放出热量”的结论,你不同意此结论,写出你的理由。(3)、(探究二)氢氧化钠的化学性质如图所示,同学们用氢氧化钠进行了下列实验,请分析并回答下列问题:

①中观察到的现象是 , ②试管中观察到的现象是。
(4)、③试管中发生反应的化学方程式。(5)、③④⑤试管中发生的反应属于复分解反应的是。(6)、实验⑤⑥为用软矿泉水瓶所做的对比实验,装的软矿泉水瓶变瘪更明显,原因是。(用化学方程式表示)(7)、(探究三)氢氧化钠在实验室中的应用①实验室中能用氢氧化钠溶液吸收的气体是(填字母序号)。
a、二氧化碳b、水蒸气c、氯化氢d、氧气
②吸收上述所选气体一般不用氢氧化钙溶液,主要是因为氢氧化钠和氢氧化钙的不同。
四、计算题
-
18. 黄铜(铜锌合金)因性能优良,被广泛用于制作钱币、饰品和生产中,铜的质量分数在59%~65%之间的黄铜性能优良。兴趣小组为了解某黄铜螺母的材料性能进行如下实验:取多个黄铜螺母放入烧杯中,另取 80g 稀硫酸,分四次等质量加入,每次均充分反应,得到实验数据如下表所示:
实验次数
1
2
3
4
稀硫酸的用量/g
20
20
20
20
剩余固体的质量/g
20.0
17.4
m
13.5
(1)、m=。所取黄铜螺母中铜的质量为g。(2)、请通过计算说明该黄铜螺母的材料性能是否优良?(3)、计算稀硫酸中溶质的质量分数(写出计算过程)。(4)、分析实验数据,在下图坐标中画出加入 80g 稀硫酸过程中相应的曲线图(纵坐标为自行设定物质的质量;并标出曲线中必要的数据)。