江苏省无锡市锡山区锡北片2021-2022学年九年级上学期化学期中考试试卷
试卷更新日期:2021-11-18 类型:期中考试
一、单选题
-
1. 下列变化属于化学变化的是( )A、蜡烛融化 B、湖水结冰 C、水分蒸发 D、蜡烛燃烧2. 下列元素符号代表氮元素的是( )A、H B、C C、N D、O3. 下列元素属于金属元素的是( )A、H B、O C、Fe D、N4. 下列化学式书写错误的是( )A、氯化钙CaCl2 B、氧化镁 MgO C、氯化氢HCl D、氧化铝AlO5. 下列实验操作中,正确的是( )
A、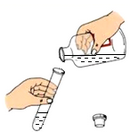 倾倒液体
B、
倾倒液体
B、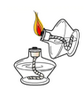 点燃酒精灯
C、
点燃酒精灯
C、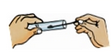 取用固体粉末
D、
取用固体粉末
D、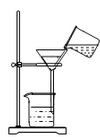 过滤
6. 物质的下列性质,属于化学性质的是( )A、铜丝导电 B、铁锅导热 C、蔗糖溶解 D、木炭可燃7. 某微粒的原子核和核外电子如图所示:
过滤
6. 物质的下列性质,属于化学性质的是( )A、铜丝导电 B、铁锅导热 C、蔗糖溶解 D、木炭可燃7. 某微粒的原子核和核外电子如图所示: ,该微粒是( ) A、分子 B、原子 C、阴离子 D、阳离子8. 二氧化碳的分子式是:CO2 , 二氧化硫的分子式是:SO2。下列说法错误的是( )A、两种物质中都含有氧元素 B、二氧化硫由两种元素组成 C、两种物质都是化合物 D、两种物质均由相同的元素组成9. 乙烯是重要的工业原料,乙烯由C和H按原子比1:2构成,乙烯具有可燃性。乙烯的分子模型如图所示。下列说法错误的是( )
,该微粒是( ) A、分子 B、原子 C、阴离子 D、阳离子8. 二氧化碳的分子式是:CO2 , 二氧化硫的分子式是:SO2。下列说法错误的是( )A、两种物质中都含有氧元素 B、二氧化硫由两种元素组成 C、两种物质都是化合物 D、两种物质均由相同的元素组成9. 乙烯是重要的工业原料,乙烯由C和H按原子比1:2构成,乙烯具有可燃性。乙烯的分子模型如图所示。下列说法错误的是( ) A、乙烯属于化合物 B、乙烯属于氧化物 C、乙烯的分子式为C2H4 D、乙烯燃烧可能会生成二氧化碳和水10. 加碘盐中往往添加了碘酸钾(KIO3)。下列有关说法错误的是( )A、加碘盐可为人体补充碘元素 B、碘酸钾既是氧化物也是化合物 C、碘酸钾中碘元素的质量分数为59.3% D、在缺碘地区应该推广使用加碘盐11. 利用过氧化氢催化分解制备氧气,其中错误的( )A、
A、乙烯属于化合物 B、乙烯属于氧化物 C、乙烯的分子式为C2H4 D、乙烯燃烧可能会生成二氧化碳和水10. 加碘盐中往往添加了碘酸钾(KIO3)。下列有关说法错误的是( )A、加碘盐可为人体补充碘元素 B、碘酸钾既是氧化物也是化合物 C、碘酸钾中碘元素的质量分数为59.3% D、在缺碘地区应该推广使用加碘盐11. 利用过氧化氢催化分解制备氧气,其中错误的( )A、 制备氧气
B、
制备氧气
B、 收集氧气
C、
收集氧气
C、 检验氧气
D、
检验氧气
D、 干燥氧气
12. 按照氮元素的化合价递变排列:NH3、X、NaNO2、NO2、NaNO3。其中X是( )A、N2 B、N2O4 C、N2O3 D、Ca(NO3)213. 下列关于过滤操作的叙述错误的是( )A、滤纸的边缘要低于漏斗口 B、液面不要低于滤纸的边缘 C、玻璃棒要靠在三层滤纸的一边 D、漏斗下端的管口要紧靠烧杯内壁14. 蜡烛在如图所示密闭的集气瓶内燃烧至熄灭,测得瓶内氧气体积分数的变化如图所示。下列判断正确的是( )
干燥氧气
12. 按照氮元素的化合价递变排列:NH3、X、NaNO2、NO2、NaNO3。其中X是( )A、N2 B、N2O4 C、N2O3 D、Ca(NO3)213. 下列关于过滤操作的叙述错误的是( )A、滤纸的边缘要低于漏斗口 B、液面不要低于滤纸的边缘 C、玻璃棒要靠在三层滤纸的一边 D、漏斗下端的管口要紧靠烧杯内壁14. 蜡烛在如图所示密闭的集气瓶内燃烧至熄灭,测得瓶内氧气体积分数的变化如图所示。下列判断正确的是( ) A、瓶内只要有氧气蜡烛就可以燃烧 B、蜡烛熄灭后集气瓶内只剩二氧化碳气体 C、蜡烛熄灭是因为容器内的氧气全部被消耗 D、燃烧过程中瓶内的水蒸气浓度会升高15. 液氦用于制造超冷环境。下列关于氦的说法错误的是( )
A、瓶内只要有氧气蜡烛就可以燃烧 B、蜡烛熄灭后集气瓶内只剩二氧化碳气体 C、蜡烛熄灭是因为容器内的氧气全部被消耗 D、燃烧过程中瓶内的水蒸气浓度会升高15. 液氦用于制造超冷环境。下列关于氦的说法错误的是( ) A、氦原子核由质子和中子构成 B、氦原子核内质子数等于核外电子数 C、氦的相对原子质量是4.003 D、氦由人工制备,空气中不含氦气16. 下列对一些事实的解释不合理的是( )
A、氦原子核由质子和中子构成 B、氦原子核内质子数等于核外电子数 C、氦的相对原子质量是4.003 D、氦由人工制备,空气中不含氦气16. 下列对一些事实的解释不合理的是( )选项
客观事实
解释
A
冬天戴眼镜进入室内,镜片出现水雾
镜片阻挡分子运动,使其液化
B
电解水得到氢气和氧气
水中含有氢和氧元素
C
粮仓充入氮气可以防止害虫入侵
氮气不支持害虫呼吸
D
澄清石灰水中通入CO2 , 出现白色浑浊
生成了难溶性物质
A、A B、B C、C D、D17. H和O可以形成A、B两种物质,相关信息如图所示。下列有关说法正确的是( )物质
分子中原子个数比
分子中元素质量比
A
2:1
1:8
B
1:1
1:16
A、物质A中氧元素的质量分数为33.3% B、物质A和B中氢元素的质量分数相同 C、两种物质均可在一定条件下分解得到氧气 D、在加热条件下物质B更稳定不易分解二、选择题组
-
18. 请阅读下列材料,回答下列问题。
我国向国际社会承诺,2030年实现“碳达峰”,2060年实现“碳中和”。“碳达峰”指的是二氧化碳排放达到最大量。“碳中和”指的是在一定时间内直接或间接产生的二氧化碳或温室气体排放总量,通过植树造林、节能减排等形式,以抵消自身产生的二氧化碳或温室气体排放量,实现正负抵消,达到相对“零排放”。如下图是自然界中碳、氧循环简图(Y为C6H12O6)。
 (1)、下列措施不利于实现“碳中和”目标的是( )A、扩大城市绿化面积 B、多开燃油车出行 C、加大风能、太阳能的利用 D、研究二氧化碳的捕集技术(2)、下列对自然界中碳、氧循环简图的分析正确的是( )A、转化1和转化2均是化合反应 B、转化1可表示绿色植物的光合作用 C、转化1和转化2都是物理变化 D、转化1和转化2中O元素的化合价不变(3)、Y是生物细胞的能量物质。下列说法错误的是( )A、Y是由6个C、12个H和6个O构成 B、Y中碳、氧元素的质量比为2∶3 C、Y中O的质量分数大于H的质量分数 D、Y的相对分子质量为180
(1)、下列措施不利于实现“碳中和”目标的是( )A、扩大城市绿化面积 B、多开燃油车出行 C、加大风能、太阳能的利用 D、研究二氧化碳的捕集技术(2)、下列对自然界中碳、氧循环简图的分析正确的是( )A、转化1和转化2均是化合反应 B、转化1可表示绿色植物的光合作用 C、转化1和转化2都是物理变化 D、转化1和转化2中O元素的化合价不变(3)、Y是生物细胞的能量物质。下列说法错误的是( )A、Y是由6个C、12个H和6个O构成 B、Y中碳、氧元素的质量比为2∶3 C、Y中O的质量分数大于H的质量分数 D、Y的相对分子质量为180三、填空题
-
19. 2021年10月20日,太湖边空气质量指数为50。空气质量良好。(1)、下列属于空气污染物的是(填序号)。
a.氮气 b.氧气 c.二氧化硫
(2)、大气中体积分数含量最大的是(填序号)。a.氮气 b.氧气 c.二氧化碳
(3)、下列属于温室气体的是(填序号)。a.氮气 b.氧气 c.二氧化碳
20. 太湖鼋头渚石崖上刻有“包孕吴越”四字。 (1)、“包孕吴越”中“吴越”指的是江浙地区的人民。 “包孕”一词的含义是。(2)、水的分子式是。(3)、保护太湖水资源的措施是(任写一条)。21. 无锡自来水出厂水样2021年10月10日检测结果如下表所示。
(1)、“包孕吴越”中“吴越”指的是江浙地区的人民。 “包孕”一词的含义是。(2)、水的分子式是。(3)、保护太湖水资源的措施是(任写一条)。21. 无锡自来水出厂水样2021年10月10日检测结果如下表所示。序
号
检测
项目
中桥水厂
雪浪水厂
锡东水厂
锡澄水厂
单位
国
标
合格
情况
最高
最低
最高
最低
最高
最低
最高
最低
1
浊度
0.12
0.06
0.05
0.04
0.09
0.05
0.07
0.03
NTU
1
合
格
2
色度
5
5
5
5
5
5
5
5
度
15
3
臭和味
0
0
0
0
0
0
0
0
度
无异味
4
肉眼可见物
无
无
无
无
无
无
无
无
无
5
COD
1.44
1.09
1.30
1.06
1.47
1.15
1.06
0.94
mg/L
3
6
余氯
0.7
0.6
0.8
0.7
0.8
0.7
0.88
0.66
mg/L
0.3-4mg/L
7
菌落总数
0
0
0
0
0
0
0
0
CFU/mL
100
8
总大肠杆菌
0
0
0
0
0
0
0
0
CFU/100mL
不得检出
9
耐热大肠杆菌群
0
0
0
0
0
0
0
0
CFU/100mL
不得检出
合格率
100%
(1)、根据检测结果,锡东水厂2021年10月10日出厂水质(填“合格”或“不合格”)。(2)、自来水生产中常用于除去嗅和味的是(填物质名称)。(3)、氯气用于杀菌。氯分子由2个氯原子构成,则氯气分子式是。(4)、出厂自来水保持含有一定量的“余氯”,其作用是。22. 为研究氧气的性质,进行下列制备氧气的实验。(1)、采用固体药品热分解制备氧气。如图所示,实验所用反应物为高锰酸钾。
①写出上述集气瓶中所收集气体的分子式。
②上述实验中需要将试管口略微向下倾斜,是为了防止。
③上述实验中收集氧气的方法可称之为。
(2)、利用液体物质分解制备氧气。如图所示,实验所用药品为过氧化氢和二氧化锰。
①实验时先按图2组装好装置,紧接着必须进行的操作步骤是。
②实验中,生成氧气的反应容器名称是。
③实验中,二氧化锰所起到的作用是。
(3)、探索液体-固体反应制备氧气的方法。资料:过氧化钠(Na2O2)为淡黄色固体,和水反应,生成氢氧化钠(NaOH)和氧气。
①水和过氧化钠反应可制备氧气。组装反应装置,至少必须选用的仪器是。(填编号)

②Na2O2中的氧元素的化合价为。
③检验反应中是否生成氧气的方法是。
④用“反应表示式”表示从反应物转化为生成物的过程。
23. STEM研究小组利用数字传感技术对教室内二氧化碳气体进行检测,结果如图所示。图中纵坐标为二氧化碳浓度,单位是ppm(每百万分之体积分数)。 (1)、二氧化碳属于氧化物,分子中C的化合价为;通常空气中氧气的体积分数约为。(2)、从检测开始,随着时间的推移,A、B两教室内二氧化碳浓度的变化趋势是;造成A、B两间教室二氧化碳浓度变化不同的原因是。(3)、通过上述实验数据分析,出于呼吸健康的考虑,你的合理化建议是。24. 可燃冰是一种在海底储量巨大的清洁能源,对可燃冰的研究方兴未艾。(1)、探究可燃冰的组成。
(1)、二氧化碳属于氧化物,分子中C的化合价为;通常空气中氧气的体积分数约为。(2)、从检测开始,随着时间的推移,A、B两教室内二氧化碳浓度的变化趋势是;造成A、B两间教室二氧化碳浓度变化不同的原因是。(3)、通过上述实验数据分析,出于呼吸健康的考虑,你的合理化建议是。24. 可燃冰是一种在海底储量巨大的清洁能源,对可燃冰的研究方兴未艾。(1)、探究可燃冰的组成。
将可燃冰加热到20℃以上,发生分解,生成甲烷气和水。
①已知甲烷分子中只含有碳和氢两种元素,且碳和氢的原子比为1:4。则甲烷的分子式是;甲烷分子中氢元素的质量分数为。
②可燃冰可以看作是1个分子的甲烷和8个分子的水结合而成。计算可燃冰中甲烷所占的质量分数。
(2)、开采和利用可燃冰。
方法一:热解法
将可燃冰在海底加热,使其分解成甲烷,再通过管道将甲烷气输送到海面上。
①热解法是一种高能耗的开采方式,原因是。
②甲烷的温室效应是二氧化碳的13倍。热解法开采可能对大气环境造成的危害是。
方法二:置换法
将二氧化碳通入海底可燃冰层中,在海水的高压下,二氧化碳和可燃冰中的水结合,形成水合二氧化碳,同时释放出甲烷气。

③水和二氧化碳在常温下即可反应生成水合二氧化碳。反应如上图所示。该反应的反应类型为。
④甲烷是清洁燃料和化工原料。高温下甲烷分解为两种单质,单质的化学式是。
四、科普阅读题
-
25. 阅读下列科普短文,回答相关问题。
2021年2月,我国在张家口建成了首个加氢站(氢气),为2022年冬奥会崇礼赛区大巴加注氢能。作为全国运营氢能公交车最多的城市,张家口市已有 214 辆氢能公交车在运行。
氢气不仅是清洁燃料,而且能实现污染物净零排放。氢气燃烧值高,单位质量氢气燃烧放出的热是天然气的2.6倍、汽油的 3.1倍、煤炭的4倍。
氢能在多个行业有着广阔的应用前景。在运输行业,与传统燃油汽车比,氢燃料汽车不产生污染,同时又比电动汽车加注时间短、续航更远。较长距离、固定路线的快递货车和载重货车等重型卡车,以及水上交通运输等都可大规模应用氢能。
氢能可作为固定能源用于建筑、社区等的备用供能。燃气(CH4)中混入一定量的氢气,燃烧使用与天然气相同,但单位质量燃烧放热更高、碳排放更低。风力发电和太阳能发电与居民用电在季节上、昼夜交替和有风无风等方面存在不匹配问题,而氢能恰好可用来补充调节备用。
氢气可作为化学过程的原料。比如,直接用氢气炼铁(氢气和氧化铁反应)已经成为绿色炼铁的重要发展方向。传统的炼铁采用一氧化碳和氧化铁高温下反应生成液态铁水和二氧化碳,是一种传统的高碳排放行业。采用氢气和氧化铁加热反应,既能降低能耗,又大大减轻了碳排放。
氢气制备来源广泛,可由多种方式制备而得。制备方式不同,得到的氢名称也不同,有绿氢、蓝氢、灰氢和棕氢( 褐氢) 之分。
绿氢由电解水得到,或由氨(NH3)高温分解得到,或生物质气化、光解水得到。电解水是绿氢制备的主要方式,整个过程零碳排放。比如利用风力发电和太阳能发电所产生的电能电解水,技能很好地生成绿氢,也能很好地解决风、光发电所存在电力浪费问题。
蓝氢来自于天然气,由蒸汽甲烷热解等方式转化制取。灰氢主要通过焦炉煤气、氯碱尾气等制备。棕氢 ( 褐氢) 由煤炭、石油等高碳化石能源制备。蓝氢、灰氢 和棕氢( 褐氢) 产自化石能源和工业尾气的制氢过程。
氢能的开发利用尚处于起步阶段,需要解决制备氢气、储存、运输和安全使用等多个瓶颈。尽管如此,氢能在环保和能效方面所具有的巨大潜力正在吸引全世界科学研究和产业投资。有志青少年可投身于氢能开发研究,未来一定大有可为!
(1)、氢能是一种清洁燃料的原因是;燃烧16g甲烷放出的热是893千焦(kJ),则燃烧16g氢气放出的热是 kJ。(2)、将天然气(甲烷)和氢气混合,充分燃烧,燃烧的产物是;在实验室将混合燃气点燃前,需要进行的操作步骤是。(3)、氨气高温分解可制得绿氢和另一种单质,该单质的分子式是;太阳能发电电解水除了生成绿氢,还可得到另一产物的分子式是。(4)、传统炼铁的反应方程式是:Fe2O3+3CO 2Fe+3CO2 。参照该方程式,写出用氢气炼铁的化学反应方程式。五、流程题
-
26. 2009年6月份,太湖水体中出现大量藻类污染。科研人员对太湖水样进行下列处理,成功探索出将太湖水净化为饮用水的方法。处理流程如下:
 (1)、藻类的大量繁殖与水体中氮、磷、钾含量升高有关。磷的原子结构示意图为;钾的元素符号是;你认为藻类大量繁殖还与因素有关。(2)、上述流程中使用复合氯化铝作为混凝剂。混凝剂的作用是;某种复合氯化铝的化学式为:[Al2(OH)nCl2]m , 期中n的值是。(3)、通常若在实验室中进行普通的过滤,需要使用到的玻璃仪器有;上述流程中使用的超滤膜能够有效提高水样的澄清度。使用的超滤膜的作用是。(4)、臭氧发生器采用高压放电条件,将空气中的氧气转变为臭氧。臭氧是由氧元素构成的单质,相对分子质量为48。臭氧的分子式为;臭氧的氧化性比氧气强,臭氧的作用是。将含有臭氧的氧气从水池的底部通入,目的是。
(1)、藻类的大量繁殖与水体中氮、磷、钾含量升高有关。磷的原子结构示意图为;钾的元素符号是;你认为藻类大量繁殖还与因素有关。(2)、上述流程中使用复合氯化铝作为混凝剂。混凝剂的作用是;某种复合氯化铝的化学式为:[Al2(OH)nCl2]m , 期中n的值是。(3)、通常若在实验室中进行普通的过滤,需要使用到的玻璃仪器有;上述流程中使用的超滤膜能够有效提高水样的澄清度。使用的超滤膜的作用是。(4)、臭氧发生器采用高压放电条件,将空气中的氧气转变为臭氧。臭氧是由氧元素构成的单质,相对分子质量为48。臭氧的分子式为;臭氧的氧化性比氧气强,臭氧的作用是。将含有臭氧的氧气从水池的底部通入,目的是。
-
-