江苏省无锡市2021-2022学年九年级上学期期中化学试题练习(提高版)
试卷更新日期:2021-11-18 类型:期中考试
一、单选题
-
1. 下列图标中,不属于危险化学品标志是( )A、
 B、
B、 C、
C、 D、
D、 2. 下列物质由离子构成的是( )A、氨气 B、氮气 C、氯化钠 D、金刚石3. M在N中充分燃烧,发生的反应为M+2N Q+2R。M、N、Q、R均是由分子构成的物质,表中列出了N、Q、R的分子示意图。下列说法错误的是( )
2. 下列物质由离子构成的是( )A、氨气 B、氮气 C、氯化钠 D、金刚石3. M在N中充分燃烧,发生的反应为M+2N Q+2R。M、N、Q、R均是由分子构成的物质,表中列出了N、Q、R的分子示意图。下列说法错误的是( )物质
N
Q
R

分子示意图


 A、反应前后分子总数不变 B、反应前后原子总数不变 C、消耗的M和N的质量比是1:4 D、生成的Q和R的质量比是22:94. 下列化学用语中关于数字“2”的意义,说法正确的是( )A、O2表示2个氧原子 B、2O表示2个氧元素 C、O2﹣表示氧元素的化合价为﹣2价 D、2O2表示2个氧分子5. 在一个密闭容器中放入 M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识正确的是( )
A、反应前后分子总数不变 B、反应前后原子总数不变 C、消耗的M和N的质量比是1:4 D、生成的Q和R的质量比是22:94. 下列化学用语中关于数字“2”的意义,说法正确的是( )A、O2表示2个氧原子 B、2O表示2个氧元素 C、O2﹣表示氧元素的化合价为﹣2价 D、2O2表示2个氧分子5. 在一个密闭容器中放入 M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识正确的是( )物质
M
N
Q
P
反应前质量(g)
18
1
2
32
反应后质量(g)
X
26
2
12
A、X>18 B、反应中N、P的质量比为4:5 C、物质Q是该反应的催化剂 D、该变化的基本反应类型是化合反应6. 科学家成功地将二氧化碳转化为乙烯,反应前后分子种类变化的微观示意图如下。下列说法错误的是( )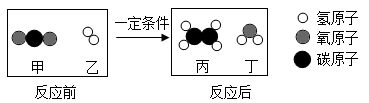 A、乙烯的化学式为C2H4 B、甲和丁均为氧化物 C、生成丙和丁的分子个数比为1:1 D、参加反应的甲与乙的质量比为22:37. 在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示,下列有关说法错误的是( )
A、乙烯的化学式为C2H4 B、甲和丁均为氧化物 C、生成丙和丁的分子个数比为1:1 D、参加反应的甲与乙的质量比为22:37. 在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示,下列有关说法错误的是( )物质
甲
乙
丙
丁
反应前的质量/g
40
3
10
15
反应t时刻的质量/g
23
19
a
反应后的质量/g
x
y
28
31
A、该反应可能是通电分解水 B、x+y=9,a=23 C、甲一定是化合物 D、乙可能是该反应的催化剂8. 分析推理是化学学习过程中常用的方法。下列推理正确的是( )A、原子是化学变化中的最小微粒,所以原子是不可再分的 B、化合物是由不同种元素组成的纯净物,所以含有不同种元素的纯净物一定是化合物 C、纸在空气中燃烧后质量减小,所以质量守恒定律不是普遍规律 D、单质是由一种元素组成的物质,所以由一种元素组成的物质一定是单质9. 逻辑推理是化学学习中常用的思维方法。下列推理正确的是( )A、氢气爆炸、火药爆炸都有新物质生成,因此爆炸都是化学变化 B、氧化物中含有氧元素,则含有氧元素的化合物一定是氧化物 C、蜡烛燃烧生成CO2和H2O,则蜡烛里一定含有碳元素和氢元素 D、分子是保持物质化学性质的最小粒子,因此分子不可再分10. 在一个密闭容器中,有a、b、c、d四种物质,化学反应前后各物质的质量关系如下图刻度纸所示(例如:c的质量为3g)。
下列说法正确的是( )
A、c一定是该反应的催化剂 B、反应结束后c的质量为14g C、a、d的相对分子质量之比为5:14 D、a、b变化的质量比一定为3:17二、多选题
-
11. 对于化学方程式 C+O2 CO2 表示的意义,叙述错误的是( )A、在点燃的条件下,碳和氧气生成二氧化碳 B、碳加氧气反应生成二氧化碳 C、每12份质量的碳和32份质量的氧气完全反应能生成44份质量的二氧化碳 D、每一个碳原子和一个氧分子化合生成一个二氧化碳分子
三、填空题
-
12. 有关水的实验装置如下图所示。
 (1)、图1是过滤装置,其中玻璃棒的作用为。(2)、图2是一种净水装置,其中所放的黑色固体为(写名称),该物质不仅可以 , 还可以。(3)、自来水经初步净化后还要进行杀菌消毒。实验小组查阅氯气杀菌消毒原理为:Cl2+H2O=X+HClO(次氯酸),则X的化学式为。(4)、图3为简易水电解器,电解水的化学方程式为 , a管中产生的气体是。(5)、水和过氧化氢组成元素相同,但化学性质不同,原因是。13. 用符号或符号表达的意义填空。
(1)、图1是过滤装置,其中玻璃棒的作用为。(2)、图2是一种净水装置,其中所放的黑色固体为(写名称),该物质不仅可以 , 还可以。(3)、自来水经初步净化后还要进行杀菌消毒。实验小组查阅氯气杀菌消毒原理为:Cl2+H2O=X+HClO(次氯酸),则X的化学式为。(4)、图3为简易水电解器,电解水的化学方程式为 , a管中产生的气体是。(5)、水和过氧化氢组成元素相同,但化学性质不同,原因是。13. 用符号或符号表达的意义填空。2个氢分子
碳酸钠
锌原子
符号
Fe2O3
3Cl-
14. “宏观-微观-符号”三重表征是化学独特的表示物质及其变化的方法。(1)、用粒子名称完成物质组成、结构和分类的概念关系图中的A、B处填空。A 、B (2)、下列各组物质中,都是由分子构成的是 (填字母)。
(2)、下列各组物质中,都是由分子构成的是 (填字母)。A水、氢气 B铁、氧气 C氯化钠、铜 D氯化钠、水
(3)、可以从不同角度对物质进行分类。现将食盐水、氢气、水、二氧化碳、铝、空气等六种物质分成三组,请填写下列空格。第一组:H2、Al,分类依据是 ;第二组: ,分类依据是都属于氧化物;第三组: ,分类依据是都属于混合物。
(4)、下表为元素周期表中某一周期元素的原子结构示意图。请回答下列问题:
①决定元素种类的是 。
②表中具有相对稳定结构的原子是 。
③铝离子符号为 。
④上述元素在周期表中处于同一周期的原因是 。
(5)、某化学反应的微观示意图如下:
该反应的化学方程式为 。
15. 在宏观、微观和符号之间建立联系是化学学科的重要思维方式,根据图示信息回答下列问题。 (1)、图甲为物质、粒子之间的关系图。
(1)、图甲为物质、粒子之间的关系图。①a的化学式是(举一例),b、c粒子的名称依次是。
②构成氯化钠的粒子是(填粒子符号)。
(2)、图乙为四种粒子的结构示意图。
①图乙中D若为原子,则X= , 其属于(填“金属元素”、“非金属元素”或“稀有气体元素”)。
②图乙中B、C属于同种元素,因为它们的相同。
③由A、B形成的化合物中,A、B元素的原子数目比为。
(3)、图丙是工业上生产尿素[化学式:CO(NH2)2]的反应的微观示意图。
①图示物质中属于氧化物的有(填字母)。
②该反应的化学方程式为。
16. 定量研究对于化学的发展有重大作用。(1)、大量实验证明,的质量总和,等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。(2)、化学反应前后肯定没有变化的是(填字母)。A 原子种类
B 原子数目
C 分子种类
D 分子数目
E 元素种类
F 元素质量
G 物质种类
H 物质的总质量
(3)、镁条燃烧的实验如图所示。取一根用砂纸打磨干净的长镁条和一个石棉网,将它们一起放在托盘天平上称量,质量为m1。在石棉网上方将镁条点燃,将镁条燃烧后的产物与石棉网一起放在托盘天平上称量,质量为m2。①镁条燃烧的化学方程式为 , 现象为。
②理论上m1应小于m2 , 请运用质量守恒定律进行解释:。
③若实际称得的m1大于m2 , 可能的原因是。
 17. 空气是大家最为熟悉的物质。
17. 空气是大家最为熟悉的物质。气体
吸入气体
呼出气体
X
77.95%
74.58%
Y
21.02%
15.16%
CO2
0.04%
3.28%
H2O
0.06%
6.06%
(1)、上表是小华用数字化实验对自己吸入的气体和呼出的气体进行探究实验记录,(以体积分数计算)。则X的化学式为。(2)、下图是对空气中氧气体积含量测定的实验装置图。
(经典赏析)法国科学家用图1装置测出空气中O2的体积分数约为20%,其反应化学方程式为 , 该实验选择汞的优点有(填字母)。
A汞常温下呈液态,便于形成液封
B反应生成的氧化汞是固态,几乎不影响装置内气体压强
C加热时汞只与氧气反应,不与其他气体反应
D汞的沸点较低,易形成蒸气,能将密闭装置内空气中的氧气几乎耗尽
(3)、(实验回顾)图2用红磷测定空气中氧气含量,红磷燃烧的化学方程式为 , 某实验小组用足量的红磷和气密性良好的此装置实验多次测量取平均值,测出的氧气含量常常远低于21%,为此进行如下再探究。(4)、(探究和分析)如图3装置,接通电源,用高压点火装置引燃红磷,利用传感器技术实时测定实验过程中装置内的压强、温度和氧气浓度,得到三条曲线,变化趋势如图4所示。
①X曲线表示压强变化趋势,Y曲线表示(填“温度”或“氧气浓度”)变化趋势。
②结合Y、Z两条曲线综合分析,图4中AB段压强变化的原因是;CD段变化的原因。
(5)、(探究结论)由图 3实验可以找出图2实验中O2含量偏低的原因是。18. 某兴趣小组开展“测定密闭容器中氧气的体积分数”的探究实验。(实验1)按图1所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。
(实验2)按图2所示装置,用蜡烛燃烧的方法测定空气中氧气的体积分数。
(实验3)按图3所示装置,在集气瓶内壁用水均匀涂某除氧剂,利用除氧剂和氧气反应的原理测定空气中氧气的体积分数。
 (1)、实验中,检查装置气密性的方法是。(2)、实验1中,红磷燃烧的主要现象是。红磷熄灭后,集气瓶冷却至室温,打开K,水能倒吸入集气瓶的原因是。(3)、实验2中测得氧气体积分数偏小,其原因是。(4)、(查阅资料)在老师的指导下,同学们又查阅了资料。
(1)、实验中,检查装置气密性的方法是。(2)、实验1中,红磷燃烧的主要现象是。红磷熄灭后,集气瓶冷却至室温,打开K,水能倒吸入集气瓶的原因是。(3)、实验2中测得氧气体积分数偏小,其原因是。(4)、(查阅资料)在老师的指导下,同学们又查阅了资料。资料1:二氧化碳因与氢氧化钠溶液发生化学反应生成碳酸钠和水,实验室常用氢氧化钠溶液来吸收二氧化碳。
资料2:蜡烛在密闭的集气瓶中燃烧,氧气浓度不断变小的同时,会有一氧化碳气体生成。常温下一氧化碳难溶于水,且不与氢氧化钠溶液反应。
(交流与讨论)根据以上信息回答下列问题:
有同学提议实验2中在集气瓶底部预先放少量氢氧化钠溶液吸收生成的二氧化碳气体,实验就能成功。该反应的化学方程式为:。但小华觉得不可行,其主要原因是。
(5)、(实验拓展)将测定氧气含量的数字传感器插入集气瓶后再次实验,测得实验1、实验2、实验3中氧气的体积分数随时间变化的关系分别如图4、图5、图6所示。依据图4、图5、图6信息,(填“实验1”、“实验2”或“实验3”)的测定方法更准确,判断依据是。 (6)、若实验3能顺利进行,结合你的学习经验,该除氧剂在反应物和生成物两方面应满足的条件是:反应物方面: , 生成物方面:。19. 实验室中,可利用下列装置制取某些气体,请回答下列问题。
(6)、若实验3能顺利进行,结合你的学习经验,该除氧剂在反应物和生成物两方面应满足的条件是:反应物方面: , 生成物方面:。19. 实验室中,可利用下列装置制取某些气体,请回答下列问题。 (1)、写出装置中标号仪器的名称:①;②。(2)、实验室用高锰酸钾制取氧气时,应选用的发生装置是(填字母),反应的化学方程式为。(3)、可以选择 G 装置收集氧气的原因是。(4)、如果用D 装置收集氧气,则氧气由端通入(填“a”或“b”)。(5)、小明用家里的注射器和废药瓶组装成一套微型装置(如图所示)替代装置C,用于实验室制备氧气,其反应的化学方程式为 , 用该装置做实验的优点是(填字母)。
(1)、写出装置中标号仪器的名称:①;②。(2)、实验室用高锰酸钾制取氧气时,应选用的发生装置是(填字母),反应的化学方程式为。(3)、可以选择 G 装置收集氧气的原因是。(4)、如果用D 装置收集氧气,则氧气由端通入(填“a”或“b”)。(5)、小明用家里的注射器和废药瓶组装成一套微型装置(如图所示)替代装置C,用于实验室制备氧气,其反应的化学方程式为 , 用该装置做实验的优点是(填字母)。
A节约药品用量B能完全消除废物的排放
C能控制液体的滴加速度D产生的气体不含任何杂质
四、计算题
-
20. N(NO2)3是科学家2011年发现的一种火箭燃料。请列式计算:(1)、N(NO2)3的相对分子质量;(2)、N(NO2)3中氮元素和氧元素的质量比;(3)、50t此火箭燃料所含氧元素的质量(结果保留一位小数)。
-