广东省湛江市2021-2022学年高一上学期期中考试化学试题
试卷更新日期:2021-11-12 类型:期中考试
一、单选题
-
1. 下列各组物质中都是纯净物的是( )A、氧化钙,碘酒 B、氢氧化铁胶体,金刚石 C、冰水混合物,干冰 D、液氧,空气2. 在我们的日常生活中出现了 “加碘食盐” 、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品这里的“碘、铁、钙、硒、氟”应理解为( )A、单质 B、元素 C、分子 D、氧化物3. 下列各组物质不属于同素异形体的是( )A、H2O和H2O2 B、O2和O3 C、金刚石和石墨 D、红磷和白磷4. 若将工业用盐亚硝酸钠(NaNO2)误作食盐,会使人中毒死亡。亚硝酸钠中氮元素化合价是( )A、+2 B、+3 C、+4 D、+55. 下列属于碱性氧化物的是( )A、Mn2O7 B、Al2O3 C、Na2O2 D、CaO6. 下列叙述正确的是( )A、直径介于1nm~100nm之间的微粒称为胶体 B、Fe(OH)3难溶于水,因此不可能均匀地分散在水里形成稳定的红褐色胶体 C、根据丁达尔效应,利用一束强光可以区别淀粉胶体和食盐溶液 D、胶体粒子是很多分子的集合体,因此不能透过滤纸,但可以通过半透膜7. 下列物质都能导电,其中属于电解质的是( )A、熔融的NaOH B、铁丝 C、稀硫酸 D、NaCl溶液8. 下列关于电解质的叙述,正确的是( )A、NaCl溶液在电流作用下电离出Na+和Cl- B、凡是溶于水后能电离出H+的化合物就叫酸 C、HCl溶液能导电,而液态的HCl难以导电 D、难溶物一定不属于电解质9. 下列物质属于电解质的是( )A、Zn B、NaOH C、CO2 D、乙醇10. 下列氧化还原反应中,电子转移的方向和数目均正确的是( )A、
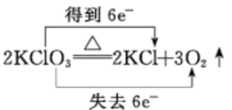 B、
B、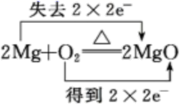 C、
C、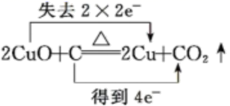 D、
D、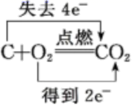 11. 下列电离方程式书写正确的是( )A、NaOH=Na++O2-+H+ B、FeCl3=Fe+3+3Cl- C、Mg(NO3)2=Mg2++ D、H2SO4=2H++12. 下列叙述中,正确的是( )A、氧化还原反应的本质是元素化合价发生了变化 B、含化合价升高元素的反应物被氧化 C、得到电子的物质被氧化 D、氧化还原反应中,氧化剂和还原剂一定是两种物质13. 下列变化过程一定需要加入还原剂的是( )A、KClO3→KCl B、KCl→AgCl C、H+→H2 D、C→CO214. 下列各组离子在溶液中能大量共存的是( )A、H+、Fe2+、Cl-、 B、Mg2+、K+、OH-、Cl- C、 、Ca2+、 、 D、K+、H+、Cl-、15. 能正确表示下列化学反应的离子方程式是( )A、氢氧化钡溶液与硝酸的反应OH-+H+=H2O B、澄清的石灰水与稀盐酸反应Ca(OH)2+2H+= Ca2++2H2O C、铜片插入硝酸银溶液中Cu+Ag+= Cu2++Ag D、碳酸钡溶于稀盐酸中CO32-+2H+= H2O+CO2↑16. 下列氧化还原反应中,水作为还原剂的是( )A、3Fe+4H2O Fe3O4+4H2 B、3NO2+H2O = 2HNO3 + NO C、2Na2O2+2H2O = 4NaOH+O2↑ D、2F2+2H2O = 4HF+O217. 下列各反应中,氧化反应与还原反应在同种元素中进行的是( )A、Cl2+2NaOH=NaCl+NaClO+H2O B、2KClO3 2KCl+3O2↑ C、2KMnO4 K2MnO4+MnO2+O2↑ D、2H2O 2H2↑+O2↑18. 下列关于钠的说法错误的是( )A、金属钠和氧气反应,条件不同,产物不同 B、钠长期置于空气中,表面不能形成致密氧化膜 C、钠与水反应时,钠熔化成小球在水面上四处游动 D、由于钠比较活泼,所以它能从盐溶液中置换出金属活动性顺序表中钠后面的金属19. 下列钠及其化合物的叙述中正确的是( )A、Na2O与Na2O2都能和水反应生成碱,他们都是化合反应 B、Na2CO3和NaHCO3都不稳定,受热容易分解 C、Na2O2可以作为呼吸面具或潜水艇里的氧气来源 D、将Na2O加到酚酞溶液中,溶液先变色后褪色20. 根据下列反应进行判断,下列各微粒氧化能力由强到弱的顺序正确的是( )
11. 下列电离方程式书写正确的是( )A、NaOH=Na++O2-+H+ B、FeCl3=Fe+3+3Cl- C、Mg(NO3)2=Mg2++ D、H2SO4=2H++12. 下列叙述中,正确的是( )A、氧化还原反应的本质是元素化合价发生了变化 B、含化合价升高元素的反应物被氧化 C、得到电子的物质被氧化 D、氧化还原反应中,氧化剂和还原剂一定是两种物质13. 下列变化过程一定需要加入还原剂的是( )A、KClO3→KCl B、KCl→AgCl C、H+→H2 D、C→CO214. 下列各组离子在溶液中能大量共存的是( )A、H+、Fe2+、Cl-、 B、Mg2+、K+、OH-、Cl- C、 、Ca2+、 、 D、K+、H+、Cl-、15. 能正确表示下列化学反应的离子方程式是( )A、氢氧化钡溶液与硝酸的反应OH-+H+=H2O B、澄清的石灰水与稀盐酸反应Ca(OH)2+2H+= Ca2++2H2O C、铜片插入硝酸银溶液中Cu+Ag+= Cu2++Ag D、碳酸钡溶于稀盐酸中CO32-+2H+= H2O+CO2↑16. 下列氧化还原反应中,水作为还原剂的是( )A、3Fe+4H2O Fe3O4+4H2 B、3NO2+H2O = 2HNO3 + NO C、2Na2O2+2H2O = 4NaOH+O2↑ D、2F2+2H2O = 4HF+O217. 下列各反应中,氧化反应与还原反应在同种元素中进行的是( )A、Cl2+2NaOH=NaCl+NaClO+H2O B、2KClO3 2KCl+3O2↑ C、2KMnO4 K2MnO4+MnO2+O2↑ D、2H2O 2H2↑+O2↑18. 下列关于钠的说法错误的是( )A、金属钠和氧气反应,条件不同,产物不同 B、钠长期置于空气中,表面不能形成致密氧化膜 C、钠与水反应时,钠熔化成小球在水面上四处游动 D、由于钠比较活泼,所以它能从盐溶液中置换出金属活动性顺序表中钠后面的金属19. 下列钠及其化合物的叙述中正确的是( )A、Na2O与Na2O2都能和水反应生成碱,他们都是化合反应 B、Na2CO3和NaHCO3都不稳定,受热容易分解 C、Na2O2可以作为呼吸面具或潜水艇里的氧气来源 D、将Na2O加到酚酞溶液中,溶液先变色后褪色20. 根据下列反应进行判断,下列各微粒氧化能力由强到弱的顺序正确的是( )①ClO3-+5Cl-+6H+=3Cl2+3H2O ②2FeCl3+2KI=2FeCl2+2KCl+I2 ③2FeCl2+Cl2=2FeCl3
A、ClO3- >Cl2 >I2 >Fe3+ B、Cl2> ClO3- >I2 >Fe3+ C、ClO3- >Cl2 >Fe3+ >I2 D、ClO3- >Fe3+ >Cl2 >I2二、填空题
-
21. 填空。(1)、下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、Na2O、CO2、CuO
②HCl、H2O、H2SO4、HNO3
③NaOH、Na2CO3、KOH、Cu(OH)2
i.三种物质依次是(填化学式):①;②;③。
ii.“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是。
A.所得液体能全部透过半透膜 B.能全部透过滤纸
C.有丁达尔效应 D.所得物质一定是悬浊液
(2)、把淀粉溶液溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是。(3)、把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体,制备氢氧化铁胶体的化学方程式为 , 向氢氧化铁胶体中滴入稀硫酸至稀硫酸过量可观察到的现象是 , 写出上述反应的化学方程式。22. 按要求完成下列问题。(1)、在下列反应中,HCl作还原剂的是 , HCl作氧化剂的是 , HCl为还原产物的是。①KOH+HCl=KCl+H2O
②K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
③Cl2+H2O=HCl+HClO
④2NaCl+H2SO4(浓) Na2SO4+2HCl↑
⑤Fe+2HCl=FeCl2+H2↑
(2)、用双线桥法表明反应②中电子转移的方向和数目(3)、用单线桥法表明反应⑤中电子转移的方向和数目(4)、书写下列反应的离子方程式①NaOH溶液和H2SO4溶液:;
②Fe与CuSO4溶液反应:;
③Na2CO3溶液与Ca(OH)2溶液反应:。
23. 国际化学年的中国宣传口号是“化学……我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空:(1)、若金属钠等活泼金属着火时,应该用来灭火。金属钠应保存在中。(2)、金属钠在空气中燃烧生成色的固体,其生成物与水反应的化学方程式:。(3)、NaHCO3固体中混有少量Na2CO3固体,除杂方法是 , 化学方程式是。三、综合题
-
24. 下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色试验均为黄色。
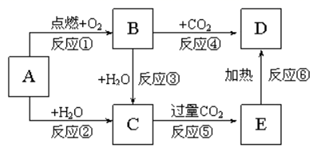
请填写下列空白:
(1)、写出下列物质的化学式:A;B;D。
(2)、以上反应中,属于氧化还原反应的有(填序号)。(3)、写出A→C反应的离子方程式: , E→D反应的化学方程式:。