河北省秦皇岛市抚宁区2020-2021学年九年级上学期期末化学试题
试卷更新日期:2021-11-10 类型:期末考试
一、单选题
-
1. 下列变化属于化学变化的是( )A、粮食酿酒 B、石蜡熔化 C、酒精挥发 D、湿衣晾干2. 下列实验操作中,错误的是( )A、连接仪器
 B、铁丝燃烧
B、铁丝燃烧 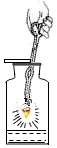 C、液体加热
C、液体加热 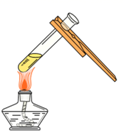 D、点燃酒精灯
D、点燃酒精灯 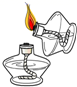 3. 有一位同学暑假去西藏发生了严重的高原反应,医生让他吸氧后症状缓解。吸氧可以帮助人缓解高原反应的原因是( )A、氧气是无色无味的气体 B、氧气可以支持燃烧 C、吸氧为人体呼吸提供了适量的氧气 D、氧气可以燃烧4. 下列说法正确的是( )A、木炭燃烧后生成黑色固体 B、铁丝伸入盛有氧气的集气瓶中剧烈燃烧 C、红磷不能在空气中燃烧 D、硫燃烧后生成有刺激性气味的气体5. 公园里能闻到花香,合理的解释是( )A、分子体积变大 B、分子在不断运动 C、分子数目变多 D、分子发生了分解6. 如图表示两种气体发生的化学反应,其中相同的球代表同种原子,下列说法正确的是( )
3. 有一位同学暑假去西藏发生了严重的高原反应,医生让他吸氧后症状缓解。吸氧可以帮助人缓解高原反应的原因是( )A、氧气是无色无味的气体 B、氧气可以支持燃烧 C、吸氧为人体呼吸提供了适量的氧气 D、氧气可以燃烧4. 下列说法正确的是( )A、木炭燃烧后生成黑色固体 B、铁丝伸入盛有氧气的集气瓶中剧烈燃烧 C、红磷不能在空气中燃烧 D、硫燃烧后生成有刺激性气味的气体5. 公园里能闻到花香,合理的解释是( )A、分子体积变大 B、分子在不断运动 C、分子数目变多 D、分子发生了分解6. 如图表示两种气体发生的化学反应,其中相同的球代表同种原子,下列说法正确的是( )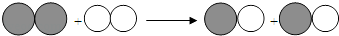 A、生成物一定是混合物 B、分子在化学变化中不可分 C、化学反应前后原子的种类不变 D、该反应既不是化合反应也不是分解反应7. 2020年6月23日,我国北斗三号全球卫星导航系统星座部署完美收官。该导航系统应用了星载氢原子钟和铷原子钟。下列有关铷的说法错误的是( )
A、生成物一定是混合物 B、分子在化学变化中不可分 C、化学反应前后原子的种类不变 D、该反应既不是化合反应也不是分解反应7. 2020年6月23日,我国北斗三号全球卫星导航系统星座部署完美收官。该导航系统应用了星载氢原子钟和铷原子钟。下列有关铷的说法错误的是( ) A、元素符号是Rb B、相对原子质量为85.47 C、铷的原子序数为37 D、属于非金属元素8. 新冠肺炎期间,为了做好自我防护,可用酒精进行消毒。下列有关酒精(C2H6O)的说法错误的是( )A、75%的酒精溶液是常见的医用消毒剂 B、实验室不慎打翻燃着的酒精灯,可用湿抹布扑灭 C、1个酒精分子是由2个碳原子、6个氢原子、1个氧原子构成 D、酒精中C、H、O元素的质量比为2:6:19. 一种作为绿色能源的物质X,其燃烧的化学反应方程式:2X+3O2 2CO2+4H2O,根据质量守恒定律判断X的化学式为( )A、CH3OH B、CH4 C、C2H5OH D、H210. 在反应A+3B=2C+3D中,已知A和B的相对分子质量之比为7:8,当2.8gA与一定量B恰好完全反应后,生成3.6gD,则C的质量为( )A、6.8g B、9.6g C、8.8g D、4.4g11. 物质是由微观粒子构成的,下列物质由原子直接构成的是( )A、汞 B、水蒸气 C、氯化钠 D、碳酸钠12. 关于燃烧和灭火,下列说法正确的是( )A、可燃性气体达到爆炸极限时就会发生爆炸 B、炒菜时油锅起火,向锅中放入较多菜叶灭火,是降低了油的着火点 C、木柴架空有利于燃烧,是因为增大了可燃物与氧气的接触面积 D、干粉灭火器可以用来扑灭图书、档案、贵重设备、精密仪器等物的失火13. 鉴别H2、CO、CH4最常用的方法是( )A、根据燃烧产物 B、根据气体的颜色 C、根据燃烧时火焰颜色 D、根据能否爆炸14. 造成酸雨的主要物质是( )A、甲烷和一氧化碳 B、二氧化硫和一氧化碳 C、一氧化碳和二氧化碳 D、二氧化硫和二氧化氮15. 2020年11月24日,我国嫦娥五号用长征五号运载火箭成功发射。火箭的芯一级和芯二级采用液氧液氢发动机。下列叙述错误的是( )A、液氢和液氧反应属于化合反应 B、燃料加注时需严禁烟火 C、液氢和液氧用作发动机的燃料 D、燃烧产物对环境无污染16. 如图是探究铁和铜金属活动性实验,关于此实验说法错误的是( )
A、元素符号是Rb B、相对原子质量为85.47 C、铷的原子序数为37 D、属于非金属元素8. 新冠肺炎期间,为了做好自我防护,可用酒精进行消毒。下列有关酒精(C2H6O)的说法错误的是( )A、75%的酒精溶液是常见的医用消毒剂 B、实验室不慎打翻燃着的酒精灯,可用湿抹布扑灭 C、1个酒精分子是由2个碳原子、6个氢原子、1个氧原子构成 D、酒精中C、H、O元素的质量比为2:6:19. 一种作为绿色能源的物质X,其燃烧的化学反应方程式:2X+3O2 2CO2+4H2O,根据质量守恒定律判断X的化学式为( )A、CH3OH B、CH4 C、C2H5OH D、H210. 在反应A+3B=2C+3D中,已知A和B的相对分子质量之比为7:8,当2.8gA与一定量B恰好完全反应后,生成3.6gD,则C的质量为( )A、6.8g B、9.6g C、8.8g D、4.4g11. 物质是由微观粒子构成的,下列物质由原子直接构成的是( )A、汞 B、水蒸气 C、氯化钠 D、碳酸钠12. 关于燃烧和灭火,下列说法正确的是( )A、可燃性气体达到爆炸极限时就会发生爆炸 B、炒菜时油锅起火,向锅中放入较多菜叶灭火,是降低了油的着火点 C、木柴架空有利于燃烧,是因为增大了可燃物与氧气的接触面积 D、干粉灭火器可以用来扑灭图书、档案、贵重设备、精密仪器等物的失火13. 鉴别H2、CO、CH4最常用的方法是( )A、根据燃烧产物 B、根据气体的颜色 C、根据燃烧时火焰颜色 D、根据能否爆炸14. 造成酸雨的主要物质是( )A、甲烷和一氧化碳 B、二氧化硫和一氧化碳 C、一氧化碳和二氧化碳 D、二氧化硫和二氧化氮15. 2020年11月24日,我国嫦娥五号用长征五号运载火箭成功发射。火箭的芯一级和芯二级采用液氧液氢发动机。下列叙述错误的是( )A、液氢和液氧反应属于化合反应 B、燃料加注时需严禁烟火 C、液氢和液氧用作发动机的燃料 D、燃烧产物对环境无污染16. 如图是探究铁和铜金属活动性实验,关于此实验说法错误的是( ) A、铁丝需要砂纸打磨 B、溶液由蓝色变为无色 C、金属活动性强弱:Fe>Cu D、化学反应方程式为:Fe+CuSO4=Cu+FeSO417. 港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施错误的是( )A、在金属制品表面镀保护层 B、改变金属结构制成合金使用 C、在金属制品表面涂油漆 D、用稀盐酸定期清洗金属制品18. 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化。根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为()A、Z、Y、X B、X、Y、Z C、Y、X、Z D、X、Z、Y19. 将一定量的铁粉加入到含有Cu(NO3)2和AgNO3的废液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。下列判断正确的是()A、滤渣中一定含有Ag和Cu,滤液中一定含有Fe(NO3)2 B、滤渣中一定不含Fe,滤液中一定含有Fe(NO3)2和Cu(NO3)2 C、滤渣中一定含有Ag,滤液中可能含有Cu(NO3)2和AgNO3 D、滤渣中一定含有Ag和Cu,滤液中可能含有Cu(NO3)2和AgNO320. 下列说法中正确的是( )A、凡是均一的、稳定的液体一定是溶液 B、溶液是均一的、稳定的混合物 C、长期放置后不会分层的液体一定是溶液 D、溶液一定是无色,且溶剂一定是水21. 如图为教材中实验室模拟炼铁的实验装置。下列说法错误的是( )
A、铁丝需要砂纸打磨 B、溶液由蓝色变为无色 C、金属活动性强弱:Fe>Cu D、化学反应方程式为:Fe+CuSO4=Cu+FeSO417. 港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施错误的是( )A、在金属制品表面镀保护层 B、改变金属结构制成合金使用 C、在金属制品表面涂油漆 D、用稀盐酸定期清洗金属制品18. 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化。根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为()A、Z、Y、X B、X、Y、Z C、Y、X、Z D、X、Z、Y19. 将一定量的铁粉加入到含有Cu(NO3)2和AgNO3的废液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。下列判断正确的是()A、滤渣中一定含有Ag和Cu,滤液中一定含有Fe(NO3)2 B、滤渣中一定不含Fe,滤液中一定含有Fe(NO3)2和Cu(NO3)2 C、滤渣中一定含有Ag,滤液中可能含有Cu(NO3)2和AgNO3 D、滤渣中一定含有Ag和Cu,滤液中可能含有Cu(NO3)2和AgNO320. 下列说法中正确的是( )A、凡是均一的、稳定的液体一定是溶液 B、溶液是均一的、稳定的混合物 C、长期放置后不会分层的液体一定是溶液 D、溶液一定是无色,且溶剂一定是水21. 如图为教材中实验室模拟炼铁的实验装置。下列说法错误的是( ) A、该实验能观察到红色粉末变黑,澄清的石灰水变浑浊 B、一氧化碳还原氧化铁的反应不属于置换反应 C、该实验的三个反应中,碳元素的化合价都发生了改变 D、导管末端的酒精灯是进行尾气处理,防止污染空气22. 某不纯的铁5.6克与足量的稀硫酸反应生成0.23克氢气,则铁中混有的物质可能是( )A、锌 B、碳 C、铝 D、银23. 一定条件下,密闭容器内发生的某化学反应,测得t1和t2时各物质的质量见表,下列说法正确的是( )
A、该实验能观察到红色粉末变黑,澄清的石灰水变浑浊 B、一氧化碳还原氧化铁的反应不属于置换反应 C、该实验的三个反应中,碳元素的化合价都发生了改变 D、导管末端的酒精灯是进行尾气处理,防止污染空气22. 某不纯的铁5.6克与足量的稀硫酸反应生成0.23克氢气,则铁中混有的物质可能是( )A、锌 B、碳 C、铝 D、银23. 一定条件下,密闭容器内发生的某化学反应,测得t1和t2时各物质的质量见表,下列说法正确的是( )物质
M
N
P
Q
t1时的质量/g
16
50
8
0
t2时的质量/g
4
18
x
44
A、x的值小于8 B、Q可能是单质 C、该反应一定是分解反应 D、M与N的质量变化比为3:824. 关于如图所示实验的相关判断错误的是( )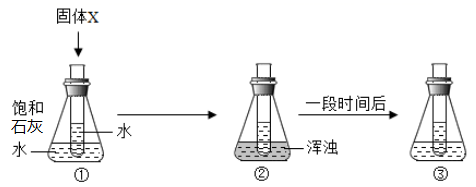 A、固体X可能是NaOH B、固体X可能是NH4NO3 C、Ca(OH)2溶解度:①>② D、Ca(OH)2质量分数:①=③25. t℃时,将一定质量的甲、乙两种溶液进行恒温蒸发,蒸发溶剂的质量与析出晶体的质量之间的关系如图所示。下列说法正确的是( )
A、固体X可能是NaOH B、固体X可能是NH4NO3 C、Ca(OH)2溶解度:①>② D、Ca(OH)2质量分数:①=③25. t℃时,将一定质量的甲、乙两种溶液进行恒温蒸发,蒸发溶剂的质量与析出晶体的质量之间的关系如图所示。下列说法正确的是( ) A、蒸发溶剂前,乙是饱和溶液 B、b点对应的乙溶液是不饱和溶液 C、t℃时,甲的溶解度更大 D、甲的饱和溶液的溶质质量分数是:
A、蒸发溶剂前,乙是饱和溶液 B、b点对应的乙溶液是不饱和溶液 C、t℃时,甲的溶解度更大 D、甲的饱和溶液的溶质质量分数是:二、填空题
-
26. 请在A—F六种物质中,选择正确的物质,用字母填空。
A.石墨 B.一氧化碳 C.干冰 D.甲烷 E.氮气 F.金刚石
(1)、天然气的主要成分是;(2)、造成煤气中毒的物质是;(3)、具有优良导电性能的单质是;(4)、可用于人工降雨的是;(5)、焊接时常用作保护气的是;(6)、可用来切割玻璃的是。27. 化学与生活、生产密切相关。请回答下列问题:(1)、生活用水在净化过程中常用吸附色素和异味;生活中可用检验水的硬度,一般可以通过的方法降低水的硬度。(2)、用洗洁精清洗油污,是利用了洗洁精的作用。(3)、合金具有良好的物理、化学性能,下列物质不属于合金的是(选填序号)。a、黄铜 b、不锈钢 c、铁矿石
28. 近年来,我国高铁飞速发展,已成为世界上唯一高铁成网运行的国家。请回答下列问题。(1)、高铁电路多用铜质导线,这是利用了铜的延展性和性。(2)、高铁刹车片由合金锻钢制作,时速300公里以上的列车紧急制动时,轮毂盘面和刹车片的温度瞬间达到700℃以上,合金锻钢应该具备耐磨和等特性。(3)、建造高铁需要消耗大量的铝、铁等金属。工业炼铁的原理是氧化铁(Fe2O3)和一氧化碳在高温条件下反应,其化学方程式为(4)、目前世界上已有50%以上的铁得到了回收利用。回收利用废旧金属的社会意义是29. 图中是a、b、c三种物质的溶解度曲线,回答下列问题。 (1)、P点的含义:。(2)、在t3℃时,将120g a物质加入到200g水中,充分溶解后所得到的溶液质量为g。(3)、b中混有少量a,提纯b的方法是(选填“蒸发结晶"或“降温结晶”)。(4)、分别将t3℃时a、b的饱和溶液降温到t2℃析出晶体的质量大小关系为(选填一个序号)。
(1)、P点的含义:。(2)、在t3℃时,将120g a物质加入到200g水中,充分溶解后所得到的溶液质量为g。(3)、b中混有少量a,提纯b的方法是(选填“蒸发结晶"或“降温结晶”)。(4)、分别将t3℃时a、b的饱和溶液降温到t2℃析出晶体的质量大小关系为(选填一个序号)。①a>b ②a<b ③a=b ④均有可能
30. 小亮同学用如图所示装置探究可燃物燃烧的条件。
(已知:白磷着火点为40℃,红磷着火点为240℃)
(1)、铜片上白磷燃烧,反应的化学方程式为(2)、铜片上的白磷燃烧,红磷不燃烧,据此可得出的结论是(3)、使水中白磷燃烧,可进行的操作是三、综合题
-
31. 图是初中化学中常见物质间的转化关系,其中甲、乙、丙、丁为单质,A、B、C、D为氧化物,D是使地球产生温室效应的一种气体,丁是一种紫红色金属(图中表示转化关系,部分反应条件已略去)。回答下列问题:
 (1)、A的化学式是。(2)、反应③的基本化学反应类型为反应。(3)、反应④和反应⑤中,化合价降低的元素是(填元素符号)。(4)、反应②的化学方程式为32. 实验室里现有氯酸钾、二氧化锰、稀硫酸、石灰石和稀盐酸以及下列仪器(如图):
(1)、A的化学式是。(2)、反应③的基本化学反应类型为反应。(3)、反应④和反应⑤中,化合价降低的元素是(填元素符号)。(4)、反应②的化学方程式为32. 实验室里现有氯酸钾、二氧化锰、稀硫酸、石灰石和稀盐酸以及下列仪器(如图):
 (1)、利用上述仪器和药品可以制取二氧化碳,你选择的仪器是(填序号),药品是 , 反应的化学方程式为 , 证明二氧化碳已集满的实验操作和现象是。(2)、若补充一种仪器(填仪器名称),再利用上述仪器和药品还可以制取氧气,你选择的药品是反应的化学方程式为。33. 小明周末从山里带回一瓶浑浊的山泉水,他在化学实验室模仿自来水厂净化过程,最终制成蒸馏水,流程如图所示:
(1)、利用上述仪器和药品可以制取二氧化碳,你选择的仪器是(填序号),药品是 , 反应的化学方程式为 , 证明二氧化碳已集满的实验操作和现象是。(2)、若补充一种仪器(填仪器名称),再利用上述仪器和药品还可以制取氧气,你选择的药品是反应的化学方程式为。33. 小明周末从山里带回一瓶浑浊的山泉水,他在化学实验室模仿自来水厂净化过程,最终制成蒸馏水,流程如图所示: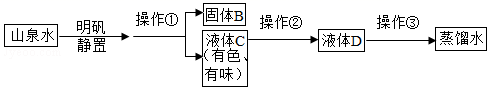 (1)、操作①的名称是 , 若经过操作后,所得液体仍然浑浊,其原因可能是(填序号)。
(1)、操作①的名称是 , 若经过操作后,所得液体仍然浑浊,其原因可能是(填序号)。A.漏斗内的滤纸有破损
B.漏斗下端未紧靠烧杯内壁
C.漏斗内液面高于滤纸的边缘
D.滤纸没有紧贴漏斗内壁
(2)、小明用得到的蒸馏水配制50g质量分数6%的氯化钠溶液,如图是配制该氯化钠溶液的实验操作示意图:
①计算:需要氯化钠固体的质量和水的体积。
②称量:用托盘天平称取所需氯化钠固体,放入烧杯中。
③量取:用规格为mL(填“10”、“50”或“100”)的量筒量取所需要的水mL(水的密度为1.0g/cm3),倒入盛有氯化钠的烧杯中;
④溶解:用玻璃棒搅拌,目的是。
经检测,小明同学配制的溶液溶质质量分数偏小,可能的原因是(填序号)。
A.氯化钠固体不纯
B.用生锈砝码称量
C.装瓶时有少量溶液洒出
D.溶解时烧杯内壁有水珠
(3)、小明用6%的氯化钠溶液(密度约为1.04g/cm3),配制50g质量分数为3%的氯化钠溶液,需要6%氯化钠溶液的体积mL;水的质量是g。34. 小明同学为了研究影响铁生锈的因素,进行了如下实验:在A、B、C、D四只烧瓶中分别放入干燥的细铁丝,浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝(使细铁丝完全浸没在食盐水中)(四只烧瓶中细铁丝的质量均相同),然后装配成如图所示的四套装置,每隔0.5小时测量导管中水面上升的高度,结果如表所示:请回答: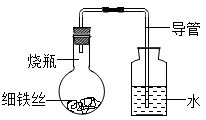
烧瓶
时间(h)
0
0.5
1.0
1.5
2.0
2.5
3.0
A
干燥的细铁丝
0
0
0
0
0
0
0
B
浸过食盐水的细铁丝
0
0.4
1.2
3.4
5.6
7.6
9.8
C
浸过清水的细铁丝
0
0
0
0.3
0.8
2.0
3.5
D
完全浸没在食盐水中的细铁丝
0
0
0
0
0
0
0
(1)、以上实验中,铁生锈速率最大的是瓶(填烧瓶号,下同)(2)、证明铁生锈需要水参与,应选择的烧瓶是。(3)、证明食盐能促进铁生锈,应选择的烧瓶是。(4)、为了防止钢铁生锈,人们常采用表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法,这些方法的共同原理是。四、计算题
-
35. 化学兴趣小组用锌和稀硫酸反应制取氢气,生成氢气质量与加入稀硫酸的质量关系如图所示。请计算:(1)、完全反应后生成氢气的质量为g。(2)、计算这种稀硫酸中溶质的质量分数。
