河北省邯郸市大名县2020-2021学年九年级上学期期末化学试题
试卷更新日期:2021-11-10 类型:期末考试
一、单选题
-
1. 以下事件中奠定近代化学基础的是( )A、火的发现与利用 B、原子论和分子学说的创立 C、元素周期表的编制 D、拉瓦锡测定出空气的组成2. 近期某地市场上发现“脚臭盐”,因其中溶有硫化氢所致。下列属于硫化氢化学性质的是( )A、无色、有臭鸡蛋气味 B、密度比空气大 C、能溶于水 D、有还原性3. 下列所示的实验操作错误的是( )A、检查气密性
 B、加入固体粉末
B、加入固体粉末  C、滴加液体
C、滴加液体  D、过滤粗盐水
D、过滤粗盐水  4. 生活中用到的下列物质,属于纯净物的是( )A、调味用的食醋 B、取暖用的木炭 C、温度计里的水银 D、炒菜用的铁锅5. 下列化学用语与含义相符的是( )A、2H表示:2个氢元素 B、2N2:表示2个氮分子 C、O3表示:3个氧原子 D、2SO4-2表示2个硫酸根离子6. 地球上有丰富的水资源,科学家一直在研究成本低、效率高的催化剂,使水发生反应获得氢能。下面说法错误的是( )A、保持水化学性质的最小微粒是水分子 B、自然界澄清透明的水都是纯净物 C、氢能是一种清洁能源 D、催化剂在化学反应前后,化学性质和质量都不改变7. 对公共场所用过氧乙酸溶液进行消毒是预防“新冠肺炎”的措施之一。已知过氧乙酸有较强的腐蚀性,并容易分解: ,则X为( )A、 B、 C、 D、8. 镁带在耐高温的容器中密封(含空气)加热,能表示容器里所盛的物质总质量变化的是( )A、
4. 生活中用到的下列物质,属于纯净物的是( )A、调味用的食醋 B、取暖用的木炭 C、温度计里的水银 D、炒菜用的铁锅5. 下列化学用语与含义相符的是( )A、2H表示:2个氢元素 B、2N2:表示2个氮分子 C、O3表示:3个氧原子 D、2SO4-2表示2个硫酸根离子6. 地球上有丰富的水资源,科学家一直在研究成本低、效率高的催化剂,使水发生反应获得氢能。下面说法错误的是( )A、保持水化学性质的最小微粒是水分子 B、自然界澄清透明的水都是纯净物 C、氢能是一种清洁能源 D、催化剂在化学反应前后,化学性质和质量都不改变7. 对公共场所用过氧乙酸溶液进行消毒是预防“新冠肺炎”的措施之一。已知过氧乙酸有较强的腐蚀性,并容易分解: ,则X为( )A、 B、 C、 D、8. 镁带在耐高温的容器中密封(含空气)加热,能表示容器里所盛的物质总质量变化的是( )A、 B、
B、 C、
C、 D、
D、 9. 金属材料被广泛应用于生产生活中。下列说法中正确的是( )A、可以用铁丝代替被熔断的保险丝 B、真金不怕火炼,是因为金的熔点高 C、铝比铁耐腐蚀,是因为铝在空气中形成致密的氧化膜 D、白炽灯的灯丝用金属钨制成,是因为金属钨的密度大10. 对图所示溶液的认识中,错误的是( )
9. 金属材料被广泛应用于生产生活中。下列说法中正确的是( )A、可以用铁丝代替被熔断的保险丝 B、真金不怕火炼,是因为金的熔点高 C、铝比铁耐腐蚀,是因为铝在空气中形成致密的氧化膜 D、白炽灯的灯丝用金属钨制成,是因为金属钨的密度大10. 对图所示溶液的认识中,错误的是( ) A、是稳定均一的混合物 B、溶质为NaCl C、溶质和溶剂的质量比为1:10 D、溶质质量分数为10%11. 下图所示是某化学反应的微观示意图,下列说法正确的是( )
A、是稳定均一的混合物 B、溶质为NaCl C、溶质和溶剂的质量比为1:10 D、溶质质量分数为10%11. 下图所示是某化学反应的微观示意图,下列说法正确的是( ) A、该反应属于置换反应 B、生成物丙由2个氢原子和1个氧原子构成 C、生成物丁中碳和氧元素的质量比为1:2 D、参加反应的甲和乙的分子个数比为2:712. 下列事实不能作为相应观点的证据的是( )A、尘土飞扬,说明分子是运动的 B、电解水得到氢气和氧气,说明分子是可分的 C、气体被压缩后体积发生了较大变化,说明气体分子间距较大 D、将两个干净平整的铅柱紧压在一起会结合起来,说明分子间存在引力13. 下列实验能够直接用于验证质量守恒定律的是( )A、
A、该反应属于置换反应 B、生成物丙由2个氢原子和1个氧原子构成 C、生成物丁中碳和氧元素的质量比为1:2 D、参加反应的甲和乙的分子个数比为2:712. 下列事实不能作为相应观点的证据的是( )A、尘土飞扬,说明分子是运动的 B、电解水得到氢气和氧气,说明分子是可分的 C、气体被压缩后体积发生了较大变化,说明气体分子间距较大 D、将两个干净平整的铅柱紧压在一起会结合起来,说明分子间存在引力13. 下列实验能够直接用于验证质量守恒定律的是( )A、 B、
B、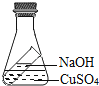 C、
C、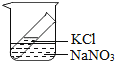 D、
D、 14. 下列所示不是体现化学造福人类的是( )A、新型农药的研制 B、单晶硅的使用 C、隔水透气材料的发明 D、杂交水稻的成功研发和推广
14. 下列所示不是体现化学造福人类的是( )A、新型农药的研制 B、单晶硅的使用 C、隔水透气材料的发明 D、杂交水稻的成功研发和推广二、综合题
-
15. 如图是二氧化碳的制取和性质实验的微型一体化装置图,该装置的气密性良好。请完成下面小题。
 (1)、挤压胶头,滴入稀盐酸,过一会儿,用燃着的木条放在微型集气瓶口,如果 , 则说明二氧化碳已收集满。(2)、装置内1、2处的溶液反应,1处的反应现象是 , 2处生成了。(3)、用橡胶塞塞紧微型集气瓶口,反复挤压几次胶头,一段时间,氢氧化钠溶液被吸进微型气体实验器和微型集气瓶中。这是由于(用化学方程式表示)。16. 空气、水是我们赖以生存的重要资源。(1)、Cu能和空气中的H2O、O2和反应生成“铜锈”(主要成分是Cu2(OH)2CO3)。(2)、生活中常用的方法降低水的硬度。(3)、电解水可制氢气。通电一段时间后,如图所示,电源X为电源的极。氢气作为新能源,其主要的优点是。
(1)、挤压胶头,滴入稀盐酸,过一会儿,用燃着的木条放在微型集气瓶口,如果 , 则说明二氧化碳已收集满。(2)、装置内1、2处的溶液反应,1处的反应现象是 , 2处生成了。(3)、用橡胶塞塞紧微型集气瓶口,反复挤压几次胶头,一段时间,氢氧化钠溶液被吸进微型气体实验器和微型集气瓶中。这是由于(用化学方程式表示)。16. 空气、水是我们赖以生存的重要资源。(1)、Cu能和空气中的H2O、O2和反应生成“铜锈”(主要成分是Cu2(OH)2CO3)。(2)、生活中常用的方法降低水的硬度。(3)、电解水可制氢气。通电一段时间后,如图所示,电源X为电源的极。氢气作为新能源,其主要的优点是。 (4)、如果打开门窗,火会烧得更旺的原因。17. 1911年若名物理学家卢瑟福等人为探索原子的内部结构进行实验:用一束质量远大于电子的高速运动的a粒子轰击金箔,发现“大多数a粒子能穿过金箔,一小部分发生偏转,极少数被反弹回来。”回答下列问题:
(4)、如果打开门窗,火会烧得更旺的原因。17. 1911年若名物理学家卢瑟福等人为探索原子的内部结构进行实验:用一束质量远大于电子的高速运动的a粒子轰击金箔,发现“大多数a粒子能穿过金箔,一小部分发生偏转,极少数被反弹回来。”回答下列问题: (1)、1个a粒子由2个中子和2个质子构成,则a粒子带(选填“正”或“负”)电。(2)、甲图为金的原子结构示意图,乙图摘自元素周期表,据此回答下列问题:
(1)、1个a粒子由2个中子和2个质子构成,则a粒子带(选填“正”或“负”)电。(2)、甲图为金的原子结构示意图,乙图摘自元素周期表,据此回答下列问题:①X= , b=。
②金原子的相对原子质量为。
18. 如图A、B、C、D是初中化学中常见的四种物质,其中A为黑色单质,D为红色单质,B、C是组成元素相同的两种气态化合物。“→”表示物质间的转化关系(部分反应物、生成物及反应条件已省略)。请回答: (1)、C的化学式是 , D的化学式是。(2)、B的一种用途。(3)、C→B反应的化学方程式是。19. 某化学兴趣小组为探究金属铝和铜的活动性强弱,开展了以下活动。(1)、(查阅资料)
(1)、C的化学式是 , D的化学式是。(2)、B的一种用途。(3)、C→B反应的化学方程式是。19. 某化学兴趣小组为探究金属铝和铜的活动性强弱,开展了以下活动。(1)、(查阅资料)经查阅,金属铝在常温下能与空气中的氧气反应生成致密的氧化铝薄膜。该反应的化学方程式为 。
(2)、(对比实验)编号
操作
现象
甲
将表面未打磨的铝丝浸入CuSO4溶液中
无明显现象
乙
将表面打磨后的铝丝浸入CuSO4溶液中
铝丝表面析出红色固体
丙
将表面未打磨的铝丝浸入CuCl2溶液中
铝丝表面析出红色固体
比较实验乙和实验 (填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。
(3)、实验乙中反应的化学方程式为 ,据此可知金属活动性Al比Cu (填“强”或“弱”)。(4)、小明同学对实验丙的现象进行分析,认为H2O对氧化铝薄膜有破坏作用。但此观点马上被其他同学否定,否定的依据是 。(5)、(猜测与探究)小组同学针对实验丙的现象,经讨论后猜测:Cl-破坏了氧化铝薄膜。
为检验此猜测是否正确,他们首先向两支试管中加入相同的CuSO4溶液,并均浸入表面未打磨的铝丝,然后进行了新的探究:
操作
现象
结论
推论
(1)向一支试管中再加入
NaCl固体
铝丝表面析
出红色固体
氧化铝薄膜
被破坏
Na+或① 能
破坏氧化铝薄膜
(2)向另一支试管中再加入
Na2SO4固体
②
氧化铝薄膜
未被破坏
Na+和SO42—都不能
破坏氧化铝薄膜
(6)、(结论与反思)得出结论:前述猜测 (填“正确”或“不正确”)。总结反思:本次探究充分运用了比较法和控制变量法。
三、计算题
-
20. 已知氯化钠溶液和硝酸银溶液反应生成氯化银(AgCl)沉淀和硝酸钠,为测定某生理盐水的溶质质量分数,将生理盐水样品与足量的硝酸银溶液混合,有关实验数据如下表:
反应前
反应后
实验数据
生理盐水样品的质量
加入硝酸银溶液的质量
过滤后剩余溶液的质量
130g
40g
167.13g
(提示: )
求:
(1)、反应后生成氯化银的质量为g。(2)、计算该生理盐水的溶质质量分数。