人教版九年级化学上册期末考试模拟试卷
试卷更新日期:2021-10-30 类型:期末考试
一、单选题
-
1. 下列过程发生了化学变化的是( )A、干冰降雨 B、海水晒盐 C、烧制陶瓷 D、活性炭净水2. 今年5月4日,习总书记在推进南水北调后续工程高质量发展座谈会上强调:“水是生存之本,文明之源,要坚持节水优先,抓好水污染的防治工作”。下列做法不合理的是( )A、实验室废水和废液直接排入下水道 B、用洗菜、淘米水浇花,用洗衣水冲厕所 C、生活污水、工业废水等经处理达标后排放 D、农业和园林浇灌改大水漫灌为喷灌和滴灌3. 中学化学实验中常用到试管。下列实验操作正确的是( )A、
 给液体加热
B、
给液体加热
B、 取用液体
C、
取用液体
C、 取用块状固体
D、
取用块状固体
D、 塞橡胶塞
4. 下列物质按照单质、化合物、混合物的顺序排列的是( )A、汞、乙醇、石油 B、干冰、氧化铜、赤铁矿 C、铁、五氧化二磷、冰水混合物 D、C60、天然气、煤5. 氮化硅(Si3N4)是一种高温陶瓷材料,其中氮元素的化合价为-3价,则硅元素的化合价为( )A、+4 B、+3 C、+2 D、+16. 下列事实从微观粒子角度解释错误的是( )A、浓氨水挥发——氨分子不断运动 B、水通电分解——水分子变成其他分子 C、水蒸发为水蒸气,所占体积变大——水分子体积变大 D、金刚石和石墨物理性质存在明显差异——碳原子排列方式不同7. 在火箭的制造中使用了钛合金,钛元素在元素周期表中的相关信息如图所示,从图中获得信息错误的是( )
塞橡胶塞
4. 下列物质按照单质、化合物、混合物的顺序排列的是( )A、汞、乙醇、石油 B、干冰、氧化铜、赤铁矿 C、铁、五氧化二磷、冰水混合物 D、C60、天然气、煤5. 氮化硅(Si3N4)是一种高温陶瓷材料,其中氮元素的化合价为-3价,则硅元素的化合价为( )A、+4 B、+3 C、+2 D、+16. 下列事实从微观粒子角度解释错误的是( )A、浓氨水挥发——氨分子不断运动 B、水通电分解——水分子变成其他分子 C、水蒸发为水蒸气,所占体积变大——水分子体积变大 D、金刚石和石墨物理性质存在明显差异——碳原子排列方式不同7. 在火箭的制造中使用了钛合金,钛元素在元素周期表中的相关信息如图所示,从图中获得信息错误的是( )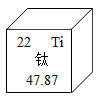 A、钛的原子序数是22 B、钛原子的核电荷数是22 C、钛元素属于金属元素 D、钛元素的相对原子质量是47.87g8. 宏观辨识和微观探析是化学学科核心素养之一。我国科学家利用复合光催化剂人工合成了燃料,反应的微观示意图如下。下列说法错误的是( )
A、钛的原子序数是22 B、钛原子的核电荷数是22 C、钛元素属于金属元素 D、钛元素的相对原子质量是47.87g8. 宏观辨识和微观探析是化学学科核心素养之一。我国科学家利用复合光催化剂人工合成了燃料,反应的微观示意图如下。下列说法错误的是( )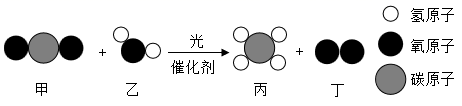 A、丙是较为清洁的燃料 B、反应后氧元素的化合价升高 C、一个乙分子中含有10个电子 D、参加反应的甲和生成丁的质量之比为11:89. 治疗虐疾的特效药一青蒿素的化学式为:C15H22O5.下列关于青蒿素的说法错误的是( )A、青蒿素是由碳、氢、氧三种元素组成的有机化合物 B、青蒿素中含有22个氢原子 C、青蒿素中碳、氢、氧三种元素的质量比为90:11:40 D、每个青蒿素分子由42个原子构成10. 在一密闭容器中放入甲、乙、丙、丁四种物质,一定条件下发生化学反应,一段时间后,测得有关数据如表,下列关于该反应的说法正确的是( )
A、丙是较为清洁的燃料 B、反应后氧元素的化合价升高 C、一个乙分子中含有10个电子 D、参加反应的甲和生成丁的质量之比为11:89. 治疗虐疾的特效药一青蒿素的化学式为:C15H22O5.下列关于青蒿素的说法错误的是( )A、青蒿素是由碳、氢、氧三种元素组成的有机化合物 B、青蒿素中含有22个氢原子 C、青蒿素中碳、氢、氧三种元素的质量比为90:11:40 D、每个青蒿素分子由42个原子构成10. 在一密闭容器中放入甲、乙、丙、丁四种物质,一定条件下发生化学反应,一段时间后,测得有关数据如表,下列关于该反应的说法正确的是( )物质
甲
乙
丙
丁
反应前的质量/g
27
x
10
6
反应后的质量/g
3
5
18
22
A、甲一定是化合物 B、乙一定是该反应的催化剂 C、甲的相对分子质量一定等于丙和丁的相对分子质量之和 D、该反应中丙和丁的质量变化之比为9:1111. 始终把人民生命安全和身体健康放在第一位是中国共产党内在的价值取向。下列说法或做法不利于安全与健康的是( )A、在食品中可适当添加含钙、铁、锌的化合物 B、剧烈运动后,可以大量饮用碳酸饮料 C、遭遇火灾时,可用湿毛巾捂住口鼻,俯下身子沿墙壁或地面跑离火灾区 D、在使用和储存易燃、易爆物时,必须严格遵守有关规定,决不允许违章操作12. 推理是学习化学的一种重要方法,以下推理正确的是( )A、质子数决定元素种类,因此质子数相同的一类原子一定属于同种元素 B、碱中含有氢元素和氧元素,所以含有氢元素和氧元素的物质一定是碱 C、溶液具有均一性和稳定性,则具有均一性和稳定性的液体一定是溶液 D、有机物含有碳元素,因此含有碳元素的化合物一定是有机物13. 下列指定反应的化学方程式正确的是( )A、用铁回收含铜废液(主要为CuSO4溶液)中的铜: B、碳酸氢钙受热分解:Ca(HCO3)2 CaCO3+CO2↑ C、点燃镁条:Mg+O2 MgO D、用熟石灰处理硫酸厂的废水:14. 现有8g某有机物与足量O2在一定条件下充分反应,生成22gCO2和18gH2O。下列说法正确的是( )A、该有机物中一定含有氧元素 B、该有机物中碳、氢元素质量比为1:3 C、参加反应的有机物与O2的质量比为1:3 D、生成的CO2和H2O的分子个数比为1:215. 质量相等的两份氯酸钾固体,在其中一份中加入少量高锰酸钾,然后分别放在酒精灯上均匀受热,放出氧气的质量(m)随反应时间(t)变化的函数图象(如图),正确的是(a为纯净的氯酸钾,b为加入了高锰酸钾的氯酸钾)( )A、 B、
B、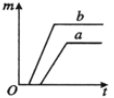 C、
C、 D、
D、
二、填空题
-
16. 请按要求填空:(1)、葡萄糖(C6H12O6)是一种重要的营养物质。其组成中氢元素和氧元素的质量整数比是。其在人体内被完全氧化的产物是(填化学式)。葡萄糖在酒化酶作用下可发生分解反应: ,x为(填数字)。(2)、我国航天领域正在建设中的天宫空间站,使用了大量的合金材料和复合材料。
①天宫空间站使用的铁合金材料的硬度比纯铁的硬度(填“大”或“小”)。
②天宫空间站广泛使用了铝、铁、铜。现利用它们完成如下实验
a.将未打磨的铝片放入FeSO4溶液中,没有明显现象
b.将打磨的铝片放入FeSO4溶液中,铝片表面有明显变化。
c.将打磨的铁片放入CuSO4溶液中,铁片表面有新物质生成。
实验a中无现象的原因是。实验b中的化学方程式为。实验c中铁片足量充分反应后,溶液变为色。
17.(1)、下图是一种处理汽车尾气的反应微观示意图,回答下列问题。①从微观上看,该化学变化中发生改变的粒子是(填“分子”或“原子”),反应前后原子的数目(填“有”或“没有”)增减。
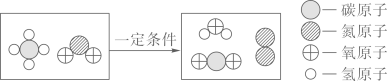
②参加反应的
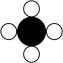 和
和 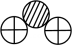 的分子个数比为 , 该反应中涉及到的单质的化学式为。(2)、下图是A、B、C、D四种粒子的结构示意图
的分子个数比为 , 该反应中涉及到的单质的化学式为。(2)、下图是A、B、C、D四种粒子的结构示意图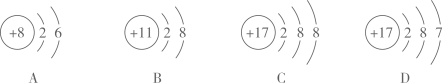
①图中共有种元素。
②C粒子的符号为 , 由B、C两种粒子构成的化合物的化学式为。
18. 金属锌在冶金、化学电源等方面具有重要作用。以闪锌矿(主要含ZnS,还含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如下:
已知:常温下PbSO4难溶于水和稀硫酸。回答下列问题:
(1)、ZnS的名称是。(2)、“焙烧”过程中金属硫化物转化成金属氧化物,焙烧时ZnS发生反应的化学方程式是。焙烧尾气必须进行净化处理的原因是。(3)、“溶浸”产生的滤渣主要成分除了SiO2外还有。(4)、“氧化除杂”的主要反应为 ,则x、y、z依次是。“电解”过程的反应为:2ZnSO4+2H2O 2Zn+O2↑+2H2SO4 , 则电解得到的溶液可返回工序继续使用。(5)、“还原除杂”利用锌粉与CdSO4反应,其化学方程式为;已知Cd放入盐酸中有气体产生,则Cd、Zn、Cu的金属活动性顺序为。三、实验探究题
-
19. 请根据下面常用化学实验装置回答以下问题。
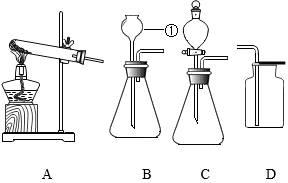
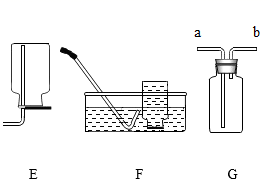 (1)、写出仪器①的名称。(2)、实验室选用B装置制取氧气的化学方程式为。(3)、若用F装置收集氧气,当时开始收集,收集完氧气后用玻璃片(填 “磨砂”或“光滑”)一面盖住集气瓶口,(填“正放”或“倒放”)在桌面上。(4)、若用G装置通过排空气的方法收集氧气,验满的方法是。(5)、实验室制取CO2的化学方程式为。(6)、实验室制取CO2时,为了控制反应速率和节约药品,最好选择(填字母)作为发生装置。检验生成气体是CO2所选用的试剂为。20. 在学习质量守恒定律时我们接触到了以下几个实验,请同学们用所学知识回答下列问题:
(1)、写出仪器①的名称。(2)、实验室选用B装置制取氧气的化学方程式为。(3)、若用F装置收集氧气,当时开始收集,收集完氧气后用玻璃片(填 “磨砂”或“光滑”)一面盖住集气瓶口,(填“正放”或“倒放”)在桌面上。(4)、若用G装置通过排空气的方法收集氧气,验满的方法是。(5)、实验室制取CO2的化学方程式为。(6)、实验室制取CO2时,为了控制反应速率和节约药品,最好选择(填字母)作为发生装置。检验生成气体是CO2所选用的试剂为。20. 在学习质量守恒定律时我们接触到了以下几个实验,请同学们用所学知识回答下列问题: (1)、其中有一个不能达到实验目的是(填序号)。(2)、实验A中观察到现象: , 当实验结束后发现小气球与初始状态相比(填“相同”、“变瘪”或“膨胀”);实验A中的反应的化学方程式:。(3)、实验C中,可观察到银白色铁钉表面析出色固体,溶液由色逐渐变为 , 色,该反应的化学反应方程式:;(4)、实验B的现象是反应后称量所得各物质的质量比反应前各物质的质量和(填“变大”、“变小”或“不变”),(5)、反思:探究或验证反应物与生成物的质量关系时,若要用到有气体参加或有气体生成的反应,反应必须在的容器中进行。
(1)、其中有一个不能达到实验目的是(填序号)。(2)、实验A中观察到现象: , 当实验结束后发现小气球与初始状态相比(填“相同”、“变瘪”或“膨胀”);实验A中的反应的化学方程式:。(3)、实验C中,可观察到银白色铁钉表面析出色固体,溶液由色逐渐变为 , 色,该反应的化学反应方程式:;(4)、实验B的现象是反应后称量所得各物质的质量比反应前各物质的质量和(填“变大”、“变小”或“不变”),(5)、反思:探究或验证反应物与生成物的质量关系时,若要用到有气体参加或有气体生成的反应,反应必须在的容器中进行。四、计算题
-
21. 实验室现有一瓶水垢样品,其成分为氢氧化镁和碳酸钙,已知:氢氧化镁受热易分解,反应的化学方程式为:Mg(OH)2 MgO+H2O;碳酸钙高温下分解。某兴趣小组为测定其中各成分的质量分数,取一定量的水垢样品加热,加热过程中剩余固体的质量随加热时间的变化如图所示。求:
 (1)、反应后剩余固体质量是g;(2)、水垢样品中氢氧化镁质量分数是多少?(写出计算过程,计算结果精确到0.1%)
(1)、反应后剩余固体质量是g;(2)、水垢样品中氢氧化镁质量分数是多少?(写出计算过程,计算结果精确到0.1%)