浙江省嘉兴市2020-2021学年高一上学期化学期末考试试卷
试卷更新日期:2021-10-19 类型:期末考试
一、单选题
-
1. 空气中含量最高的气体的分子式是( )A、H2 B、O2 C、CO2 D、N22. 2020年10月,黑龙江省一家九口在家聚餐时食用了“酸汤子”,不幸全部中毒身亡,据调查中毒原因是该食物变质产生了米酵菌酸(分子式为:C28H38O7)。米酵菌酸属于( )A、氧化物 B、混合物 C、有机化合物 D、碱3. 下列仪器名称为“容量瓶”的是( )A、
 B、
B、 C、
C、 D、
D、 4. 反应3Fe+4H2O(g) Fe3O4+4H2中,氧化剂是( )A、Fe B、H2O C、Fe3O4 D、H25. 下列物质属于电解质的是( )A、酒精 B、NaCl溶液 C、SO2 D、KNO36. 用激光笔照射下列物质时,无法观察到丁达尔效应的是( )A、CuSO4溶液 B、有色玻璃 C、雾 D、向沸水中滴入FeCl3饱和溶液所得的液体7. 下列表示错误的是( )A、氯离子的结构示意图
4. 反应3Fe+4H2O(g) Fe3O4+4H2中,氧化剂是( )A、Fe B、H2O C、Fe3O4 D、H25. 下列物质属于电解质的是( )A、酒精 B、NaCl溶液 C、SO2 D、KNO36. 用激光笔照射下列物质时,无法观察到丁达尔效应的是( )A、CuSO4溶液 B、有色玻璃 C、雾 D、向沸水中滴入FeCl3饱和溶液所得的液体7. 下列表示错误的是( )A、氯离子的结构示意图 B、二氧化碳的结构式 O=C=O
C、CH4的分子结构模型
B、二氧化碳的结构式 O=C=O
C、CH4的分子结构模型  D、NaCl的电子式
D、NaCl的电子式  8. 化学与生活息息相关,下列说法错误的是( )A、铝合金是制造飞机和宇宙飞船的理想材料 B、氯气是重要的化工原料,可大量用于制造盐酸、农药、染料和药品等 C、铁粉可用作食品脱氧剂 D、汽车的尾气催化转化器中发生了反应:NO+CO=C+NO29. 下列说法错误的是( )A、H2O、D2O、T2O互为同位素 B、 的原子核内中子数为10 C、红氧(O8)与氧气(O2)互为同素异形体 D、 和 的质量数相等,质子数不等,不是同一种元素10. 为除去括号内的杂质,所选用的试剂或方法错误的是( )A、FeCl2溶液(FeCl3):加入过量铁粉,过滤 B、NaHCO3溶液(Na2CO3):通入过量的CO2气体 C、CO2气体(CO气体):通入O2点燃 D、MnO2固体(KCl固体):加水充分溶解,过滤,取滤渣,洗涤,干燥11. 下列生活中的物质与其主要成分的化学式、用途的对应关系中,错误的是( )A、食盐的主要成分是NaCl,可用作调味品 B、小苏打的主要成分是Na2CO3 , 可用作发酵粉 C、不锈钢的成分主要是Fe、Cr、Ni,可用作医疗器械,厨房用具和餐具 D、漂粉精的主要成分是Ca(ClO)2 , 可用作消毒剂12. 下列物质中,不能由单质直接化合制得的是( )A、HCl B、FeCl2 C、AlCl3 D、CuCl213. 对于实验室突发事件的应对措施和常见废弃物处理不恰当的是( )A、对于酸、碱、氧化剂或还原剂的废液应分别收集 B、如果不慎将碱液沾到皮肤上,应立即用大量的水冲洗,然后涂上盐酸 C、易燃物如钠、钾等若随便丢弃易引起火灾,可将未用完的钠、钾放回原试剂瓶 D、对于含重金属离子的废液,可利用沉淀法进行处理14. 相同温度和压强下,1molCO和1molCO2相比较,下列说法错误的是( )A、分子数相同,但原子数不同 B、体积相同,但不一定是22.4L C、质子数不同,电子数也不同 D、两者的密度相同15. 在下列溶液中一定能大量共存的离子组是( )A、在强酸性溶液中:Na+、K+、Cl-、 B、无色溶液中:Fe2+、Mg2+、Cl-、 C、含有大量 Fe3+的溶液中:OH-、I-、K+、Br- D、滴入酚酞变红的溶液中:K+、Na+、 、16. 下列离子反应方程式错误的是( )A、钠单质投入水中:Na+ 2H2O=Na++2OH-+H2↑ B、稀硫酸与氢氧化钡溶液反应:2H++ Ba2++2OH-= 2H2O+BaSO4↓ C、大理石被盐酸溶解:2H++CaCO3=Ca2++H2O+CO2↑ D、FeCl2溶液中滴加氯水:2Fe2++Cl2=2Fe3++2Cl-17. 如表为元素周期表的一部分,四种元素均为短周期元素,若X原子核外的最外层上有5个电子,则下列叙述中合理的是( )
8. 化学与生活息息相关,下列说法错误的是( )A、铝合金是制造飞机和宇宙飞船的理想材料 B、氯气是重要的化工原料,可大量用于制造盐酸、农药、染料和药品等 C、铁粉可用作食品脱氧剂 D、汽车的尾气催化转化器中发生了反应:NO+CO=C+NO29. 下列说法错误的是( )A、H2O、D2O、T2O互为同位素 B、 的原子核内中子数为10 C、红氧(O8)与氧气(O2)互为同素异形体 D、 和 的质量数相等,质子数不等,不是同一种元素10. 为除去括号内的杂质,所选用的试剂或方法错误的是( )A、FeCl2溶液(FeCl3):加入过量铁粉,过滤 B、NaHCO3溶液(Na2CO3):通入过量的CO2气体 C、CO2气体(CO气体):通入O2点燃 D、MnO2固体(KCl固体):加水充分溶解,过滤,取滤渣,洗涤,干燥11. 下列生活中的物质与其主要成分的化学式、用途的对应关系中,错误的是( )A、食盐的主要成分是NaCl,可用作调味品 B、小苏打的主要成分是Na2CO3 , 可用作发酵粉 C、不锈钢的成分主要是Fe、Cr、Ni,可用作医疗器械,厨房用具和餐具 D、漂粉精的主要成分是Ca(ClO)2 , 可用作消毒剂12. 下列物质中,不能由单质直接化合制得的是( )A、HCl B、FeCl2 C、AlCl3 D、CuCl213. 对于实验室突发事件的应对措施和常见废弃物处理不恰当的是( )A、对于酸、碱、氧化剂或还原剂的废液应分别收集 B、如果不慎将碱液沾到皮肤上,应立即用大量的水冲洗,然后涂上盐酸 C、易燃物如钠、钾等若随便丢弃易引起火灾,可将未用完的钠、钾放回原试剂瓶 D、对于含重金属离子的废液,可利用沉淀法进行处理14. 相同温度和压强下,1molCO和1molCO2相比较,下列说法错误的是( )A、分子数相同,但原子数不同 B、体积相同,但不一定是22.4L C、质子数不同,电子数也不同 D、两者的密度相同15. 在下列溶液中一定能大量共存的离子组是( )A、在强酸性溶液中:Na+、K+、Cl-、 B、无色溶液中:Fe2+、Mg2+、Cl-、 C、含有大量 Fe3+的溶液中:OH-、I-、K+、Br- D、滴入酚酞变红的溶液中:K+、Na+、 、16. 下列离子反应方程式错误的是( )A、钠单质投入水中:Na+ 2H2O=Na++2OH-+H2↑ B、稀硫酸与氢氧化钡溶液反应:2H++ Ba2++2OH-= 2H2O+BaSO4↓ C、大理石被盐酸溶解:2H++CaCO3=Ca2++H2O+CO2↑ D、FeCl2溶液中滴加氯水:2Fe2++Cl2=2Fe3++2Cl-17. 如表为元素周期表的一部分,四种元素均为短周期元素,若X原子核外的最外层上有5个电子,则下列叙述中合理的是( )X
Y
Z
W
A、Y的氢化物的化学式一定是H2Y B、W的氧化物对应的水化物一定为强酸 C、四种元素的原子半径由小到大的顺序为X<Y<Z<W D、X、Y、Z三种元素中任意两种化合均可形成共价化合物18. 下列说法正确的是( )A、MgCl2固体中的化学键是共价键 B、某物质在熔融态能导电,则该物质中一定含有离子键 C、N2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构 D、H2O的空间结构呈直线形19. 下列实验操作或装置正确的是( ) A、图甲装置可用于完成过滤操作 B、图乙可用于比较碳酸钠和碳酸氢钠的热稳定性 C、图丙可实现制备Fe(OH)2并观察其颜色 D、图丁表示为配制一定物质的量浓度NaOH溶液时称量溶质的操作20. 相同质量的两份铝粉,分别放入足量的盐酸和氢氧化钠溶液中,放出的氢气在同温同压下的体积之比是( )A、1:1 B、1:6 C、2:3 D、3:221. 设NA为阿伏加德罗常数的值,下列说法中正确的是( )A、标准状况下,22.4 L H2O含有的分子数为NA B、2.3 g Na与足量水反应转移电子数为0.1NA C、1 L 1 mol·L-1 C2H5OH水溶液中含有的氢原子数为6NA D、22.4 L Cl2中含有Cl-Cl键的数目一定为NA22. 新型陶瓷AlN可通过反应: 合成。下列叙述正确的是( )A、上述反应中,N2是还原剂,Al2O3是氧化剂 B、AlN中氮元素的化合价为+3 C、上述反应中,每生成1molAlN需转移3mol电子 D、AlN的摩尔质量为41g23. 某化学兴趣小组在学习铁及其化合物知识时,做了如下探究实验:
A、图甲装置可用于完成过滤操作 B、图乙可用于比较碳酸钠和碳酸氢钠的热稳定性 C、图丙可实现制备Fe(OH)2并观察其颜色 D、图丁表示为配制一定物质的量浓度NaOH溶液时称量溶质的操作20. 相同质量的两份铝粉,分别放入足量的盐酸和氢氧化钠溶液中,放出的氢气在同温同压下的体积之比是( )A、1:1 B、1:6 C、2:3 D、3:221. 设NA为阿伏加德罗常数的值,下列说法中正确的是( )A、标准状况下,22.4 L H2O含有的分子数为NA B、2.3 g Na与足量水反应转移电子数为0.1NA C、1 L 1 mol·L-1 C2H5OH水溶液中含有的氢原子数为6NA D、22.4 L Cl2中含有Cl-Cl键的数目一定为NA22. 新型陶瓷AlN可通过反应: 合成。下列叙述正确的是( )A、上述反应中,N2是还原剂,Al2O3是氧化剂 B、AlN中氮元素的化合价为+3 C、上述反应中,每生成1molAlN需转移3mol电子 D、AlN的摩尔质量为41g23. 某化学兴趣小组在学习铁及其化合物知识时,做了如下探究实验: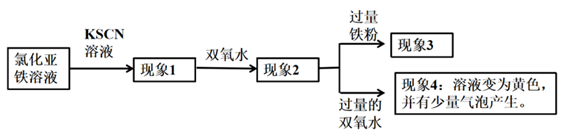
下列说法错误的是( )
A、若现象1有淡红色,说明有少量的Fe2+被氧化了 B、现象2有血红色沉淀 C、现象3为血红色褪去,说明发生了反应:2Fe3++Fe =3Fe2+ D、由现象4可推测加入过量的双氧水后硫氰根离子可能被氧化生成了气体24. 我国化学家侯德榜改进国外的纯碱生产工艺,生产流程可简要表示如图:
以下说法中错误的是( )
A、向饱和食盐水中先通入足量的NH3 , 再通入足量的CO2 B、沉淀池中得到的沉淀为碳酸钠 C、使原料氯化钠的利用率从70%提高到90%以上,主要是设计了循环1 D、循环2中的气体X为CO225. X 溶液中可能含有下列离子中的若干种:Cl-、 、Na+、K+、Fe2+、Fe3+、Mg2+。现对X 溶液进行如图所示的实验,其现象和结果如下:
下列说法错误的是( )
A、X 溶液中一定含有Fe2+ 、Cl- B、取溶液B进行焰色试验,若能看到黄色火焰,则X溶液中有Na+ C、取溶液B进行焰色试验,若透过蓝色钴玻璃能看到紫色火焰,则X溶液中有K+ D、白色沉淀A在空气中变红褐色的反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3二、填空题
-
26. 按要求回答下列问题(1)、写出高氯酸的化学式。(2)、写出中子数为1的氦原子符号。(3)、写出氯酸钾在水溶液中的电离方程式。(4)、写出实验室制备氯气的化学方程式。27. 已知氢化钠(NaH)可在野外用作生氢剂,其中氢元素的化合价为-1价。NaH用作生氢剂时的化学反应原理为:NaH+H2O=NaOH+H2↑。请回答以下问题:(1)、氢化钠属于化合物(填“共价”或“离子”)。(2)、该反应中氧化剂是 , 被氧化的氢原子与被还原的氢原子的个数比为。(3)、若反应恰好转移了1mol电子时,消耗的氢化钠的质量为g。
三、综合题
-
28. X、Y、Z、U、V、W六种短周期主族元素,原子序数依次增大。元素Y与V同主族,且V的原子序数是Y的两倍,金属元素Z的化合物ZX的电子总数为12,U离子的半径是同周期元素中最小的。请用实际推断的元素或化学式回答以下问题:(1)、Y元素在周期表中的位置是。(2)、化合物X2Y的电子式为。(3)、U的氧化物对应水化物与氢氧化钠溶液反应的离子方程式为。(4)、比较W与V 的氢化物的稳定性>。(5)、比较W、Z、Y的简单离子半径由大到小的顺序是。29. 硫酸铜是一种具有很多用途的化学物质,在工业领域(涂料工业、印染工业及有机工业)和农业领域(配制杀菌剂)都有广泛应用。现用胆矾(CuSO4·5H2O,式量为250)为原料配制220mL浓度为0.2mol/L的硫酸铜溶液。(1)、在实验过程中,选用最合适的容量瓶为_______。A、200 mL容量瓶 B、250 mL容量瓶 C、500 mL容量瓶(2)、容量瓶上标有_______。(填字母)
①温度 ②物质的量浓度 ③容积 ④压强 ⑤刻度线
A、①③⑤ B、①③④ C、②④ D、②④⑤(3)、通过计算,应该使用托盘天平称取胆矾g。(4)、下列操作会使所配溶液浓度偏高的是。①实验前,容量瓶用蒸馏水洗涤后未用标准液润洗;
②所用的胆矾晶体由于保存不善,导致失去部分结晶水;
③溶解时,不小心有少量溶液溅出;
④移液后,洗涤烧杯和玻璃棒2-3次,并将洗涤液也移入容量瓶;
⑤定容时,俯视液面;
⑥摇匀后,发现液面低于刻度线,又加水至刻度线。
(5)、将蓝色胆矾晶体加热会逐步失去结晶水,最终变为白色的硫酸铜粉末,则该变化过程为变化(填“物理”或“化学”)。30. 请选择合适的实验用品和化学试剂,用下图所示装置(C中盛放的是过氧化钠固体)进行实验,证明过氧化钠可以用作呼吸面具和潜水艇中的供氧剂。 (1)、仪器C的名称是。(2)、若分液漏斗中盛放的试剂是盐酸,为了除去混合气体中的氯化氢,装置B中盛放的试剂是。(3)、C中可能发生的化学反应的化学方程式为。(4)、D中盛放的试剂作用是。(5)、检验F中收集到的气体的方法是。
(1)、仪器C的名称是。(2)、若分液漏斗中盛放的试剂是盐酸,为了除去混合气体中的氯化氢,装置B中盛放的试剂是。(3)、C中可能发生的化学反应的化学方程式为。(4)、D中盛放的试剂作用是。(5)、检验F中收集到的气体的方法是。四、计算题
-
31. 现有CuO和Fe2O3组成的混合物若干克,向其中加入一定浓度的硫酸溶液50.0mL,恰好完全反应。向反应后的溶液中不断加入铁粉,加入铁粉的质量与充分反应后剩余固体的质量关系如图所示。

试计算:
(1)、固体混合物中CuO的质量分数为%;(2)、硫酸溶液的物质的量浓度为mol/L