初中科学浙教版九年级上册专题复习: 常见的盐
试卷更新日期:2021-10-17 类型:复习试卷
一、单选题
-
1. 下列物质的俗名、化学式、物质类别完全对应的是( )A、汞 Hg 非金属 B、生石灰 CaO 氧化物 C、胆矾 CuSO4 盐 D、纯碱 NaOH 碱2. 下列化学反应中,属于复分解反应的是( )。A、2H2+O2 =2H2O B、NaCl+AgNO3=AgCl↓+NaNO3 C、Mg+2HCl=MgCl2+H2↑ D、2HgO 2Hg+O2↑3. 农作物茎秆软弱易倒伏,抗病虫害能力弱,可施加下列哪种肥料( )A、NH4NO3 B、K2CO3 C、CaSO4 D、Mg3(PO4)24. “一带一路”赋予古丝绸之路崭新的时代内涵。古代染坊常用下列物质中的一种盐来处理丝绸,这种盐可能是( )A、熟石灰 B、碳酸钾 C、乙醇 D、烧碱5. 下列物质的名称、俗称和化学式都相符的是( )A、氢氧化钠 食盐 NaCl B、氧化钙 熟石灰 CaO C、氧化钠 苛性钠 NaOH D、碳酸钠 纯碱 Na2CO36. 合理施用化肥,有利于农作物的生长。下列有关农业应用的叙述中正确的是( )A、钾肥能促进作物根系发达,增强抗旱和抗寒能力 B、化学肥料的大量施用,会使得农作物“烧苗”,但并不会破坏土壤结构 C、不能将尿素 CO(NH2) 2 与熟石灰混放或混用 D、用石灰乳与硫酸铜溶液配制农药波尔多液7. 下列化学反应中,属于复分解反应的是( )A、 CaCO3 CaO+CO2↑ B、H2O+CO2=H2CO3 C、H2 + CuO Cu + H2O D、BaCl2 +H2SO4=BaSO4↓+2HCl8. 我们初中阶段学习了四种基本化学反应类型,其中复分解反应是九年级学习的重要反应类型,请同学们判断一下下列物质组合能发生复分解反应的有( )个
①K2CO3+CaCl2 ②H2SO4+KCl ③CuO+HCl ④Fe+CuSO4
⑤CO2+NaOH ⑥K2SO4+BaCl2 ⑦Mg(OH)2+CuSO4 ⑧BaCO3+NaOH.
A、3 B、4 C、5 D、69. 化肥对提高农作物的产量有重要作用。下列有关化肥的说法,不正确的是( )A、长期使用化肥会导致土壤板结,故提倡农家肥与化肥综合施用 B、草木灰是一种农家肥,可以促进植物茎秆强壮 C、磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿 D、常用作氮肥的化合物有尿素、碳酸氢铵等10. 物质王国发生了一起团伙盗窃案,“警察” 把三名“嫌疑犯”(分别是稀硫酸、氯化钠溶液和石灰水,见右图)带回了“警察局”。上级派出下列四名“警察”分别去审问“他们”(即把“他们”鉴别出来)。无法完成任务的“警察”是( ) A、
A、 紫色石蕊试液“警察”
B、
紫色石蕊试液“警察”
B、 稀硫酸“警察”
C、
稀硫酸“警察”
C、 无色酚酞试液“警察”
D、
无色酚酞试液“警察”
D、 纯碱溶液“警察”
11. 游泳是体育中考的项目之一。小明第一次去学习游泳时发现,泳池中的水看上去似乎有点蓝色,而必经之路上还有一个小水池,里面的水似乎有点紫红色。教练告诉他,这里面分别加入了两种小明学过的盐,它们均有一定的杀菌消毒作用。请你根据所学知识帮助小明判断这两种盐的成分是 ( )A、氯化铁和硫酸铜 B、氢氧化钙和氯化钠 C、硫酸铜和高锰酸钾 D、氯化铁和氯化钠12. 下列有关物质的化学式、名称、俗名不完全对应的是( )A、Ca(OH)2 氢氧化钙 消石灰 B、NaOH 氢氧化钠 烧碱 C、Na2CO3 碳 酸钠 纯碱 D、CaO 氧化钙 熟石灰13. 下列物质的名称、俗称和化学式表示的是同一种物质的是( )A、胆矾、硫酸铜、CuSO4 B、铁锈、氢氧化铁、Fe(OH)3 C、烧碱、苛性钠、NaOH D、消石灰、石灰石、CaCO314. 下列物质名称、俗称、化学式、物质类别完全正确的是( )A、氢氧化钠、苛性钠、NaOH、碱 B、碳酸钠、纯碱、Na2CO3、碱 C、氢氧化钙、生石灰、Ca(OH)2、碱 D、硫酸铜、胆矾、CuSO4·5H2O、混合物15. “测土配方施肥”技术能有效解决施肥比例不合理的问题,如下为农技人员通过该技术对某农田开出的施肥配方,有NH4H2PO4、K2SO4、KCl、NH4NO3等肥料,其中属于复合肥料的是( )A、NH4H2PO4 B、K2SO4 C、KCl D、NH4NO3
纯碱溶液“警察”
11. 游泳是体育中考的项目之一。小明第一次去学习游泳时发现,泳池中的水看上去似乎有点蓝色,而必经之路上还有一个小水池,里面的水似乎有点紫红色。教练告诉他,这里面分别加入了两种小明学过的盐,它们均有一定的杀菌消毒作用。请你根据所学知识帮助小明判断这两种盐的成分是 ( )A、氯化铁和硫酸铜 B、氢氧化钙和氯化钠 C、硫酸铜和高锰酸钾 D、氯化铁和氯化钠12. 下列有关物质的化学式、名称、俗名不完全对应的是( )A、Ca(OH)2 氢氧化钙 消石灰 B、NaOH 氢氧化钠 烧碱 C、Na2CO3 碳 酸钠 纯碱 D、CaO 氧化钙 熟石灰13. 下列物质的名称、俗称和化学式表示的是同一种物质的是( )A、胆矾、硫酸铜、CuSO4 B、铁锈、氢氧化铁、Fe(OH)3 C、烧碱、苛性钠、NaOH D、消石灰、石灰石、CaCO314. 下列物质名称、俗称、化学式、物质类别完全正确的是( )A、氢氧化钠、苛性钠、NaOH、碱 B、碳酸钠、纯碱、Na2CO3、碱 C、氢氧化钙、生石灰、Ca(OH)2、碱 D、硫酸铜、胆矾、CuSO4·5H2O、混合物15. “测土配方施肥”技术能有效解决施肥比例不合理的问题,如下为农技人员通过该技术对某农田开出的施肥配方,有NH4H2PO4、K2SO4、KCl、NH4NO3等肥料,其中属于复合肥料的是( )A、NH4H2PO4 B、K2SO4 C、KCl D、NH4NO3二、填空题
-
16. 硫酸钡不容易被X射线透过,在医疗上可用作检查肠胃的内服剂,俗称“钡餐"。某同学将硫酸镁溶液滴入硝酸钡[Ba(NO3)2]溶液中得到硫酸钡,右图表示该实验过程中溶液总质量随加入硫酸镁溶液质量的变化情况。图像AB段对应的实验现象是 , C点处溶液中的溶质有。
 17. 有一瓶白色固体可能含有NaCl、Na2CO3和Na2SO4中的一种或几种。将白色固体溶解于水中,再滴加足量BaCl2溶液,出现白色沉淀,再滴加过量盐酸,沉淀不消失。
17. 有一瓶白色固体可能含有NaCl、Na2CO3和Na2SO4中的一种或几种。将白色固体溶解于水中,再滴加足量BaCl2溶液,出现白色沉淀,再滴加过量盐酸,沉淀不消失。请据此回答下列问题:
(1)、写出白色沉淀的化学式。(2)、白色粉末中不能确定的物质是。18. 小宁同学取了适量实验室制二氧化碳发生装置中的剩余溶液。逐滴滴加纯碱溶液,绘制产生沉淀的图象如甲图所示。 (1)、请写出B点对应溶液的溶质是(写化学式)。(2)、乙图是甲图中0点到A点的反应微观实质模型图。则“
(1)、请写出B点对应溶液的溶质是(写化学式)。(2)、乙图是甲图中0点到A点的反应微观实质模型图。则“ ”表示(写化学符号)。 (3)、写出OA之间发生的化学反应方程式。19. 小明家是种植蔬菜的专业户,他学习了化学后知道:施用适量氮肥可以使种植的蔬菜叶色浓绿。(1)、下列属于氮肥的是__________(填字母序号)。A、碳酸氢铵(NH4HCO3) B、硫酸钾(K2SO4) C、磷矿粉[Ca3(PO4)2](2)、氯化铵(NH4Cl)与氢氧化钠溶液混合加热,生成了氯化钠、水和有刺激性气味的氨气(NH3),该反应可以用于铵态氮肥的检验,请写出该反应的化学方程式:。因此,铵态氮肥不能和物质混合使用,否则会降低肥效20. 现有H、S、O、Na四种元素,请选用其中的元素写出符合下列要求的化学式各一个:(1)、相对分子质量最小的氧化物;(2)、用于金属表面除锈的酸;(3)、一种常见的碱;(4)、由三种元素组成的一种盐;21. 现有失去标签的四瓶溶液,分别是氯化铁、氯化钙、稀盐酸、氯化钠溶液中的一种,要鉴别出它们,可进行以下实验:(1)、通过观察,溶液呈黄色的是。(2)、将剩余溶液分别取样,加入溶液,可以将它们一次性鉴别出来。22. 向一定质量的CaCl2和HCl的混合溶液中逐滴加入Na2CO3溶液,并振荡。如图表示反应过程中溶液质量随加入Na₂CO3溶液质量的变化情况。图线AB段对应的实验现象是 , 在C点时溶液中的溶质是。
”表示(写化学符号)。 (3)、写出OA之间发生的化学反应方程式。19. 小明家是种植蔬菜的专业户,他学习了化学后知道:施用适量氮肥可以使种植的蔬菜叶色浓绿。(1)、下列属于氮肥的是__________(填字母序号)。A、碳酸氢铵(NH4HCO3) B、硫酸钾(K2SO4) C、磷矿粉[Ca3(PO4)2](2)、氯化铵(NH4Cl)与氢氧化钠溶液混合加热,生成了氯化钠、水和有刺激性气味的氨气(NH3),该反应可以用于铵态氮肥的检验,请写出该反应的化学方程式:。因此,铵态氮肥不能和物质混合使用,否则会降低肥效20. 现有H、S、O、Na四种元素,请选用其中的元素写出符合下列要求的化学式各一个:(1)、相对分子质量最小的氧化物;(2)、用于金属表面除锈的酸;(3)、一种常见的碱;(4)、由三种元素组成的一种盐;21. 现有失去标签的四瓶溶液,分别是氯化铁、氯化钙、稀盐酸、氯化钠溶液中的一种,要鉴别出它们,可进行以下实验:(1)、通过观察,溶液呈黄色的是。(2)、将剩余溶液分别取样,加入溶液,可以将它们一次性鉴别出来。22. 向一定质量的CaCl2和HCl的混合溶液中逐滴加入Na2CO3溶液,并振荡。如图表示反应过程中溶液质量随加入Na₂CO3溶液质量的变化情况。图线AB段对应的实验现象是 , 在C点时溶液中的溶质是。 23. 厨房里有两瓶白色固体,分别为食盐(NaCl) 和纯碱(Na2CO3)。(1)、可用于腌制肉类和蔬菜,使食物不易腐败的是。(2)、为鉴别这两种物质,某同学取少量白色固体,进行如下实验。
23. 厨房里有两瓶白色固体,分别为食盐(NaCl) 和纯碱(Na2CO3)。(1)、可用于腌制肉类和蔬菜,使食物不易腐败的是。(2)、为鉴别这两种物质,某同学取少量白色固体,进行如下实验。方案一:分别滴加少量食醋,有气泡产生的是。
方案二:加水溶解,分别滴加溶液,有沉淀产生的是纯碱。
24. 两种互相交换成分,生成另外两种的反应,叫做复分解反应。在初中阶段接触到的反应中,当两种化合物互相交换成分后,生成物里有或有或有时,复分解反应才能发生。25. 将无色的碳酸钠溶液滴入盛有澄清石灰水的试管,试管中出现;在盛有10毫升氯化铁溶液的试管中,滴人几滴硫氰化钾溶液,可以观察到。这些现象都为我们判断化学反应的发生提供了证据。三、实验探究题
-
26. 某化学兴趣小组的同学在学习了纯碱(Na2CO3)的性质后,联想到家中蒸制馒头时常用的物质小苏打(NaHCO3),于是采用市售的小苏打样品进行了如下实验探究碳酸氢钠的化学性质。

⑴取样品溶于适量的水中,测得溶液的pH大于7。
⑵向小苏打样品中滴加盐酸,有大量气泡产生,经检验该气体是二氧化碳,则该反应的化学方程式为。
⑶向小苏打的溶液中加入溢清石灰水,生成了白色沉淀。
⑷同学们通过查阅资料,在老师的指导下采用了如图所示装置对小苏打和纯截做了对比实验。实验中小试管内沾有无水硫酸铜粉末的棉花变成蓝色,a烧杯中右灰水无明显现象,b烧杯中石灰水出现白色浑浊,试回答:
①在实验结束时,操作主要注意的问题是:。
②请归纳小苏打的化学性质(至少两点) , 。
27. 某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如下图),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
【提出猜想】这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;猜想三:碳酸钠溶液。
【实验推断】
⑴小丽取样滴加无酚酞试液,溶液呈红色。
⑵小刚另取样滴加稀盐酸有产生,小刚得出结论:该溶液是碳酸钠溶液。
⑶小青认为小刚的结论不完全正确,理由是。
小组同学讨论后一致认为还需要进行如下实验:
【继续探究】另取样加入过量的CaCl2溶液,观察到有白色沉淀产生,设计这一步骤的目的是;静置后,取上层清液,滴入酚酞试液,溶液呈红色。
【实验结论】猜想是正确的。
28. 血液长期呈酸性会使大脑和神经功能退化,导致记忆力减退。补养之道就是常吃碱性食物。那么, 苹果到底是酸性物质还是碱性物质呢?小金进行了探究。请回答:【查阅资料】①在营养学中,食品的酸碱性分为“食品的口味酸碱性”和“食品的生理酸碱性”(指食品被身 体吸收后的酸碱性);②可以利用灼烧的方法来判断食品的生理酸碱性。
【进行实验】①测定苹果的口味酸碱性:取苹果20克,榨汁,取滤液测得pH<7。②测定苹果的生理酸碱性:另取苹果20克,切碎,放入坩埚内,加强热至质量不再变化,将残渣用少量水溶解,取滤液测得pH>7。在此过程中,下列可采用的是。(填序号,多选)①石蕊试液 ②pH试纸 ③石蕊试纸
【继续探究】苹果是口味“酸性”、生理“碱性”的食品,小金猜想:食品的口味酸碱性与生理酸碱性是否正好相反?又选了一些常见食品用上述方法继续进行实验验证,设计实验记录表,收集有关数据。在实验记录表中必须出现的栏目是。(填字母,多选)
A.食品名称 B.加热时间 C.残渣质量D.坩埚质量 E.口味酸碱性 F.生理酸碱性
【反思与分享】若要比较香蕉和蛋黄这两种食品的生理酸碱性强弱,你认为必须控制的实验条件之一是。实验表明,有些物质口味酸碱性与生理酸碱性正好相反。
29. 因碳酸钠既能与酸反应又能与碱反应,小金利用碳酸钠、稀盐酸和澄清石灰水 3 种试剂分别设计实验方案,探究复分解反应发生的实质。(1)、小金探究碳酸钠溶液与稀盐酸的反应①小金认为碳酸钠溶液与稀盐酸的复分解反应能够发生的原因:反应物中实际参加反应的阴离子
(CO32-)、阳离子(H+)能相互结合。而在上述反应中,Na+、Cl-并没有参加反应,得出此结论的理由是:。3
②小金用画图的方法来体现碳酸钠溶液和稀盐酸反应的实质。请你在答题卷对应的图中,填入适当的分子或离子符号,与小金一起完成学习任务:
 (2)、小金探究碳酸钠溶液与澄清石灰水的反应①碳酸钠溶液与澄清石灰水的反应实质是。
(2)、小金探究碳酸钠溶液与澄清石灰水的反应①碳酸钠溶液与澄清石灰水的反应实质是。②为确定碳酸钠溶液与澄清石灰水是否恰好完全反应,小金先将反应后的物质进行过滤,然后对滤液的成分提出了下列四个假设:
甲:滤液中只含氢氧化钠 乙:滤液中含氢氧化钠、氢氧化钙和碳酸钠 丙:滤液中含氢氧化钠和氢氧化钙 丁:滤液中含氢氧化钠和碳酸钠
请指出哪种假设不合理,并说明理由:。
③接着,小金继续进行如下探究:
实验步骤
实验现象
结论
取少量滤液放在试管中,再滴入氯化钙溶液
若生成白色沉淀
碳酸钠过量
若无明显现象
恰好反应
小金的设计方案能说明碳酸钠溶液和澄清石灰水恰好完全反应吗?评判理由是。
30. 小科在学习复分解反应时,对复分解反应发生的条件产生了兴趣,于是他和小组内的同学仅用以下药品展开了探究活动。实验药品:稀硫酸、稀盐酸、NaOH溶液、Na2CO3溶液、Ba(NO3)2溶液、NaCl溶液、酚酞溶液。小科用上述物质做了下列几组实验。
组合序号
①
②
③
④
⑤
⑥
组合物质
H2SO4
NaOH
H2SO4
NaCl
H2SO4
Na2CO3
H2SO4
Ba(NO3)2
NaOH
Ba(NO3)2
Na2CO3
Ba(NO3)2
【记录和解释】
组合①、②、⑤均无明显现象,其中组合与另外两组的实质不同。为证明该不同之处,小科在实验过程中使用了酚酞溶液。
【实验结论】他们请教老师并讨论后知道,只有当两种化合物互相交换成分,生成物中有生产时,复分解反应才可以发生。
【交流与反思】根据你对物质溶解性的了解,结合复分解反应发生的条件,请写出一种在水溶液中一般不能发生复分解反应的可溶性盐(写化学式)。
四、解答题
-
31. 小金同学按如图实验测定部分变质的NaOH固体中Na2CO3的质量分数。
 (1)、根据题中信息填“能”或“不能”)计算Ca(OH)2溶液的溶质质量分数。(2)、计算固体混合物中Na2CO3的质量分数。32. BaCl2 是一种重金属盐,其水溶液具有很强的毒性。(1)、若误服了 BaCl2 溶液,为减轻毒性,最好服用下列物质中的 。A、H2SO4 溶液 B、肥皂水 C、蛋清 D、Na2SO4 溶液(2)、为测定某 BaCl2 溶液的溶质质量分数,现取 100 克BaCl2 溶液,不断加入 MgSO4 溶液,反应过程中溶液总质量与加入 MgSO4 溶液的质量关系如图所示,请回答:
(1)、根据题中信息填“能”或“不能”)计算Ca(OH)2溶液的溶质质量分数。(2)、计算固体混合物中Na2CO3的质量分数。32. BaCl2 是一种重金属盐,其水溶液具有很强的毒性。(1)、若误服了 BaCl2 溶液,为减轻毒性,最好服用下列物质中的 。A、H2SO4 溶液 B、肥皂水 C、蛋清 D、Na2SO4 溶液(2)、为测定某 BaCl2 溶液的溶质质量分数,现取 100 克BaCl2 溶液,不断加入 MgSO4 溶液,反应过程中溶液总质量与加入 MgSO4 溶液的质量关系如图所示,请回答: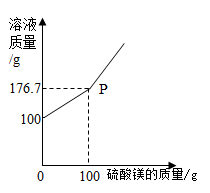
①P 点意义。
②反应生成沉淀的最大质量为克;
③求原 BaCl2 溶液的溶质质量分数。
33. 现有一定质量含有少量泥沙等不溶性杂质和少量Na2SO4 , MgCl2 , CaCl2等可溶性杂质的粗盐样品,某实验小组利用化学实验室常用仪器对粗盐样品进行提纯,提纯步骤如下:请根据提纯步骤回答下列问题.
(1)、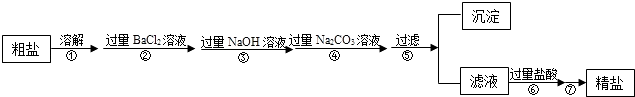 步骤⑦的操作名称为 . (2)、请写出实验步骤②中所涉及的化学方程式。(3)、步骤⑥中加入过量盐酸的目的是。(4)、步骤②和步骤④(填“可以”或“不可以”)颠倒,理由是。(5)、检验步骤④中Na2CO3溶液已过量的方法是。
步骤⑦的操作名称为 . (2)、请写出实验步骤②中所涉及的化学方程式。(3)、步骤⑥中加入过量盐酸的目的是。(4)、步骤②和步骤④(填“可以”或“不可以”)颠倒,理由是。(5)、检验步骤④中Na2CO3溶液已过量的方法是。