浙教版科学九年级上册第二章 物质转化与材料利用 5~6节夯实基础训练题
试卷更新日期:2021-10-14 类型:同步测试
一、单选题
-
1. 工业炼铁的部分反应如图所示,则( )
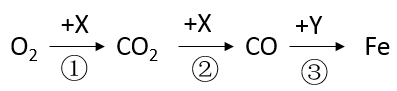 A、X可以是木炭 B、X与CO都具有氧化性 C、③反应后的尾气可直接排放 D、Y中铁元素以游离态存在2. 现有① NaOH溶液、② KCl溶液、③ MgCl2溶液、④ CuSO4溶液,不用其他试剂,可通 过实验方法将它们一一鉴别开来,鉴别出来的先后顺序可能是( )A、①②③④ B、①④③② C、④③②① D、④①③②3.
A、X可以是木炭 B、X与CO都具有氧化性 C、③反应后的尾气可直接排放 D、Y中铁元素以游离态存在2. 现有① NaOH溶液、② KCl溶液、③ MgCl2溶液、④ CuSO4溶液,不用其他试剂,可通 过实验方法将它们一一鉴别开来,鉴别出来的先后顺序可能是( )A、①②③④ B、①④③② C、④③②① D、④①③②3.某废液中只含有Fe(NO3)2、Cu(NO3)2、Ba(NO3)2三种溶质。为了回收金属、保护环境,小科设计了如图方案(所加试剂均过量)。下列判断正确的是( )
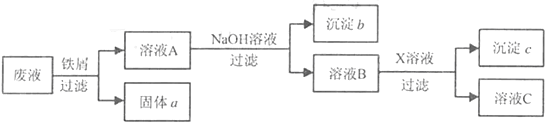 A、固体a是铜 B、X一定是Na2SO4 C、溶液B中含有的盐有Ba(NO3)2和NaNO3 D、若回收到6.4g固体a,则加入的铁屑质量为5.6g4. 在混合物中逐渐滴加X溶液,产生的气体或沉淀质量与X溶液质量之间的关系如图所示,则符合的选项是( )
A、固体a是铜 B、X一定是Na2SO4 C、溶液B中含有的盐有Ba(NO3)2和NaNO3 D、若回收到6.4g固体a,则加入的铁屑质量为5.6g4. 在混合物中逐渐滴加X溶液,产生的气体或沉淀质量与X溶液质量之间的关系如图所示,则符合的选项是( )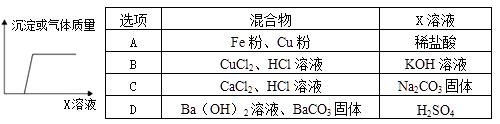 A、A B、B C、C D、D5. “接龙”是化学扑克(和普通扑克相似,牌面标注物质的化学式)的一种游戏,其规则是:当上家出牌时,下家跟出的牌所标注的物质必须能与上家的反应。某局游戏中,甲到戊五人各有一张不同的牌,标注“CuSO4”、“H2SO4”、“NaOH”、“Fe”、“Fe2O3”。若甲的牌为“Fe2O3”,且按甲→乙→丙→丁→戊依次出牌时能满足“接龙”规则,则丁的牌是( )
A、A B、B C、C D、D5. “接龙”是化学扑克(和普通扑克相似,牌面标注物质的化学式)的一种游戏,其规则是:当上家出牌时,下家跟出的牌所标注的物质必须能与上家的反应。某局游戏中,甲到戊五人各有一张不同的牌,标注“CuSO4”、“H2SO4”、“NaOH”、“Fe”、“Fe2O3”。若甲的牌为“Fe2O3”,且按甲→乙→丙→丁→戊依次出牌时能满足“接龙”规则,则丁的牌是( )
A、NaOH B、Fe C、H2SO4 D、CuSO46. 某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8 g,装置④增重2.2 g。
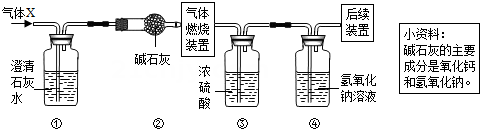
下列关于气体X成分的分析中,错误的是( )A、一定没有二氧化碳 B、可能含有甲烷和氢气 C、可能只有甲烷 D、可能含有氢气和一氧化碳7. 火星上存在针铁矿[FeO(OH)]和黄钾铁矾[KFe3(SO4)2(OH)n],两种物质中的铁元素的化合价相同,黄钾铁矾易溶于硫酸。下列有关叙述中,正确的是( )A、FeO(OH)中铁元素的化合价为+2 B、KFe3(SO4)2(OH)n中n的值为5 C、KFe3(SO4)2(OH)n属于碱 D、黄钾铁矾溶于硫酸后,滴加KSCN溶液,溶液变红8. 如图为氢气还原氧化铜的实验装置图,下列有关分析正确的是( )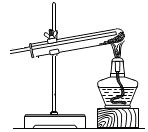 A、装置中试管口需略向下倾斜,主要是为了利于通入氢气 B、在给试管内药品加热前,需先通氢气排尽试管内的空气 C、待药品完全反应后,需同时撤去酒精灯和通氢气的导管 D、该实验装置也可直接用于一氧化碳还原氧化铜的实验9. 如图所示的甲、乙两个装置中,胶头滴管中含有某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是( )
A、装置中试管口需略向下倾斜,主要是为了利于通入氢气 B、在给试管内药品加热前,需先通氢气排尽试管内的空气 C、待药品完全反应后,需同时撤去酒精灯和通氢气的导管 D、该实验装置也可直接用于一氧化碳还原氧化铜的实验9. 如图所示的甲、乙两个装置中,胶头滴管中含有某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是( )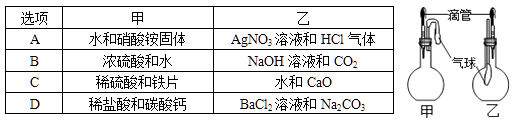 A、A B、B C、C D、D10. 某一种或几种物质的水溶液中,可能含有以下几种离子:Na+、Cl-、Ca2+、Ba2+、SO42-、CO32- , 现取两份100mL溶液进行如下实验:(1)第一份加入AgNO3溶液有沉淀产生。(2)第二份加足量的Ba(NO3)2溶液,有白色沉淀产生,再加入过量的稀硝酸,沉淀部分溶解。根据上述实验,以下推测正确的是( )
A、A B、B C、C D、D10. 某一种或几种物质的水溶液中,可能含有以下几种离子:Na+、Cl-、Ca2+、Ba2+、SO42-、CO32- , 现取两份100mL溶液进行如下实验:(1)第一份加入AgNO3溶液有沉淀产生。(2)第二份加足量的Ba(NO3)2溶液,有白色沉淀产生,再加入过量的稀硝酸,沉淀部分溶解。根据上述实验,以下推测正确的是( )
A、一定存在Cl﹣ B、一定存在CO32﹣ , 可能存在Ba2+ C、一定存在Na+ D、一定存在SO42﹣ , 可能存在Ca2+11. 三种物质间只通过一步反应就能实现如图箭头所指方向的转化,符合要求的组合( )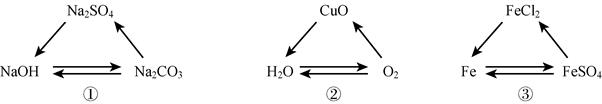 A、①② B、①③ C、②③ D、①②③12. 下列的检验及结论中一定正确的是( )A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液一定有碳酸盐 B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液一定有硫酸盐 C、分别含有Mg2+、Cu2+和Na+的三种盐酸盐溶液,用NaOH溶液就能一次鉴别开 D、加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+13. 根据下列实验得出的结论,正确的是( )A、某固体加入稀盐酸,产生了无色气体,证明该固体一定含有 B、某溶液中滴加 BaCl2 溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定有 C、某无色溶液滴入酚酞溶液后显红色,该溶液不一定是碱溶液 D、验证某烧碱样品中是否含有 Cl- , 先加入稀盐酸除去 OH- , 再加入 AgNO3 溶液,有不溶于稀硝酸的白色沉淀出现,证明含有 Cl-14. 对下列各组物质的鉴别分析错误的是( )A、黑色粉末:FeO、Fe、CuO、C 只用一种试剂即可鉴别 B、无色溶液:KOH、H2SO4、BaCl2、NaNO3 只用一种试剂即可鉴别 C、无色溶液:Na2CO3、AgNO3、BaCl2、HCl 不用其他试剂就可以鉴别 D、无色溶液:Ba(OH)2、Na2CO3、BaCl2、HNO3 不用其他试剂就无法鉴别15. 科学中较多的化学实验,据图判断下列能达到实验目的的实验是( )A、探究Cu、Ag两种金属的活动性强弱
A、①② B、①③ C、②③ D、①②③12. 下列的检验及结论中一定正确的是( )A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液一定有碳酸盐 B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液一定有硫酸盐 C、分别含有Mg2+、Cu2+和Na+的三种盐酸盐溶液,用NaOH溶液就能一次鉴别开 D、加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+13. 根据下列实验得出的结论,正确的是( )A、某固体加入稀盐酸,产生了无色气体,证明该固体一定含有 B、某溶液中滴加 BaCl2 溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定有 C、某无色溶液滴入酚酞溶液后显红色,该溶液不一定是碱溶液 D、验证某烧碱样品中是否含有 Cl- , 先加入稀盐酸除去 OH- , 再加入 AgNO3 溶液,有不溶于稀硝酸的白色沉淀出现,证明含有 Cl-14. 对下列各组物质的鉴别分析错误的是( )A、黑色粉末:FeO、Fe、CuO、C 只用一种试剂即可鉴别 B、无色溶液:KOH、H2SO4、BaCl2、NaNO3 只用一种试剂即可鉴别 C、无色溶液:Na2CO3、AgNO3、BaCl2、HCl 不用其他试剂就可以鉴别 D、无色溶液:Ba(OH)2、Na2CO3、BaCl2、HNO3 不用其他试剂就无法鉴别15. 科学中较多的化学实验,据图判断下列能达到实验目的的实验是( )A、探究Cu、Ag两种金属的活动性强弱 B、 鉴别化肥KNO3和NH4Cl
B、 鉴别化肥KNO3和NH4Cl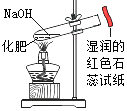 C、干燥氨气
C、干燥氨气 D、粗测空气中氧气的体积分数
D、粗测空气中氧气的体积分数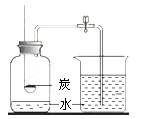 16. 将一定量的铜锌混合粉末放入盛有硝酸银溶液的烧杯中,充分反应后过滤。向滤渣中加入足量的稀盐酸,无现象。则滤渣中( )A、一定有银,可能有铜和锌 B、一定有银,可能有铜,一定没有锌 C、一定有银和铜,可能有锌 D、一定有银和铜,一定没有锌17. 下列实验操作中能与实验预期结果相一致的是( )A、验证质量守恒定律
16. 将一定量的铜锌混合粉末放入盛有硝酸银溶液的烧杯中,充分反应后过滤。向滤渣中加入足量的稀盐酸,无现象。则滤渣中( )A、一定有银,可能有铜和锌 B、一定有银,可能有铜,一定没有锌 C、一定有银和铜,可能有锌 D、一定有银和铜,一定没有锌17. 下列实验操作中能与实验预期结果相一致的是( )A、验证质量守恒定律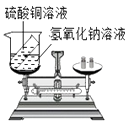 B、检验Cl-
B、检验Cl- 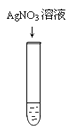 C、配制溶液时量取水
C、配制溶液时量取水  D、干燥氧气
D、干燥氧气  18. 下列物质的转化,不能一步实现的是( )A、Cu→Cu(OH)2 B、Ba(NO3)2→BaSO4 C、Zn→ZnCl2 D、Ca(OH)2→NaOH19. 甲、乙、丙、丁四种物质的转化关系如图所示。下列说法正确的是( )
18. 下列物质的转化,不能一步实现的是( )A、Cu→Cu(OH)2 B、Ba(NO3)2→BaSO4 C、Zn→ZnCl2 D、Ca(OH)2→NaOH19. 甲、乙、丙、丁四种物质的转化关系如图所示。下列说法正确的是( )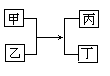 A、若丙、丁为盐和水,则甲、乙一定是酸、碱 B、若丙为气体,则甲、乙中一定有单质 C、若丁为水,则该反应一定是复分解反应 D、若只有甲、丁是单质,则该反应一定是置换反应20. 下列物质的转化在给定条件下均能实现的是( )
A、若丙、丁为盐和水,则甲、乙一定是酸、碱 B、若丙为气体,则甲、乙中一定有单质 C、若丁为水,则该反应一定是复分解反应 D、若只有甲、丁是单质,则该反应一定是置换反应20. 下列物质的转化在给定条件下均能实现的是( )
A、Fe Fe2O3 FeCl3 B、SO2 H2SO3 H2SO4 C、Na2CO3 NaNO3 KNO3 D、CaCl2溶液 CaCO3 Ca(OH)2二、填空题
-
21. 某气体可能由CO、H2、水蒸气中的一种或几种组成。小科利用下图的装置探究其成分,已知无水硫酸铜遇水会变蓝色。
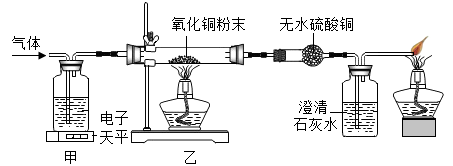 (1)、甲装置中盛放的液体是 。(2)、实验过程中观察到无水硫酸铜不变色,澄清石灰水变浑浊,则原气体中一定含有 (填化学式),同时乙装置中黑色固体变色。22. 下图是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“一”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。
(1)、甲装置中盛放的液体是 。(2)、实验过程中观察到无水硫酸铜不变色,澄清石灰水变浑浊,则原气体中一定含有 (填化学式),同时乙装置中黑色固体变色。22. 下图是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“一”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。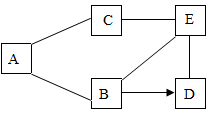 (1)、A物质是(填化学式)。(2)、C与E反应的基本类型是。(3)、从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与B反应生成D的物质有(填序号)。
(1)、A物质是(填化学式)。(2)、C与E反应的基本类型是。(3)、从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与B反应生成D的物质有(填序号)。①2类 ②3类 ③4类 ④5类
23.有一包白色粉末,可能是由硫酸铜、氯化钠、碳酸钠、硫酸钠中的一种或几种组成。为检验其中的成分,按以下流程进行实验:
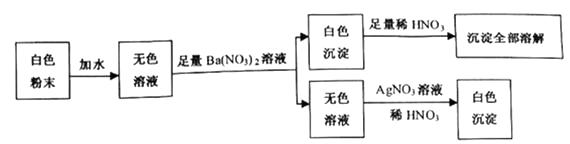 (1)、根据实验现象,白色粉末中一定有。(2)、实验中不能用BaCl2溶液代替Ba(NO3)2溶液的理由是。24. 铁的化合物有广泛用途,如碳酸亚铁(FeCO3)可作补血剂。某硫酸厂产生的炉渣中除了有Fe2O3、FeO,还有一定量的SiO2。兴趣小组利用炉渣尝试制备FeCO3 , 其流程如下:
(1)、根据实验现象,白色粉末中一定有。(2)、实验中不能用BaCl2溶液代替Ba(NO3)2溶液的理由是。24. 铁的化合物有广泛用途,如碳酸亚铁(FeCO3)可作补血剂。某硫酸厂产生的炉渣中除了有Fe2O3、FeO,还有一定量的SiO2。兴趣小组利用炉渣尝试制备FeCO3 , 其流程如下: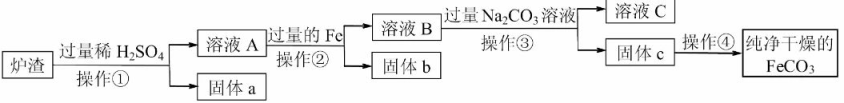
【已知:Fe+Fe2(SO4)3=3FeSO4;SiO2不溶于水,也不与稀硫酸反应】
(1)、操作①的名称是。(2)、溶液A中的溶质除H2SO4外,还存在。(3)、上述流程中生成固体c的化学方程式。25. 某化工厂利用含有1%-2%BaCO3的废料制取BaCl2(废料中其他物质不溶于水和稀盐酸、且不与稀盐酸反应)。其部分流程如下: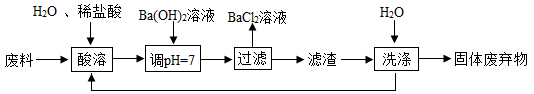
滤渣必须经过充分洗涤,确保其中Ba2+含量达到规定标准才能作为固体废弃物处理,检验Ba2+的试剂可用 , 洗涤滤渣的主要目的是。
26. A、B、C为初中科学常见的三种无机物,它们之间有如图所示的转化关系(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。请回答: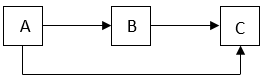 (1)、若C是气体,它能使带火星的木条复燃,A、B所属的物质类别和组成元素都相同,则A→B的化学方程式为;(2)、若A为光合作用的原料之一,A与B属于不同物质类别,B和C属于同种物质类别,A、B、C三种物质中都含有相同的两种元素,则C可能的物质类别是。
(1)、若C是气体,它能使带火星的木条复燃,A、B所属的物质类别和组成元素都相同,则A→B的化学方程式为;(2)、若A为光合作用的原料之一,A与B属于不同物质类别,B和C属于同种物质类别,A、B、C三种物质中都含有相同的两种元素,则C可能的物质类别是。三、实验探究题
-
27. 有一包白色粉末可能含有CaCO3、Na2CO3、Na2SO4、CuSO4、NaNO3中的一种或几种,某学生为了确定其组成,做如下实验,请根据实验现象进行推断:
⑴在试管中加入少量粉末,注入足量的蒸馏水充分振荡溶液无色透明;
⑵取少量上述溶液滴入盐酸, 有气泡产生;
⑶另取(1)中少量溶液滴入氯化钡溶液,有白色沉淀产生
⑷在(3)中滴加稀硝酸沉淀部分溶解,并有气泡产生.
该白色粉末中一定含有;一定没有;可能含有.(均填化学名称)
28.解决淡水资源危机对社会发展有重要意义。小柯设计如图装置模拟海水淡化,请回答:
 (1)、实验过程中发生的物态变化是。(2)、实验结束后,向乙装置的试管内滴加硝酸银和稀硝酸,目的是(3)、为使冷凝效果更好,可以对乙装置进行的操作是(写出一点即可)。29. 做酸碱实验时,小敏将稀盐酸逐滴加到氢氧化钡溶液中(如图),发现一直无明显现象,突然想起忘记加无色酚酞试液,为探究反应的进程,过程如下:(已知BaCl2溶液呈中性)
(1)、实验过程中发生的物态变化是。(2)、实验结束后,向乙装置的试管内滴加硝酸银和稀硝酸,目的是(3)、为使冷凝效果更好,可以对乙装置进行的操作是(写出一点即可)。29. 做酸碱实验时,小敏将稀盐酸逐滴加到氢氧化钡溶液中(如图),发现一直无明显现象,突然想起忘记加无色酚酞试液,为探究反应的进程,过程如下:(已知BaCl2溶液呈中性)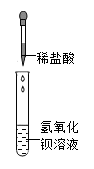 (1)、【建立猜想】①氢氧化钡过量②盐酸过量③(2)、【实验设计】步骤一:取少量反应后的溶液于试管中,滴入几滴无色酚酞试液,溶液不变色,得出猜想①错误。
(1)、【建立猜想】①氢氧化钡过量②盐酸过量③(2)、【实验设计】步骤一:取少量反应后的溶液于试管中,滴入几滴无色酚酞试液,溶液不变色,得出猜想①错误。步骤二:继续探究
实验方案
实验操作
实验现象
实验结论
Ⅰ
重新取样,滴加少量AgNO3溶液
白色沉淀
猜想②正确
Ⅱ
重新取样,滴加足量Na2CO3溶液
▲
猜想②正确
白色沉淀
猜想③正确
①对方案Ⅰ的结论进行评价:。
②表格空白处的实验现象是:。
(3)、【表达交流】为确定猜想②是否正确,还可以选择的试剂有 _________。A、紫色石蕊试液 B、铜片 C、铁锈30. 某混合气体可能有CO2、CO、H2中的一种或几种,某学习小组的同学为了探究气体的组成,设计了如下装置进行实验(夹持装置已省略)。实验中出现的现象及在反应前后测量C、D装置的质量(各步反应均完全)记录如下表: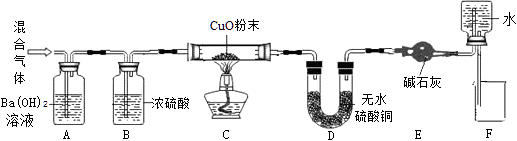
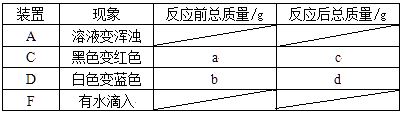
试分析回答下列问题:
(1)、请写出A装置中反应的化学方程式。(2)、能证明原混合气体中有氢气存在的实验现象应该是。(3)、若混合气体中含有CO,则a、b、c、d之间满足的关系式为。31. 某兴趣小组在实验室相对封闭的装置内燃烧某种含碳、氢、氧元素的垃圾,对产生的废气成分(不考虑气态有机物)按如图所示的装置进行检验。【实验研究】
拉动注射器,让废气依次通过装置。
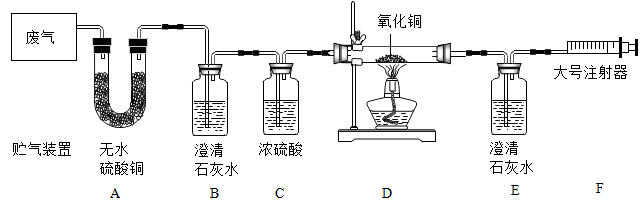
【实验分析】
(1)、能证明废气中有水蒸气存在的现象是;(2)、F处的大号注射器,可以引导气体流向,其另一个主要作用是;(3)、【反思评价】小金认为,仅根据E中澄清石灰水变浑浊,无法确定一氧化碳的存在,其理由是;(4)、小金根据D中的粉末由黑色变为红色,得出废气中存在一氧化碳。小丽认为该结论不够严密,若废气中存在氢气也会出现该现象。要使上述结论更加严密,还应添加的一个实验装置及位置是。【实验结果】经检验,废气中存在CO2、CO、H2O。
32. 已知木炭还原氧化铜实验中发生的主要反应:C+2CuO 2Cu+CO2↑。化学兴趣小组对该实验产物(假设反应物已完全反应)作如下探究:(1)、探究一:检验产物的成分【提出问题】实验产物是暗红色固体,很难观察到紫红色固体。暗红色固体是什么?
【查阅资料】氧化亚铜(Cu2O)为红色固体;Cu2O+H2SO4═CuSO4+Cu+H2O。
【猜想与假设】暗红色固体除铜外还可能含有Cu2O。
【设计实验】取少量暗红色固体,加入稀硫酸,如果观察到现象: , 说明猜想正确
(2)、探究二:测定产物中Cu2O的含量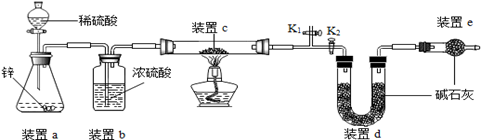
原理:Cu2O+H2 2Cu+H2O,称取一定质量的固体样品,用如图装置进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠混合物),通过测定反应前后装置d的质量达到实验目的。
a.装置a中用稀硫酸而不用稀盐酸,原因是;
b.若不加装置e,实验结果会偏高,原因是;
c.点燃酒精灯前涉及的部分操作如下,正确的顺序是
①打开K2 , 关闭K1 ②检查装置的气密性 ③关闭K2 , 打开K1 , 通氢气一段时间
四、解答题
-
33.
有一包白色固体,可能由硫酸钾、氢氧化钾、碳酸钙、氯化钡中的一种或几种物质组成,为探究该白色固体的组成,某小组取适量样品按下列流程进行实验,请回答下列问题。
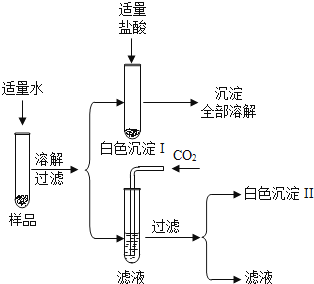
(1)白色沉淀Ⅰ与稀盐酸反应的化学方程式。
(2)白色沉淀Ⅱ的化学式。
(3)原白色固体中含有的物质。
34. 在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验:①将试管中反应的剩余物过滤并多次用蒸馏水洗涤,得到滤液和滤渣。
②向滤渣中滴加稀盐酸,无明显的现象。
③将滤渣干燥后称量,质量为0.5g。
④向滤液中加入10%的Na2CO3溶液,获得了相关的数据,并绘制成如下图所示的图像。
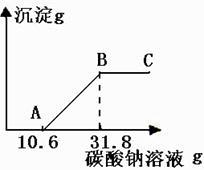
请根据小明的实验过程回答下列问题。(假设石灰石中的其余杂质不与稀盐酸反应)
(1)、第②步中小明向滤渣中加入稀盐酸的目的是 。(2)、在Na2CO3溶液加到图像中显示的C点时,溶液中所含的溶质为 。(3)、根据图像及相关的数据可求得石灰石中碳酸钙的含量为多少?(4)、第①步中如果在过滤时没有用蒸馏水多次洗涤,则测得碳酸钙的含量将 。(选填“偏大”、“不变”或“偏小)35. 在一烧杯中盛有CaCl2和HCl的混合溶液100g,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入的Na2CO3溶液的质量关系图像如图所示。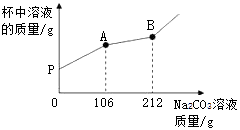 (1)、在实验过程中,其中出现冒气泡的是(填“PA”或“AB”)段。(2)、逐渐滴入碳酸钠溶液的过程中,杯中溶液的pH如何变化?(3)、原溶液中HCl的质量是多少g?(4)、当滴入Na2CO3溶液至图中B点时,通过计算求烧杯中(不饱和溶液)溶质的质量分数为多少?(计算结果精确到0.1%)36. 为探究铜及其化合物的性质, 进行如下实验:称取已部分被H,还原的氧化铜粉末(含Cu和CuO)7.2g置于烧杯中,向其中加入50g稀硫酸,充分反应后,再向烧杯中加入溶质质量分数为20%的NaOH溶液,烧杯内固体物质的质量与加入NaOH溶液的质量关系如图所示。请分析计算:
(1)、在实验过程中,其中出现冒气泡的是(填“PA”或“AB”)段。(2)、逐渐滴入碳酸钠溶液的过程中,杯中溶液的pH如何变化?(3)、原溶液中HCl的质量是多少g?(4)、当滴入Na2CO3溶液至图中B点时,通过计算求烧杯中(不饱和溶液)溶质的质量分数为多少?(计算结果精确到0.1%)36. 为探究铜及其化合物的性质, 进行如下实验:称取已部分被H,还原的氧化铜粉末(含Cu和CuO)7.2g置于烧杯中,向其中加入50g稀硫酸,充分反应后,再向烧杯中加入溶质质量分数为20%的NaOH溶液,烧杯内固体物质的质量与加入NaOH溶液的质量关系如图所示。请分析计算: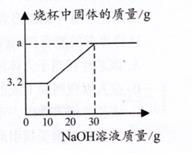 (1)、加完50克稀硫酸后溶液中的溶质为(写出化学式);(2)、Cu和CuO的混合物中,Cu元素和O元素的质量比为;(3)、a的值;(4)、实验所用稀硫酸中溶质的质量分数。37. 为探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液224.4克于烧杯中,在不断振荡的条件下,向其中逐滴滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示。经测定A中只含有一种溶质。根据题中有关信息和图像分析回答下列问题。
(1)、加完50克稀硫酸后溶液中的溶质为(写出化学式);(2)、Cu和CuO的混合物中,Cu元素和O元素的质量比为;(3)、a的值;(4)、实验所用稀硫酸中溶质的质量分数。37. 为探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液224.4克于烧杯中,在不断振荡的条件下,向其中逐滴滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示。经测定A中只含有一种溶质。根据题中有关信息和图像分析回答下列问题。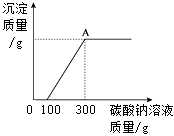 (1)、根据图像分析判断可知:
(1)、根据图像分析判断可知:原废液中的溶质成分有(填化学式)
(2)、图像上A点的纵坐标为多少?(3)、A点处溶液中溶质的质量分数是多少?