安徽省淮北市濉溪县2020-2021学年九年级上学期化学期末考试试卷
试卷更新日期:2021-09-29 类型:期末考试
一、单选题
-
1. 2020年春,“新冠病毒”肆虐,全国上下齐心协力、众志成城,坚决打赢“新冠肺炎”阻击战。下列行动中发生了化学变化的是( )A、分发口罩
 B、消毒杀菌
B、消毒杀菌  C、测量体温
C、测量体温  D、排查统计
D、排查统计  2. 李燕同学发现青色的生虾煮熟后颜色会变成红色,认为生虾外壳上的青色物质遇到某些物质发生了颜色的变化。就李燕同学的“看法”而言,应属于科学探究中的( )
2. 李燕同学发现青色的生虾煮熟后颜色会变成红色,认为生虾外壳上的青色物质遇到某些物质发生了颜色的变化。就李燕同学的“看法”而言,应属于科学探究中的( )
A、观察 B、实验 C、假设 D、做结论3. 下列客观事实的微观解释正确的是( )A、品红在水中扩散——分子间有空隙 B、原子不显电性——原子中没有带电微粒 C、物质的热胀冷缩——分子的大小改变 D、金刚石和石墨的物理性质不同——原子的排列方式不同4. 84消毒液是一种生活中常见的消毒剂,由于其消毒效果理想、价格低廉、使用方便,具有广谱、高效的杀菌特点而深受大家的欢迎,其主要成分是次氯酸钠(NaClO),其中氯元素的化合价为( )A、-1价 B、0价 C、+1价 D、+5价5. 在实验操作考查中,小明抽到的题目是“二氧化碳的制取、收集和验满”。下图是他的主要实验步骤,其中操作有误的是( )A、加入药品 B、收集气体
B、收集气体  C、检查装置气性
C、检查装置气性  D、验满
D、验满  6. 瑞德西韦是一种新型的抗病毒药物,其化学式为:C27H35N6O8P。下列说法正确的是( )A、瑞德西韦是一种混合物 B、瑞德西韦由27个碳原子、35个氢原子、6个氮原子、8个氧原子和1个磷原子构成 C、瑞德西韦完全燃烧的产物只有二氧化碳和水 D、瑞德西韦的相对分子质量是6027. 下列词语或俗语的有关化学原理解释中不合理的是( )A、釜底抽薪——燃烧需要可燃物 B、钻木取火——使可燃物的着火点升高 C、真金不怕火烧——金的化学性质不活泼 D、没有金刚钻,不揽瓷器活——金刚石硬度大8. 下列变化过程一定发生化学反应的是( )A、燃烧 B、爆炸 C、颜色发生了改变 D、状态发生了改变9. 下列关于物质的组成、结构、性质以及用途的总结中,正确的是( )A、在SO2、CO2两种物质中,都含有氧气 B、Cl、Cl-两种微粒的核内质子数相同,化学性质也相同 C、H2O2和H2O都是由氢、氧两种元素组成的物质,H2O2和H2O的化学性质一定相同 D、C、CO都能与灼热CuO反应生成铜,体现了C、CO都具有还原性10. 下列灭火措施中不恰当的是( )
6. 瑞德西韦是一种新型的抗病毒药物,其化学式为:C27H35N6O8P。下列说法正确的是( )A、瑞德西韦是一种混合物 B、瑞德西韦由27个碳原子、35个氢原子、6个氮原子、8个氧原子和1个磷原子构成 C、瑞德西韦完全燃烧的产物只有二氧化碳和水 D、瑞德西韦的相对分子质量是6027. 下列词语或俗语的有关化学原理解释中不合理的是( )A、釜底抽薪——燃烧需要可燃物 B、钻木取火——使可燃物的着火点升高 C、真金不怕火烧——金的化学性质不活泼 D、没有金刚钻,不揽瓷器活——金刚石硬度大8. 下列变化过程一定发生化学反应的是( )A、燃烧 B、爆炸 C、颜色发生了改变 D、状态发生了改变9. 下列关于物质的组成、结构、性质以及用途的总结中,正确的是( )A、在SO2、CO2两种物质中,都含有氧气 B、Cl、Cl-两种微粒的核内质子数相同,化学性质也相同 C、H2O2和H2O都是由氢、氧两种元素组成的物质,H2O2和H2O的化学性质一定相同 D、C、CO都能与灼热CuO反应生成铜,体现了C、CO都具有还原性10. 下列灭火措施中不恰当的是( )①炒菜时,锅里的油起火应采取的最佳灭火措施是端下油锅
②秸秆、柴草着火,用水泼灭
③熄灭酒精灯最好用嘴吹灭
④电器着火,最先应当切断电源,再用干粉灭火器灭火
⑤汽油着火,应该立即用水浇灭
⑥撒在实验桌上的酒精着火,应用湿抹布盖灭.
A、①③⑤ B、②④⑥ C、①③⑥ D、②③⑤11. 下列排列顺序错误的是()A、相对分子质量:二氧化碳>氮气>氢气 B、氯元素的化合价:KClO3>Cl2>HCl C、空气中组成物质的含量:氮气>氧气>稀有气体 D、地壳中元素含量:Al<Fe<Si12. 下图表示治理汽车尾气所涉及反应的微观过程。下列说法正确的是( ) A、图中单质的化学式为O2 B、该反应使有害气体转化为无害气体 C、该反应属于置换反应 D、该反应分子个数发生了改变,不符合质量守恒定律13. 下列实验操作能达到实验目的的是( )
A、图中单质的化学式为O2 B、该反应使有害气体转化为无害气体 C、该反应属于置换反应 D、该反应分子个数发生了改变,不符合质量守恒定律13. 下列实验操作能达到实验目的的是( )选项
实验目的
实验操作
A
除去CO2中的少量CO
点燃
B
除去CuSO4溶液中的少量FeSO4
加入足量铜粉
C
鉴别CO和CH4
分别点燃,在火焰上方罩一干冷烧杯
D
鉴别炭粉和CuO
观察颜色
A、A B、B C、C D、D14. 有X,Y,Z三种金属片,分别放入稀硫酸中,X,Z表面有气泡产生,Y没有明显现象X放入ZCln溶液,没有明显现象。判断这三种金属的活动性由强到弱的顺序是( )
A、X>Y>Z B、Z>X>Y C、X>Z>Y D、Y>X>Z15. 在一个密闭容器中放入W,G,H,P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:物质
W
G
H
P
反应前质量/g
18
1
2
32
反应后质量/g
待测
26
2
12
对该反应的认识正确的是( )
A、W待测值是13 B、该反应是分解反应 C、P是生成物 D、物质H是该反应的催化剂16. 探究铁生锈的条件,有利于寻找防止铁制品锈蚀的方法。下列对比实验设计与所探究的条件(蒸馏水经煮沸并迅速冷却),对应关系正确的是( )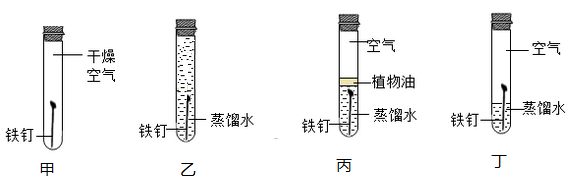 A、甲和乙:水 B、乙和丙:空气 C、甲和丙:空气 D、甲和丁:水
A、甲和乙:水 B、乙和丙:空气 C、甲和丙:空气 D、甲和丁:水二、填空题
-
17. 按要求用正确的化学符号回答。(1)、2个氮原子。(2)、3个碳酸根离子。(3)、氯化钠。(4)、保持水的化学性质的最小粒子是。(5)、+3价铝元素的氧化物。18. 如图中的①、②分别是氟元素、钙元素在元素周期表中的信息,A、B、C、D分别是四种粒子的结构示意图。请你回答:
 (1)、氟元素的原子序数为;钙元素的相对原子质量为。(2)、当D为原子时,X=。(3)、A,B,C,D中属于同种元素的粒子是和(填序号);(4)、A粒子的化学性质与B,C,D中哪一种粒子的化学性质相似(填序号);(5)、加钙牛奶中的“钙”是指(填“元素”或“原子”),19. 水对我们的生产和生活都是非常重要的:
(1)、氟元素的原子序数为;钙元素的相对原子质量为。(2)、当D为原子时,X=。(3)、A,B,C,D中属于同种元素的粒子是和(填序号);(4)、A粒子的化学性质与B,C,D中哪一种粒子的化学性质相似(填序号);(5)、加钙牛奶中的“钙”是指(填“元素”或“原子”),19. 水对我们的生产和生活都是非常重要的: (1)、图①所示电解水的实验中,往往向水中加入少量硫酸钠或氢氧化钠,目的是 , 试管(填“1”或“2”)中收集到的气体是氧气,试管1与试管2中收集到的气体体积比为 , 该反应的化学方程式为。(2)、某同学要净化收集到的雨水,自制了一个简易的净水器(如图②),其中活性炭的作用。在生活中,区分硬水和软水可用(填试剂名称),硬水软化的方法。(3)、我们应当珍惜每一滴水,下列做法不利于节约用水的是。
(1)、图①所示电解水的实验中,往往向水中加入少量硫酸钠或氢氧化钠,目的是 , 试管(填“1”或“2”)中收集到的气体是氧气,试管1与试管2中收集到的气体体积比为 , 该反应的化学方程式为。(2)、某同学要净化收集到的雨水,自制了一个简易的净水器(如图②),其中活性炭的作用。在生活中,区分硬水和软水可用(填试剂名称),硬水软化的方法。(3)、我们应当珍惜每一滴水,下列做法不利于节约用水的是。A 洗菜的水用来浇花
B 使用节水龙头
C 用不间断的水流冲洗碗筷
D 洗手擦肥皂时,关上水龙头
(4)、用水灭火时,将水喷成细雾状的主要原因是(填序号)。A 降低着火点 B 增大与可燃物接触面积 C 与空气中气体反应生成CO2
三、综合题
-
20. 实验室用如图所示装置进行相关实验,请回答问题。
 (1)、写出①的仪器名称。(2)、实验室制取氧气和二氧化碳均可选择的装置组合是。(填字母)(3)、加热混有二氧化锰的氯酸钾固体制取氧气的化学方程式是。(4)、A装置还可作为加热高锰酸钾制取氧气的发生装置则需对A装置的改进是。(5)、F装置可用于检验二氧化碳,瓶中液体是澄清石灰水,气体应从(填“a”或“b”)端通入,该反应的化学方程式为。21. 铁矿石是怎样炼成铁的呢?某活动小组在实验室模拟了铁矿石炼铁化学原理,如图所示。
(1)、写出①的仪器名称。(2)、实验室制取氧气和二氧化碳均可选择的装置组合是。(填字母)(3)、加热混有二氧化锰的氯酸钾固体制取氧气的化学方程式是。(4)、A装置还可作为加热高锰酸钾制取氧气的发生装置则需对A装置的改进是。(5)、F装置可用于检验二氧化碳,瓶中液体是澄清石灰水,气体应从(填“a”或“b”)端通入,该反应的化学方程式为。21. 铁矿石是怎样炼成铁的呢?某活动小组在实验室模拟了铁矿石炼铁化学原理,如图所示。 (1)、该活动小组将实验装置组装好后,设计了下列实验操作步骤:①给玻璃管加热;②停止加热;③通入一氧化碳气体;④停止通入一氧化碳气体。正确的操作步骤是(填序号);(2)、实验过程中,玻璃管中固体由色变成色,玻璃管中反应的化学方程式是 , 试管中出现的现象是;(3)、图中有一处明显不正确,请说明改进方法。22. 下列是初中化学中的三个实验,请按要求填空:
(1)、该活动小组将实验装置组装好后,设计了下列实验操作步骤:①给玻璃管加热;②停止加热;③通入一氧化碳气体;④停止通入一氧化碳气体。正确的操作步骤是(填序号);(2)、实验过程中,玻璃管中固体由色变成色,玻璃管中反应的化学方程式是 , 试管中出现的现象是;(3)、图中有一处明显不正确,请说明改进方法。22. 下列是初中化学中的三个实验,请按要求填空: (1)、A实验中红磷燃烧的化学方程式为 , 实验说明氧气的体积约占空气的 , 实验成功的关键是(填序号).
(1)、A实验中红磷燃烧的化学方程式为 , 实验说明氧气的体积约占空气的 , 实验成功的关键是(填序号).①装置气密性好; ②实验前夹紧止水夹; ③红磷过量或足量;
④冷却后再打开止水夹; ⑤要选用教室内的空气
(2)、B实验中,由铜片上的白磷燃烧而热水中的白磷没有燃烧可以得知,可燃物燃烧的条件之一是 .(3)、C实验中烧杯(填编号)中的溶液变红.23. M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动。(提出问题)M,铜、铝的金属活动性顺序是怎样的?
(1)、(猜想与假设)小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu。你的猜想是。(2)、(设计与实验)为了三种金属的活动性顺序,同学们取粗细相同的M丝,铝丝及相关溶液,进行了如图所示的实验:
观察到只有试管乙中发生明显变化。
(交流与表达)
同学们一致认为试管丙中也应该有明显变化,之所以出现这种情况的原因可能是。
(3)、于是同学们对实验进行了改进,把甲、丙中的铝丝打磨干净后又分别插入原试管中,结果甲、丙试管中都出现了明显变化,则丙试管中发生反应的化学方程式为。(解释与结论)通过以上实验,同学们得出了三种金属的活动性顺序
(4)、(评价与反思)实验结束后,同学们对实验过程进行了如下反思:①同学们经过讨论后认为该实验可以优化,去掉试管(填试管编号)中的实验,也可以得出正确的结论。
②除了上述实验外,还可以将(填一种物质)分别插入到硫酸铝、硫酸铜溶液中,根据实验现象进行判断。
24. (探究活动一)为探究催化剂的种类对氯酸钾分解速率的影响,甲同学设计如表对比实验:氯酸钾的质量
催化剂的种类
MnO2的质量
反应条件
收集45.0mLO2所需的时间(s)
Ⅰ
3.0g
MnO2
1.0g
混合加热
21
Ⅱ
xg
CuO
1.0g
混合加热
48
(1)、表中x的值应为;通过分析上表数据,可以得出的实验结论是:在相同的条件下,KClO3在MnO2作催化剂比CuO作催化剂的分解速率(选填“快”或“慢”)。(2)、(探究活动二)为探究双氧水浓度对过氧化氢分解速率的影响,乙同学设计以下实验:(进行实验)
室温下,选用50.0g不同溶质质量分数的双氧水(1%、2%和4%)分别与0.1g二氧化锰进行实验(如图1,固定夹持仪器略去)。
写出双氧水分解的化学方程式 , MnO2在H2O2分解前后其质量和没有发生改变。
(3)、按下图装置图1进行实验,在装药品前应检查该装置的气密性,具体做法是关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后则证明该装置气密性良好。 (4)、(数据处理)
(4)、(数据处理)乙同学进行实验后,获得的相关实验数据记录如表所示:
双氧水的质量
双氧水的浓度
MnO2的质量
温度
相同时间(10s)内产生O2体积(mL)
Ⅰ
50.0g
1%
0.1g
20℃
9
Ⅱ
50.0g
2%
0.1g
20℃
16
Ш
50.0g
4%
0.1g
20℃
31
①本实验中,测量O2体积的装置也可以选用如图2的哪套装置来代替(填编号)。
②分析上表数据,可以得出不同浓度的双氧水对过氧化氢分解速率影响的结论是:。
(5)、丙同学认为用图3装置进行实验,通过比较也能探究双氧水浓度对过氧化氢分解速率的影响。四、计算题
-
25. 鸡蛋壳的主要成分是碳酸钙,为了测定某鸡蛋壳中碳酸钙的含量,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入足量的稀盐酸90g,充分反应后,称得烧杯中物质的总质量为97.8g。(假设鸡蛋壳中的其他物质不与盐酸反应)(1)、产生二氧化碳气体g。(2)、计算10g该鸡蛋壳中碳酸钙的质量分数,要求写出完整的解题步骤。