山东省泰安市宁阳县十校2020-2021学年九年级上学期化学期中考试试卷
试卷更新日期:2021-09-16 类型:期中考试
一、单选题
-
1. 下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )A、
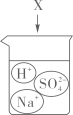 B、
B、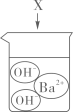 C、
C、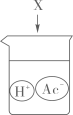 D、
D、 2. 下列关于海水晒盐原理的分析正确的是( )A、利用阳光照射,使海水升温得到食盐 B、利用海风降温析出食盐晶体 C、利用海水在阳光下发生分解反应制得食盐 D、利用阳光和风力使水分蒸发得到食盐3. 如图是X、Y、Z三种液体的对应近似pH,下列判断错误的是( )
2. 下列关于海水晒盐原理的分析正确的是( )A、利用阳光照射,使海水升温得到食盐 B、利用海风降温析出食盐晶体 C、利用海水在阳光下发生分解反应制得食盐 D、利用阳光和风力使水分蒸发得到食盐3. 如图是X、Y、Z三种液体的对应近似pH,下列判断错误的是( )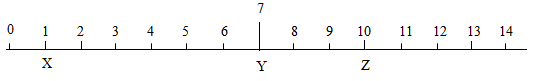 A、X显酸性 B、Y一定是水 C、Z可能是碳酸钠溶液 D、Z可使紫色石蕊试液变蓝4. 选择下列部分实验操作可完成两个实验,甲实验为除去粗盐中难溶性的杂质,乙实验为配制溶质质量分数一定的氯化钠溶液。下列说法正确的是( )
A、X显酸性 B、Y一定是水 C、Z可能是碳酸钠溶液 D、Z可使紫色石蕊试液变蓝4. 选择下列部分实验操作可完成两个实验,甲实验为除去粗盐中难溶性的杂质,乙实验为配制溶质质量分数一定的氯化钠溶液。下列说法正确的是( ) A、乙实验在操作③时,若俯视读数,会使所配制溶液的溶质质量分数偏小 B、甲实验三步骤中都要用到玻璃棒,且①和⑤中玻璃棒的作用是相同的 C、甲实验和乙实验都要用到的实验操作① D、甲实验在操作⑤时,将水全部蒸发后停止加热5. 下列选项中物质的俗名、化学式、类别、用途完全对应的是( )A、纯碱 Na2CO3 碱 制玻璃 B、生石灰 CaO 氧化物 补钙剂 C、食盐 NaCl 盐 除铁锈 D、火碱 NaOH 碱 制造橡胶6. 现有下列5种物质:①浓盐酸 ②生石灰 ③浓硫酸 ④烧碱,把他们长期露置在空气中,其中会发生化学变化且质量增加的是( )A、①、②、③ B、②、④ C、②、③、④ D、③、④、7. 下列实验操作正确且能达到实验目的是( )A、稀释浓硫酸
A、乙实验在操作③时,若俯视读数,会使所配制溶液的溶质质量分数偏小 B、甲实验三步骤中都要用到玻璃棒,且①和⑤中玻璃棒的作用是相同的 C、甲实验和乙实验都要用到的实验操作① D、甲实验在操作⑤时,将水全部蒸发后停止加热5. 下列选项中物质的俗名、化学式、类别、用途完全对应的是( )A、纯碱 Na2CO3 碱 制玻璃 B、生石灰 CaO 氧化物 补钙剂 C、食盐 NaCl 盐 除铁锈 D、火碱 NaOH 碱 制造橡胶6. 现有下列5种物质:①浓盐酸 ②生石灰 ③浓硫酸 ④烧碱,把他们长期露置在空气中,其中会发生化学变化且质量增加的是( )A、①、②、③ B、②、④ C、②、③、④ D、③、④、7. 下列实验操作正确且能达到实验目的是( )A、稀释浓硫酸 B、测定溶液pH
B、测定溶液pH  C、除去CO2中的CO
C、除去CO2中的CO  D、称量5.2g氧化铜
D、称量5.2g氧化铜  8. 下列做法不是利用中和反应原理的是( )A、用食醋除去水垢中的氢氧化镁 B、用含碳酸氢钠的发酵粉烘焙糕点 C、用含氢氧化铝的药物治疗胃酸过多 D、用氨水(NH3・H2O)处理工厂污水中的硫酸9. 如图所示实验,将稀盐酸滴到含有酚酞试液的氢氧化钠溶液中,直至最终烧杯内溶液呈现无色.则下列说法正确的是( )
8. 下列做法不是利用中和反应原理的是( )A、用食醋除去水垢中的氢氧化镁 B、用含碳酸氢钠的发酵粉烘焙糕点 C、用含氢氧化铝的药物治疗胃酸过多 D、用氨水(NH3・H2O)处理工厂污水中的硫酸9. 如图所示实验,将稀盐酸滴到含有酚酞试液的氢氧化钠溶液中,直至最终烧杯内溶液呈现无色.则下列说法正确的是( ) A、酚酞使氢氧化钠溶液变红色 B、溶液中所有物质均以离子形式存在 C、烧杯内显示无色,说明溶液中一定存在大量H+ D、烧杯内显示无色,说明溶液中溶质一定有氯化钠,可能有氯化氢10. 物质的性质决定其用途。下列物质的用途与性质对应关系错误的是( )A、氢氧化钙可用来改良酸性土壤——氢氧化钙溶液呈碱性 B、氮气常用作保护气——氮气化学性质稳定 C、固体二氧化碳可用人工降雨——二氧化碳能与碱反应 D、氧化钙可做食品干燥剂——氧化钙能与水反应11. 如图所示:装置气密性良好,广口瓶内装有某种固体,向其中滴加某种液体后U型管内液面a低于b,不符合上述实验现象的一组试剂是( )
A、酚酞使氢氧化钠溶液变红色 B、溶液中所有物质均以离子形式存在 C、烧杯内显示无色,说明溶液中一定存在大量H+ D、烧杯内显示无色,说明溶液中溶质一定有氯化钠,可能有氯化氢10. 物质的性质决定其用途。下列物质的用途与性质对应关系错误的是( )A、氢氧化钙可用来改良酸性土壤——氢氧化钙溶液呈碱性 B、氮气常用作保护气——氮气化学性质稳定 C、固体二氧化碳可用人工降雨——二氧化碳能与碱反应 D、氧化钙可做食品干燥剂——氧化钙能与水反应11. 如图所示:装置气密性良好,广口瓶内装有某种固体,向其中滴加某种液体后U型管内液面a低于b,不符合上述实验现象的一组试剂是( ) A、生石灰和水 B、铁粉和稀盐酸 C、硝酸铵和水 D、纯碱和稀盐酸12. 下列物质间的转化,不能由一步实现的是( )A、O2→ H2O B、CuO→ CuSO4 C、Fe(OH)3 →FeCl3 D、CaCO3→Ca(OH)213. 只用一种试剂就可将Ba(OH)2 稀硫酸 KOH三种溶液鉴别出来的是( )A、K2CO3溶液 B、NaCl溶液 C、石蕊试液 D、酚酞试液14. 下列叙述正确的是( )A、盐酸能使紫色石蕊试液变蓝 B、浓硫酸露置于空气中,溶质质量分数会变大 C、打开盛浓盐酸的试剂瓶,瓶口会产生白雾 D、露置于空气中的固体氢氧化钠,其成分不会发生变化15. 下列实验设计或结论合理的是( )A、向某固体滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐 B、除去MgCl2溶液中混有的少量CuCl2 , 加入适量的Mg(OH)2充分搅拌后过滤 C、CO32-、Na+、NO3-、K+ 四种离子可在pH=12的溶液中大量共存 D、熟石灰、烧碱、纯碱都是碱16. 以下是四位同学对生活中的现象进行探究后的结果的表述,其中错误的是( )A、“纯碱”的水溶液能使无色酚酞变红 B、可用纯碱代替洗涤灵洗涤餐具表面的油污 C、用纯碱可除去表面团发酵产生的酸 D、用酚酞试液检验氢氧化钠是否变质17. 某化学兴趣小组对A、B、C、D四种未知溶液的成分进行了检验,检验结果见下表。其中检验结果错误的是( )
A、生石灰和水 B、铁粉和稀盐酸 C、硝酸铵和水 D、纯碱和稀盐酸12. 下列物质间的转化,不能由一步实现的是( )A、O2→ H2O B、CuO→ CuSO4 C、Fe(OH)3 →FeCl3 D、CaCO3→Ca(OH)213. 只用一种试剂就可将Ba(OH)2 稀硫酸 KOH三种溶液鉴别出来的是( )A、K2CO3溶液 B、NaCl溶液 C、石蕊试液 D、酚酞试液14. 下列叙述正确的是( )A、盐酸能使紫色石蕊试液变蓝 B、浓硫酸露置于空气中,溶质质量分数会变大 C、打开盛浓盐酸的试剂瓶,瓶口会产生白雾 D、露置于空气中的固体氢氧化钠,其成分不会发生变化15. 下列实验设计或结论合理的是( )A、向某固体滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐 B、除去MgCl2溶液中混有的少量CuCl2 , 加入适量的Mg(OH)2充分搅拌后过滤 C、CO32-、Na+、NO3-、K+ 四种离子可在pH=12的溶液中大量共存 D、熟石灰、烧碱、纯碱都是碱16. 以下是四位同学对生活中的现象进行探究后的结果的表述,其中错误的是( )A、“纯碱”的水溶液能使无色酚酞变红 B、可用纯碱代替洗涤灵洗涤餐具表面的油污 C、用纯碱可除去表面团发酵产生的酸 D、用酚酞试液检验氢氧化钠是否变质17. 某化学兴趣小组对A、B、C、D四种未知溶液的成分进行了检验,检验结果见下表。其中检验结果错误的是( )组别
溶液中检验出的离子
A
K+、Na+、OH-、
B
Ba2+、Na+、Cl-、OH-
C
Cu2+、Mg2+、 、Cl-
D
H+、 、 、
A、A B、B C、C D、D18. 以下推理正确的是( )A、酸中都含有氢元素,所以含有氢元素的化合物一定是酸 B、碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定呈碱性 C、中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 D、酸溶液能使石蕊试液变红,所以能使石蕊试液变红的溶液一定是酸的溶液19. 除去下列各物质中混有的少量杂质,所用试剂和操作方法均正确的是( )物质
杂质
所用试剂和操作方法
A
Na2CO3溶液
Na2SO4溶液
加入过量的Ba(NO3)2溶液,过滤
B
H2
HCl
通过足量的NaOH溶液、浓硫酸
C
NaCl固体
细沙
加入足量的水溶解,过滤
D
铁粉
Fe2O3
加入适量的稀盐酸,过滤、洗涤、干燥
A、A B、B C、C D、D20. 如图所示的图象能反映相对应实验的是( ) A、①高温煅烧一定质量的石灰石 B、②用相同质量、相同溶质质量分数的过氧化氢溶液分别制取氧气 C、③向一定体积的稀盐酸中逐滴加入氢氧化钠溶液 D、④某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
A、①高温煅烧一定质量的石灰石 B、②用相同质量、相同溶质质量分数的过氧化氢溶液分别制取氧气 C、③向一定体积的稀盐酸中逐滴加入氢氧化钠溶液 D、④某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体二、填空题
-
21. 从H、O、C、Na、Cl、Ca六种元素中选择一种或多种按要求填写下列物质的化学式:(1)、可用作馒头膨松剂的是;(2)、可用作建筑材料的盐是;(3)、可用于金属除锈的酸是;(4)、可用于改良酸性土壤的碱是;(5)、可作干燥剂的氧化物是;22. 归纳总结是学习化学的重要方法,小明同学用图l总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)。
 (1)、为了验证反应①,小明将无色酚嗽试液滴入NaOH液中,溶液变成色。(2)、依据反应②说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:(3)、小明用微观示意图(图2)来说明反应③的发生,用化学反
(1)、为了验证反应①,小明将无色酚嗽试液滴入NaOH液中,溶液变成色。(2)、依据反应②说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:(3)、小明用微观示意图(图2)来说明反应③的发生,用化学反应方程式表示为:;
从该图可以看出,反应前后没有发生变化的微观粒子有;
(4)、为了验证反应④能够发生,你选择的物质是。A.Na2CO3 B HCl C CuSO4 D NaCl
三、综合题
-
23. 在图中化学反应的溶液颜色变化体现了“魔法世界、魅力化学”,请回答:
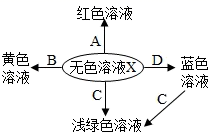 (1)、X是(填“酸”、“碱”或“盐”),试剂A的名称为。(2)、若X是稀硫酸,B是氧化物,则B的化学式为。(3)、若X是稀盐酸,C是单质,则C的名称为;X与C反应的化学方程式为。(4)、若X是稀硫酸,D是碱,则X与D反应的化学方程式为。24. 化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(其中部分操作和条件已略去),请回答相关问题:
(1)、X是(填“酸”、“碱”或“盐”),试剂A的名称为。(2)、若X是稀硫酸,B是氧化物,则B的化学式为。(3)、若X是稀盐酸,C是单质,则C的名称为;X与C反应的化学方程式为。(4)、若X是稀硫酸,D是碱,则X与D反应的化学方程式为。24. 化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(其中部分操作和条件已略去),请回答相关问题: (1)、提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。 粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序为(填字母序号);
(1)、提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。 粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序为(填字母序号);a、稍过量的Na2CO3溶液 b、稍过量的BaCl2溶液 c、稍过量的NaOH溶液
(2)、母液中有MgCl2 , 却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是;(3)、步骤Ⅱ中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,这样做的目的是 , 写出该反应的化学方程式;(4)、步骤Ⅳ中验证母液中MgCl2已完全转化为Mg(OH)2沉淀的方法是25. 某化学学习小组的同学围绕“澄清石灰水与碳酸钠溶液的反应”展开了如下探究活动。(1)、该反应的化学方程式为。(2)、反应后溶液中的溶质是什么?同学们一致认为有以下三种情况:①氢氧化钠和氢氧化钙;
②氢氧化钠和碳酸钠;
③。
(3)、小新取少量溶液于试管中,滴加过量稀盐酸,发现无气泡产生,说明情况(填序号)是不可能的。(4)、为了进一步确定溶液的成分,同学们设计了如下实验方案:(实验步骤) 。
(5)、(实验现象)。(6)、(实验结论)情况①正确小红选择了另外一种不同类别的物质(填化学式),也得到了同样的结论。
四、计算题
-
26. 某化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,进行了如下实验:取25.0g洗净、粉碎后的鸡蛋壳样品放于烧杯中,向烧杯中滴加稀盐酸(整个过程不考虑盐酸的挥发和气体的溶解),实验测得烧杯中剩余物质的质量与加入盐酸的质量之间的关系如图所示

求:
(1)、产生CO2的总质量为g。(2)、鸡蛋壳中碳酸钙的质量分数。