浙江省嘉兴市六校联盟2020-2021学年九年级上学期科学期中素质检测试卷(到第3章第3节)
试卷更新日期:2021-09-10 类型:期中考试
一、选择题(本大题共30分,每小题2分,每小题只有一个选项符合题意)
-
1. 出行是人们工作、生活必不可少的环节,出行的工具多种多样,使用的能源也不尽相同。燃油汽车所消耗能量的类型是( )A、生物能 B、电能 C、太阳能 D、化学能2. 科学离不开实验和观察,以下实验操作不正确的是( )A、检查气密性
 B、测定溶液的pH
B、测定溶液的pH  C、蒸发食盐溶液
C、蒸发食盐溶液  D、稀释浓硫酸
D、稀释浓硫酸  3. 下列化学方程式书写正确的是( )A、BaCO3+2HCl=BaCl2+H2O+CO2↑ B、Cu+2AgCl=CuCl2+2Ag C、Ca(NO3)2+BaCl2=Ba(NO3)2+CaCl2 D、CuO+H2O=Cu(OH)24. 下列物质能在pH=13的无色溶液中大量共存的是( )A、NaNO3、NaCl、 KNO3、(NH4)2SO4 B、H2SO4、HCl、 AgNO3、Na2SO4 C、KMnO4、CuCl2、Fe2(SO4)3、 NaNO3 D、K2SO4、NaCl、 K2CO3、NaOH5. 加油机在给战斗机加油过程中,若战斗机高度、速度不变,则战斗机的( )A、动能增加,势能增加,机械能增加 B、动能不变,势能不变,机械能不变 C、动能减小,势能不变,机械能减小 D、动能增加,势能减小,机械能不变6. 逻辑推理是化学学习中常用的思维方法,下列推理正确的是 ( )A、化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 B、金属氧化物和酸反应生成盐和水,则生成盐和水的反应一定是金属氧化物和酸反应 C、单质中只含有一种元素,所以只含有一种元素的物质一定是单质 D、活泼金属与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属7. 一辆满载浓硫酸的槽罐车在路上因车祸翻倒,浓硫酸大量泄漏,为了不污染旁边的水源,下列采取的措施适宜的是( )A、用水冲洗泄漏的浓硫酸 B、将熟石灰撒在泄漏出的浓硫酸上 C、将氯化钡撒在泄漏出的浓硫酸上 D、用土将泄漏的浓硫酸掩埋8. 小乐完成了图示甲、乙实验后,依次将反应后的溶液缓慢倒入同一洁净的废液缸中,观察到废液缸中先有气泡产生,然后又出现白色沉淀。则下列说法中,正确的是( )
3. 下列化学方程式书写正确的是( )A、BaCO3+2HCl=BaCl2+H2O+CO2↑ B、Cu+2AgCl=CuCl2+2Ag C、Ca(NO3)2+BaCl2=Ba(NO3)2+CaCl2 D、CuO+H2O=Cu(OH)24. 下列物质能在pH=13的无色溶液中大量共存的是( )A、NaNO3、NaCl、 KNO3、(NH4)2SO4 B、H2SO4、HCl、 AgNO3、Na2SO4 C、KMnO4、CuCl2、Fe2(SO4)3、 NaNO3 D、K2SO4、NaCl、 K2CO3、NaOH5. 加油机在给战斗机加油过程中,若战斗机高度、速度不变,则战斗机的( )A、动能增加,势能增加,机械能增加 B、动能不变,势能不变,机械能不变 C、动能减小,势能不变,机械能减小 D、动能增加,势能减小,机械能不变6. 逻辑推理是化学学习中常用的思维方法,下列推理正确的是 ( )A、化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 B、金属氧化物和酸反应生成盐和水,则生成盐和水的反应一定是金属氧化物和酸反应 C、单质中只含有一种元素,所以只含有一种元素的物质一定是单质 D、活泼金属与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属7. 一辆满载浓硫酸的槽罐车在路上因车祸翻倒,浓硫酸大量泄漏,为了不污染旁边的水源,下列采取的措施适宜的是( )A、用水冲洗泄漏的浓硫酸 B、将熟石灰撒在泄漏出的浓硫酸上 C、将氯化钡撒在泄漏出的浓硫酸上 D、用土将泄漏的浓硫酸掩埋8. 小乐完成了图示甲、乙实验后,依次将反应后的溶液缓慢倒入同一洁净的废液缸中,观察到废液缸中先有气泡产生,然后又出现白色沉淀。则下列说法中,正确的是( ) A、甲实验结束后,试管中的溶液含稀盐酸和CaCl2 B、乙实验结束后,试管中的溶液含稀盐酸和NaCl C、最终,废液缸中一定含NaCl,CaCl2两种溶质 D、最终,废液缸中一定含NaCl,Na2CO3两种溶质9. 现有甲、乙、丙三种金属,将甲、乙两种金属分别放入相同浓度的稀硫酸中,乙表面产生气泡,甲表面无明显现象;将甲、丙分别放入AgNO3溶液中,甲表面有银析出,丙表面无明显现象.下列对甲、乙、丙三种金属活动性顺序的排列正确的是( )A、甲>乙>丙 B、乙>丙>甲 C、乙>甲>丙 D、丙>甲>乙10. 某同学欲检验一瓶NaOH溶液是否变质,设计了下列三种检验方法:①加少量澄清的石灰水,有沉淀生成,则氢氧化钠溶液已变质;②加入少量稀硫酸,有气泡产生,则氢氧化钠溶液已变质;③加少量BaCl2溶液,有沉淀生成,则氢氧化钠溶液已变质。其中方法和结论都正确的是( )A、①② B、②③ C、①③ D、①②③11.
A、甲实验结束后,试管中的溶液含稀盐酸和CaCl2 B、乙实验结束后,试管中的溶液含稀盐酸和NaCl C、最终,废液缸中一定含NaCl,CaCl2两种溶质 D、最终,废液缸中一定含NaCl,Na2CO3两种溶质9. 现有甲、乙、丙三种金属,将甲、乙两种金属分别放入相同浓度的稀硫酸中,乙表面产生气泡,甲表面无明显现象;将甲、丙分别放入AgNO3溶液中,甲表面有银析出,丙表面无明显现象.下列对甲、乙、丙三种金属活动性顺序的排列正确的是( )A、甲>乙>丙 B、乙>丙>甲 C、乙>甲>丙 D、丙>甲>乙10. 某同学欲检验一瓶NaOH溶液是否变质,设计了下列三种检验方法:①加少量澄清的石灰水,有沉淀生成,则氢氧化钠溶液已变质;②加入少量稀硫酸,有气泡产生,则氢氧化钠溶液已变质;③加少量BaCl2溶液,有沉淀生成,则氢氧化钠溶液已变质。其中方法和结论都正确的是( )A、①② B、②③ C、①③ D、①②③11.如图,甲和乙分别是氢气和一氧化碳还原氧化铜的实验,下列有关说法正确的是( )
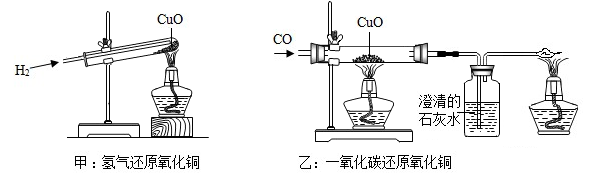 A、甲实验试管口向下倾斜可防止氢气逸出 B、乙实验只能通过澄清石灰水是否变浑浊判断反应是否发生 C、甲、乙两实验中,都应先通入气体,再使试管、玻璃管均匀受热,以防止发生爆炸 D、甲、乙两实验中,氢气和一氧化碳都将氧化铜变成游离态的铜,都发生了置换反应12. 将下列试剂分别加入KOH溶液、饱和石灰水和稀H2SO4中,能出现三种不同现象的是 ( )A、紫色石蕊试液 B、Na2CO3溶液 C、CuCl2溶液 D、NaCl溶液13. 过山车是一项惊险刺激的游戏项目,下列关于过山车的机械能说法正确的是( )A、刚开始过山车匀速被拉升时,机械能不变 B、过山车向下俯冲时,重力势能转化为动能 C、通过环形轨道最高点时,重力势能最大,动能为0 D、过山车在运行过程中机械能守恒14. 等质量的镁和铁分别放置在两只烧杯中,向其中分别逐滴加入质量分数相等的稀硫酸到过量。图中能正确反映其过程的是( )A、
A、甲实验试管口向下倾斜可防止氢气逸出 B、乙实验只能通过澄清石灰水是否变浑浊判断反应是否发生 C、甲、乙两实验中,都应先通入气体,再使试管、玻璃管均匀受热,以防止发生爆炸 D、甲、乙两实验中,氢气和一氧化碳都将氧化铜变成游离态的铜,都发生了置换反应12. 将下列试剂分别加入KOH溶液、饱和石灰水和稀H2SO4中,能出现三种不同现象的是 ( )A、紫色石蕊试液 B、Na2CO3溶液 C、CuCl2溶液 D、NaCl溶液13. 过山车是一项惊险刺激的游戏项目,下列关于过山车的机械能说法正确的是( )A、刚开始过山车匀速被拉升时,机械能不变 B、过山车向下俯冲时,重力势能转化为动能 C、通过环形轨道最高点时,重力势能最大,动能为0 D、过山车在运行过程中机械能守恒14. 等质量的镁和铁分别放置在两只烧杯中,向其中分别逐滴加入质量分数相等的稀硫酸到过量。图中能正确反映其过程的是( )A、 B、
B、 C、
C、 D、
D、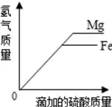 15. 粗盐中常含有MgCl2、CaCl2、Na2SO4及泥沙等杂质,常用下面的流程进行提纯。下列说法正确的是( )
15. 粗盐中常含有MgCl2、CaCl2、Na2SO4及泥沙等杂质,常用下面的流程进行提纯。下列说法正确的是( ) A、加入试剂a的顺序可以是过量的NaOH溶液、Na2CO3溶液,BaCl2溶液 B、加入试剂a后,将混合物过滤,得到的沉淀中除泥沙外还含有3种不溶物 C、向溶液Ⅰ中加入的盐酸也可以是过量的 D、操作b的名称为过滤
A、加入试剂a的顺序可以是过量的NaOH溶液、Na2CO3溶液,BaCl2溶液 B、加入试剂a后,将混合物过滤,得到的沉淀中除泥沙外还含有3种不溶物 C、向溶液Ⅰ中加入的盐酸也可以是过量的 D、操作b的名称为过滤二、填空题(16.17.18题每空1分,其余2分,共25分)
-
16. 下列变化中,
①雕琢玉石 ②食物变馊 ③千里冰封,万里雪飘 ④野火烧不尽,春风吹又生
⑤夜来风雨声,花落知多少 ⑥钢铁生锈
(1)、属于化学变化的是(填序号,下同),
(2)、属于物理变化的是。
17. 盐酸和硫酸是两种重要的酸。(1)、浓硫酸使木棒或棉花变黑,体现了浓硫酸的性。(2)、如图为实验室稀释浓硫酸的操作示意图,其中烧杯中的液体A是。(填“浓硫酸”或“水”)
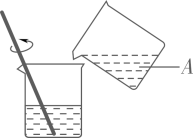 (3)、打开浓盐酸试剂瓶的瓶盖,瓶口出现白雾,这是因为浓盐酸具有性。18. 测定人体体液的pH 可以帮助我们了解身体状况,如图是小茗同学体检报告单截图,看图后回答问题:
(3)、打开浓盐酸试剂瓶的瓶盖,瓶口出现白雾,这是因为浓盐酸具有性。18. 测定人体体液的pH 可以帮助我们了解身体状况,如图是小茗同学体检报告单截图,看图后回答问题:项目
检测值
正常pH范围
血浆
7.4
7.35-7.45
胃液
0.8
0.9-1.5
胆汁
7.21
7.1-7.3
胰液
7.8
7.5-8.0
(1)、小茗同学的指标中有一项出现异常,医生除了给他开了药物之外,还提醒他注意饮食,下列食物(近似pH如下) 中适合该同学得有 。A、番茄(4.0--4.4) B、苹果(2.9--3.3) C、牛奶(6.3-6.6) D、豆浆(7.4--7.9)(2)、小茗同学想到在实验室中可用pH试纸测量溶液酸碱度,于是他从家里找来苹果,并用湿润的pH试纸进行了测量,那么测得的pH比实际结果 。A、偏大 B、偏小 C、不变 D、无法判断19. 氢氧化钠是一种重要的化工基础原料,广泛地应用于造纸、纺织、石油化工、印染等行业。(1)、氢氧化钠固体敞口放置容易变质,写出氢氧化钠变质的化学方程式。(2)、课堂上老师做了其中一个实验,在试管中加入2~3mL氯化铁溶液,然后滴加1~2mL氢氧化钠溶液,观察到的实验现象是 , 反应的化学方程式为.20. 有四种物质的溶液:①Ba(OH)2、②Na2SO4、③HNO3、④FeCl3 , 不用其他试剂就可将它们逐一鉴别出来,其鉴别顺序是21. 有一包白色粉末,可能由硫酸铜、硝酸钡、氢氧化钠、碳酸钠、氯化钾、碳酸钙中的一种或几种物质混合而成。为探究其组成,进行如下实验。请回答:
白色粉末中一定存在的物质有 , 一定不存在的物质。
22. 甲、乙是两个完全相同的网球。如图所示,在同一高度同时以大小相等的速度,将甲球竖直向下抛出、乙球竖直向上抛出,不计空气阻力。抛出时两球机械能(选填“相等”或“不相等”);落地前的运动过程中,甲球的动能(选填“增大”“减小”或“不变”),乙球的机械能(选填“增大”“先增大后减小”“减小”或“不变”)。
三、实验探究题(每空2分,共26分)
-
23. 小强同学用三支试管,分别取适量的稀盐酸、澄清石灰水、碳酸钠溶液,进行相关实验探究.
步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,
说明Na2CO3溶液显性;
步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含 .
(选填答案:A、稀盐酸 B、澄清石灰水 C、碳酸钠溶液)
【实验猜想】步骤3所得滤液中溶质可能为:
①NaCl Na2CO3; ②NaCl CaCl2和NaOH; ③NaCl Na2CO3和NaOH; ④…
【实验验证】(提示:CaCl2溶液显中性)
实验操作
实验现象
实验结论
取少量滤液于试管中,加入足量CaCl2溶液
猜想③成立
【反思评价】有同学提出CaCl2溶液改为稀盐酸,若观察到有气泡产生且红色消失,则证明猜想③成立。小刚同学认为不正确,其理由是:。
24. 小苏同学的物理兴趣小组准备探究“弹簧弹性势能的大小与什么因素有关”。他们猜想:弹簧弹性势能可能与弹簧长度变化量、弹簧螺纹圈直径、弹簧的材料等因素有关。他们的实验装置如图所示,把弹簧放在水平面上,其左端固定在墙上,AO等于弹簧原长,水平面O点左侧光滑,右侧粗糙。将物体M从O点压缩弹簧到P点,然后由静止释放,当物体M运动到O点与弹簧分开,最终运动到Q点静止。请补充完成他们的探究过程: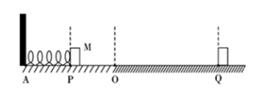 (1)、弹簧弹性势能的大小是通过来衡量的。(2)、探究弹簧弹性势能与弹簧长度变化量的关系,应该选用(选填“相同”或“不同”)弹簧进行实验,并先后改变之间的距离,测出OQ的距离,重复实验,测量多组数据并记录。(3)、小苏的实验小组经过多次实验得出了结论。在上面的实验中,他们运用到了转换法和两种物理思想方法。25. 已知某混合气体由H2、CO和CO2三种气体组成。为验证该混合气体成分,科学研究小组的同学经过讨论,设计了如图甲所示的实验方案。
(1)、弹簧弹性势能的大小是通过来衡量的。(2)、探究弹簧弹性势能与弹簧长度变化量的关系,应该选用(选填“相同”或“不同”)弹簧进行实验,并先后改变之间的距离,测出OQ的距离,重复实验,测量多组数据并记录。(3)、小苏的实验小组经过多次实验得出了结论。在上面的实验中,他们运用到了转换法和两种物理思想方法。25. 已知某混合气体由H2、CO和CO2三种气体组成。为验证该混合气体成分,科学研究小组的同学经过讨论,设计了如图甲所示的实验方案。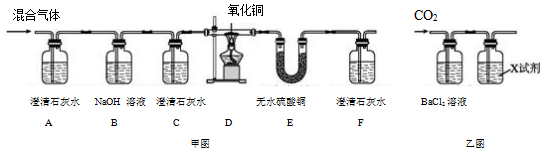
根据方案回答下列问题:
(1)、装置A、C、F装的都是澄清石灰水,但它们的作用各不相同。装置C在实验中的作用是;装置F在实验中的作用是。(2)、仅根据D装置中黑色粉末变红这一现象,能否证明混合气体中一定存在H2?请判断并说明理由。
(3)、图甲方案B装置可用来吸收但没有现象。为证明和能发生反应,小丁又设计了图乙所示的方案。则图乙方案中所加试剂X应该是和的混合溶液。四、计算题(5+7+7,共19分)
-
26. 实验室有一瓶未知浓度的盐酸,小华为测定该盐酸中溶质的质量分数,取10g溶质的质量分数为16%的氢氧化钠溶液,逐滴滴加该盐酸至恰好完全反应,共消耗盐酸20g,请计算:(1)、10g氢氧化钠溶液中溶质的质量为 g.(2)、该盐酸中溶质的质量分数.27. 用“侯氏联合制碱法”制取的纯碱中常含有少量的氯化钠.化学实验小组同学为测定某厂生产的纯碱中碳酸钠的含量,称取12g样品放入烧杯中并滴加稀盐酸,当盐酸滴加至73g时,气泡不再冒出,此时称得烧杯内溶液的总质量为80.6g.
试计算:
(1)、产生二氧化碳气体的质量是g.(2)、求该纯碱样品中氯化钠的质量。(3)、求反应所得溶液中溶质质量分数。(计算结果精确到0.1%)28. 科学兴趣小组的同学为了测定某铜铁合金的组成,取20克样品于烧杯中,向其中分4次加入相同溶质质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量及剩余固体的质量记录如下表:实验序号
第一次
第二次
第三次
第四次
加入稀硫酸的质量(克)
20
20
20
20
充分反应后剩余固体的质量(克)
17.2
14.4
12.0
m
请分析回答下列问题:
(1)、上述表格中m的值为。(2)、此样品中铁的质量分数为。(3)、所用稀硫酸中硫酸的质量分数是多少?