江苏省常州市溧阳市2020-2021学年九年级上学期化学期中考试试卷
试卷更新日期:2021-09-10 类型:期中考试
一、单选题
-
1. 下列典故中,主要体现化学变化的是( )A、火烧赤壁 B、刻舟求剑 C、司马光砸缸 D、铁杵磨成针2. 下列有关铁性质的叙述中,属于化学性质的是( )A、质软 B、能导电 C、银白色固体 D、能与食醋反应3. 下列实验操作正确的是( )A、
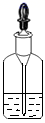 滴管用后放回原瓶
B、
滴管用后放回原瓶
B、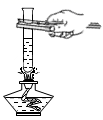 加热液体
C、
加热液体
C、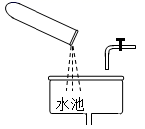 处理废弃药品
D、
处理废弃药品
D、 取用固体
4. 板栗是溧阳的土特产之一,素有“干果之王”的美称。板栗中富含淀粉、蛋白质、脂肪、维生素、及钙、铁、等多种营养成分。其中的“钙、铁、”是指( )A、单质 B、分子 C、元素 D、原子5. 室温时将少量干冰放入塑料袋中并密封,塑料袋会快速鼓起,其原因是( )
取用固体
4. 板栗是溧阳的土特产之一,素有“干果之王”的美称。板栗中富含淀粉、蛋白质、脂肪、维生素、及钙、铁、等多种营养成分。其中的“钙、铁、”是指( )A、单质 B、分子 C、元素 D、原子5. 室温时将少量干冰放入塑料袋中并密封,塑料袋会快速鼓起,其原因是( )
A、分子的体积变大 B、分子分解变成了原子 C、分子的间隔变大 D、分子由静止变为运动6. 下列实验现象描述中,错误的是( )A、铜绿和稀盐酸反应:溶液由绿色变成蓝色 B、灼烧蔗糖:固体先熔化后被烧焦 C、加热碳酸氢铵:固体消失 D、铁丝在氧气中燃烧:火星四射、生成黑色固体7. 下列对历史上几项重要化学研究成果的介绍错误的是( )A、中国科学家合成了结晶牛胰岛素 B、拉瓦锡发现了电子 C、门捷列夫发表了元素周期表 D、居里夫妇发现了钋和镭8. 下列物质中,由原子直接构成的是( )A、氮气 B、铜 C、水 D、氯化钠9. 下列说法中,正确的是( )A、不同元素之间的本质区别在于相对原子质量不同 B、由同种元素组成的物质一定是纯净物 C、缺铁元素严重时会得侏儒症 D、钙是人体中含量最多的金属元素10. 下列方法中,能鉴别空气、氧气、二氧化碳的是( )A、观察颜色 B、闻气味 C、分别加入石灰水 D、分别插入燃着的木条11. 下列说法中,错误的是( )A、分子和原子都能直接构成物质 B、相同的原子可以构成不同的分子 C、凡带电的粒子都是离子 D、化学变化中元素的化合价可能改变12. 6月5日是世界环境日。2020年世界环境日的主题具体为“关爱自然,刻不容缓”,下列做法与这一主题不符的是( )A、在校园内将散落的塑料袋、树叶集中露天焚烧 B、保护野生动物 C、使用新型可降解的塑料,减少“白色污染” D、治理露天烧烤13. 过氧乙酸(C2H4O3)等消毒液能有效杀灭新冠肺炎疾毒。下列有关说法中,正确的是( )A、过氧乙酸分子由碳、氢、氧三种元素组成 B、过氧乙酸中H的质量分数最高 C、过氧乙酸由两个碳原子、四个氢原子和三个氧原子构成 D、过氧乙酸的相对分子质量为7614. 下列大小关系正确的是( )A、电解水时生成气体的体积:正极>负极 B、空气中气体的体积分数:氮气>氧气 C、地壳中元素的含量:Al<Fe D、电子数:氯原子=氯离子15. 下列物质属于氧化物的是( )A、O2 B、N2O C、NaCl D、Na2CO316. 下列说法中,正确的是( )A、分子参与化学变化时,分子本身没有改变 B、常用活性炭给自来水消毒 C、用过滤的方法可将食盐水中的食盐与水分离 D、可用肥皂水来鉴别硬水和软水17. 如图是铁元素和氧元素常见化合价的坐标图,试判断 a 点上形成化 合物的化学式为() A、Fe B、FeO C、Fe2O3 D、Fe3O418. 在一定条件下,下列物质间的转化,不能一步实现的是( )A、CO→O2 B、CO2→H2O C、H2O2→H2O D、NH4HCO3→H2O19. 向一定量的稀过氧化氢溶液中加入一定量的二氧化锰后,下列图示中的图象中不能正确反应对应关系的是( )A、
A、Fe B、FeO C、Fe2O3 D、Fe3O418. 在一定条件下,下列物质间的转化,不能一步实现的是( )A、CO→O2 B、CO2→H2O C、H2O2→H2O D、NH4HCO3→H2O19. 向一定量的稀过氧化氢溶液中加入一定量的二氧化锰后,下列图示中的图象中不能正确反应对应关系的是( )A、 B、
B、 C、
C、 D、
D、 20. 基酸钙是人的牙齿中比较坚硬的物质,也是骨的主要组成成分,化学式为Cax(PO4)(OH)y , (其中元素的化合价为+5)。经分析,其中钙、氧元素质量比为25:26,则( )A、x:y=5:1 B、x:y=5:2 C、x:y=5:3 D、x:y=5:4
20. 基酸钙是人的牙齿中比较坚硬的物质,也是骨的主要组成成分,化学式为Cax(PO4)(OH)y , (其中元素的化合价为+5)。经分析,其中钙、氧元素质量比为25:26,则( )A、x:y=5:1 B、x:y=5:2 C、x:y=5:3 D、x:y=5:4二、填空题
-
21. 用符合要求物质的序号填空:①二氧化碳;②空气;③氧气;④金刚石;⑤石墨(1)、可用于抢救危重病人的是;(2)、可用于刻划玻璃的是;(3)、可用作电极的是;(4)、可用于工业制氧的是。22. 按要求写出相应的化学用语:(1)、两个硫原子;(2)、一个碳酸根离子;(3)、两个氢分子;(4)、氧化镁中镁元素显正二价。23. 最近,英国皇家天文学会发布了一条激动人心的新进展:金星上可能存在着生命迹象,因为科学家发现,金星大气中存在着浓度异常的磷化氢(pH3)气体,达到20ppb(亿分之二)。资料显示:金星大气浓厚,主要成分为二氧化碳(占96.5%)、氮气(占3.5%)、水蒸气(约为地球的万分之一)、二氧化硫、氧气和一氧化碳等。请回答下列问题:(1)、金星大气中属于单质的有。(2)、磷化氢中磷元素的化合价为 , 其中磷元素与氢元素的质量比为。(3)、科学家成功合成了新型催化剂将CO2转化为甲醇(CH4OH)其微观示意图如下图所示

该反应的表达式为 , 分析该微观示意图得出的下列关于反应前后结论正确的是(选填字母)。
a 分子的种类改变 b 分子的数目不变 c 原子的种类改变 d 原子的数目不变
(4)、若生产96t甲醇相当于吸收了多少t碳元素?(列式计算)三、综合题
-
24. 某兴趣小组开展“测定空气中氧气的体积分数”的探究实验。

(实验1)按图1所示装置,用红磷燃烧的方法测定空气中氧气的体积分数.
(实验2)按图2所示装置,并按下列步骤进行实验:
Ⅰ.向玻璃管和水槽内加适量的水,上下移动水槽至两边水面相平于玻璃管的零刻度位置,在燃烧匙里放足量红磷,塞紧塞子。
Ⅱ.接通电源,待红磷燃烧后断开电源。
Ⅲ.当温度恢复至室温,水不再进入玻璃管时,上下移动水槽至两边水面相平。
回答下列问题:
(1)、实验3中,红磷燃烧的文字表达式是。(2)、为提高实验的准确性,在进行以上两个实验前都要进行的操作是。(3)、实验4的操作Ⅰ、Ⅱ中,上下移动水槽至两边水面相平的目的是。实验结束后,玻璃管内水面最终到达刻度线处。(4)、与实验3相比,实验4的优点是(写出一点即可)。25. 请根据下列实验装置图,回答有关问题: (1)、写出仪器名称:①;②。(2)、实验室用高锰酸钾制取氧气可采用的发生装置是(填字母),反应的文字表达式为该反应属于(选填:“分解”或“化合”)反应。(3)、可用E装置收集H2 , 说明H2具有的性质是。(4)、①实验室制取二氧化碳的文字表达式为
(1)、写出仪器名称:①;②。(2)、实验室用高锰酸钾制取氧气可采用的发生装置是(填字母),反应的文字表达式为该反应属于(选填:“分解”或“化合”)反应。(3)、可用E装置收集H2 , 说明H2具有的性质是。(4)、①实验室制取二氧化碳的文字表达式为②向盛有二氧化碳的集气瓶中倒入一定量的水,立即塞紧有两端开口细玻璃管的橡皮塞,用注射器向玻璃管中注水至P处,装置如图F所示。振荡集气瓶后,看到玻璃管中的液面将(选填:“上升”、“下降”或“不变”)。下列有关该实验的说法错误的是(选填字母)。
a 可说明二氧化碳能溶于水 b 可说明二氧化碳能与水反应 c 该装置可不用检查气密性
26. 化学兴趣小组同学利用手持技术(利用传感器和数据采集器实时测量技术)对制氧气进行了深入的探究。图1是利用传感器研究“氯酸钾以及加入一定量二氧化锰后的分解温度”的实验装置。实验测得相关数据分别如图2和图3所示。 已知:Ⅰ.氯酸钾的熔点的为356℃,二氧化锰的分解温度约为535℃,用酒精灯给物质加热,受热物质的温度一约为400℃左右;
已知:Ⅰ.氯酸钾的熔点的为356℃,二氧化锰的分解温度约为535℃,用酒精灯给物质加热,受热物质的温度一约为400℃左右;Ⅱ.不同配比是指氯酸钾和二氧化锰混合物中,氯酸钾和二氧化锰的质量比。
Ⅲ.氯酸钾分解时,传感器得到氧气浓度随温度的变化示意图(图2)及不同配比时氧气浓度随温度的变化示意图(图3)
请回答问题:
(1)、分析图2,氯酸钾的熔点(选填:“高于”、“等于”成“低于”)其分解温度;甲同学认为图1装置中试管口应略向下斜,面乙同学认为图装置正确,你支持(选填:“甲或“乙”)同学的观点,理由是。(2)、分析图2,在氯酸钾分解前,传感器得到氧气浓度降低的可能原因是。(3)、分析图3,氯酸钾分解温度随物质配比变化的规律是:当物质配比为2:1时,氯酸钾分解温度为℃。(4)、丙同学认为仅通过以上实验还不能说明二氧化锰是氢酸钾分解的催化剂,还需证明在此反应中二氧化锰的不变。(5)、写出实験室利用氯酸钾和二氧化锰制取氧气的表达式为。27. 燃煤烟气含有的二氧化硫(SO2)是一种无色有刺激性气味的有毒气体,进入大气后会形成酸雨,某化学兴趣小组的同学对其进行了如下探究:(1)、Ⅰ.甲同学认为SO2与CO2都属于非金属氧化物,它们具有相似的化学性质,并设计了下列实验进行验证:实验操作
实验现象
实验结论
文字表达式
将SO2通入滴有紫色石蕊试液的蒸馏水中
SO2能与水反应
二氧化硫+水→亚硫酸(H2SO3)
将SO2通入澄清石灰水
石灰水变浑浊
SO2能与石灰水反应
(2)、Ⅱ.乙同学猜想SO2与CO2还具有不同的化学性质。他分别将SO2与CO2通入25%的Ba(NO3)2溶液(含Ba2+、NO3-、H2O等微粒)中,发现CO2通入Ba(NO3)2溶液后无明显现象,而SO2通入Ba(NO3)2溶液后产生白色沉淀,经进一步研究确定该白色沉淀为硫酸钡(BaSO4),为探究Ba(NO3)2溶液中何种微粒与通入的SO2反应生成BaSO4 , 乙同学提出了如下假设:假设一:溶液中的NO3-
假设二:溶液中溶解的O2
验证假设一:
实验步骤
实验现象
实验结论
在盛有煮沸后迅速冷却的20mL、25%的BaCl2溶液的烧杯中,缓慢通入SO2
假设一成立
在盛有煮沸后迅速冷却的20mL、25%的Ba(NO3)2溶液的烧杯中,缓慢通入SO2
实验所用的溶液先要煮沸的目的是尽可能除去溶解在溶液中的O2 , 由此说明O2在水中的溶解能力随温度的升高而 (选填:“增强”、“减弱”或“不变”)。
(3)、验证假设二:实验步骤
实验现象
实验结论
无明显现象
假设二成立
在盛未经脱O2处理的20mL、25%的BaCl2溶液的烧杯中,缓慢通入SO2
产生白色沉淀
(4)、(实验结论)SO2能与Ba(NO3)2溶液中的Ba2+、NO3-共同作用产生白色沉淀BaSO4;SO2也能与BaCl2溶液中的(填微粒符号)共同作用产生白色沉淀BaSO4。28. 新型材料纳米级Fe粉具有广泛的用途,它比普通Fa粉更易与氧气反应。某工厂以粗盐(主要成分是NaCl,含少量泥沙等杂质)为原料,生产纳米级Fe粉的主要工艺流程如下图所示: 已知:在化学反应前后元素的种类不变。(1)、操作a的名称是 , 该操作中玻璃棒的作用是。(2)、写出电解NaCl溶液所发生的反应中,反应物的化学式。(3)、在该制备纳米级Fe粉的主要工艺流程中,所用到的原料有:粗盐、水、氮气和(填物质名称):其中N2的作用是。(4)、纳米级Fe粉在氧气中能自发燃烧生成一种黑色固体,此黑色固体的化学式为
已知:在化学反应前后元素的种类不变。(1)、操作a的名称是 , 该操作中玻璃棒的作用是。(2)、写出电解NaCl溶液所发生的反应中,反应物的化学式。(3)、在该制备纳米级Fe粉的主要工艺流程中,所用到的原料有:粗盐、水、氮气和(填物质名称):其中N2的作用是。(4)、纳米级Fe粉在氧气中能自发燃烧生成一种黑色固体,此黑色固体的化学式为