福建省福州市闽江口联盟校2020-2021学年高二上学期化学期中考试试卷
试卷更新日期:2021-09-09 类型:期中考试
一、单选题
-
1. 下列反应中,属于吸热反应的是( )A、活泼金属跟酸反应 B、制造水煤气 C、酸碱中和反应 D、镁条燃烧2. 下列电池属于二次电池的是( )A、银锌纽扣电池 B、氢氧燃料电池 C、铅蓄电池 D、锌锰干电池3. 下列变化过程中,ΔS<0的是( )A、氯化钠溶于水中 B、CaCO3(s)分解为CaO(s)和CO2(g) C、干冰的升华 D、NH3(g)和HCl(g)反应生成NH4Cl4. 含NaOH 20.0g的稀溶液与足量稀盐酸反应,放出28.7 kJ的热量,表示该反应的热化学方程式正确的是( )A、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H= +28.7 kJ·mol-1 B、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H= _28.7 kJ·mol-1 C、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.4 kJ·mol-1 D、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H= _57.4 kJ·mol-15. 在2A(g)+B(s) 3C(g)+5D(g)反应中,表示该反应速率最快的是( )A、υ(A)= 0.5 mol/(L·s) B、υ(B)= 0.3 mol/(L·s) C、υ(C)= 0.8 mol/(L·s) D、υ(D)= 1 mol/(L·s)6. 在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,则用该气体表示该反应的平均反应速率为( )A、0.4 mol·L−1·s−1 B、0.3 mol·L−1·s−1 C、0.2 mol·L−1·s−1 D、0.1 mol·L−1·s−17. 在一定温度下,可逆反应A(g)+3B(g) 2C(g)达到平衡状态的标志是( )A、生成C的速率等于消耗A的速率的2倍 B、单位时间生成n mol A,同时生成3n mol B C、A,B,C的浓度不再变化 D、A,B,C的分子数比为1∶3∶28. 下列有关化学反应速率的说法,正确的是( )A、用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 B、100mL 的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 C、二氧化硫的催化氧化是一个放热反应,所以升高温度,反应减慢 D、汽车尾气中的 和 可以缓慢反应生成 和 ,减小压强,反应速率减小9. 已知298K下反应2Al2O3(s)+3C(s)=4Al(s)+3CO2(g) ΔH=+2171kJ·mol-1 ΔS=+635.5J·mol-1·K-1 , 则此反应( )A、高温下可自发进行 B、任何条件下都可自发进行 C、任何条件下都不可自发进行 D、低温下可自发进行10. 下列各图中表示正反应是吸热反应的图是( )A、
 B、
B、 C、
C、 D、
D、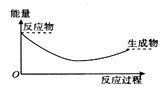 11. 下列说法或表示方法正确的是( )A、由C(石墨)= C(金刚石);△H=+1.90 kJ/mol可知,金刚石比石墨稳定 B、等物质的量的固体硫和硫蒸气分别完全燃烧,后者放出热量多 C、在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)= 2H2O(l);△H=-285.8kJ/mol D、在稀溶液中,H+(aq)+ OH-(aq) = H2O(l);△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量等于57.3kJ12. 下列有关金属腐蚀的说法正确的是( )A、电化学腐蚀是在外加电流作用下不纯金属发生化学反应被损耗的过程 B、金属的电化学腐蚀和化学腐蚀本质相同,但电化学腐蚀伴有电流产生 C、钢铁腐蚀最普遍的是吸氧腐蚀,负极吸收氧气,产物最终转化为铁锈 D、镀锌的铁板比镀锡的铁板更容易被腐蚀13. 下列事实,不能用勒夏特列原理解释的是( )A、反应CO(g)+NO2(g) ⇌CO2(g)+NO(g) △H<0,升高温度可使平衡向逆反应方向移动 B、钢铁在潮湿的空气中容易生锈 C、开启啤酒瓶后,瓶中马上泛起大量泡沫 D、SO2催化氧化成SO3的反应,往往加入过量的空气14. 下列各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )
11. 下列说法或表示方法正确的是( )A、由C(石墨)= C(金刚石);△H=+1.90 kJ/mol可知,金刚石比石墨稳定 B、等物质的量的固体硫和硫蒸气分别完全燃烧,后者放出热量多 C、在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)= 2H2O(l);△H=-285.8kJ/mol D、在稀溶液中,H+(aq)+ OH-(aq) = H2O(l);△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量等于57.3kJ12. 下列有关金属腐蚀的说法正确的是( )A、电化学腐蚀是在外加电流作用下不纯金属发生化学反应被损耗的过程 B、金属的电化学腐蚀和化学腐蚀本质相同,但电化学腐蚀伴有电流产生 C、钢铁腐蚀最普遍的是吸氧腐蚀,负极吸收氧气,产物最终转化为铁锈 D、镀锌的铁板比镀锡的铁板更容易被腐蚀13. 下列事实,不能用勒夏特列原理解释的是( )A、反应CO(g)+NO2(g) ⇌CO2(g)+NO(g) △H<0,升高温度可使平衡向逆反应方向移动 B、钢铁在潮湿的空气中容易生锈 C、开启啤酒瓶后,瓶中马上泛起大量泡沫 D、SO2催化氧化成SO3的反应,往往加入过量的空气14. 下列各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( ) A、4>2>1>3>5 B、2>1>5>3>4 C、5>4>2>3>1 D、3>5>2>4>115. 当可逆反应2SO2(g)+O2(g)=2SO3(g),达到平衡后通入18O2再次达到平衡时18O存在于( )A、SO3、O2中 B、SO2、SO3中 C、SO2、O2、SO3中 D、SO2、O2中16. 已知反应A2(g)+2B2(g) 2AB2(g)的△H<0,达到平衡后,改变外界条件能使平衡正向移动的是:( )A、升高温度 B、增大压强 C、使用催化剂 D、增大AB2的浓度
A、4>2>1>3>5 B、2>1>5>3>4 C、5>4>2>3>1 D、3>5>2>4>115. 当可逆反应2SO2(g)+O2(g)=2SO3(g),达到平衡后通入18O2再次达到平衡时18O存在于( )A、SO3、O2中 B、SO2、SO3中 C、SO2、O2、SO3中 D、SO2、O2中16. 已知反应A2(g)+2B2(g) 2AB2(g)的△H<0,达到平衡后,改变外界条件能使平衡正向移动的是:( )A、升高温度 B、增大压强 C、使用催化剂 D、增大AB2的浓度二、综合题
-
17.(1)、氢能的优点是燃烧热值高,无污染。目前工业制氢气的一个重要反应为CO(g)+H2O(g)=CO2(g)+H2(g)ΔH , 反应过程和能量的关系如图所示:

①CO(g)+H2O(g)=CO2(g)+H2(g)ΔH 0(填“>”“<”或“=”);
②过程Ⅱ是加入催化剂后的反应过程,则过程Ⅰ和Ⅱ的反应热 (填“相等”或“不相等”),原因是;
③已知:H2(g)+ O2(g)=H2O(g)ΔH=-242.0kJ·mol-1
H2O(l)=H2O(g)ΔH=+44.0kJ·mol-1
则H2(g)燃烧生成H2O(l)的热化学方程式为。
(2)、在一定条件下,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图所示,则
①该反应的化学方程式为:;
②t1s时反应物A的转化率为:;
③0~t1s内A的反应速率为(假设t1=6)v(A)=。
18.(1)、已知拆开1molH-H键、1molI-I键、1molH-I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1molHI需要(填“放出”或“吸收”) kJ的热量。(2)、为分别验证温度、浓度、催化剂颗粒大小对化学反应速率的影响规律,某同学设计了如下4组实验。实验序号
温度
H2O2溶液初始浓度
MnO2颗粒大小
1
25℃
4%
无MnO2
2
25℃
12%
1g细颗粒MnO2
3
25℃
4%
1g细颗粒MnO2
4
25℃
4%
1g粗颗粒MnO2
①上表中,反应速率最快的是(填实验序号);
②设计实验2、3的目的是;
③实验3、4预期可得出的结论是。
19.(1)、在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如表所示:t/℃
700
800
830
1000
1200
K
0.6
0.9
1.0
1.7
2.6
回答下列问题:
①该反应的化学平衡常数表达式为K=。
②该反应为(填“吸热”或“放热”)反应。
③能判断该反应达到化学平衡状态的依据是。
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
④某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),则此时的温度为℃。
(2)、反应3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g)在高温可变容积的密闭容器中进行,回答:①增加Fe的量,其反应速率(填“增大”、“不变”或“减小”,下同)。
②其它条件不变,将容器的体积缩小一半,其反应速率。
③其它条件不变,加入一定量H2 , 其平衡移动方向(填“正移”、“不移”或“逆移”,下同)。
④其它条件不变,加入一定量的催化剂,其平衡移动方向。
20.(1)、如图所示,将锌、铜通过导线相连,置于稀硫酸中。
①锌片上的现象是锌片逐渐溶解,电极反应为;
②电流由经导线流向 , 说明为正极;
③当收集到氢气4.48L(标况下)时,通过导线的电子为mol。
(2)、在25℃时,用石墨电极电解2.0L2.5mol/LCuSO4溶液;5min后,在一个石墨电极上有6.4gCu生成。试回答下列问题:①极发生氧化反应,电极反应式为;
②得到O2的体积(标准状况)是L。