高中化学人教版(2019)选择性必修1第三章实验活动2强酸与强碱的中和滴定
试卷更新日期:2021-08-27 类型:同步测试
一、单选题
-
1. 常温下,某H3AsO4溶液中逐滴加入NaOH,溶液中含砷微粒的分布分数(某含砷微粒的物质的量浓度占所有含砷微粒物质的量浓度之和的分数)与pH的变化关系如下图所示。下列说法正确的是( )
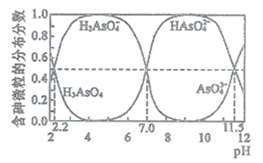 A、H3AsO4的第一步电离常数Ka1>0.01 B、pH=11.5时,c(H2AsO )+2c(HAsO )+3c(AsO )+c(OH-)=c(H+) C、Na3AsO4溶液中,3c(Na+)=c(AsO )+ c(HAsO )+c(H2AsO )+c(H3AsO4) D、以酚酞为指示剂,将 NaOH 溶液逐滴加入到H3AsO4溶液中,当溶液由无色变为浅红色时停止滴加。该反应的离子方程式为2OH-+H3AsO4= HAsO +2H2O2. 测定浓硫酸试剂中 含量的主要操作包括:①量取一定量的浓硫酸,稀释;②转移定容得待测液;③移取 待测液,用 的 溶液滴定。上述操作中,不需要用到的仪器为( )A、
A、H3AsO4的第一步电离常数Ka1>0.01 B、pH=11.5时,c(H2AsO )+2c(HAsO )+3c(AsO )+c(OH-)=c(H+) C、Na3AsO4溶液中,3c(Na+)=c(AsO )+ c(HAsO )+c(H2AsO )+c(H3AsO4) D、以酚酞为指示剂,将 NaOH 溶液逐滴加入到H3AsO4溶液中,当溶液由无色变为浅红色时停止滴加。该反应的离子方程式为2OH-+H3AsO4= HAsO +2H2O2. 测定浓硫酸试剂中 含量的主要操作包括:①量取一定量的浓硫酸,稀释;②转移定容得待测液;③移取 待测液,用 的 溶液滴定。上述操作中,不需要用到的仪器为( )A、 B、
B、 C、
C、 D、
D、
3. 常温下用0.2mol·L-1NaOH溶液分别滴定0.2mol·L-1一元酸HA和HB,混合溶液的pH与离子浓度变化的关系如图所示。下列有关叙述错误的是( )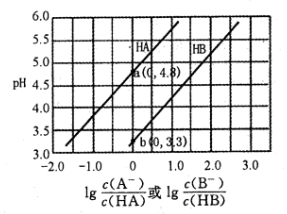 A、Ka(HA)的数量级为10-5 B、酸碱恰好反应时,HB溶液中的pH为9.15 C、反应HA+B-=HB+A-的平衡常数为10-1.5 D、相同条件下对水的电离影响程度:NaA>NaB4. 用0.1000 mol·L-1 NaOH溶液分别滴定20 mL 0.1000 mol·L-1 HCl和HAc(醋酸)的滴定曲线如图。下列说法正确的是( )
A、Ka(HA)的数量级为10-5 B、酸碱恰好反应时,HB溶液中的pH为9.15 C、反应HA+B-=HB+A-的平衡常数为10-1.5 D、相同条件下对水的电离影响程度:NaA>NaB4. 用0.1000 mol·L-1 NaOH溶液分别滴定20 mL 0.1000 mol·L-1 HCl和HAc(醋酸)的滴定曲线如图。下列说法正确的是( )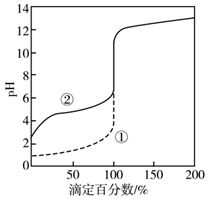 A、0.1000 mol·L-1 HAc的电离百分数约为10% B、两个滴定过程均可用甲基橙做指示剂 C、滴定百分数为50%时,曲线②溶液中c(Ac-)>c(Na+) D、图像的变化证实了Ac-的碱性很强5. 保持温度始终为T℃,用滴定管量取一定体积的浓氯水置于锥形瓶中,用NaOH溶液以恒定速率来滴定,根据测定结果绘制出ClO-、ClO 的物质的量浓度c与时间t的关系曲线(如图)。下列说法正确的是( )
A、0.1000 mol·L-1 HAc的电离百分数约为10% B、两个滴定过程均可用甲基橙做指示剂 C、滴定百分数为50%时,曲线②溶液中c(Ac-)>c(Na+) D、图像的变化证实了Ac-的碱性很强5. 保持温度始终为T℃,用滴定管量取一定体积的浓氯水置于锥形瓶中,用NaOH溶液以恒定速率来滴定,根据测定结果绘制出ClO-、ClO 的物质的量浓度c与时间t的关系曲线(如图)。下列说法正确的是( ) A、0~t1时发生反应的离子方程式:OH-+Cl2=Cl-+ClO-+H2O B、a点溶液中:c(ClO-)>c(ClO )>c(Na+)>c(OH-)>c(H+) C、b点溶液中:c(Na+)+c(H+)=8c(ClO-)+c(OH-) D、t2~t4过程中: 一直减小6. 实验室用标准盐酸溶液测定某NaOH溶液的浓度,用酚酞作指示剂,下列操作中可能使测定结果偏高的是( )A、盛NaOH溶液的锥形瓶用蒸馏水清洗后没有再用NaOH溶液润洗 B、锥形瓶内溶液颜色变化由粉红色刚好变成无色,立即记下滴定管液面所在刻度 C、开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 D、滴定前仰视读数,滴定后俯视读数7. 常温下,向20.00mL0.1000 盐酸中滴加0.1000 NaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。已知:① ;②甲基红是一种常用的酸碱指示剂,其pH在4.4~6.2区间时呈橙色, 时呈红色, 时呈黄色。下列说法错误的是( )
A、0~t1时发生反应的离子方程式:OH-+Cl2=Cl-+ClO-+H2O B、a点溶液中:c(ClO-)>c(ClO )>c(Na+)>c(OH-)>c(H+) C、b点溶液中:c(Na+)+c(H+)=8c(ClO-)+c(OH-) D、t2~t4过程中: 一直减小6. 实验室用标准盐酸溶液测定某NaOH溶液的浓度,用酚酞作指示剂,下列操作中可能使测定结果偏高的是( )A、盛NaOH溶液的锥形瓶用蒸馏水清洗后没有再用NaOH溶液润洗 B、锥形瓶内溶液颜色变化由粉红色刚好变成无色,立即记下滴定管液面所在刻度 C、开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 D、滴定前仰视读数,滴定后俯视读数7. 常温下,向20.00mL0.1000 盐酸中滴加0.1000 NaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。已知:① ;②甲基红是一种常用的酸碱指示剂,其pH在4.4~6.2区间时呈橙色, 时呈红色, 时呈黄色。下列说法错误的是( )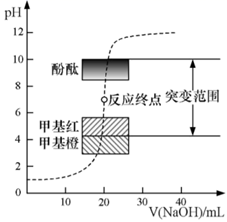 A、滴定时,边摇动锥形瓶边观察锥形瓶中溶液的颜色变化 B、NaOH与盐酸恰好完全反应时,pH=7 C、选择甲基红指示反应终点,误差比甲基橙的大 D、V(NaOH)=30.00mL时,所得溶液的pH=12.38. 用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考下图,从下表中选出正确选项( )
A、滴定时,边摇动锥形瓶边观察锥形瓶中溶液的颜色变化 B、NaOH与盐酸恰好完全反应时,pH=7 C、选择甲基红指示反应终点,误差比甲基橙的大 D、V(NaOH)=30.00mL时,所得溶液的pH=12.38. 用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考下图,从下表中选出正确选项( )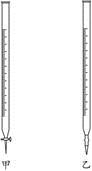
选项
锥形瓶中溶液
滴定管中溶液
选用指示剂
选用滴定管
A
碱
酸
石蕊
乙
B
酸
碱
酚酞
甲
C
碱
酸
甲基橙
乙
D
酸
碱
酚酞
乙
A、A B、B C、C D、D9. 用0.1000 mol·L-1 NaOH标准溶液滴定25.00mL未知浓度的盐酸,下列说法正确的是( )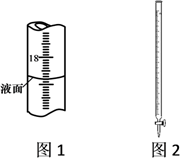 A、NaOH标准溶液应装在如图2所示的滴定管中 B、滴定时NaOH的滴速应保持匀速,并不停摇动锥形瓶 C、图1所示液体的体积读数为18.20mL D、若滴定前滴定管尖嘴有气泡,滴定终了气泡消失,则所测盐酸的浓度偏大10. 以酚酞溶液为指示剂,用 的盐酸对某新制的 溶液仅限中和滴定实验,数据记录如下表:
A、NaOH标准溶液应装在如图2所示的滴定管中 B、滴定时NaOH的滴速应保持匀速,并不停摇动锥形瓶 C、图1所示液体的体积读数为18.20mL D、若滴定前滴定管尖嘴有气泡,滴定终了气泡消失,则所测盐酸的浓度偏大10. 以酚酞溶液为指示剂,用 的盐酸对某新制的 溶液仅限中和滴定实验,数据记录如下表:待测液
消耗标准盐酸的体积
①
溶液
②
溶液
水
③
敞口隔夜放置的 溶液
该新制的 溶液的浓度 合理的是( )
A、 B、 C、 D、11. 常温下,用0.1000mol·L-1的NaOH溶液滴定20.00mL未知浓度的某酸HX,滴定曲线如图所示。下列说法正确的是( )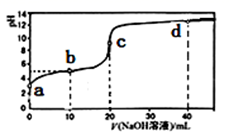 A、该酸的常温下的电离常数约为1×10-5 B、d点的溶液中:c(Na+)<c(X-) C、需用甲基橙作指示剂 D、b点溶液中:c(HX)>c(Na+)>c(H+)>c(OH-)12. 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定体积均是20mL、浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是( )
A、该酸的常温下的电离常数约为1×10-5 B、d点的溶液中:c(Na+)<c(X-) C、需用甲基橙作指示剂 D、b点溶液中:c(HX)>c(Na+)>c(H+)>c(OH-)12. 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定体积均是20mL、浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是( )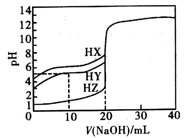 A、酸性强弱顺序是HX>HY>HZ B、由图象可知,HY为弱酸,其电离常数数量级为10-6 C、pH=2的HZ溶液加水稀释10倍,pH为3 D、加入20mLNaOH溶液时,只有HY溶液达到滴定终点13. 用NaOH标准溶液测定未知浓度的盐酸,下列实验操作不会引起误差的是( )A、用待测液润洗锥形瓶 B、用蒸馏水洗净后的酸式滴定管直接量取待测液 C、选用酚酞作指示剂,实验时不小心多加了两滴指示剂 D、实验开始时碱式滴定管尖嘴部分无气泡,结束实验时有气泡14. 25℃时,用一定浓度NaOH溶液滴定某醋酸溶液,混合溶液的导电能力变化曲线如图所示,其中b点为恰好反应点。下列说法错误的是( )
A、酸性强弱顺序是HX>HY>HZ B、由图象可知,HY为弱酸,其电离常数数量级为10-6 C、pH=2的HZ溶液加水稀释10倍,pH为3 D、加入20mLNaOH溶液时,只有HY溶液达到滴定终点13. 用NaOH标准溶液测定未知浓度的盐酸,下列实验操作不会引起误差的是( )A、用待测液润洗锥形瓶 B、用蒸馏水洗净后的酸式滴定管直接量取待测液 C、选用酚酞作指示剂,实验时不小心多加了两滴指示剂 D、实验开始时碱式滴定管尖嘴部分无气泡,结束实验时有气泡14. 25℃时,用一定浓度NaOH溶液滴定某醋酸溶液,混合溶液的导电能力变化曲线如图所示,其中b点为恰好反应点。下列说法错误的是( )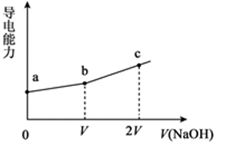 A、b点溶液的pH=7 B、溶液的导电能力与离子种类和浓度有关 C、a→c过程中,n(CH3COO-)不断增大 D、c点的混合溶液中c(Na+)>c(OH-)>c(CH3COO-)15. 水合乙二胺 是一种二元弱碱,在水中的电离方式与 相似,其 .常温下,用 盐酸滴定 乙二胺溶液.下列说法错误的是( )A、乙二胺在水溶液中的第一步电离方程式为 B、滴定时选用酚酞作指示剂产生的误差最小 C、滴入 盐酸时,溶液呈碱性 D、滴入 盐酸时,加水稀释,溶液中 减小16. 次氯酸具有漂白和杀菌的作用。室温下,向20mL0.1mol·L-1次氯酸溶液中滴加同浓度的NaOH溶液,所得的滴定曲线如图所示。下列说法正确的是( )
A、b点溶液的pH=7 B、溶液的导电能力与离子种类和浓度有关 C、a→c过程中,n(CH3COO-)不断增大 D、c点的混合溶液中c(Na+)>c(OH-)>c(CH3COO-)15. 水合乙二胺 是一种二元弱碱,在水中的电离方式与 相似,其 .常温下,用 盐酸滴定 乙二胺溶液.下列说法错误的是( )A、乙二胺在水溶液中的第一步电离方程式为 B、滴定时选用酚酞作指示剂产生的误差最小 C、滴入 盐酸时,溶液呈碱性 D、滴入 盐酸时,加水稀释,溶液中 减小16. 次氯酸具有漂白和杀菌的作用。室温下,向20mL0.1mol·L-1次氯酸溶液中滴加同浓度的NaOH溶液,所得的滴定曲线如图所示。下列说法正确的是( )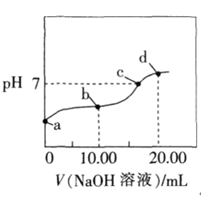 A、c、d两点时,水的电离程度:d>c B、d点溶液中:c(H+)=c(ClO-)-c(Na+) C、滴定时,由a点到c点, 增大 D、a点时,溶液的pH=l
A、c、d两点时,水的电离程度:d>c B、d点溶液中:c(H+)=c(ClO-)-c(Na+) C、滴定时,由a点到c点, 增大 D、a点时,溶液的pH=l二、多选题
-
17. 用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作中正确的是( )A、酸式滴定管用蒸馏水洗净后,直接加入已知浓度的盐酸 B、锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液 C、滴定时,没有逐出滴定管下口的气泡 D、读数时,视线与滴定管内液体的凹液面最低处保持水平
三、填空题
-
18. 用25mL移液管量取市售食醋25mL,置于250mL容量瓶中,加水稀释至刻度,摇匀得到待测食醋溶液,用0.100 0mol•L﹣1NaOH标准溶液滴定,滴定过程中记录如下数据:
实验次数
第一次
第二次
第三次
待测食醋的体积初读数/mL
0.02
0.03
0.00
待测食醋的体积终读数/mL
25.01
25.04
25.02
氢氧化钠标准液的体积初读数/mL
0.01
0.03
0.04
氢氧化钠标准液的体积终读数/mL
12.52
12.55
12.58
由以上数据可求得该市售食醋总酸含量的平均值为(g/100mL).(答案保留三位小数)
19. 某化学兴趣小组取一定量的双氧水,欲准确测定其中H2O2的含量:取双氧水25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释.用一定浓度的高锰酸钾标准溶液滴定,其反应的离子方程式为:2MnO4﹣+5H2O2+4H+═2Mn2++5O2↑+2H2O,滴定时,将高锰酸钾标准溶液注入(填“酸式”或“碱式”)滴定管中,滴定到达终点的现象是 .四、实验探究题
-
20.(1)、Ⅰ.实验室用0.100mol/LNaOH标准溶液滴定未知浓度的盐酸。
盛NaOH标准液的滴定管尖嘴部分留有气泡,排除气泡的方法应采用图1中的操作(填“甲”、“乙”、“丙”)。选择酚酞作为指示剂,滴定终点的现象为。
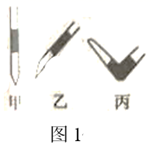 (2)、下列操作会导致实验结果偏低的是___________(填标号)。A、碱式滴定管未用标准NaOH溶液润洗 B、盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗 C、滴定终点读数时,仰视滴定管的刻度 D、滴定过程中振荡锥形瓶,液体不慎溅出(3)、某学生进行3次实验得到相关数据如表所示。
(2)、下列操作会导致实验结果偏低的是___________(填标号)。A、碱式滴定管未用标准NaOH溶液润洗 B、盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗 C、滴定终点读数时,仰视滴定管的刻度 D、滴定过程中振荡锥形瓶,液体不慎溅出(3)、某学生进行3次实验得到相关数据如表所示。滴定次数
待测盐酸的体积/mL
消耗0.100mol/LNaOH溶液的体积/mL
滴定前读数
滴定后读数
第一次
25.00
0.00
26.11
第二次
25.00
1.56
30.30
第三次
25.00
0.22
26.31
则盐酸的物质的量浓度为mol/L。(保留三位小数)
(4)、Ⅱ.一定浓度的 溶液中含硫元素所有微粒的物质的量分数随pH的变化如图2所示。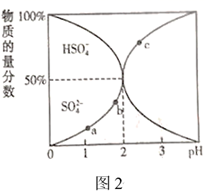
图中a、b、c三点,水电离的 由大到小的顺序分为(用a、b、c表示),pH=3时, 。
21. 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验,请完成下列填空:(1)、配制100mL0.1000 mol∙L-1NaOH标准溶液。滴定操作步骤:①准备:检漏→洗涤→→→排气泡→读数。
②滴定:用移液管取25.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用标准NaOH溶液进行滴定,重复上述滴定操作2-3次,记录数据如下。
实验编号
NaOH溶液的浓度(mol·L-1)
NaOH标准液初始读数(mL)
NaOH标准液终点读数(mL)
1
0.1000
0.62
20.60
2
0.1000
0.72
20.74
3
0.1000
0.00
23.00
(2)、滴定达到终点的标志是。(3)、排去碱式滴定管中气泡的方法应采用操作。然后轻轻挤压玻璃球使尖嘴部分充满碱液。 (4)、根据上述数据,可计算出该盐酸的浓度约为mol·L-1(5)、在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有。
(4)、根据上述数据,可计算出该盐酸的浓度约为mol·L-1(5)、在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有。A.开始滴定前,滴定管尖悬挂的液滴未擦去
B.滴定终点读数时仰视读数
C.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
22. 常温下,用0.100 0 mol·L−1的 NaOH溶液滴定20.00 mL 0.1000 mol·L−1 的某酸HA溶液所得滴定曲线如图所示。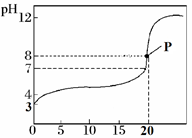

回答下列问题:
(1)、该酸为酸(填“强”或者“弱”),你的判断理由是。(2)、点P时溶液中的 c(HA)=mol·L−1。(3)、①该中和滴定应选择做指示剂,滴定终点时的现象是。指示剂变色范围(pH)
甲基橙(3.1~4.4)
石蕊(5~8)
酚酞(8.2~10.0)
颜色
<3.1
3.1~4.4
>4.4
<5
5~8
>8
<8.2
8.2~10.0
>10.0
红
橙
黄
红
紫
蓝
无色
粉红
红
②滴定起始和终点的液面位置如图2所示,则消耗NaOH溶液的体积为mL。
③下列操作使滴定结果偏高的是。
a.滴定前,碱式滴定管未用NaOH溶液润洗
b.锥形瓶的待测液中加少量水稀释
c.碱式滴定管滴定前有气泡,滴定后无气泡
d.读数时,滴定前仰视,滴定后俯视
23. 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验。请你完成下列填空:步骤一:配制250mL 0.10mol/L NaOH标准溶液。
步骤二:取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作3次,记录数据如下。
实验
编号
NaOH溶液的浓度
(mol/L)
滴定完成时,消耗NaOH溶液的体积(mL)
待测盐酸溶液的体积(mL)
1
0.10
20.02
20.00
2
0.10
20.00
20.00
3
0.10
19.98
20.00
(1)、步骤一需要用托盘天平称量氢氧化钠固体的质量为g,配制标准溶液除用到玻璃棒和烧杯,还需要的玻璃仪器有(2)、步骤二中量取20.00mL的稀盐酸用到的仪器是。判断滴定终点的现象是(3)、根据上述数据,可计算出该盐酸的浓度为(4)、在上述实验中,下列操作(其他操作正确)会造成测定结果(待测液浓度值)偏高的有(_______)A、配制标准溶液定容时,加水超过刻度 B、锥形瓶水洗后直接装待测液 C、酸式滴定管水洗后未用待测稀盐酸溶液润洗 D、滴定到达终点时,仰视读出滴定管读数; E、碱式滴定管尖嘴部分有气泡,滴定后消失24. 某学生欲用已知浓度的氢氧化钠标准溶液来滴定未知浓度的盐酸溶液,以酚酞试液为滴定指示剂。请填写下列空白:(1)、用标准NaOH溶液滴定时,应将标准NaOH溶液注入图中(填“甲”或“乙”)中。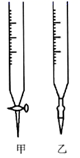 (2)、碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是。(3)、若第一次滴定开始和结束时,碱式滴定管中的液面如图所示,请将数据填入下面表格的横线处。
(2)、碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是。(3)、若第一次滴定开始和结束时,碱式滴定管中的液面如图所示,请将数据填入下面表格的横线处。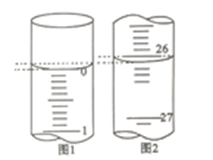
滴定次数
待测盐酸溶液的体积/mL
0.1000 mol·L-1氢氧化钠的体积/mL
滴定前刻度
滴定后刻度
溶液体积/mL
第一次
25.00
0.00
第二次
25.00
1.00
26.80
25.80
第三次
25.00
2.00
28.10
26.10
第四次
25.00
0.22
29.17
28.95
(4)、请根据表中数据计算该盐酸溶液的物质的量浓度c(HCl)=。(5)、请简述滴定终点的判定。(6)、下列操作中可能使所测盐酸溶液的浓度偏低的。A碱式滴定管在滴定前有气泡,滴定后气泡消失
B滴定前盛放盐酸溶液的锥形瓶用蒸馏水洗净后没有干燥
C量取一定体积的待测液,最后读数时滴定管尖嘴处悬挂一滴溶液
D读取氢氧化钠溶液体积时,开始时仰视读数,滴定结束时俯视读数
25. 回答下列问题:(1)、25℃时,已知部分物质的电离平衡常数:NH3·H2O:2×10-5 , HClO:3×10-8;则0.1mol·L-1NH4ClO溶液中离子浓度由大到小的顺序是;ClO-水解反应的平衡常数Kh=(保留两位有效数字)。(2)、某小组同学探究饱和NaClO和KAl(SO4)2溶液混合反应的实验,发现产生大量的白色胶状沉淀。出现上述现象的原因是(请用反应的离子方程式表示)。(3)、用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液。Ⅰ.准备标准溶液
a.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100 mL 0.100 0 mol·L-1 NH4SCN标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00 mL于锥形瓶中。
b.加入25.00 mL AgNO3标准溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.100 0 mol·L-1 NH4SCN溶液滴定过量的Ag+ , 使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号
1
2
3
消耗NH4SCN标准溶液体积/mL
10.24
10.02
9.98
f.数据处理。回答下列问题:
①滴定应在pH<0.5的条件下进行,其原因是。
②测得c(I-)=mol·L-1。
③在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为。
④下列操作对c(I-)测定结果的影响偏高的是。
A.若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出
B.若在滴定终点读取滴定管刻度时,俯视标准液液面
C.用滴定管量取25.00 mL待测NaI溶液,读取初始液面示数时有气泡,后来无气泡
五、综合题
-
26. 25℃时,取浓度均为0.1mol/L的醋酸溶液和氨水溶液各20mL,分别用0.1mol/LNaOH溶液、0.1mol/L盐酸进行中和滴定。滴定过程中pH随滴加溶液的体积变化关系如图所示。回答下列问题:
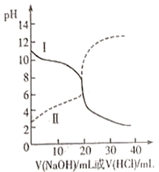 (1)、表示氨水滴定过程中pH变化情况的是曲线(填“Ⅰ”或“Ⅱ”)。由图中信息可知,25℃时0.1mol/L醋酸溶液的电离程度(填“大于”“小于”或“等于”,下同)10%。当横坐标为20mL时,曲线Ⅰ对应的纵坐标应7。(2)、滴加溶液到10mL时,曲线Ⅱ所表示的溶液中c(H+)-c(OH-)(结果中不能包含阳离子浓度)。27.(1)、25℃时,NaHCO3溶液呈碱性,原因是水解引起的(填“Na+”或“HCO ”);(2)、常温下,0.0100mol/L盐酸的pH=。(3)、用0.0100mol/L盐酸滴定未知浓度的NaOH溶液,酚酞作指示剂,滴定终点时,溶液的颜色由浅红色变为(填“蓝色”或“无色”),且半分钟内保持不变。
(1)、表示氨水滴定过程中pH变化情况的是曲线(填“Ⅰ”或“Ⅱ”)。由图中信息可知,25℃时0.1mol/L醋酸溶液的电离程度(填“大于”“小于”或“等于”,下同)10%。当横坐标为20mL时,曲线Ⅰ对应的纵坐标应7。(2)、滴加溶液到10mL时,曲线Ⅱ所表示的溶液中c(H+)-c(OH-)(结果中不能包含阳离子浓度)。27.(1)、25℃时,NaHCO3溶液呈碱性,原因是水解引起的(填“Na+”或“HCO ”);(2)、常温下,0.0100mol/L盐酸的pH=。(3)、用0.0100mol/L盐酸滴定未知浓度的NaOH溶液,酚酞作指示剂,滴定终点时,溶液的颜色由浅红色变为(填“蓝色”或“无色”),且半分钟内保持不变。
-