山西省晋中市灵石县2020-2021学年九年级上学期化学12月月考试卷
试卷更新日期:2021-08-23 类型:月考试卷
一、单选题
-
1. 日常生活中的下列做法,一定含有化学变化的是( )A、用胶带粘合破损书画 B、用白醋泡制软壳鸡蛋 C、用钢丝球擦除灶具污渍 D、用煮沸降低水的硬度2. 下列关于化学方程式 的含义的叙述中,正确的是( )A、可表示水是由氢气和氧气组成的 B、2个水分解生成2个氢气和1个氧气 C、通电时水分解生成氢气和氧气 D、通电时,每9份质量的水分解生成1份质量的氧气和8份质量的氢气3. 下列做法存在严重事故隐患的是( )A、用石灰沙浆抹墙 B、用干冰制造舞台上的云雾 C、用水来防止一氧化碳中毒 D、将活性炭放在冰箱内去除异味4. 某物质在纯氧中燃烧生成了氮气和水蒸气,该物质一定含有( )A、氮元素和氧元素 B、氢元素和氧元素 C、氮元素和碳元素 D、氮元素和氢元素5. 下列物质的用途中,主要利用其化学性质的是( )A、炭黑制笔芯 B、金刚石裁玻璃 C、焦炭冶炼金属 D、石墨做电极6. 关于C、CO、CO2三种物质,下列说法中正确的是( )
①三种物质都含有碳元素,都具有还原性
②CO、CO2都是没有颜色、没有气味的气体
③CO2可用于光合作用,CO可用于人工降雨
④CO2排放过多会导致温室效应,CO易引起中毒
⑤CO2可用来灭火,CO可用作燃料
A、①②③ B、②④⑤ C、②③④ D、①③7. 如图为三种碳单质的结构模型图,图中小球代表碳原子。下列说法错误的是( ) A、上图中,①②③依次表示C60、金刚石、石墨 B、原子的排列方式改变,则构成的物质种类改变 C、石墨在一定条件下可转变为金刚石,该变化属于物理变化 D、《清明上河图》至今图案清晰可见,是因为在常温下碳单质的化学性质稳定8. 下列有关二氧化碳的说法正确的是( )A、二氧化碳通入紫色石蕊溶液,溶液变为红色,说明二氧化碳具有酸性 B、二氧化碳的过度排放会加剧温室效应,因此应合理使用化石燃料 C、二氧化碳和一氧化碳的组成元素相同,化学性质相同 D、进入久未开启的菜窖之前,必须做灯火试验,是因为二氧化碳有毒9. 构建化学基本观念是学好化学的基础,下列对化学基本观念的认识错误的是( )A、元素观:一氧化碳、二氧化碳都是由碳元素和氧元素组成的 B、微粒观:保持金刚石化学性质的最小粒子是碳原子 C、转化观:氧化汞在一定条件下可生成金属汞 D、守恒观:4g氢气和16g氧气反应,应该生成20g水10. 在化学反应A +2B=C+2D中,已知B和C的相对分子质量之比为8∶11,当16 g A与一定量B恰好完全反应后,生成44 g C,则生成D的质量是( )A、36 g B、18 g C、4g D、48 g
A、上图中,①②③依次表示C60、金刚石、石墨 B、原子的排列方式改变,则构成的物质种类改变 C、石墨在一定条件下可转变为金刚石,该变化属于物理变化 D、《清明上河图》至今图案清晰可见,是因为在常温下碳单质的化学性质稳定8. 下列有关二氧化碳的说法正确的是( )A、二氧化碳通入紫色石蕊溶液,溶液变为红色,说明二氧化碳具有酸性 B、二氧化碳的过度排放会加剧温室效应,因此应合理使用化石燃料 C、二氧化碳和一氧化碳的组成元素相同,化学性质相同 D、进入久未开启的菜窖之前,必须做灯火试验,是因为二氧化碳有毒9. 构建化学基本观念是学好化学的基础,下列对化学基本观念的认识错误的是( )A、元素观:一氧化碳、二氧化碳都是由碳元素和氧元素组成的 B、微粒观:保持金刚石化学性质的最小粒子是碳原子 C、转化观:氧化汞在一定条件下可生成金属汞 D、守恒观:4g氢气和16g氧气反应,应该生成20g水10. 在化学反应A +2B=C+2D中,已知B和C的相对分子质量之比为8∶11,当16 g A与一定量B恰好完全反应后,生成44 g C,则生成D的质量是( )A、36 g B、18 g C、4g D、48 g二、填空题
-
11. 为了预防“新冠肺炎”,各学校进行了全面消毒工作,为工作人员配发了84消毒液和过氧乙酸,84消毒液的有效成分为次氯酸钠,和空气中的二氧化碳反应会生成次氯酸( HClO)。(1)、标出次氯酸中氯元素的化合价:。(2)、利用过氧乙酸杀灭病毒,发生的是(选填“物理”或“化学”)变化。12. 即热盒饭是一种快餐食品,其加热原理有多种。
 (1)、如图中即热盒饭的加热材料是生石灰,加水后放热原理可用化学方程式表示为 , 该过程是将化学能转化为能。(2)、有一种新型的即热盒饭,它的底部有两层,一层存放水,:另一层存放镁、铁及氯化钠的混合物,使用时打开隔离层,在铁和氯化钠的作用下,镁与水能迅速发生反应,反应的化学方程式为 ,其中X的化学式为判断依据是13. 家庭小实验:将洗净的碎鸡蛋壳(主要成分是碳酸钙)放入小玻璃杯中,再加入适量的稀盐酸,观察到鸡蛋壳表面 , 该反应的化学方程式是 , 立即用蘸有澄清石灰水的玻璃片盖住,一会儿,便可观察到澄清石灰水 , 该反应的化学方程式是 .14. 2019年诺贝尔化学奖授予锂电池,对于现代人而言,这一高性能电池如同空气和水一般不可或缺。根据如图,回答下列问题:
(1)、如图中即热盒饭的加热材料是生石灰,加水后放热原理可用化学方程式表示为 , 该过程是将化学能转化为能。(2)、有一种新型的即热盒饭,它的底部有两层,一层存放水,:另一层存放镁、铁及氯化钠的混合物,使用时打开隔离层,在铁和氯化钠的作用下,镁与水能迅速发生反应,反应的化学方程式为 ,其中X的化学式为判断依据是13. 家庭小实验:将洗净的碎鸡蛋壳(主要成分是碳酸钙)放入小玻璃杯中,再加入适量的稀盐酸,观察到鸡蛋壳表面 , 该反应的化学方程式是 , 立即用蘸有澄清石灰水的玻璃片盖住,一会儿,便可观察到澄清石灰水 , 该反应的化学方程式是 .14. 2019年诺贝尔化学奖授予锂电池,对于现代人而言,这一高性能电池如同空气和水一般不可或缺。根据如图,回答下列问题: (1)、锂的相对原子质量为。(2)、上面结构示意图表示的粒子与锂原子的化学性质相似的是(填字母)。若在化合物中的化合价锂也与该元素类似,则碳酸锂的化学式为。(3)、锂电池可为新能源汽车提供动力,新能源汽车除了节约化石能源外,其主要优点是。
(1)、锂的相对原子质量为。(2)、上面结构示意图表示的粒子与锂原子的化学性质相似的是(填字母)。若在化合物中的化合价锂也与该元素类似,则碳酸锂的化学式为。(3)、锂电池可为新能源汽车提供动力,新能源汽车除了节约化石能源外,其主要优点是。三、综合题
-
15. 〖科普阅读理解〗

农药在农业生产中发挥着至关重要的作用,可以有效地防控农作物病虫害。但某些地区确实出现过农药残留超标事件,让一些人“谈药色变”。怎样科学地减少果蔬中的农药残留呢?
有些农药随着温度的升高,分解会加快。通过在沸水中焯或使用蒸、炒等烹饪手段可以去除蔬菜中氨基甲酸酯类农药的残留。
部分农药在空气中能够缓慢地分解为对人体无害的物质。所以对一些易于保存的农产品,如胡萝卜、南瓜、土豆等,可以在室外存放一定时间来减少农药残留量。有科研人员监测了番茄中三唑酮(C14H16ClN3O2)在温室大棚内和室外的分解规律,如图1。
去皮可以有效减少果蔬中的农药残留。但部分果蔬不容易去皮,如生菜、草莓、樱桃等,因此清洗成为了消费者去除农药残留的重要方式。由于大多数农药难溶于水,可利用洗菜机或加入洗涤盐等方式提高农药残留的去除效果,有人研究了利用不同方法去除黄瓜中嘧菌酯农药残留的效果,如图2所示。
可见,减少农药残留的关键是认识物质的性质。基于农药的不同性质,采用有针对性的方法来去除。
依据文章内容回答下列问题。
(1)、在沸水中焯蔬菜可以去除氨基甲酸酯类杀虫剂的残留,这是利用了氨基甲酸酯类的 (填“物理”或“化学”)性质。(2)、三唑酮C14H16ClN3O2由 种元素组成。(3)、依据图1,影响番茄中三唑酮残留量的因素有温度和 。(4)、为了最大量地去除黄瓜中的嘧菌酯,在清洗黄瓜时,应采用的方法是 。(5)、下列说法合理的是 (填字母序号)。A 为了防止农药在农产品中残留,必须全面禁止使用农药
B 采摘瓜果后,建议清洗干净再食用
C 削去果皮,也能减少农药残留
D 利用农药的某些物理和化学性质可以有效地减少农药残留量
16. 已知A、B、C、D、E是初中化学常见的五种物质。它们分别由C、H、O中的一种或几种元素组成,通常状况下A、B、C为气体,D、E为液体。“﹣”表示相连的两种物质能发生反应,“→”表示相连物质能向箭头所指一方转化,部分反应物、生成物及反应条件已省略。根据所学知识,回答下列问题: (1)、请写出E→C+D的化学方程式。(2)、自然界中,A→C可以通过实现。(3)、A和D反应的化学方程式是。(4)、①②③④四个反应中,一定是化合反应的是。(填序号)17. 为了探究物质在化学变化时,参加反应的反应物总质量与生成物总质量是否相等。某校甲、乙两个兴趣小组分别设计了如下的实验来验证自己的假设。
(1)、请写出E→C+D的化学方程式。(2)、自然界中,A→C可以通过实现。(3)、A和D反应的化学方程式是。(4)、①②③④四个反应中,一定是化合反应的是。(填序号)17. 为了探究物质在化学变化时,参加反应的反应物总质量与生成物总质量是否相等。某校甲、乙两个兴趣小组分别设计了如下的实验来验证自己的假设。(实验方案)

(查阅资料)①硫酸铜溶液是蓝色的,氢氧化铜是蓝色沉淀,硫酸铜溶液和氢氧化钾溶液反应生成氢氧化铜沉淀和硫酸钾;②碳酸钠溶液和稀盐酸反应生成氯化钠、水和二氧化碳。
(进行实验)如图所示,甲小组把盛有适量CuSO4溶液的小试管放入盛有KOH溶液的烧杯中,乙小组把盛有适量Na2CO3溶液的小试管放入盛有稀盐酸的烧杯中;然后将烧杯放到天平上,用砝码平衡;接着取下烧杯并将其倾斜,使试管同和烧杯内的两种溶液混合发生反应,待反应后再把烧杯放到天平上,观察天平是否平衡。根据要求,请回答:
(1)、(实验现象)甲小组的同学看到烧杯中有现象。
(2)、乙小组同学看到烧杯中有现象。反应后,乙小组的天平指针指向刻度盘的(选填“左边”、“右边”或“中间”)。(3)、(反思与评价)比较两个小组的实验设计,使用的试剂不变,若要验证质量守恒定律,应改进的是;由此,你将得出新的结论:探究或验证反应物与生成物的质量关系时,。18. 实验课上同学们在实验室制取二氧化碳时,错拿稀硫酸倒入盛有石灰石的试管中,发现产生气泡速度越来越慢。于是同学们展开探究。(1)、(查阅资料)石灰石与稀硫酸反应与稀盐酸反应非常相似,但是由于反应生成的硫酸钙微溶物会覆盖在石灰石的表面,阻碍了石灰石与稀硫酸的接触,反应会逐渐缓慢,因此通常不选用大理石与稀硫酸反应制取二氧化碳,请写出石灰石与稀硫酸反应的化学方程式。(2)、实验活动一 选择合适浓度的硫酸操作:室温下,用装有5mL硫酸溶液的注射器向盛有1g 直径为2mm石灰石的试管中注入不同浓度的稀硫酸,记录15分钟内生成气体的体积,观察现象,记录见表一。表一
试管编号
1
2
3
4
5
硫酸浓度(%)
15
20
25
30
35
气体体积( mL)
35
47
55
51
42
实验活动二 选择合适反应温度:
操作:在盛有1g直径约为2mm石灰石的试管中分别加入5mL相同合适浓度但温度不同的稀硫酸溶液,观察现象,记录见表二。
表二
试管编号
A
B
C
D
E
温度(℃)
40
50
60
70
80
现象和比较
有少量气泡
气泡比A试管多
气泡明显比B试管多
大量气泡产生,与常温用盐酸反应相似
反应激烈,迅速产生大量气泡
分析处理以上表中数据,可得出的结论有:①室温下,稀硫酸与大理石反应选用硫酸的浓度最合适为;
②当硫酸浓度一定时,反应速度与温度之间存在的关系是;其中最合适用于实验室制取二氧化碳的反应温度为。
 (3)、上述实验活动后有同学又进一步提出问题:化学反应速率还受什么因素影响?设计装置如图所示。本实验采用的方法是 , 装置中红墨水的作用是实验中可观察到 , 由此可得出的结论是。
(3)、上述实验活动后有同学又进一步提出问题:化学反应速率还受什么因素影响?设计装置如图所示。本实验采用的方法是 , 装置中红墨水的作用是实验中可观察到 , 由此可得出的结论是。四、计算题
-
19. 向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据关系图分析并计算:
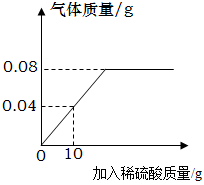 (1)、铁粉反应完时,产生氢气的质量为g。(2)、原稀硫酸中溶质的质量分数(写出计算过程)。
(1)、铁粉反应完时,产生氢气的质量为g。(2)、原稀硫酸中溶质的质量分数(写出计算过程)。