浙教版科学九上第二章 物质转化与材料利用 复习题
试卷更新日期:2021-08-11 类型:单元试卷
一、选择题(每题只有一个选项正确)
-
1. 下列各组物质中,前一种是混合物,后一种是化合物的是( )。A、石灰水和氯化钠 B、硫酸和氧气 C、铁粉和氢氧化钠 D、红磷和干冰2. 在进行物质分类时,下列各组物质中,后者包含在前者之中的一组是( )。A、混合物和化合物 B、含氧酸和酸 C、化合物和盐 D、可溶性碱和碱3. 在金属表面覆盖保护膜是普遍采用的金属防锈措施之一。下列自行车的防锈措施中,不属于覆盖保护膜的是( ) 。A、擦拭保洁 B、链条上油 C、轮圈镀铬 D、车架喷漆4. 下列物质的水溶液能使紫色石蕊试液变红的是( )。A、氢氧化钠 B、碳酸钠 C、生石灰 D、氯化氢5. 下图是表示气体微粒的示意图 ,图中“
 ”和“
”和“  ”分别表示不同元素的原子,其中表示的物质可能是氧化物的是( )。 A、
”分别表示不同元素的原子,其中表示的物质可能是氧化物的是( )。 A、 B、
B、 C、
C、 D、
D、 6. 某同学为确认所回收易拉罐的主要成分是铝还是铁,剪取金属片打磨后,设计了如图所示的两种不同方法进行检验。这样设计的依据是( ) 。
6. 某同学为确认所回收易拉罐的主要成分是铝还是铁,剪取金属片打磨后,设计了如图所示的两种不同方法进行检验。这样设计的依据是( ) 。 A、活泼金属易与氧气反应 B、铁与铝有不同的物理性质 C、排在氢前面的金属可以把酸中的氢置换出来 D、活动性较强的金属可把活动性较弱的金属从它的盐溶液中置换出来7. 下列制备物质的方案切实可行的是( )。A、用铜片和稀硫酸制取氢气 B、用铁和盐酸制备氯化铁 C、用块状石灰石和稀硫酸制取二氧化碳 D、用硫酸铜溶液和氢氧化钠溶液制备氢氧化铜8. 读碳和碳的化合物间的转化关系图,下列有关说法正确的是( )
A、活泼金属易与氧气反应 B、铁与铝有不同的物理性质 C、排在氢前面的金属可以把酸中的氢置换出来 D、活动性较强的金属可把活动性较弱的金属从它的盐溶液中置换出来7. 下列制备物质的方案切实可行的是( )。A、用铜片和稀硫酸制取氢气 B、用铁和盐酸制备氯化铁 C、用块状石灰石和稀硫酸制取二氧化碳 D、用硫酸铜溶液和氢氧化钠溶液制备氢氧化铜8. 读碳和碳的化合物间的转化关系图,下列有关说法正确的是( )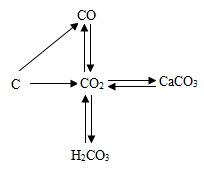 A、“C→CO”的反应中碳发生还原反应 B、“CO→CO2“的反应类型为置换反应 C、“CO2→CaCO3"的反应可用于检验二氧化碳 D、“CO2 H2CO3”的反应可用酚酞试液验证9. 如图是一个二氧化碳发生装置,下列评价错误的是( )。
A、“C→CO”的反应中碳发生还原反应 B、“CO→CO2“的反应类型为置换反应 C、“CO2→CaCO3"的反应可用于检验二氧化碳 D、“CO2 H2CO3”的反应可用酚酞试液验证9. 如图是一个二氧化碳发生装置,下列评价错误的是( )。 A、所用材料均为家庭废品,有较好的资源利用意识 B、使用碱石灰(主要成分为NaOH和生石灰)有利于得到干燥的二氧化碳气体 C、将石灰石放入铜丝网,拉起铜丝可使反应中止 D、要保证装置的气密性良好,方能使实验成功10. 下列各选项中,括号内物质是除去杂质所用的试剂(适量),其中错误的是( )。A、硫酸铜中混有氯化钠(AgNO3) B、铜粉中混有铁粉(HCI) C、氧气中混有二氧化碳(NaOH) D、氯化亚铁溶液中混有氯化铜(Fe)11. 将质量均为10克的Mg、Fe、Zn三种金属,分别放入质量和溶质质量分数均相同的三份稀硫酸中,下列各图表示反应完成后生成氢气的质量,其中不可能的是( )。A、
A、所用材料均为家庭废品,有较好的资源利用意识 B、使用碱石灰(主要成分为NaOH和生石灰)有利于得到干燥的二氧化碳气体 C、将石灰石放入铜丝网,拉起铜丝可使反应中止 D、要保证装置的气密性良好,方能使实验成功10. 下列各选项中,括号内物质是除去杂质所用的试剂(适量),其中错误的是( )。A、硫酸铜中混有氯化钠(AgNO3) B、铜粉中混有铁粉(HCI) C、氧气中混有二氧化碳(NaOH) D、氯化亚铁溶液中混有氯化铜(Fe)11. 将质量均为10克的Mg、Fe、Zn三种金属,分别放入质量和溶质质量分数均相同的三份稀硫酸中,下列各图表示反应完成后生成氢气的质量,其中不可能的是( )。A、 B、
B、 C、
C、 D、
D、 12. 如图所示,分别向甲,乙两支试管中加入形状和大小完全相同的铁片,再向甲中加入植物油,U形玻璃管内为红墨水(开始时两端液面相平),塞上橡皮塞后,放置一段时间。下列说法错误的是( )。
12. 如图所示,分别向甲,乙两支试管中加入形状和大小完全相同的铁片,再向甲中加入植物油,U形玻璃管内为红墨水(开始时两端液面相平),塞上橡皮塞后,放置一段时间。下列说法错误的是( )。 A、植物油用于隔绝氧气和水 B、甲试管中铁片比乙试管中铁片不易生锈 C、U形玻璃管两端的液面变为右低左高 D、U形玻璃管两端的液面变为左低右高
A、植物油用于隔绝氧气和水 B、甲试管中铁片比乙试管中铁片不易生锈 C、U形玻璃管两端的液面变为右低左高 D、U形玻璃管两端的液面变为左低右高二、简答题
-
13. 下列物质:①石墨;②食盐;③甲烷;④千冰;⑤空气;⑥熟石灰;⑦高锰酸钾;⑧水银,指出其类别,并将物质的序号填写在各类别的横线上。
混合物:;单质:;非金属氧化物:;盐:;有机物:;碱: 。
14. 某化工厂在三废处理中采取以下措施,请写出有关反应的化学方程式。(1)、用氢氧化钠吸收含二氧化硫的尾气:。(2)、用铁屑处理含汞盐( HgSO4)的废水:。15. 填写除去下列物质中少量杂质所选用的试剂名称,并用化学方程式表示相应的过程。物质
杂质
试剂
化学方程式
①
KCl
FeCl3
②
HCl
H2SO4
③
Cu(NO3)2
Hg(NO3)2
16. 硫酸钡不容易被X射线透过,在医疗上可用作检查肠胃的内服剂,俗称“钡餐"。某同学将硫酸镁溶液滴入硝酸钡[Ba(NO3)2]溶液中得到硫酸钡,右图表示该实验过程中溶液总质量随加入硫酸镁溶液质量的变化情况。图像AB段对应的实验现象是 , C点处溶液中的溶质有。 17. 现有A、B、C三种物质,已知A为一种氯化物,B为一种钠盐,C为一种碱。如图表示无明显现象的是A、B、C的溶液两两反应的实验现象。
17. 现有A、B、C三种物质,已知A为一种氯化物,B为一种钠盐,C为一种碱。如图表示无明显现象的是A、B、C的溶液两两反应的实验现象。请根据有关实验现象回答下列问题。
 (1)、A物质为 , D物质为。(2)、B和C反应的化学方程式:。(3)、A溶液与洁净的铁丝反应的化学方程式: 。
(1)、A物质为 , D物质为。(2)、B和C反应的化学方程式:。(3)、A溶液与洁净的铁丝反应的化学方程式: 。三、实验探究题
-
18. 某科学兴趣小组为研究不同金属跟稀硫酸反应的快慢,将甲、乙、丙、丁四种金属片分别与相同体积、相同溶质质量分数的稀硫酸反应,观察30秒内产生的氢气泡的多少,记录在下表中。(“+”越多表示产生的气泡越多)
金属
甲
乙
丙
丁
氢气泡的多少
++
++++
+++
+
(1)、从实验结果可看出,甲、乙、丙、丁四种金属与稀硫酸反应由快到慢的顺序是。(2)、要获得令人信服的实验结论,除了稀硫酸的体积和溶质质量分数必须相同外,4种金属的也必须相同。19. 废旧金属可以回收利用,用合金废料(含Fe、Cu)制取FeSO4和CusO4溶液的实验流程如下(部分生成物省略): (1)、合金属于(填“纯净物“或“混合物”)。(2)、由Cu制取CuSO4溶液有以下两种途径:
(1)、合金属于(填“纯净物“或“混合物”)。(2)、由Cu制取CuSO4溶液有以下两种途径:Ⅰ.Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O
Ⅱ.2Cu+O2 2CuO CuO+H2SO4=CuSO4+H2O
从两种途径可以看出,通常情况下不反应的两种物质,在改变和后,也可以发生反应。相对于第二种方法,第一种方法的不足之处是 , (写两点)。
20. 工业生产常用“苛化法”制取氢氧化钠,其原料为碳酸钠、石灰乳[由Ca(OH)2和水组成的混合物],反应流程如图所示。某科学兴趣小组模拟图中的流程,在实验室中制备氢氧化钠。请回答下列问题。 (1)、实验室“操作1”的名称是 , 需要用到下列器材中的(填字母)。
(1)、实验室“操作1”的名称是 , 需要用到下列器材中的(填字母)。 (2)、制备氢氧化钠的化学方程式为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓。将53克溶质质量分数为20%的碳酸钠溶液与17克石灰乳混合,若二者恰好完全反应,计算所得氢氧化钠溶液的溶质质量分数。(写出计算过程,计算结果精确到0.1% )
(2)、制备氢氧化钠的化学方程式为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓。将53克溶质质量分数为20%的碳酸钠溶液与17克石灰乳混合,若二者恰好完全反应,计算所得氢氧化钠溶液的溶质质量分数。(写出计算过程,计算结果精确到0.1% )