四川省巴中市巴州区2021年中考化学模拟试卷
试卷更新日期:2021-08-10 类型:中考模拟
一、单选题
-
1. 诗词是民族灿烂文化的瑰宝,下列著名诗句中隐含有化学变化的是( )
①千里冰封,万里雪飘
②落红不是无情物,化作春泥更护花
③野火烧不尽,春风吹又生
④粉身碎骨浑不怕,要留清白在人间
⑤夜来风雨声,花落知多少
A、②③④ B、①②③ C、③④⑤ D、②③⑤2. 我国的高铁以安全、速度快闻名世界。高铁在建造时使用了大量的新材料,下列属于金属材料的是( )A、生产高铁车头的玻璃钢 B、制造高铁车身的镁铝合金 C、制造轨道枕木的聚氨酯材料 D、建筑高铁路基的钢筋混凝土3. 实验是学习化学的重要手段,下列实验操作正确的是( )A、 过滤操作
B、
过滤操作
B、 加热固体
C、
加热固体
C、 稀释浓硫酸
D、
稀释浓硫酸
D、 检查气密性)
4. 下列对某一主题的知识归纳,有错误的是( )
检查气密性)
4. 下列对某一主题的知识归纳,有错误的是( )A.化学与安全
B.化学与健康
重金属中毒﹣﹣喝鲜牛奶、豆浆等解毒
煤气泄漏﹣﹣关闭气阀、严禁烟火
糖类、油脂﹣﹣组成元素相同
缺铁﹣﹣会引发缺铁性贫血
C.化学与生活
D.化学与材料
蛋白质、淀粉﹣﹣用碘溶液来鉴别
纯棉织物、纯毛织物﹣﹣用灼烧闻气味来鉴别
水泥、玻璃﹣﹣都属于无机非金属材料
玻璃钢、铝合金﹣﹣都属于复合材料
A、A B、B C、C D、D5. 2021年第29届119消防安全日主题口号是“提高消防安全意识,增强自救互助能力。”下列场所挂的图标与“消防安全”不相符的是( )A、 B、
B、 C、
C、 D、
D、 6. 2020年初我国突发“新型冠状病毒肺炎”疫情,严重危害人体健康。为防治“新冠肺炎”,可用漂白粉对公共场所进行消毒。漂白粉的有效成分是次氯酸钙(化学式为Ca(ClO)2),次氯酸钙可发生如下反应: 。下列说法正确的是( )A、X的化学式为CO B、次氯酸钙中氯元素的化合价为+1 C、X由离子构成 D、HClO的相对分子质量为527. 如图是 A、B、C三种物质的溶解度曲线,下列说法正确的是( )
6. 2020年初我国突发“新型冠状病毒肺炎”疫情,严重危害人体健康。为防治“新冠肺炎”,可用漂白粉对公共场所进行消毒。漂白粉的有效成分是次氯酸钙(化学式为Ca(ClO)2),次氯酸钙可发生如下反应: 。下列说法正确的是( )A、X的化学式为CO B、次氯酸钙中氯元素的化合价为+1 C、X由离子构成 D、HClO的相对分子质量为527. 如图是 A、B、C三种物质的溶解度曲线,下列说法正确的是( ) A、t2℃时,将 A 和 C的混合溶液(两者均已达到饱和)降温到t1℃,析出的晶体含有 A 和 C B、t2℃时,A,B,C三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数的大小关系是B>A=C C、从混有少量B的A物质中提纯得到较纯净的A,可通过冷却它的热饱和溶液实现 D、t1℃时,要配制A的饱和溶液,只需要量筒、烧杯、胶头滴管三种玻璃仪器8. 鉴别下列各组物质,所选试剂或方法正确的是( )A、硬水和软水:分别滴在玻璃片上烘干,看有无固体留下 B、浓盐酸和浓硫酸:打开瓶盖,看试剂瓶口是否出现白烟 C、氯化铵和氯化钾:加入熟石灰研磨,看能否产生刺激性气味 D、硝酸银溶液和硫酸钠溶液:滴加氯化钡溶液,看是否有沉淀产生9. 下图是某反应的微观示意图。下列说法错误的是()
A、t2℃时,将 A 和 C的混合溶液(两者均已达到饱和)降温到t1℃,析出的晶体含有 A 和 C B、t2℃时,A,B,C三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数的大小关系是B>A=C C、从混有少量B的A物质中提纯得到较纯净的A,可通过冷却它的热饱和溶液实现 D、t1℃时,要配制A的饱和溶液,只需要量筒、烧杯、胶头滴管三种玻璃仪器8. 鉴别下列各组物质,所选试剂或方法正确的是( )A、硬水和软水:分别滴在玻璃片上烘干,看有无固体留下 B、浓盐酸和浓硫酸:打开瓶盖,看试剂瓶口是否出现白烟 C、氯化铵和氯化钾:加入熟石灰研磨,看能否产生刺激性气味 D、硝酸银溶液和硫酸钠溶液:滴加氯化钡溶液,看是否有沉淀产生9. 下图是某反应的微观示意图。下列说法错误的是() A、甲中氢、硫元素的质量比为1:16 B、反应后硫元素的化合价为+4 C、参加反应的甲、乙分子个数比为1:2 D、反应后分子总数减少10. 下列对氢氧化钠变质情况进行探究的相关实验,其中合理的是( )
A、甲中氢、硫元素的质量比为1:16 B、反应后硫元素的化合价为+4 C、参加反应的甲、乙分子个数比为1:2 D、反应后分子总数减少10. 下列对氢氧化钠变质情况进行探究的相关实验,其中合理的是( )序号
实验目的
实验过程
①
证明变质
取少量溶液,滴加盐酸,将生成的气体通入澄清的石灰水中
②
确定成分
取少量溶液,加入澄清的石灰水,过滤,向滤液中滴加酚酞溶液
③
测定纯度
取一定量溶液,加入盐酸,用澄清的石灰水吸收气体,称量装置增重
④
除去杂质
取溶液,滴加澄清的石灰水至恰好完全反应,过滤
A、②④ B、②③ C、①③ D、①④11. 下列图像与相应的文字描述相符的是( )A、 甲图表示一定温度时,向一定量的饱和石灰水中加入生石灰
B、
甲图表示一定温度时,向一定量的饱和石灰水中加入生石灰
B、 乙图反映了某个化合反应中各物质质量与时间的关系
C、
乙图反映了某个化合反应中各物质质量与时间的关系
C、 丙图表示等质量的锌和铁与等质量、等溶质质量分数的稀硫酸(足量)的反应
D、
丙图表示等质量的锌和铁与等质量、等溶质质量分数的稀硫酸(足量)的反应
D、 丁图表示向硫酸和硫酸镁的混合溶液中加氢氧化钠溶液至过量
12. 2019年10月1日,我国举行了盛大的国庆70周年阅兵活动,其中空中梯队飞过天安门上空时,拉出一条彩色烟带,产生烟带的药品除燃料外还有锌、氯化铵、三硫化二锑等。下图是锑元素在周期表的信息,下列说法正确的是( )
丁图表示向硫酸和硫酸镁的混合溶液中加氢氧化钠溶液至过量
12. 2019年10月1日,我国举行了盛大的国庆70周年阅兵活动,其中空中梯队飞过天安门上空时,拉出一条彩色烟带,产生烟带的药品除燃料外还有锌、氯化铵、三硫化二锑等。下图是锑元素在周期表的信息,下列说法正确的是( ) A、锑属于非金属元素 B、锑的相对原子质量为121.8g C、锑原子的中子数为51 D、三硫化二锑的化学式为Sb2S313. 下列各组物质的溶液,不用其他试剂,无法将其一一区别的是( )A、HCl、Ba(NO3)2、KCl、Na2CO3 B、H2SO4、NaOH、Ba(OH)2、CuSO4 C、BaCl2、Na2SO4、K2CO3、NaNO3 D、HNO3、AgNO3、NaNO3、K2CO314. 验证铝、铜、银的金属活动性强弱,小明设计了以下四组实验,下列说法错误的是( )
A、锑属于非金属元素 B、锑的相对原子质量为121.8g C、锑原子的中子数为51 D、三硫化二锑的化学式为Sb2S313. 下列各组物质的溶液,不用其他试剂,无法将其一一区别的是( )A、HCl、Ba(NO3)2、KCl、Na2CO3 B、H2SO4、NaOH、Ba(OH)2、CuSO4 C、BaCl2、Na2SO4、K2CO3、NaNO3 D、HNO3、AgNO3、NaNO3、K2CO314. 验证铝、铜、银的金属活动性强弱,小明设计了以下四组实验,下列说法错误的是( )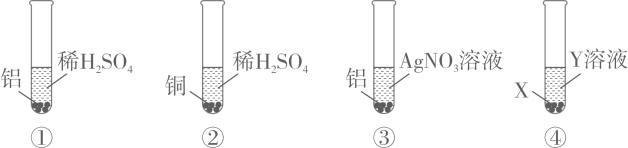 A、通过①②实验,可以证明金属活动性Al>Cu B、通过①②③实验,可以证明金属活动性Al>Cu>Ag C、若要用实验④证明金属活动性Al>Cu,X可以为Al,Y为CuSO4溶液 D、若要用实验④证明金属活动性Cu>Ag,X可以为Cu,Y为AgNO3溶液15. 下列除去杂质所选用的方法正确的是( )
A、通过①②实验,可以证明金属活动性Al>Cu B、通过①②③实验,可以证明金属活动性Al>Cu>Ag C、若要用实验④证明金属活动性Al>Cu,X可以为Al,Y为CuSO4溶液 D、若要用实验④证明金属活动性Cu>Ag,X可以为Cu,Y为AgNO3溶液15. 下列除去杂质所选用的方法正确的是( )选项
物质
杂质
除杂方法
A
O2
CO2
点燃
B
Cu(OH)2固体
NaOH固体
加足量水搅拌,过滤,洗涤,干燥
C
NaOH溶液
Na2CO3
加入过量稀盐酸
D
银粉
锌粉
加入过量硫酸亚铁溶液
A、A B、B C、C D、D16. 在24.9g Ca(OH)2、CaCl2、CaCO3的混合固体中,测得钙元素和碳元素的质量比为30:7,将160.0g稀盐酸加入该固体中,固体全部溶解得到177.2g溶液。则该混合固体中钙元素的质量为( )A、2.1g B、7.7g C、9.0g D、17.2g二、填空题
-
17. 二氧化硅(SiO2)可用于制造分离膜,利用“膜分离”技术二氧化碳被氨水吸收转化为可做氮肥的碳酸氢铵(NH4HCO3)。(1)、SiO2中硅元素的化合价为;(2)、保持二氧化碳化学性质的最小粒子是(填具体粒子名称);(3)、铵根离子的符号;(4)、分析过氧化氢(H2O2)和过氧化钠(Na2O2)中氧元素的化合价,可写出过氧化钙的化学式为。18. 化学与生活、科技息息相关。请填写下列空格(1)、第24届冬奥会将于2022年2月在北京和张家口举行。冰上运动场馆外墙将铺设新型塑料聚氟乙烯膜[(C2H2F2)n],该材料属于(填“金属材料”或“有机合成材料”)。(2)、我国“可燃冰”开采技术世界领先,将“可燃冰”进行二次能源开发意义重大。甲烷和水在一定条件下可制备合成气(主要成分是一氧化碳和氢气),该反应的化学方程式为。(3)、水是宝贵的自然资源,是人类生命之源。对工农业生产和人类生活具有重要作用。近年来党和政府非常重视人们饮水安全,为城乡人民饮用“安全水”,我市投巨资建设红鱼洞水库。

①蒸馏水、矿泉水、白醋、酒精都是常见的无色液体,其中白醋具有酸味,酒精具有特殊气味,常被称为绿色能源。另外两种无色液体可用多种方法区分,例如:加入 , 根据产生泡沫的多少来区分
②将浑浊的河水用简易净水器进行净化(如图),净化后得到的水属于(填“纯净物”或“混合物”)。
(4)、高考是百姓的头等大事,很多父母为了表示重视,积极为孩子准备一些菜谱为他们加油打气。某考生家长为孩子准备了一份“黑椒牛柳”高考午餐:米饭,黑椒牛柳,蘑菇烧肉,蒜蓉茼蒿叶,西红柿鸡蛋汤。其中富含蛋白质的是。19. 某反应的表达式为:X(单质)+Y(化合物)→甲(单质)+乙(化合物),完成下列填空。(1)、该反应的基本反应类型是反应(2)、若Y的溶液为蓝色,甲为红色固体单质,其反应的化学方程式可能为(3)、若XY均为黑色固体,甲是年产量最高的金属,该反应的化学方程式可以是(4)、若甲是最轻的气体,则Y的化学式可能是三、综合题
-
20. 结合下列实验装置图,回答有关问题:
 (1)、仪器b的名称为。(2)、实验室用高锰酸钾制取氧气应选择的发生装置是(填字母),该反应的化学方程式为。(3)、实验室取二氧化碳,用到的药品是稀盐酸和 , 应选择的发生装置 , 若要得到干燥的二氧化碳,应在装置D中盛放试剂(填试剂名称),并把气体从端通入。(4)、用E收集二氧化碳,从③端通入,请把装置图补画齐全。
(1)、仪器b的名称为。(2)、实验室用高锰酸钾制取氧气应选择的发生装置是(填字母),该反应的化学方程式为。(3)、实验室取二氧化碳,用到的药品是稀盐酸和 , 应选择的发生装置 , 若要得到干燥的二氧化碳,应在装置D中盛放试剂(填试剂名称),并把气体从端通入。(4)、用E收集二氧化碳,从③端通入,请把装置图补画齐全。 21. 某NaCl溶液中含有少量的MgCl2、CaCl2和Na2SO4杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按如图所示流程对其进行除杂。
21. 某NaCl溶液中含有少量的MgCl2、CaCl2和Na2SO4杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按如图所示流程对其进行除杂。
回答下列问题:
(1)、实验Ⅰ中加入试剂A除去的杂质是。(2)、实验Ⅱ中加入的试剂B是溶液。(3)、写出实验Ⅲ中发生的中和反应的化学方程式:。22. 某校化学兴趣小组在探究“酸碱盐的相关性质”时,做了如图一所示的两个实验,实验结束后,小组同学将两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示)观察到有气泡产生,为确认烧杯内溶液中溶质的成分,同学们进行了如下探究。 (1)、(查阅资料)Na2SO4溶液、NaCl溶液呈中性。
(1)、(查阅资料)Na2SO4溶液、NaCl溶液呈中性。(提出猜想)猜想1:Na2SO4、NaCl;
猜想2:Na2SO4、NaCl和;
猜想3:Na2SO4、NaCl和H2SO4;
猜想4:Na2SO4、NaCl、H2SO4和Na2CO3。
(2)、(交流讨论)小强同学认为猜想4一定是错误的,他的理由是(用化学方程式表示)。(3)、(进行实验)小明同学设计如下两个实验方案:实验步骤
实验现象
实验结论
方案一
取少量烧杯中的溶液于洁净的试管中,加入几滴紫色石蕊溶液
猜想3正确
方案二
取少量烧杯中的溶液于洁净的试管中,加入少量铁粉
请写出方案二中有关反应的化学方程式。
(4)、(反思与总结)分析反应后溶液中溶质成分,除要考虑生成物外,还需考虑。四、计算题
-
23. 某粗盐中除NaCl以外还含有少量杂质MgCl2 , 为了测定粗盐中MgCl2的质量分数。取固体样品50.0g完全溶解于150.0g水中,并向其中逐渐加入一定浓度的NaOH溶液,实验过程中生成沉淀的质量与加入NaOH溶液的质量的关系如图所示:

注:发生反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl
请根据相关信息完成下列计算:
(1)、反应完全时,生成氢氧化镁的质量为g;(2)、在粗盐中氯化镁的质量分数;(3)、恰好完全反应时得到的溶液中溶质的质量分数。