黑龙江省哈尔滨香坊区2021年中考化学二模试卷
试卷更新日期:2021-08-09 类型:中考模拟
一、单选题
-
1. 哈尔滨市北门街高架桥正在建设中,下列有关说法错误的是( )
 A、建高架桥用的钢筋属于金属材料 B、高架桥建成后,交通将更加便捷 C、桥两边铁栏杆上刷漆可以起到防锈的作用 D、桥上路灯照明时的能量转化是化学能转化为电能2. 下列过程中没有发生化学变化的是( )A、钢轨锈蚀
A、建高架桥用的钢筋属于金属材料 B、高架桥建成后,交通将更加便捷 C、桥两边铁栏杆上刷漆可以起到防锈的作用 D、桥上路灯照明时的能量转化是化学能转化为电能2. 下列过程中没有发生化学变化的是( )A、钢轨锈蚀 B、燃放烟花
B、燃放烟花  C、冰山融化
C、冰山融化  D、火力发电
D、火力发电  3. 下列实验操作错误的是( )A、读取液体体积
3. 下列实验操作错误的是( )A、读取液体体积 B、检查装置气密性
B、检查装置气密性  C、倾倒二氧化碳气体
C、倾倒二氧化碳气体  D、检验氢气纯度
D、检验氢气纯度  4. 下列实验现象描述错误的是( )A、—氧化碳燃烧:无色气体燃烧,产生蓝色火焰,放热 B、铁钉与硫酸铜溶液反应:银白色固体表面有紫红色固体生成,溶液由浅绿色变为蓝色 C、硫酸铁溶液与氢氧化钠溶液反应:溶液中产生红褐色沉淀 D、向稀盐酸中滴加紫色石蕊溶液:石蕊溶液由紫色变为红色5. 下列物质的用途错误的是( )A、聚乙烯用作电线外皮
4. 下列实验现象描述错误的是( )A、—氧化碳燃烧:无色气体燃烧,产生蓝色火焰,放热 B、铁钉与硫酸铜溶液反应:银白色固体表面有紫红色固体生成,溶液由浅绿色变为蓝色 C、硫酸铁溶液与氢氧化钠溶液反应:溶液中产生红褐色沉淀 D、向稀盐酸中滴加紫色石蕊溶液:石蕊溶液由紫色变为红色5. 下列物质的用途错误的是( )A、聚乙烯用作电线外皮 B、钛合金用来制造人造骨
B、钛合金用来制造人造骨  C、氧气用于气焊
C、氧气用于气焊  D、大理石用作建筑材料
D、大理石用作建筑材料  6. 下列有关说法或做法正确的是( )A、蚊虫叮咬后涂抹氢氧化钠溶液止痒 B、用钢丝球擦拭铝制品表面使之光亮 C、室内起火,立即打开门窗大声呼救 D、堆放杂物的纸箱着火,用水浇灭7. 下列应用、相应原理(用化学方程式表示)及基本反应类型都正确的是( )A、高炉炼铁: 还原反应 B、检验二氧化碳: 复分解反应 C、证明铜的金属活动性比银强: 置换反应 D、酒精燃烧: 氧化反应8. 下列有关叙述错误的是( )A、张青莲为相对原子质量的测定做出卓越贡献 B、阿伏加德罗创立了原子论 C、人体内碘元素缺乏或过量都会引起甲状腺肿大 D、人体胃液正常的pH范围是0.9~1.59. “珍爱生命,远离毒品”。冰毒是一种毒品,其主要成分是甲基苯丙胺(化学式为C10H15N),有关甲基苯丙胺的说法正确的是( )A、甲基苯丙胺由碳、氢、氮三种元素构成 B、甲基苯丙胺属于有机高分子化合物 C、甲基苯丙胺分子中含有26个原子核 D、甲基苯丙胺中碳、氢、氮原子个数比为10:15:110. 下列有关资源或能源的叙述正确的是( )A、铁是人类最早使用的金属 B、空气中稀有气体的质量分数约为0.96% C、煤、石油、天然气属于化石燃料 D、地球上可利用的淡水资源约占全球水储量的2.53%11. 下列相关事实用微观粒子的知识解释正确的是( )
6. 下列有关说法或做法正确的是( )A、蚊虫叮咬后涂抹氢氧化钠溶液止痒 B、用钢丝球擦拭铝制品表面使之光亮 C、室内起火,立即打开门窗大声呼救 D、堆放杂物的纸箱着火,用水浇灭7. 下列应用、相应原理(用化学方程式表示)及基本反应类型都正确的是( )A、高炉炼铁: 还原反应 B、检验二氧化碳: 复分解反应 C、证明铜的金属活动性比银强: 置换反应 D、酒精燃烧: 氧化反应8. 下列有关叙述错误的是( )A、张青莲为相对原子质量的测定做出卓越贡献 B、阿伏加德罗创立了原子论 C、人体内碘元素缺乏或过量都会引起甲状腺肿大 D、人体胃液正常的pH范围是0.9~1.59. “珍爱生命,远离毒品”。冰毒是一种毒品,其主要成分是甲基苯丙胺(化学式为C10H15N),有关甲基苯丙胺的说法正确的是( )A、甲基苯丙胺由碳、氢、氮三种元素构成 B、甲基苯丙胺属于有机高分子化合物 C、甲基苯丙胺分子中含有26个原子核 D、甲基苯丙胺中碳、氢、氮原子个数比为10:15:110. 下列有关资源或能源的叙述正确的是( )A、铁是人类最早使用的金属 B、空气中稀有气体的质量分数约为0.96% C、煤、石油、天然气属于化石燃料 D、地球上可利用的淡水资源约占全球水储量的2.53%11. 下列相关事实用微观粒子的知识解释正确的是( )选项
事实
解释
A
盐酸和硫酸具有相似的化学性质
溶液中含有氢元素
B
氯化钠溶液导电
溶液中有大量自由移动的电子
C
有机物的性质有很大差异
原子排列方式不同
D
CO有毒性,而CO2无毒
原子结构不同
A、A B、B C、C D、D12. 实验室区分下列物质的两神实验方案都合理的是( )选项
A
B
C
D
物质
黄金和18K黄金
呼出的气体和吸入的空气
碳酸氢铵和尿素
硬水和软水
第一方案
灼烧
伸入燃着的木条
闻气味
观察颜色
第二方案
观察颜色
滴加等量的澄清石灰水
加水溶解
加入肥皂水
A、A B、B C、C D、D13. 如图为甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下 列有关说法中错误的是() A、60℃时,100g甲溶液中含甲物质的质量小于60g B、40℃时,等质量甲、乙饱和溶液中含溶质的质量相等 C、50℃时,甲物质的溶解度大于乙物质的溶解度 D、60℃时,将甲、乙两种物质的饱和溶液分别降温至40℃,析出晶体的质量甲大于乙14. 除去下列各物质中少量杂质,所选用的试剂和操作方法都正确的是( )
A、60℃时,100g甲溶液中含甲物质的质量小于60g B、40℃时,等质量甲、乙饱和溶液中含溶质的质量相等 C、50℃时,甲物质的溶解度大于乙物质的溶解度 D、60℃时,将甲、乙两种物质的饱和溶液分别降温至40℃,析出晶体的质量甲大于乙14. 除去下列各物质中少量杂质,所选用的试剂和操作方法都正确的是( )选项
物质(杂质)
试剂
操作方法
A
CO2(CO)
足量氧化铜
通过灼热的氧化铜
B
CaO(CaCO3)
足量稀盐酸
蒸发
C
KCl(KClO3)
少量二氧化锰
加热
D
CuO(C)
无
隔绝空气加热至高温
A、A B、B C、C D、D15. 向氧化铁和氧化亚铁的固体混合物中加入一定量的稀硫酸,恰好完全反应,得到100g含硫元素6.4%的溶液,将反应后的溶液蒸干得到24g固体,则原固体混合物中氧元素的质量分数为( )A、32% B、20% C、40% D、60%二、填空题
-
16. “端午节”吃粽子、吃鸡蛋。包粽子需要准备:糯米、瘦肉、红枣、红豆等食材。请回答问题:
 (1)、鸡蛋和瘦肉富含的营养素(水除外)的作用:是构成的基本物质,是机体生长和的主要原料。(2)、粽叶中含有大量的叶绿素。粽叶生长过程中需要适量施加氮肥,氮肥有促进植物 , 叶色浓绿,提高植物含量的作用。(3)、家庭用天然气作燃料煮饭,天然气主要成分化学式为。从柴草、树木到煤,再到天然气,家庭燃料的变迁体现了社会的发展。为了节约燃料、减少污染,人们将煤制成蜂窝煤,增大了 , 从而达到使煤充分燃烧的目的。17. 2021年4月29日,中国空间站“天和”核心舱搭载长征五号B遥二运载火箭升空。长征五号B遥二运载火箭是我国首型“一级半”火箭,它采用无毒无污染的液氧、液氢和煤油作为推进剂。请回答问题:
(1)、鸡蛋和瘦肉富含的营养素(水除外)的作用:是构成的基本物质,是机体生长和的主要原料。(2)、粽叶中含有大量的叶绿素。粽叶生长过程中需要适量施加氮肥,氮肥有促进植物 , 叶色浓绿,提高植物含量的作用。(3)、家庭用天然气作燃料煮饭,天然气主要成分化学式为。从柴草、树木到煤,再到天然气,家庭燃料的变迁体现了社会的发展。为了节约燃料、减少污染,人们将煤制成蜂窝煤,增大了 , 从而达到使煤充分燃烧的目的。17. 2021年4月29日,中国空间站“天和”核心舱搭载长征五号B遥二运载火箭升空。长征五号B遥二运载火箭是我国首型“一级半”火箭,它采用无毒无污染的液氧、液氢和煤油作为推进剂。请回答问题: (1)、煤油是炼制出的一种产品,炼制时利用各成分沸点不同将各成分分离,该过程属于变化。(2)、火箭整流罩一般为“蚌壳式”结构,整流罩各部件用到了铝合金、不锈钢、玻璃钢等,其中属于复合材料的是。在功能不变的前提下,火箭的某些部件最大化的使用铝合金代替玻璃钢,减轻了火箭自身重量,由此信息可知,铝合金具有的一点优良性能是(填字母)。
(1)、煤油是炼制出的一种产品,炼制时利用各成分沸点不同将各成分分离,该过程属于变化。(2)、火箭整流罩一般为“蚌壳式”结构,整流罩各部件用到了铝合金、不锈钢、玻璃钢等,其中属于复合材料的是。在功能不变的前提下,火箭的某些部件最大化的使用铝合金代替玻璃钢,减轻了火箭自身重量,由此信息可知,铝合金具有的一点优良性能是(填字母)。A.抗腐蚀性强 B.密度小 C.硬度大
(3)、工业上通过电解氧化铝的方法制得金属铝,同时生成一种常见的气体单质。请写出该反应的化学方程式。三、综合题
-
18. 质量守恒定律的发现,对化学的发展作出了重要贡献。图一是某反应中固体物质质量变化情况,图二是某反应的微观过程。请回答问题:
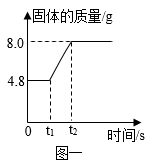
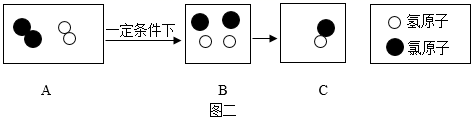 (1)、符合图一的化学反应是______(填字母)。A、2Mg+O2 2MgO B、Fe+CuSO4=FeSO4+Cu C、2Cu+O2 2CuO(2)、在图二中将C图粒子图形补充完整。(3)、图二中B到C变化的微观实质是 , 该变化中发生改变的粒子是(填粒子名称)。19. 分类、类比是初中化学常用的学习方法。(1)、设计化学实验时除了考虑能否达到实验目的外,还要考虑“实验安全、对环境的影响、节约药品”等因素。据此,我们可以将实验A与实验(填字母)归为一类,分类依据是。
(1)、符合图一的化学反应是______(填字母)。A、2Mg+O2 2MgO B、Fe+CuSO4=FeSO4+Cu C、2Cu+O2 2CuO(2)、在图二中将C图粒子图形补充完整。(3)、图二中B到C变化的微观实质是 , 该变化中发生改变的粒子是(填粒子名称)。19. 分类、类比是初中化学常用的学习方法。(1)、设计化学实验时除了考虑能否达到实验目的外,还要考虑“实验安全、对环境的影响、节约药品”等因素。据此,我们可以将实验A与实验(填字母)归为一类,分类依据是。



A.在通风橱中进行
B.将试管换成白瓷板
C.集气瓶底部铺水
D.装置右侧加一个酒精灯
(2)、已知氨水(NH3·H2O)是一种可溶性碱,在水中能解离出 和OH-。请写出氨水与硫酸发生中和反应的化学方程式 , 氨水中氮元素的化合价是。20. 请根据下列实验装置回答问题: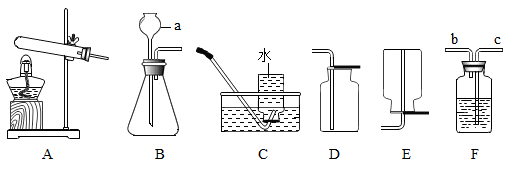 (1)、仪器a的名称。(2)、写出实验室用装置A加热固体混合物制取氧气的化学方程式。(3)、制取氧气时,首先要检查装置气密性:连接仪器,将浸入水中,用手握住试管,观察到 , 证明装置气密性良好。原理是:手握试管,试管内 , 大于外界气压,在压强差的作用下产生上述现象。(4)、实验室制取二氧化碳选择的装置是(填字母),制得的二氧化碳气体中常混有少量水蒸气,可选用F装置除去水蒸气,则F装置中盛装的药品名称是 , 气体应从F装置的口(填“b”或“c”)通入。21. A、B、C、D、E是初中化学常见的五种物质,分别为酸、碱、盐、氧化物、单质中的一种。其中A为蓝色溶液,常用于配制波尔多液,A与C发生复分解反应生成两种沉淀,E为红棕色固体,用“→”表示一种物质可以通过化学反应转化为另一种物质,“一”相连的两种物质 能够发生化学反应。请回答问题:
(1)、仪器a的名称。(2)、写出实验室用装置A加热固体混合物制取氧气的化学方程式。(3)、制取氧气时,首先要检查装置气密性:连接仪器,将浸入水中,用手握住试管,观察到 , 证明装置气密性良好。原理是:手握试管,试管内 , 大于外界气压,在压强差的作用下产生上述现象。(4)、实验室制取二氧化碳选择的装置是(填字母),制得的二氧化碳气体中常混有少量水蒸气,可选用F装置除去水蒸气,则F装置中盛装的药品名称是 , 气体应从F装置的口(填“b”或“c”)通入。21. A、B、C、D、E是初中化学常见的五种物质,分别为酸、碱、盐、氧化物、单质中的一种。其中A为蓝色溶液,常用于配制波尔多液,A与C发生复分解反应生成两种沉淀,E为红棕色固体,用“→”表示一种物质可以通过化学反应转化为另一种物质,“一”相连的两种物质 能够发生化学反应。请回答问题: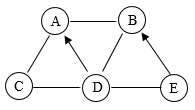 (1)、写出C、E的化学式:C,E。(2)、足量D与粉末状B反应的实验现象。(3)、写出A与C反应的化学方程式。
(1)、写出C、E的化学式:C,E。(2)、足量D与粉末状B反应的实验现象。(3)、写出A与C反应的化学方程式。四、计算题
-
22. 为了测定黄铜样品中铜的质量分数,某化学小组的同学们进行了如下实验:
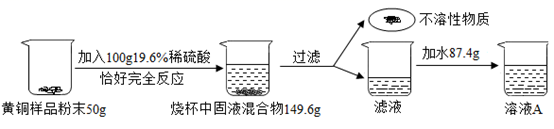 (1)、发生反应的化学方程式为。(2)、用98%的浓硫酸配制100g质量分数19.6%的稀硫酸,需要浓硫酸与水的质量比为。(3)、根据已知条件列出求解50g这种黄铜样品中参加反应的物质质量(X)的比例式。(4)、该黄铜样品中铜的质量分数为。(5)、向反应后所得滤液中加入87.4g水,则最终所得溶液A中溶质的质量分数为。(6)、若工业上用100t含Cu2S74%的辉铜矿炼制该黄铜,则理论上能炼制出该黄铜的质量为。23. 中考三项测试中,有一道化学测试题“区分氯化钠溶液和纯碱溶液”,现将两种溶液分别标记为A和B,甲乙两位同学的实验过程如下:
(1)、发生反应的化学方程式为。(2)、用98%的浓硫酸配制100g质量分数19.6%的稀硫酸,需要浓硫酸与水的质量比为。(3)、根据已知条件列出求解50g这种黄铜样品中参加反应的物质质量(X)的比例式。(4)、该黄铜样品中铜的质量分数为。(5)、向反应后所得滤液中加入87.4g水,则最终所得溶液A中溶质的质量分数为。(6)、若工业上用100t含Cu2S74%的辉铜矿炼制该黄铜,则理论上能炼制出该黄铜的质量为。23. 中考三项测试中,有一道化学测试题“区分氯化钠溶液和纯碱溶液”,现将两种溶液分别标记为A和B,甲乙两位同学的实验过程如下: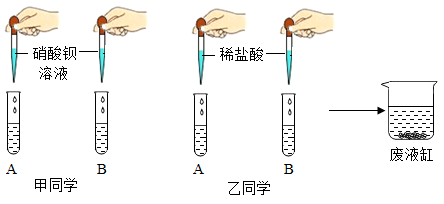 (1)、(收集证据)甲同学实验中,装有A的试管中无明显现象,则乙同学的实验中,装有B的试管中的实验现象为 , 两位同学都得出了正确的结论。实验后他们将四只试管内的所有物质倒入同一废液缸中,充分混合,静置一段时间,发现废液缸底部仍有白色沉淀。同学们对废液缸内上层清液中含有的离子成分进一步探究:(2)、(提出问题)废液缸内上层清液中含有的离子成分是什么?
(1)、(收集证据)甲同学实验中,装有A的试管中无明显现象,则乙同学的实验中,装有B的试管中的实验现象为 , 两位同学都得出了正确的结论。实验后他们将四只试管内的所有物质倒入同一废液缸中,充分混合,静置一段时间,发现废液缸底部仍有白色沉淀。同学们对废液缸内上层清液中含有的离子成分进一步探究:(2)、(提出问题)废液缸内上层清液中含有的离子成分是什么?(猜想与假设)
甲的猜想:Na+、Cl-、 、 乙的猜想:Na+、Cl-、
丙的猜想: Na+、Cl-、 、H+丁的猜想:。
以上三位同学的猜想中不合理的是同学的猜想。
(3)、(实验与探究)乙同学为了验证自己的猜想,进行如下实验:实验操作
实验现象
实验结论
取少量废液缸内上层清液于试管中,向其中滴加。
。
废液缸内上层清液中含有的离子是:Na+、Cl-、
大家一致认为乙同学的实验能够得出符合题意结论。
(4)、(总结与提升)通过上述探究可知,对几种溶液混合后所得溶液中的离子成分做出猜想时,可以对混合前进行分析:不参加反应的离子一定存在,的离子不能同时存在。