河北省石家庄市2020-2021学年高二下学期化学期末考试试卷
试卷更新日期:2021-08-04 类型:期末考试
一、单选题
-
1. 化学与人类生产、生活密切相关。下列说法错误的是( )A、用氨水处理硫酸工业产生的废气并生产氮肥 B、用硅制作太阳能电池可以减少对煤、石油等化石燃料的依赖 C、用于制造医用护目镜的聚碳酸酯(PC)属于有机高分子化合物 D、不断开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理2. 下列实验装置或操作不能达到相应实验目的的是( )
 A、图甲是中和滴定 B、图乙是中和热的测定 C、图丙是验证化学能转化为电能 D、图丁是 萃取碘水中的碘的分离操作3. 某化学兴趣小组为探究干燥的氯气是否具有漂白性,设计如图所示装置进行实验,下列对装置中Ⅰ、Ⅱ、Ⅲ处分别放置的物品判断正确的是( )
A、图甲是中和滴定 B、图乙是中和热的测定 C、图丙是验证化学能转化为电能 D、图丁是 萃取碘水中的碘的分离操作3. 某化学兴趣小组为探究干燥的氯气是否具有漂白性,设计如图所示装置进行实验,下列对装置中Ⅰ、Ⅱ、Ⅲ处分别放置的物品判断正确的是( )
选项
Ⅰ
Ⅱ
Ⅲ
A
干燥的有色布条
碱石灰
湿润的有色布条
B
干燥的有色布条
硅胶
湿润的有色布条
C
湿润的有色布条
浓硫酸
干燥的有色布条
D
湿润的有色布条
无水氯化钙
干燥的有色布条
A、A B、B C、C D、D4. 下列去除杂质的方法中,能达到相应目的的是( )选项
物质(杂质)
方法
A
(炭粉)
在氧气流中灼烧
B
加热升华
C
HCl气体( )
通过KI溶液
D
加入盐酸溶解、过滤、洗涤及干燥
A、A B、B C、C D、D5. A、B、C、D、E、F均为中学里常见的物质,一定条件下存在如图所示转化。已知:A是不含结晶水的酸式盐,气体D在标准状况下的密度为2.857 ,溶液E的焰色反应呈黄色。下列有关推断错误的是( ) A、A的化学式为 B、固体B具有还原性,是常用的抗氧化剂 C、气体D能使品红溶液﹑酸性高锰酸钾溶液褪色 D、A,B,C,D,E,F均属于电解质6. 下列关于晶体的说法错误的是( )
A、A的化学式为 B、固体B具有还原性,是常用的抗氧化剂 C、气体D能使品红溶液﹑酸性高锰酸钾溶液褪色 D、A,B,C,D,E,F均属于电解质6. 下列关于晶体的说法错误的是( )①含有离子的晶体一定是离子晶体 ②分子晶体若采取密堆积方式,其配位数是12 ③含有共价键的晶体一定是原子晶体 ④分子晶体的熔点一定比金属晶体的低 ⑤MgO远比NaCl的晶格能大 ⑥共价键的强弱决定分子晶体熔、沸点的高低
A、①③④⑥ B、①②③⑤ C、①②④ D、②③④⑥7. 下列物质属于晶体的是( )A、塑料 B、玻璃 C、石英 D、石蜡8. 下列比较错误的是( )A、离子半径:r(Li+)>r(H-) B、键能:C—C >C—Si C、键长:N—N >N=N D、H2O与CH4分子中的键角:CH4>H2O9. 向 溶液中滴加 溶液,产生的沉淀主要是( )A、 B、AgCl C、AgBr和AgCl D、AgBr10. 已知:乙烯在酸性 溶液的作用下,碳碳双键完全断裂生成 ;在银作催化剂时,可与氧气反应生成环氧乙烷。① ②

下列说法错误的是( )
A、反应①是氧化反应 B、反应②是还原反应 C、Mn基态原子的价电子排布式为 D、环氧乙烷分子中的氧原子是 杂化11. 氮化铝属类金刚石氮化物、六方晶系,最高可稳定到2200℃,硬度大,热膨胀系数小,是良好的耐热冲击材料,氮化铝晶胞结构如图所示。下列有关描述错误的是( ) A、AlN是共价晶体 B、Al的配位数为4 C、AlN属于离子化合物 D、与每个铝原子距离相等且最近的铝原子共有12个12. 下列各组微粒的空间构型相同的是( )
A、AlN是共价晶体 B、Al的配位数为4 C、AlN属于离子化合物 D、与每个铝原子距离相等且最近的铝原子共有12个12. 下列各组微粒的空间构型相同的是( )① 和 ② 和 ③ 和 ④ 和 ⑤ 和 ⑥ 和 ⑦ 和
A、全部 B、除④⑥⑦以外 C、③④⑤⑥ D、②④⑤⑥13. X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示。若Y原子为其所在周期中未成对电子最多的原子,下列说法中正确的是( ) A、 的空间构型为V形 B、Y的最简单气态氢化物的水溶液显碱性 C、Z的氯化物中各原子最外层一定满足8电子稳定结构 D、W的氧化物对应水化物的酸性比Z的氧化物对应水化物的酸性强14. 我国嫦娥五号探测器带回 的月球土壤,经分析发现其构成与地球土壤类似土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15。X、Y、Z为同周期相邻元素,且均不与W同族,下列结论正确的是( )A、原子半径大小顺序为 B、化合物XW中的化学键为离子键 C、Y单质的导电性能弱于Z单质的 D、Z的氧化物的水化物的酸性强于碳酸15. 昆虫信息素是昆虫之间传递信号的化学物质。人工合成信息素可用于诱捕害虫、测报虫情等。一种信息素的分子结构简式如图所示,关于该化合物说法错误的是( )
A、 的空间构型为V形 B、Y的最简单气态氢化物的水溶液显碱性 C、Z的氯化物中各原子最外层一定满足8电子稳定结构 D、W的氧化物对应水化物的酸性比Z的氧化物对应水化物的酸性强14. 我国嫦娥五号探测器带回 的月球土壤,经分析发现其构成与地球土壤类似土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15。X、Y、Z为同周期相邻元素,且均不与W同族,下列结论正确的是( )A、原子半径大小顺序为 B、化合物XW中的化学键为离子键 C、Y单质的导电性能弱于Z单质的 D、Z的氧化物的水化物的酸性强于碳酸15. 昆虫信息素是昆虫之间传递信号的化学物质。人工合成信息素可用于诱捕害虫、测报虫情等。一种信息素的分子结构简式如图所示,关于该化合物说法错误的是( ) A、属于烷烃 B、可发生水解反应 C、可发生加聚反应 D、具有一定的挥发性16. 通过古“丝绸之路”运出的货物有如下8种:①丝绸 ②茶叶 ③白糖 ④瓷器 ⑤纸张 ⑥植物油 ⑦明矾 ⑧金银铜器。下列说法正确的是( )A、①②③⑤的主要成分都是糖类 B、④⑦⑧都属于无机非金属材料 C、①③⑤⑥⑦的主要成分都可以发生水解反应 D、①②③⑤⑥⑦的主要成分都是有机物17. 分子式为 的芳香醇,其苯环上只含有一个支链,经催化氧化后可与新制的氢氧化铜悬浊液反应生成砖红色沉淀,符合条件的芳香醇有(不考虑立体异构) ( )A、12种 B、8种 C、6种 D、4种18. 有机物A是一种重要的化工原料,其结构简式为
A、属于烷烃 B、可发生水解反应 C、可发生加聚反应 D、具有一定的挥发性16. 通过古“丝绸之路”运出的货物有如下8种:①丝绸 ②茶叶 ③白糖 ④瓷器 ⑤纸张 ⑥植物油 ⑦明矾 ⑧金银铜器。下列说法正确的是( )A、①②③⑤的主要成分都是糖类 B、④⑦⑧都属于无机非金属材料 C、①③⑤⑥⑦的主要成分都可以发生水解反应 D、①②③⑤⑥⑦的主要成分都是有机物17. 分子式为 的芳香醇,其苯环上只含有一个支链,经催化氧化后可与新制的氢氧化铜悬浊液反应生成砖红色沉淀,符合条件的芳香醇有(不考虑立体异构) ( )A、12种 B、8种 C、6种 D、4种18. 有机物A是一种重要的化工原料,其结构简式为 ,下列有关有机物A描述正确的是( ) A、加入硝酸酸化的 溶液,有淡黄色沉淀生成 B、加入新制 悬浊液,充分反应后加入溴水,若溴水褪色,则证明A中含碳碳双键 C、A的分子式为 D、A中能使酸性 溶液褪色的官能团有2种19. 绿原酸等多酚类物质被称为“第七类营养素”,广泛用于保健行业,其结构如图所示。下列说法错误的是( )
,下列有关有机物A描述正确的是( ) A、加入硝酸酸化的 溶液,有淡黄色沉淀生成 B、加入新制 悬浊液,充分反应后加入溴水,若溴水褪色,则证明A中含碳碳双键 C、A的分子式为 D、A中能使酸性 溶液褪色的官能团有2种19. 绿原酸等多酚类物质被称为“第七类营养素”,广泛用于保健行业,其结构如图所示。下列说法错误的是( ) A、绿原酸分子中含有4个手性碳原子 B、绿原酸分子中含有6种官能团 C、1mol绿原酸与足量Na反应生成的气体在标准状况下的体积为67.2L D、1mol绿原酸最多能与4mol NaOH反应20. 葡萄糖在人体中进行无氧呼吸产生乳酸,乳酸结构简式为 。下列有关乳酸的说法正确的是( )A、乳酸与羟基乙酸互为同分异构体 B、乳酸和葡萄糖均能与新制 悬浊液作用并使溶液出现绛蓝色 C、乳酸分子能通过缩聚反应生成高分子化合物 D、乳酸与 一样具有两性21. L-多巴可用于帕金森综合症的治疗,其结构简式为
A、绿原酸分子中含有4个手性碳原子 B、绿原酸分子中含有6种官能团 C、1mol绿原酸与足量Na反应生成的气体在标准状况下的体积为67.2L D、1mol绿原酸最多能与4mol NaOH反应20. 葡萄糖在人体中进行无氧呼吸产生乳酸,乳酸结构简式为 。下列有关乳酸的说法正确的是( )A、乳酸与羟基乙酸互为同分异构体 B、乳酸和葡萄糖均能与新制 悬浊液作用并使溶液出现绛蓝色 C、乳酸分子能通过缩聚反应生成高分子化合物 D、乳酸与 一样具有两性21. L-多巴可用于帕金森综合症的治疗,其结构简式为 。下列关于L-多巴的说法中,错误的是( ) A、分子式为C9H11O4N B、能缩合生成高分子 C、能与酸、碱反应生成盐 D、核磁共振氢谱有8个吸收峰22. 化合物M经质谱法分析得知其相对分子质量为136.M分子的苯环上只有一个取代基,M分子的核磁共振氢谱与红外光谱如图。下列关于M的说法正确的是( )
。下列关于L-多巴的说法中,错误的是( ) A、分子式为C9H11O4N B、能缩合生成高分子 C、能与酸、碱反应生成盐 D、核磁共振氢谱有8个吸收峰22. 化合物M经质谱法分析得知其相对分子质量为136.M分子的苯环上只有一个取代基,M分子的核磁共振氢谱与红外光谱如图。下列关于M的说法正确的是( )
 A、不能使酸性高锰酸钾溶液褪色,也不与任何酸或碱溶液反应 B、符合题中M的结构特征的有机物只有1种 C、M在一定条件下可与4mol 发生加成反应 D、与M属于同类化合物的同分异构体只有2种(不考虑立体异构)23. “异丙苯氧化法”生产丙酮和苯酚的合成路线如下,各反应的原子利用率均为100%。下列说法正确的是( )
A、不能使酸性高锰酸钾溶液褪色,也不与任何酸或碱溶液反应 B、符合题中M的结构特征的有机物只有1种 C、M在一定条件下可与4mol 发生加成反应 D、与M属于同类化合物的同分异构体只有2种(不考虑立体异构)23. “异丙苯氧化法”生产丙酮和苯酚的合成路线如下,各反应的原子利用率均为100%。下列说法正确的是( ) A、X的分子式为C3H8 B、Y与异丙苯可用酸性KMnO4溶液鉴别 C、CHP与CH3COOH含有相同的官能团 D、可以用分液的方法分离苯酚和丙酮
A、X的分子式为C3H8 B、Y与异丙苯可用酸性KMnO4溶液鉴别 C、CHP与CH3COOH含有相同的官能团 D、可以用分液的方法分离苯酚和丙酮二、多选题
-
24. 用 代表阿伏加德罗常数的值,下列说法正确的是( )A、所含共价键数目均为0.4 的白磷(
 )和甲烷的物质的量相等
B、常温下,向1L 0.1 醋酸钠溶液中加入醋酸至中性,则溶液中 的数目为0.1
C、通入了1mol 的新制氯水中,HClO、 、 粒子数目之和为2
D、向 溶液中通入适量 ,当有1mol 被氧化时,反应转移的电子数为
25. 德国科学家发现新配方:他使用了远古地球上存在的 、 、 、 、 和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法错误的是( )A、基态 价电子排布为 B、 、 、 分子间均存在氢键 C、 、 、HCN中均存在 键和 键 D、沸点: (乙硫醇)>26. 如图所示是一种麻醉剂的分子结构式。其中,X的原子核内只有1个质子;元素Y、Z、W原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电子。下列说法错误的是( )
)和甲烷的物质的量相等
B、常温下,向1L 0.1 醋酸钠溶液中加入醋酸至中性,则溶液中 的数目为0.1
C、通入了1mol 的新制氯水中,HClO、 、 粒子数目之和为2
D、向 溶液中通入适量 ,当有1mol 被氧化时,反应转移的电子数为
25. 德国科学家发现新配方:他使用了远古地球上存在的 、 、 、 、 和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法错误的是( )A、基态 价电子排布为 B、 、 、 分子间均存在氢键 C、 、 、HCN中均存在 键和 键 D、沸点: (乙硫醇)>26. 如图所示是一种麻醉剂的分子结构式。其中,X的原子核内只有1个质子;元素Y、Z、W原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电子。下列说法错误的是( ) A、 是一种强酸 B、 中,Z的化合价为 价 C、原子半径: D、非金属性:27. 纳米分子机器日益受到关注,机器的“车轮”常用组件如图。下列说法正确的是( )
A、 是一种强酸 B、 中,Z的化合价为 价 C、原子半径: D、非金属性:27. 纳米分子机器日益受到关注,机器的“车轮”常用组件如图。下列说法正确的是( ) A、三蝶烯分子中所有的原子都处于同一平面 B、扭曲烷的一氯代物只有3种 C、富勒烯和 互为同分异构体 D、金刚烷分子中有4个六元环28. 番木鳖酸具有一定的抗炎、抗菌活性,结构简式如图。下列说法错误的是( )
A、三蝶烯分子中所有的原子都处于同一平面 B、扭曲烷的一氯代物只有3种 C、富勒烯和 互为同分异构体 D、金刚烷分子中有4个六元环28. 番木鳖酸具有一定的抗炎、抗菌活性,结构简式如图。下列说法错误的是( )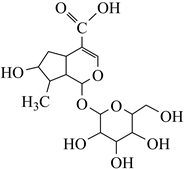 A、1mol该物质与足量饱和NaHCO3溶液反应,可放出22.4L(标准状况)CO2 B、一定量的该物质分别与足量Na、NaOH反应,消耗二者物质的量之比为5:1 C、1mol该物质最多可与2molH2发生加成反应 D、该物质可被酸性KMnO4溶液氧化
A、1mol该物质与足量饱和NaHCO3溶液反应,可放出22.4L(标准状况)CO2 B、一定量的该物质分别与足量Na、NaOH反应,消耗二者物质的量之比为5:1 C、1mol该物质最多可与2molH2发生加成反应 D、该物质可被酸性KMnO4溶液氧化三、综合题
-
29. 草酸铵[ ]为无色柱状晶体,不稳定,受热易分解,是一种有机合成中间体,可用于测定 、 的含量。(1)、Ⅰ.某同学利用如图所示实验装置检验草酸铵的分解产物。
 反应开始前通入氮气的目的是。(2)、装置C的作用是。(3)、实验过程中,观察到浸有酚酞溶液的滤纸变红,装置B中澄清石灰水变浑浊,说明分解产物中含有(填化学式);若观察到 , 说明分解产物中含有CO。(4)、除CO外,还有一种分解产物在一定条件下也能还原CuO,并生成一种无污染的气体,该反应的化学方程式为。(5)、Ⅱ.该同学利用草酸铵测定血液中钙元素的含量。
反应开始前通入氮气的目的是。(2)、装置C的作用是。(3)、实验过程中,观察到浸有酚酞溶液的滤纸变红,装置B中澄清石灰水变浑浊,说明分解产物中含有(填化学式);若观察到 , 说明分解产物中含有CO。(4)、除CO外,还有一种分解产物在一定条件下也能还原CuO,并生成一种无污染的气体,该反应的化学方程式为。(5)、Ⅱ.该同学利用草酸铵测定血液中钙元素的含量。取20.00mL血液样品,定容至100mL,分别取三份体积均为25.00mL稀释后的血液样品,加入草酸铵,生成草酸钙沉淀,过滤,将该沉淀溶于过量稀硫酸中,然后用0.010 溶液进行滴定。滴定至终点时的实验现象为。三次滴定实验消耗 溶液的体积分别为0.43mL,0.41mL,0.52mL,则该血液样品中含钙元素的量为 。
30. 已知:X、Y和Z三种元素的原子序数之和为42,基态X原子的4p轨道上有3个未成对电子,基态Y原子的2p轨道上有2个未成对电子,X与Y可形成化合物 ,Z元素可形成 价离子。回答下列问题:(1)、X的元素符号为。(2)、Y原子的L层电子的电子排布图为。(3)、X、Y、Z三种元素之间可形成多种化合物。①化合物 的沸点(填“高于”、“低于”或“等于”)XZ3 , 原因是。
②化合物XZ3的立体构型为。
③X、Y、Z三种元素可形成化合物 ,该化合物在水溶液中呈酸性,则该物质为(填“强酸”或“弱酸”),属于(填“一元”、“二元”或“三元”)酸, 分子中 键与 键的数目之比为。
(4)、法医在鉴定 中毒时,常用马氏法。取试样(含 )与锌、盐酸混合,反应生成氯化锌、水和XZ3 , 然后将生成的XZ3气体导入玻璃管中隔绝空气加热,如果试样中含有X的化合物,那么生成的XZ3在管内受热分解生成亮黑色的单质X,称为“X镜”。写出 与锌、盐酸反应的化学方程式:。31. 人们发现,纸张会发生酸性腐蚀而变脆、破损,这严重威胁纸质文物的保存。经分析检验发现,酸性腐蚀主要与造纸中涂敷明矾的工艺有关,为了防止纸张的酸性腐蚀,可在纸浆中加入碳酸钙等添加剂。回答下列问题:(1)、上述涉及的物质中,原子序数最大的元素是(填化学符号),其位于元素周期表中的区。(2)、H、C、O元素的电负性由大到小的顺序为(用元素符号表示)。(3)、熔融 可生成具有挥发性的二聚体,二聚体 的结构式为 , 其中Al的配位数为。(4)、 的一种晶胞结构如图所示。
① 属于(填“离子”或“共价”)化合物。
②下列说法错误的是(填标号)。
A. 晶体有较高的熔、沸点 B. 晶体硬而脆
C. 晶体易溶于水 D. 晶体不导电
③若将 形成的立方体分割成8个小立方体,则每个小立方体的中心有个 。
(5)、由碳元素形成的某种晶体的晶胞结构如图所示,设阿伏加德罗常数的值为 ,晶体的密度为 ,则该晶胞的棱长为(用含 、 的代数式表示)pm。 32. 对氨基水杨酸钠(G)是抗结核药物,主要用于结核菌感染的综合治疗,其合成路线如下:
32. 对氨基水杨酸钠(G)是抗结核药物,主要用于结核菌感染的综合治疗,其合成路线如下:
已知:
①


②


回答下列问题:
(1)、B的化学名称为;F中含氧官能团的名称为。(2)、C的结构简式为;合成路线的6步反应中属于还原反应的是(填标号)。(3)、反应③中所加试剂Ⅰ为(填化学式,下同);反应⑥中所加试剂Ⅱ为。(4)、写出反应④的化学方程式:;其有机反应类型为。(5)、M为A的同分异构体,符合下列条件的M的结构有种,其中有6个碳原子在一条直线上的结构简式为。a.属于链状烃 b.分子中只有碳碳三键一种官能团
33. G是一种新型香料的主要成分之一,其结构中含有三个六元环。G的合成路线(部分产物和部分反应条件已略去)如下:
已知:
① ;
②B中核磁共振氢谱图显示分子中有6种不同环境的氢原子;
③D和F是同系物。
请回答下列问题:
(1)、 的化学名称为。(2)、写出反应④的化学方程式:。(3)、G的合成路线中,属于氧化反应的有个,D分子中官能团的名称为。(4)、同时满足下列条件的F的同分异构体有种。①苯环上有两个取代基;②有羟基且能发生银镜反应;③可以发生水解反应。
其中能与 溶液发生显色反应,且核磁共振氢谱有5组峰的结构简式为。
(5)、已知: +
+ 
 。参照上述合成路线和信息,设计由
。参照上述合成路线和信息,设计由  制取
制取  的合成路线 (无机试剂及有机溶剂任选)。
的合成路线 (无机试剂及有机溶剂任选)。