广西河池市宜州区2021年中考化学二模试卷
试卷更新日期:2021-08-03 类型:中考模拟
一、单选题
-
1. 下列过程中,只发生物理变化的是( )A、青稞酿酒 B、空气液化 C、火药爆炸 D、红磷燃烧2. 下列不属于空气污染物的是( )A、NO2 B、CO C、粉尘 D、H2O3. 下列微粒中不能直接构成物质的是( )A、分子 B、原子 C、中子 D、离子4. 下列物质中富含蛋白质的是( )A、豆浆 B、糖水 C、生理盐水 D、苹果5. 缉毒犬能通过嗅觉寻找毒品的原因是( )A、分子之间有间隔 B、分子在不断运动 C、分子质量很小 D、分子体积很小6. 下列变化与空气中氧气有关的是( )A、生石灰在空气中变质 B、浓盐酸在空气中变稀 C、烧碱在空气中潮解 D、铁制品在空气中生锈7. 2019年度诺贝尔化学奖颁给了三位科学家,以表彰他们在锂离子电池领域做出的贡献。锂元素的一种原子中质子数为3,中子数为4,该锂原子的核外电子数为( )
 A、3 B、4 C、6 D、78. 5月12日是全国防灾减灾日。下列说法正确的是( )A、高层楼房着火,乘电梯逃生 B、加油站内拨打或接听电话 C、燃气泄漏时,点火检查 D、火灾逃生时弯腰前行9. 下列物质在氧气中燃烧,有刺激性气味的气体生成的是( )A、镁条 B、铁丝 C、白磷 D、硫10. 蔗糖(C12H22O11)是一种常用的食品甜味剂。下列关于蔗糖的说法正确的是()A、蔗糖是由碳、氢、氧三种元素组成 B、蔗糖中含有45个原子 C、蔗糖中氢元素的质量分数最高 D、蔗糖的相对分子质量为342g11. 下列关于二氧化碳和一氧化碳的比较,完全正确的是( )A、都能与碳反应 B、都可以用碳和氧气反应得到 C、都具有还原性 D、常温都是气体,都难溶于水12. 下列鉴别物质的方法错误的是( )A、汽油和蒸馏水(闻气味) B、炭粉和二氧化锰固体(观察颜色) C、羊毛和涤纶(灼烧) D、NH4Cl固体和KCl固体(与熟石灰混合研磨)13. 利用如图装置验证了空气中氧气的含量。下列叙述错误的是( )
A、3 B、4 C、6 D、78. 5月12日是全国防灾减灾日。下列说法正确的是( )A、高层楼房着火,乘电梯逃生 B、加油站内拨打或接听电话 C、燃气泄漏时,点火检查 D、火灾逃生时弯腰前行9. 下列物质在氧气中燃烧,有刺激性气味的气体生成的是( )A、镁条 B、铁丝 C、白磷 D、硫10. 蔗糖(C12H22O11)是一种常用的食品甜味剂。下列关于蔗糖的说法正确的是()A、蔗糖是由碳、氢、氧三种元素组成 B、蔗糖中含有45个原子 C、蔗糖中氢元素的质量分数最高 D、蔗糖的相对分子质量为342g11. 下列关于二氧化碳和一氧化碳的比较,完全正确的是( )A、都能与碳反应 B、都可以用碳和氧气反应得到 C、都具有还原性 D、常温都是气体,都难溶于水12. 下列鉴别物质的方法错误的是( )A、汽油和蒸馏水(闻气味) B、炭粉和二氧化锰固体(观察颜色) C、羊毛和涤纶(灼烧) D、NH4Cl固体和KCl固体(与熟石灰混合研磨)13. 利用如图装置验证了空气中氧气的含量。下列叙述错误的是( ) A、实验前需检查装置气密性 B、白磷的作用是消耗试管中的氧气 C、白磷熄火、试管冷却后再打开止水夹 D、最终量筒中液面约降至40mL刻度线处14. 下列实验操作符合规范要求的是( )A、点燃氢气前必须检验氢气的纯度以防爆炸 B、加热氯酸钾制氧气结束时,先停止加热再将导管移出水槽 C、“粗盐中难溶性杂质的去除”实验中,蒸发皿中水分蒸干时停止加热 D、给试管加热时,为了便于观察,试管口应对着自己15. 氨催化氧化是制硝酸的主要反应之一,该反应前后分子种类变化的微观示意图如图。下列说法正确的是()
A、实验前需检查装置气密性 B、白磷的作用是消耗试管中的氧气 C、白磷熄火、试管冷却后再打开止水夹 D、最终量筒中液面约降至40mL刻度线处14. 下列实验操作符合规范要求的是( )A、点燃氢气前必须检验氢气的纯度以防爆炸 B、加热氯酸钾制氧气结束时,先停止加热再将导管移出水槽 C、“粗盐中难溶性杂质的去除”实验中,蒸发皿中水分蒸干时停止加热 D、给试管加热时,为了便于观察,试管口应对着自己15. 氨催化氧化是制硝酸的主要反应之一,该反应前后分子种类变化的微观示意图如图。下列说法正确的是()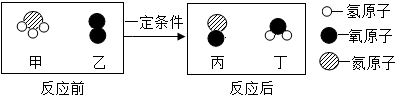 A、生成的丙与丁的分子个数比为2:3 B、乙的相对分子质量为32g C、反应前后分子的个数不变 D、反应过程中共涉及三种氧化物16. 如图是初中化学中有关甲、乙、丙、丁四种常见物质间的转化关系图,下列说法正确的是( )
A、生成的丙与丁的分子个数比为2:3 B、乙的相对分子质量为32g C、反应前后分子的个数不变 D、反应过程中共涉及三种氧化物16. 如图是初中化学中有关甲、乙、丙、丁四种常见物质间的转化关系图,下列说法正确的是( ) A、若甲、乙均为化合物,则丙不可能为单质 B、若甲为酸,乙为碱,则该反应一定是中和反应 C、若甲为化合物,乙为单质,则该反应为置换反应 D、若丁为水,则甲、乙至少有一种物质为酸17. 下列物质间的转化,不能一步实现的是( )A、CO2→O2 B、Cu(OH)2→CuCl2 C、Fe→FeCl3 D、Na2CO3→NaCl18. 下列有关实验方案设计正确的是( )
A、若甲、乙均为化合物,则丙不可能为单质 B、若甲为酸,乙为碱,则该反应一定是中和反应 C、若甲为化合物,乙为单质,则该反应为置换反应 D、若丁为水,则甲、乙至少有一种物质为酸17. 下列物质间的转化,不能一步实现的是( )A、CO2→O2 B、Cu(OH)2→CuCl2 C、Fe→FeCl3 D、Na2CO3→NaCl18. 下列有关实验方案设计正确的是( )选项
实验目的
实验方案
A
除去Cu中混有的少量C
在空气中充分灼烧
B
除去MnO2中混有少量的KCl
加入足量水溶解,过滤、洗涤、干燥
C
分离NaCl和CuCl2混合溶液
加入适量的NaOH溶液,过滤
D
除去CO2中含有的少量CO
通入氧气,点燃
A、A B、B C、C D、D19. 下列各组离子在溶液中能大量共存,并能使紫色石蕊溶液变蓝的是( )A、H+、Ba2+、 、 B、Fe3+、K+、 、Cl- C、Na+、Ba2+、OH-、Cl- D、Na+、Ba2+、OH-、20. 下列图像分别与选项的操作相对应,其中合理的是( )A、 电解水实验
B、
电解水实验
B、 向一定质量MnO2固体中加入一定质量的H2O2溶液
C、
向一定质量MnO2固体中加入一定质量的H2O2溶液
C、 温度不变,向一定质量饱和Ca(OH)2溶液中加入CaO
D、
温度不变,向一定质量饱和Ca(OH)2溶液中加入CaO
D、 向一定质量H2SO4和CuSO4的混合溶液中加入NaOH溶液
向一定质量H2SO4和CuSO4的混合溶液中加入NaOH溶液
二、填空题
-
21. 请用化学用语填空。(1)、硫原子;(2)、碱溶液中的阴离子;(3)、氦气;(4)、下图所示粒子符号为;
 (5)、碳酸铵((NH4)2CO3)中氮元素显-3价。22. 化学与我们的日常生活紧密相关。现有①金刚石 ②赤铁矿 ③小苏打 ④甲烷 ⑤聚乙烯塑料,请用相应物质的序号填空。(1)、高炉炼铁的原料之一;(2)、可用于刻划玻璃的是;(3)、最简单的有机物是;(4)、发酵粉的主要成分是;(5)、可用于制食品包装袋的是。23. 化学来源于生活,回答下列问题:(1)、空气中氮气的体积分数为 , 食品包装袋中充入氮气以防腐,是因为氮气的化学性质。(2)、在简易净水器中,常加入活性炭,是因为活性炭具有性。(3)、用酒精进行室内消毒时,若不小心引起小面积失火,可用湿抹布扑灭,其灭火主要原理是。(4)、含磷洗衣粉中含有Na5PxO10 , 其洗涤废水的任意排放会污染环境,已知Na5PxO10中磷元素的化合价为+5,则X为。(5)、84消毒液中的次氯酸钠(NaClO)的制取是将氯气(Cl2)与氢氧化钠反应生成氯化钠、次氯酸钠和水,该反应的化学方程式为。24. 回答下列与金属有关的问题。(1)、黄铜制的钥匙在纯铜板上划出痕迹,说明合金的硬度一般组成它的纯金属(填“>”“<”或“=”);生铁和钢中最主要的元素是。(2)、铝的化学性质比较活泼,但铝制品具有良好的抗腐蚀性能,其原因是铝表面容易形成。(3)、向溶质是AgNO3、Cu(NO3)2、KNO3的溶液中加入一定量的镁粉,充分反应后过滤,得到蓝色溶液和金属滤渣,则滤液中除一定含有的溶质外,可能含有的溶质是。25. 20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图I,加热到50℃时现象如图II,甲、乙两种物质的溶解度曲线如图III,请结合图示回答下列问题:
(5)、碳酸铵((NH4)2CO3)中氮元素显-3价。22. 化学与我们的日常生活紧密相关。现有①金刚石 ②赤铁矿 ③小苏打 ④甲烷 ⑤聚乙烯塑料,请用相应物质的序号填空。(1)、高炉炼铁的原料之一;(2)、可用于刻划玻璃的是;(3)、最简单的有机物是;(4)、发酵粉的主要成分是;(5)、可用于制食品包装袋的是。23. 化学来源于生活,回答下列问题:(1)、空气中氮气的体积分数为 , 食品包装袋中充入氮气以防腐,是因为氮气的化学性质。(2)、在简易净水器中,常加入活性炭,是因为活性炭具有性。(3)、用酒精进行室内消毒时,若不小心引起小面积失火,可用湿抹布扑灭,其灭火主要原理是。(4)、含磷洗衣粉中含有Na5PxO10 , 其洗涤废水的任意排放会污染环境,已知Na5PxO10中磷元素的化合价为+5,则X为。(5)、84消毒液中的次氯酸钠(NaClO)的制取是将氯气(Cl2)与氢氧化钠反应生成氯化钠、次氯酸钠和水,该反应的化学方程式为。24. 回答下列与金属有关的问题。(1)、黄铜制的钥匙在纯铜板上划出痕迹,说明合金的硬度一般组成它的纯金属(填“>”“<”或“=”);生铁和钢中最主要的元素是。(2)、铝的化学性质比较活泼,但铝制品具有良好的抗腐蚀性能,其原因是铝表面容易形成。(3)、向溶质是AgNO3、Cu(NO3)2、KNO3的溶液中加入一定量的镁粉,充分反应后过滤,得到蓝色溶液和金属滤渣,则滤液中除一定含有的溶质外,可能含有的溶质是。25. 20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图I,加热到50℃时现象如图II,甲、乙两种物质的溶解度曲线如图III,请结合图示回答下列问题:
 (1)、图I中一定为饱和溶液的是(填甲或乙)。(2)、图II中甲、乙两溶液中溶质质量分数的大小关系为甲乙(填“>”“<”或“=”)。(3)、图III中表示乙的溶解度曲线是(填 “M”或“N”)。(4)、50℃时,将甲物质的不饱和溶液变为饱和溶液,可采取的方法是。(5)、欲配制100g10%的乙溶液,用量筒量取水时,俯视读数,这样配得的溶液溶质质量分数会(填“偏大”、“偏小”、或“无影响”)。26. “长征”系列火箭为我国卫星发射、嫦娥探月等太空工程立下汗马功劳。(1)、运载火箭采用液氢、煤油等做燃料。生产煤油的原料是 , 要使煤油等燃料充分燃烧通常考虑两点,一是燃烧时要有足够多的空气;二是;采用液氢做燃料的优点是(写一点)。(2)、长征5号火箭将载人飞船送入太空。航天飞行时宇航员体内的钙会流失,钙属于人体中的(填“常量”或“微量”)元素,钙流失会引起的健康问题是。(3)、2020年12月22日,长征8号运载火箭首次飞行试验成功。制造火箭需要大量的钛合金,主要是因为钛合金有(填一条物理性质)。
(1)、图I中一定为饱和溶液的是(填甲或乙)。(2)、图II中甲、乙两溶液中溶质质量分数的大小关系为甲乙(填“>”“<”或“=”)。(3)、图III中表示乙的溶解度曲线是(填 “M”或“N”)。(4)、50℃时,将甲物质的不饱和溶液变为饱和溶液,可采取的方法是。(5)、欲配制100g10%的乙溶液,用量筒量取水时,俯视读数,这样配得的溶液溶质质量分数会(填“偏大”、“偏小”、或“无影响”)。26. “长征”系列火箭为我国卫星发射、嫦娥探月等太空工程立下汗马功劳。(1)、运载火箭采用液氢、煤油等做燃料。生产煤油的原料是 , 要使煤油等燃料充分燃烧通常考虑两点,一是燃烧时要有足够多的空气;二是;采用液氢做燃料的优点是(写一点)。(2)、长征5号火箭将载人飞船送入太空。航天飞行时宇航员体内的钙会流失,钙属于人体中的(填“常量”或“微量”)元素,钙流失会引起的健康问题是。(3)、2020年12月22日,长征8号运载火箭首次飞行试验成功。制造火箭需要大量的钛合金,主要是因为钛合金有(填一条物理性质)。三、综合题
-
27. 一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,同学们设计了如下实验方案,请分析:
 (1)、操作1的名称是。(2)、X的化学式为;蓝色溶液B中的阳离子一定有。(3)、写出生成白色沉淀D的化学方程式。(4)、原固体粉末不能确定的物质是。28. 实验室制取气体时需要的一些装置如图所示。请回答下列问题。
(1)、操作1的名称是。(2)、X的化学式为;蓝色溶液B中的阳离子一定有。(3)、写出生成白色沉淀D的化学方程式。(4)、原固体粉末不能确定的物质是。28. 实验室制取气体时需要的一些装置如图所示。请回答下列问题。 (1)、写出图中标有序号的仪器的名称:①;② 。(2)、在实验室连接B、D装置进行实验,若D中蜡烛燃得更旺,则B中反应的化学方程式为。(3)、CO2能用向上排空气法收集,是因为;若用E装置干燥二氧化碳气体,E中应盛放的药品名称为。(4)、SO2易溶于水,溶于水可生成亚硫酸,实验室常用亚硫酸钠固体和稀硫酸反应常温下制取SO2 , 若想控制反应速率,图中最适宜的发生装置是;F实验中可观察到试管内且液体变为红色。29. 同学们学习“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究。
(1)、写出图中标有序号的仪器的名称:①;② 。(2)、在实验室连接B、D装置进行实验,若D中蜡烛燃得更旺,则B中反应的化学方程式为。(3)、CO2能用向上排空气法收集,是因为;若用E装置干燥二氧化碳气体,E中应盛放的药品名称为。(4)、SO2易溶于水,溶于水可生成亚硫酸,实验室常用亚硫酸钠固体和稀硫酸反应常温下制取SO2 , 若想控制反应速率,图中最适宜的发生装置是;F实验中可观察到试管内且液体变为红色。29. 同学们学习“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究。
(提出问题)废液中所含溶质是什么?
(1)、(作出猜想)猜想1:溶质只有NaCl;猜想2:溶质是NaCl和HCl;
猜想3:溶质可能是NaCl、Na2CO3和HCl;
猜想4:溶质是。
(2)、(讨论与交流)小明认为猜想3无需验证就知道是错误的,他的理由是(用化学方程式说明)。(3)、(实验与结论)小亮同学为验证猜想2,取少量废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮认为猜想2正确,你认为他的结论(填“正确”和“不正确”),理由是。
请你另设计实验方案验证猜想2。
实验步骤
实验现象
实验结论
取少量废液于试管中,加入适量
产生气泡
猜想2正确
(4)、验证猜想4,可选用的试剂有(填字母序号)。A .酚酞溶液 B. 氢氧化钙溶液 C. 稀硫酸 D. 氯化钡溶液
(5)、(拓展与应用)若废液中的溶质是NaCl和HCl,无需另加试剂,只要对废液进行操作即可从废液中得到NaCl固体。四、计算题
-
30. 称取NaCl和BaCl2的固体混合物32、5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4↓+2NaCl)
 (1)、完全反应后生成BaSO4沉淀g.(2)、恰好完全反应时消耗Na2SO4溶液的质量是克?(3)、恰好完全反应时所得溶液中溶质的质量分数是?(精确到0.1%)
(1)、完全反应后生成BaSO4沉淀g.(2)、恰好完全反应时消耗Na2SO4溶液的质量是克?(3)、恰好完全反应时所得溶液中溶质的质量分数是?(精确到0.1%)