华师大版初中科学九上2.1生活中的酸和碱同步练习
试卷更新日期:2021-07-30 类型:同步测试
一、单选题
-
1. 小正同学测得下列水果的pH值,其中酸性最强的是( )A、葡萄pH=4.5
 B、菠萝pH=4.1
B、菠萝pH=4.1  C、柠檬pH=2.2
C、柠檬pH=2.2  D、草莓pH=3.1
D、草莓pH=3.1  2. 台州气候适宜,盛产各种酸甜爽口的水果。深受市民喜爱,分析下表,酸性最强的水果是( )
2. 台州气候适宜,盛产各种酸甜爽口的水果。深受市民喜爱,分析下表,酸性最强的水果是( )水果名称
东魁杨梅
涌泉蜜桔
楚门文旦
玉麟西瓜
pH值
2.5~3.5
4.0-5.0
4.5~5.5
5.5-6.5
A、东魁杨梅 B、涌泉蜜桔 C、楚门文旦 D、玉麟西瓜3. 在一定质量的NaOH溶液中逐滴加入蒸馏水,如图中能正确表示溶液pH变化的是(横坐 标表示加入蒸馏水的质量,纵坐标表示溶液的pH)( )A、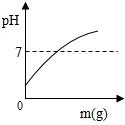 B、
B、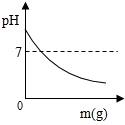 C、
C、 D、
D、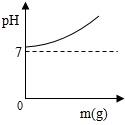 4. 测定人体内体液的pH,可以帮助人们了解身体的健康状况,一些体液的近似pH如下:下列体液中,碱性最强的是( )
4. 测定人体内体液的pH,可以帮助人们了解身体的健康状况,一些体液的近似pH如下:下列体液中,碱性最强的是( )体液
胃液
胰液
胆汁
血液
pH
0.8~1.5
7.5~8.0
6.8~7.4
7.35~7.45
A、胃液 B、胰液 C、胆汁 D、血液5. 夏季很多同学喜欢喝酸梅汤来消暑解渴,经实验测定酸梅汤呈弱酸性,下列接近酸梅汤pH的选项是( ) A、7.2 B、11 C、6.7 D、26. ①酸奶:②肥皂水;③食盐水是生活中常见的三种物质。酸奶能使紫色石蕊试液变红,肥皂水显碱性,食盐水的pH=7。它们的pH由小到大排列,正确的是( )A、①②③ B、①③② C、②①③ D、③②①7. 为了维持人体的健康生命活动,人体不同器官内的体液保持不同的酸碱性:
A、7.2 B、11 C、6.7 D、26. ①酸奶:②肥皂水;③食盐水是生活中常见的三种物质。酸奶能使紫色石蕊试液变红,肥皂水显碱性,食盐水的pH=7。它们的pH由小到大排列,正确的是( )A、①②③ B、①③② C、②①③ D、③②①7. 为了维持人体的健康生命活动,人体不同器官内的体液保持不同的酸碱性:体液
尿液
胃液
血液
汗液
pH
4.7~8.4
0.9~1.5
7.35~7.45
5.5~6.6
根据上表可知,在正常情况下( )
A、尿液一定呈酸性 B、血液一定呈碱性 C、胃液能使石蕊试液变蓝色 D、汗液能使酚酞试液变红色8. 向稀硫酸中加入下列物质,溶液的 pH 没有明显变化的是(不考虑溶液体积变化)( )A、铁 B、碳酸钙 C、硝酸钡 D、氢氧化钠9. 新鲜果汁是常见的饮料,下列四种饮料呈弱碱性的是( )A、柠檬汁(pH:2~3) B、苹果汁(pH:3~4)
B、苹果汁(pH:3~4)  C、西瓜汁(pH:5~6)
C、西瓜汁(pH:5~6)  D、玉米汁(pH:7~8)
D、玉米汁(pH:7~8)  10. 图示为某些物品对应的pH范围,其中显弱碱性的是( )
10. 图示为某些物品对应的pH范围,其中显弱碱性的是( ) A、小苏打 B、杨梅 C、栗子 D、菠萝11. 用碱性溶液浸泡蔬菜能有效除去蔬菜上的残留农药,降低对人体的损害。可用来浸泡蔬菜的碱性溶液是( )。A、食盐溶液 B、烧碱溶液 C、食醋溶液 D、纯碱溶液12. 将两种溶液混合未发生化学反应,所得溶液的pH等于3,则原来两种溶液的pH可能分别是( )。A、2和10 B、2和3 C、2和7 D、7和1013. 不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法错误的是( )
A、小苏打 B、杨梅 C、栗子 D、菠萝11. 用碱性溶液浸泡蔬菜能有效除去蔬菜上的残留农药,降低对人体的损害。可用来浸泡蔬菜的碱性溶液是( )。A、食盐溶液 B、烧碱溶液 C、食醋溶液 D、纯碱溶液12. 将两种溶液混合未发生化学反应,所得溶液的pH等于3,则原来两种溶液的pH可能分别是( )。A、2和10 B、2和3 C、2和7 D、7和1013. 不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法错误的是( )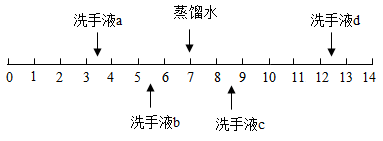 A、洗手液a用蒸馏水稀释后pH减小 B、洗手液b的酸性比a弱 C、洗手液c能使石蕊试液变蓝色 D、洗手液d和a混合液的pH可能等于714. 推理和归纳是科学学习和研究中常用的思维方法,下列推理正确的是( )A、大多数物质燃烧需要氧气,所以氧气具有可燃性 B、碱溶液呈碱性,所以呈碱性的溶液一定是碱的溶液 C、酸性溶液的pH都小于7,所以酸溶液的pH一定小于7 D、氧化物都含有氧元素,所以含氧元素的物质都是氧化物15. 如图是盐酸与氢氧化钠溶液反应过程中溶液pH变化图象,a点溶液的微观粒子图形是( )
A、洗手液a用蒸馏水稀释后pH减小 B、洗手液b的酸性比a弱 C、洗手液c能使石蕊试液变蓝色 D、洗手液d和a混合液的pH可能等于714. 推理和归纳是科学学习和研究中常用的思维方法,下列推理正确的是( )A、大多数物质燃烧需要氧气,所以氧气具有可燃性 B、碱溶液呈碱性,所以呈碱性的溶液一定是碱的溶液 C、酸性溶液的pH都小于7,所以酸溶液的pH一定小于7 D、氧化物都含有氧元素,所以含氧元素的物质都是氧化物15. 如图是盐酸与氢氧化钠溶液反应过程中溶液pH变化图象,a点溶液的微观粒子图形是( ) A、
A、 B、
B、 C、
C、 D、
D、 16. 以下是生活中常见水果的 pH 值,其中酸性最强的是( )
16. 以下是生活中常见水果的 pH 值,其中酸性最强的是( ) A、西瓜 B、青柠檬 C、葡萄 D、白梨17. 经检测,四种溶液除水分子外分别只含有下列粒子,其中属于酸的水溶液是( )A、H+ 、Na+、SO42- B、Ca2+ 、Cl- C、Ba2+ 、NO3- D、H+、Cl-18. 有A、B两种酸碱指示剂,它们显示的颜色与溶液pH的关系如图,它们在甲溶液和乙溶液中显示的颜色如表,下列判断错误的是( )
A、西瓜 B、青柠檬 C、葡萄 D、白梨17. 经检测,四种溶液除水分子外分别只含有下列粒子,其中属于酸的水溶液是( )A、H+ 、Na+、SO42- B、Ca2+ 、Cl- C、Ba2+ 、NO3- D、H+、Cl-18. 有A、B两种酸碱指示剂,它们显示的颜色与溶液pH的关系如图,它们在甲溶液和乙溶液中显示的颜色如表,下列判断错误的是( ) A、甲溶液肯定呈酸性 B、乙溶液的pH可能为11 C、只用A指示剂就可鉴别甲溶液、乙溶液和蒸馏水三种液体 D、在滴有A指示剂的甲溶液中不断加乙溶液,溶液最后一定呈绿色19. 下列检测某溶液pH的操作正确的是( )A、将pH试纸投入待测液,对照标准比色卡读数 B、用干燥、洁净的玻璃棒蘸取少量待测液,沾在置于洁净表面皿的pH试纸上,待试纸变色后,再对照标准比色卡读数 C、用玻璃棒蘸取待测液沾在用蒸馏水润湿的pH试纸上,对照标准比色卡读数 D、用蒸馏水冲洗玻璃棒,蘸取待测液沾在pH试纸上,对照标准比色卡读数20. 一些物质在常温下的近似pH如下表:
A、甲溶液肯定呈酸性 B、乙溶液的pH可能为11 C、只用A指示剂就可鉴别甲溶液、乙溶液和蒸馏水三种液体 D、在滴有A指示剂的甲溶液中不断加乙溶液,溶液最后一定呈绿色19. 下列检测某溶液pH的操作正确的是( )A、将pH试纸投入待测液,对照标准比色卡读数 B、用干燥、洁净的玻璃棒蘸取少量待测液,沾在置于洁净表面皿的pH试纸上,待试纸变色后,再对照标准比色卡读数 C、用玻璃棒蘸取待测液沾在用蒸馏水润湿的pH试纸上,对照标准比色卡读数 D、用蒸馏水冲洗玻璃棒,蘸取待测液沾在pH试纸上,对照标准比色卡读数20. 一些物质在常温下的近似pH如下表:物质
血浆
胃液
正常雨水
葡萄汁
pH
7.35~7.45
0.9~1.5
5.6
3.5~4.5
下列有关上述四种物质的说法中正确的是( )
A、只有葡萄汁显酸性 B、只有血浆显碱性 C、正常雨水显中性 D、胃酸过多的人应多饮用葡萄汁21. 如图“五环旗”中的上面3个环个代表一种液体,下面2个环各代表一种酸碱指示剂,两环相交部分表示指示剂跟有关液体混合后显示的颜色,如图表示相交部分显示的颜色,其中显示颜色不正确的是( ) A、红色 B、蓝色 C、红色 D、蓝色22. 图为喷墨打印机工作原理示意图,溶解在打印墨水(pH:7.5~9.0)中的染料。从喷嘴喷到打印纸(pH:4.5~6.5)上,变为不溶于水的固体。下列说法正确的是( )
A、红色 B、蓝色 C、红色 D、蓝色22. 图为喷墨打印机工作原理示意图,溶解在打印墨水(pH:7.5~9.0)中的染料。从喷嘴喷到打印纸(pH:4.5~6.5)上,变为不溶于水的固体。下列说法正确的是( ) A、打印墨水偏酸性 B、打印墨水呈中性 C、打印纸偏酸性 D、打印纸偏碱性23. 检测无色溶液酸碱性的实验中,下列根据实验现象得出的结论,错误的是( )。A、在溶液中滴人紫色石蕊试液,颜色变红,则所测溶液呈酸性 B、在溶液中滴人酚酞试液,溶液保持无色,则所测溶液呈酸性 C、将溶液滴在红色石蕊试纸上,试纸变蓝色,则所测溶液呈碱性 D、将溶液滴在蓝色石蕊试纸上,试纸变红色,则所测溶液呈酸性24. 为了证明能使石蕊试液变红的是硫酸溶液中的H+ , 某同学设计了如图所示实验。已知硫酸溶液中存在H+、 和H2O。下列哪几个实验的组合能证明使石蕊试液变红的是硫酸溶液中的H+( )。
A、打印墨水偏酸性 B、打印墨水呈中性 C、打印纸偏酸性 D、打印纸偏碱性23. 检测无色溶液酸碱性的实验中,下列根据实验现象得出的结论,错误的是( )。A、在溶液中滴人紫色石蕊试液,颜色变红,则所测溶液呈酸性 B、在溶液中滴人酚酞试液,溶液保持无色,则所测溶液呈酸性 C、将溶液滴在红色石蕊试纸上,试纸变蓝色,则所测溶液呈碱性 D、将溶液滴在蓝色石蕊试纸上,试纸变红色,则所测溶液呈酸性24. 为了证明能使石蕊试液变红的是硫酸溶液中的H+ , 某同学设计了如图所示实验。已知硫酸溶液中存在H+、 和H2O。下列哪几个实验的组合能证明使石蕊试液变红的是硫酸溶液中的H+( )。 A、①②④ B、②③④ C、①② D、②③
A、①②④ B、②③④ C、①② D、②③二、填空题
-
25. 雨、雪在形成和降落过程中,吸收、溶解了空气中的SO2及氮氧化物等物质,形成pH小于5.6的降水,称为酸雨。请回答下列有关酸雨的问题。
 (1)、若要测定某地采集到的雨水是否为酸雨,应选用更为精密的pH试纸进行检测,不能用石蕊或酚酞试液检测,其理由是。(2)、已知CO2的饱和溶液常温下pH不小于5.6。通常空气中CO2的含量高于SO2的含量,但人们反而将空气中的SO2认定为形成酸雨的主要原因之一。有同学想通过如图所示的实验寻找证据,你认为下一步的实验步骤是测定 , 只要出现的实验结果,就可认定SO2溶于水有可能形成酸雨。26. ①HClO3 , ②Na2SO4 , ③Ba(OH)2 , ④Na2SO4 , ⑤H2S,⑥KOH,这六种物质在水溶液中的电离状况如下:
(1)、若要测定某地采集到的雨水是否为酸雨,应选用更为精密的pH试纸进行检测,不能用石蕊或酚酞试液检测,其理由是。(2)、已知CO2的饱和溶液常温下pH不小于5.6。通常空气中CO2的含量高于SO2的含量,但人们反而将空气中的SO2认定为形成酸雨的主要原因之一。有同学想通过如图所示的实验寻找证据,你认为下一步的实验步骤是测定 , 只要出现的实验结果,就可认定SO2溶于水有可能形成酸雨。26. ①HClO3 , ②Na2SO4 , ③Ba(OH)2 , ④Na2SO4 , ⑤H2S,⑥KOH,这六种物质在水溶液中的电离状况如下:①HClO3=H++
②Na2SO3=2Na++
③Ba(OH)2=Ba2++2OH
④Na2SO4=2Na++
⑤H2S=H++HS-
⑥KOH=K++OH-
(1)、这六种物质中,属于酸的是 , 其判断的依据是 ;属于碱的是 , 其判断的依据是。(2)、小苏打的化学式为NaHCO3 , 它溶于水后溶液中会含有Na+、H+、 。小苏打是否属于酸类物质? , 其理由是 。
27. 如图所示装置中观察到紫色石蕊变红,物质A是(选填序号)。
①浓氨水②浓盐酸③浓硫酸
28. 画知识结构图有助于我们认清知识间的关系。某同学在学习了氢氧化钠的性质后画出了右图所示的化学性质关系图(“一”表示相连的两.种物质能发生反应,五个圈中的物质分别属于不同类别)。 (1)、已知X是一种指示剂,则X可能是(填一种即可)(2)、若Y是一种含硫元素且能形成酸雨的气体,写出氢氧化钠与Y反应的方程式:。29. 科学实验方案是根据特定实验目的而设计的。学习了“酸能使紫色石蕊试液变色”的知识后,进一步了解到“盐酸能电离产生H+和Cl- , 氯化钠能电离产生Na+和Cl-”。为深人研究某一问题,小科同学设计了如图所示的实验方案,请回答:
(1)、已知X是一种指示剂,则X可能是(填一种即可)(2)、若Y是一种含硫元素且能形成酸雨的气体,写出氢氧化钠与Y反应的方程式:。29. 科学实验方案是根据特定实验目的而设计的。学习了“酸能使紫色石蕊试液变色”的知识后,进一步了解到“盐酸能电离产生H+和Cl- , 氯化钠能电离产生Na+和Cl-”。为深人研究某一问题,小科同学设计了如图所示的实验方案,请回答: (1)、往三支试管中分别滴人2滴紫色石蕊试液后,乙试管中的溶液将变为色;(2)、小科设计的实验方案研究的主要问题是。30. 测定人体体液的pH 可以帮助我们了解身体状况,如图是小茗同学体检报告单截图,看图后回答问题:
(1)、往三支试管中分别滴人2滴紫色石蕊试液后,乙试管中的溶液将变为色;(2)、小科设计的实验方案研究的主要问题是。30. 测定人体体液的pH 可以帮助我们了解身体状况,如图是小茗同学体检报告单截图,看图后回答问题:项目
检测值
正常pH范围
血浆
7.4
7.35-7.45
胃液
0.8
0.9-1.5
胆汁
7.21
7.1-7.3
胰液
7.8
7.5-8.0
(1)、小茗同学的指标中有一项出现异常,医生除了给他开了药物之外,还提醒他注意饮食,下列食物(近似pH如下) 中适合该同学得有 。A、番茄(4.0--4.4) B、苹果(2.9--3.3) C、牛奶(6.3-6.6) D、豆浆(7.4--7.9)(2)、小茗同学想到在实验室中可用pH试纸测量溶液酸碱度,于是他从家里找来苹果,并用湿润的pH试纸进行了测量,那么测得的pH比实际结果 。A、偏大 B、偏小 C、不变 D、无法判断31. 物质的酸碱性与我们的生活密切相关。(1)、酸性是因为物质能电离出 , 可以使紫色石蕊试液变色。(2)、酸碱性强弱可用pH表示,通常洗衣粉、香皂呈碱性,即pH7.32. 向NaOH溶液中滴入HCl溶液至恰好完全反应。 (1)、如图表示该反应前后溶液中存在的主要离子,在横线上写出每种图形表示的离子(填离子符号)。(2)、发生反应的化学方程式是 。(3)、下列物质中只有一种能与KOH溶液发生上述类似反应,应是(填序号)
(1)、如图表示该反应前后溶液中存在的主要离子,在横线上写出每种图形表示的离子(填离子符号)。(2)、发生反应的化学方程式是 。(3)、下列物质中只有一种能与KOH溶液发生上述类似反应,应是(填序号)①HNO3②CusO4③CaCl2
33. 往一定量的酸(或碱)溶液中逐滴加入某碱(或酸)溶液至恰好完全中和时, 溶液的pH 随滴加的某溶液质量的变化而变化的关系如下图所示。请回答: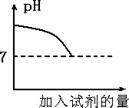 (1)、有同学根据右下图中的曲线判断实验中采用了 A 和 B 中的哪一个装置的操作?该同学判断的依据是。(2)、在以上实验中用了酚酞作指示剂,能够说明盐酸和氢氧化钠溶液恰好完全中和的实验现象是。34. 大多数农作物一般适宜在中性或接近中性的土壤里生长,为测定某农田土壤的酸碱度,同学们取来适量土样,请完成其pH的测定:(1)、把适量土样放入烧杯,并。(2)、用玻璃棒蘸取少许土壤浸出液滴在上,显色后将其与标准比色卡对照,即可测得土壤的酸碱度。
(1)、有同学根据右下图中的曲线判断实验中采用了 A 和 B 中的哪一个装置的操作?该同学判断的依据是。(2)、在以上实验中用了酚酞作指示剂,能够说明盐酸和氢氧化钠溶液恰好完全中和的实验现象是。34. 大多数农作物一般适宜在中性或接近中性的土壤里生长,为测定某农田土壤的酸碱度,同学们取来适量土样,请完成其pH的测定:(1)、把适量土样放入烧杯,并。(2)、用玻璃棒蘸取少许土壤浸出液滴在上,显色后将其与标准比色卡对照,即可测得土壤的酸碱度。三、解答题
-
35. 许多植物花瓣的浸出液遇到酸性或碱性溶液都会呈现出不同的颜色,在化学实验室中,常用作酸碱指示剂。现提取几中植物花瓣的浸出液分别滴入三种溶液中,实验记录如下表:
植物浸出液
稀盐酸溶液
氯化钠溶液
稀氢氧化钠溶液
万寿菊
黄色
黄色
黄色
牵牛花
红色
紫色
蓝色
玫瑰花
浅红色
浅红色
绿色
请分析并回答下列问题:
(1)、上述花瓣浸出液中,不能作酸碱指示剂的是(2)、若将牵牛花浸出液加入到食醋中,溶液会变 红色,若将玫瑰花浸出液加入某无色溶液中,溶液变绿色,则该溶液呈 性。四、实验探究题
-
36. 某同学要在一块空地上种植作物,于是对这块空地的土壤酸碱度进行测定。(1)、在空地上确定5~6个位置进行取样测定土壤酸碱度。以下三种取样位置设定合理的是。
 (2)、将采集到的土样进行处理后,用玻璃棒蘸取土壤浸出液,滴在上,将其呈现的颜色与标准比色卡比色,确定了空地土壤的pH约为7。查阅资料,常见作物最适生长的土壤pH范围如下表,则这块空地上适合种植的作物是。
(2)、将采集到的土样进行处理后,用玻璃棒蘸取土壤浸出液,滴在上,将其呈现的颜色与标准比色卡比色,确定了空地土壤的pH约为7。查阅资料,常见作物最适生长的土壤pH范围如下表,则这块空地上适合种植的作物是。作物
大蒜
丝瓜
茄子
沙枣
最适pH范围
5.6~6.0
6.0~6.5
6.8~7.3
8.0~8.7
37. 科学课上,小明已经学习了有关酸、碱、盐的内容,但有一个问题还困扰着小明同学,苹果到底是酸性物质还是碱性物质昵?爸爸认为:苹果富含苹果酸,肯定是酸性物质;妈妈认为:苹果是碱性物质,多吃苹果对身体有好处。为弄清楚这个问题,小明进行了课外自主学习和探究。[查阅资料]①在营养学中,食品的酸碱性分为“食品的口味酸碱性”和“食品的生理酸碱性”指食品被身体吸收后的酸碱性)
②多食用生理碱性食品,对维持人体体液的酸碱平衡有好处
③可以利用灼烧的方法来判断食品的生理酸碱性
[进行实验]①测定苹果的口味酸碱性:取苹果20克,榨汁,取滤液测得pH<7。
②测定苹果的生理酸碱性:另取苹果20克,切碎,放入坩埚内,加强热至质量不再变化,将残渣用少量水溶解,取滤液测得pH>7。
[初步认识]苹果是口味“酸性”,生理“碱性”的食品,常食用苹果对健康有利。
[继续探究]小明对实验结果感到很惊讶,他猜想:食品的口味酸碱性与生理酸碱性是否正好相反?又选了一些常见食晶用上述方法继续进行实验,小明设计一个实验记录表,收集存关数据。
[反思与分享]实验中,欲比较几种食品的生理酸碱性强弱,必须控制实验条件。
[实验结论]实验结果表明,呈生理碱性的食品有:柠檬、四季豆、菠菜、香蕉、海带等;呈生理酸性的食品有:猪肉、鸡肉、蛋黄、鲤鱼、花生等。有些物质口味酸碱性与生理酸碱性正好相反。
(1)、若要大致测定某溶液是酸性还是碱性的,下列可采用的是(填序号)①石蕊试液 ②pH试纸 ③石蕊试纸
(2)、根据小明继续探究的实验目的,你认为下列必测的项目是 (填序号),是必须在实验记录表中出现的栏目。A、食品名称 B、加热时间 C、残渣质量 D、坩埚质量 E、口味酸碱性 F、生理酸碱性(3)、若要比较香蕉和蛋黄这两种食品的生理酸碱性强弱,你认为必须控制的实验条件是 。38. 学习氢氧化钠的性质之后,知道氢氧化钠溶液中含有H2O、Na+、OH- , 能使无色酚酞试液变成红色。某科学小组想进一步探究是哪一种粒子使无色酚酞试液变成红色。[提出猜想]猜想①:可能是H2O;猜想②:可能是Na+;猜想③:可能是OH-。
[实验验证]
实验操作
实验现象
结论
①用试管取少量蒸馏水,滴入1~2滴无色酚酞试液,振荡
试管内溶液仍为无色
H2O不能使无色酚酞试液变红色
②用试管取少量氯化钠溶液,滴入1~2滴无色酚酞试液,振荡
试管内溶液仍为无色
③用试管取少量氢氧化钠溶液,滴入1~2滴无色酚酞试液,振荡
[讨论反思]有同学认为猜想①不需要实验验证就可以排除,你认为该同学的理由是 。
39. 某同学要在一块空地上种植作物,于是对这块空地的土壤酸碱度进行测定。(1)、在空地上确定5~6个位置进行取样测定壤酸碱度。以下三种取样位置设定合理的是。 (2)、将采集到的土样进行处理后,用玻璃棒蘸取土壤浸出液,滴在上,将其呈现的颜色与标准比色卡比色.确定了空地土壤的pH约为7.查阅资料,常见作物最适宜生长的土壤pH范围如下表,则这块空地上适合种植的作物有。
(2)、将采集到的土样进行处理后,用玻璃棒蘸取土壤浸出液,滴在上,将其呈现的颜色与标准比色卡比色.确定了空地土壤的pH约为7.查阅资料,常见作物最适宜生长的土壤pH范围如下表,则这块空地上适合种植的作物有。作物
大蒜
丝瓜
茄子
沙枣
最适pH范围
5.6~6.0
6.0~6.5
6.8~7.3
8.0~8.7
五、综合说理题
-
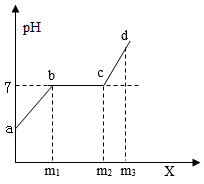
40. 在制取二氧化碳气体后,获得盐酸与氯化钙的混合溶液,往混合液中逐滴加入碳酸钠溶液时,混合溶液pH随加入碳酸钠溶液质量(X)的变化曲线大致如图所示。请解释pH变化的原因(氯化钙溶液显中性)。
-