备战2022 浙教版科学 中考高频考点 加强练 第77讲 离子或物质共存的问题
试卷更新日期:2021-07-29 类型:一轮复习
一、单选题
-
1. 某一电中性溶液中存在有五种离子,其中离子个数比Cl-:SO42-:Fe3+:K+:M=2:3:1:3:1,则M为( )A、碳酸根离子 B、铝离子 C、钠离子 D、镁离子2. 小明将一定量的铁粉加入氯化铜溶液中,反应前后溶液中存在的微粒模型如图所示。则表示Fe2+的模型是( )
 A、
A、 B、
B、 C、
C、 D、
D、 3. 下列各组离子在pH=1的溶液中能大量共存的是( )A、 B、 C、 D、4. 某固体由Ba2+、Cu2+、Na+、Cl﹣、CO32﹣、SO42﹣中的几种离子构成,取一定质量的该固体样品,进行如下实验:
3. 下列各组离子在pH=1的溶液中能大量共存的是( )A、 B、 C、 D、4. 某固体由Ba2+、Cu2+、Na+、Cl﹣、CO32﹣、SO42﹣中的几种离子构成,取一定质量的该固体样品,进行如下实验:①将固体溶于水得无色透明溶液,加入足量BaCl2溶液,过滤后得到5克白色沉淀。
②在沉淀中加入过量稀硝酸,仍有3克白色沉淀。
③在滤液中滴加AgNO3溶液,产生白色沉淀。则该固体中一定含有( )
A、Na+、CO32﹣、SO42﹣ B、Cu2+、CO32﹣、SO42﹣ C、Cl﹣、CO32﹣、SO42﹣ D、Na+、Ba2+、Cl-5. 甲、乙、丙、丁四种溶液中,分别含有Ba2+、Mg2+、Na+、H+、Cl-、CO32-、SO42-、OH-中的一种阳离子和一种阴离子。为确定四种溶液中所含的离子,小科进行了下面实验:①将甲溶液分别与其他三种溶液混合,都有白色沉淀生成;
②将乙溶液与丁溶液混合,有气泡产生;
③向丙溶液中滴入AgNO3溶液,出现白色沉淀,加稀硝酸后,沉淀不消失;
分析实验得到的以下结论中错误的是( )
A、甲溶液中一定含有Ba2+ B、乙溶液中可能含有SO42- C、丙溶液中一定含有Cl- D、丁溶液中一定含有Na+6. 下列离子能在pH=1的无色溶液中大量共存的是( )A、Ba2+、SO42-、Cl-、Na+ B、OH-、K+、NO3-、Ba2+ C、Mg2+、SO42-、Al3+、NO3- D、Na+、CO32-、Ca2+、Cl-7. 下列离子在水中能大量共存,并形成无色溶液的是( )A、Ba2+ , Cu2+ , OH- , NO3- B、Fe3+ , Cl- , NO3- , Mg2+ C、Na+ , H+ , CO32- , K+ D、Na+,Cl- , SO42- , Al3+8. 在含有大量Na+、H+、Cl﹣的溶液中,还可能大量存在的是( )A、OH﹣ B、Ag+ C、K+ D、CO32﹣9. 下列各组物质在给定条件下能大共存的是( )A、在PH=1的溶液中:NaCl、 Na2CO3、 Na2SO4 B、在PH=2的溶液中:KCl、Na2SO4、HNO3 C、在PH=13的溶液中:BaCl2、Na2CO3、NaOH D、在PH=14的溶液中:FeCl3、Ba(NO3)2、CaCl210. 室温下,在pH=1的溶液中可能大量共存的是( )A、K+、Cl−、 、OH− B、Na+、 、 、 C、NH4+、Cl−、 、 D、Ba2+、 、Cl−、11. 甲、乙、丙、丁四种溶液中,分别含有Ba2+,Mg2+,Na+ , H+ , OH-,Cl- , CO32-,SO42-中的一种阳离子和一种阴离子,为确定四种溶液中分别含有哪种阳离子和阴离子,进行了下面的实验:将甲溶液分别与其他三种溶液混合,都观察到白色沉淀生成;将乙、丁溶液混合,有气泡产生;向丙溶液中滴入硝酸银溶液,可明显观察到白色沉淀,加稀硝酸后,沉淀不消失。以下结论不正确的是( )A、甲溶液中一定含有钡离子 B、乙溶液中可能含有硫酸根离子 C、丙溶液中一定含有氯离子 D、丁溶液中一定含有钠离子12. 通过海水晒盐的方法得到的仅仅是粗盐,其中还含有少量的硫酸钠、氯化镁、氯化钙等杂质,它们在溶液中主要以SO42-、Ca2+、Mg2+的形式存在。为将这些杂质除净,可向食盐溶液中加过量的氢氧化钠溶液、碳酸钠溶液、氯化钡溶液,然后加入盐酸调至溶液pH=7,最后经过滤、蒸发得到精盐。下列操作及加入溶液顺序错误的是( )A、Na2CO3、BaCl2、NaOH、过滤、HCl B、NaOH、BaCl2、Na2CO3、过滤、HCl C、BaCl2、Na2CO3、NaOH、过滤、HCl D、BaCl2、NaOH、Na2CO3、过滤、HCl13. 下列各组物质能在同一溶液中大量共存的是( )A、NaCl、HCl、MgSO4、Cu(NO3)2 B、AgNO3、NaCl、Mg(NO3)2、NaOH C、Ca(OH)2、NaNO3、Na2CO3、NH4Cl D、HCl、K2SO4、NaOH、NaNO314. 在 pH=12 时,下列各组物质能大量共存的是( )A、NH4Cl Na2SO4 MgCl2 B、HCl KNO3 Ca(NO3)2 C、Na2CO3 Ba(OH)2 KCl D、NaOH KNO3 BaCl215. 下列离子能在pH=13的水溶液中大量共存的是( )A、 、Cl-、Na+、H+ B、K+、 、Cu2+、 C、Cl-、K+、 、Na+ D、Ca2+、Cl-、 、Na+16. 若在酸性溶液中,分别加入下列各组离子,可能共存的是下列哪一组( )A、Mg2+、K+、NO3-、Cl- B、NO3-、Cu2+、SO42-、OH- C、NH4+、Na+、NO3-、CO32- D、Ba2+、Na+、Mg2+、HCO3-17. 下列各组离子能在指定溶液中大量共存的一组是( )A、在稀盐酸中:Ba2-、CO32- 、Zn2+ B、在氢氧化钠溶液中:H+、Mg2-、Cl- C、在氯化钠溶液中:K+、Ca2+、 NO3- D、在硫酸铵溶液中:Na+、Cu2+、 OH-18. 下列各组物质,能在pH=1的溶液中大量共存,且形成无色溶液的是( )A、NaNO3、NaCl、CuSO4 B、NaOH、BaCl2、Na2SO4 C、NaCl、Na2SO4、Na2CO3 D、NaNO3、HCl、Na2SO419. 某造纸厂排放的碱性污水和某电镀厂排放的污水中,共含有以下8种离子中的各四种:Na+、H+、Ag+、Cu2+、OH-、CO32-、NO33-、Cl-,则电镀厂排放的污水中所含有的4种离子是( )A、Cu2+、H+、Ag+、NO3- B、OH-、Cl-、CO32-、Na+ C、H+、Cu2+、Cl-、Na+ D、H+、Na+、Ag+、NO3-20. 若两种不同的物质相互混合不发生反应,我们常称这两种物质能共存。下列各组物质,在溶液中能够共存的是( ) 。A、盐酸和硝酸银 B、硫酸和硝酸钡 C、盐酸和氯化钡 D、铁和稀盐酸二、填空题
-
21. 右表是小明收集的一些微粒的资料,请根据表格数据,回答下列问题。
粒子名称
质子数
中子数
电子数
A
14
14
14
B
26
30
24
C
14
14
18
D
14
18
14
(1)、表中的元素共有种。(2)、属于阳离子的是(填字母)。(3)、与A互为同位素原子的是。22. 甲乙两车间的废水中含有K+、Ag+、Cu2+、CO32-、OH-、NO3- 六种离子:(1)、乙车间的废水呈蓝色,其中的阴离子为;(2)、如果将甲乙两车间的废水混合,可以使废水的某些离子转化为沉淀,经过滤后的废水中含有(填氮肥,磷肥,钾肥或复合肥);(3)、写出检验其中一个车间废水中含有OH-的方法23. 现有甲、乙两种溶液,共有8种离子,分别为H+ , Ag+ , Ba2+ , K+,OH- , Cl- , NO3-和CO32- , 且两种溶液里所含的离子各不相同。已知向甲溶液里滴入紫色石蕊试液,溶液变成红色,说明甲溶液呈(填“酸性”、“碱性”或“中性”),那么乙溶液里含有的4种离子是(填离子符号)。24.(1)、某无色溶液中可能有Na+、Mg2+、Fe3+、Cl-、OH-、SO42-等离子中的一种或几种,经pH试纸测定,该溶液的pH为11。由此可知,该溶液中一定存在的阴离子有 , 一定不存在的离子有。(2)、有失去标签的碳酸钠溶液,氯化钡溶液和盐酸溶液,要求用一种试剂鉴别它们.学生甲选用一种酸溶液,学生乙选的是含钾的盐溶液,学生丙在得知氯化钡溶液的pH=7后,选用了一种有色溶液.这三位学生都成功了,请写出乙、丙学生选用试剂的名称.乙: 丙: .25. 有一包固体,可能由硝酸铜、硫酸钠、氯化钠、碳酸氢钠、氢氧化钠中的一种或几种组成。为了探究该固体的组成,某化学小组设计并开展以下实验:
已知,步骤Ⅰ中固体全部消失,溶液呈蓝色。有气泡产生。步骤Ⅱ、Ⅲ中均可观察到有白色沉淀生成。请回答下列问题:
(1)、原固体中一定含有的物质是 . 依据是 .(2)、步骤II中产生白色沉淀的化学方程式是 .(3)、步骤Ⅲ所得蓝色滤液中一定含有的溶质是 .26. 在分开盛放的A、B两溶液中。共含有Na+、Cu2+、Ba2+、Mg2+、NO3-、OH-、SO42-七种离子,两溶液里所含离子各不相同,已知A溶液里含三种阳离子和两种阴离子,其余的在B溶液里,则B溶液里所含离子应该是。27. 甲乙两车间的废水中含有Na+、Ag+、Cu2+、CO32-、OH–、NO3–六种离子(甲乙车间各含三种离子):(1)、乙车间的废水呈蓝色,其中的阴离子为 。(2)、如果将甲乙两车间的废水混合,可以使废水的某些离子转化为沉淀,经过滤后的废水中含有;28. 皮蛋是我国传统风味食品,制作皮蛋的方法有多种,一种制作含锌皮蛋的方法是把鸭蛋放在培养液中浸泡,培养液由水、食盐、氢氧化钠、少量硫酸锌等物质配制而成。(1)、取少量培养液于试管中,滴入无色酚酞溶液后变红,则培养液的 pH7(填“<”、“>”或“=”);(2)、在(1)的试管中滴加过量稀硫酸,红色褪去,其中反应的化学方程式:;这时在所得的溶液中加入一种盐溶液产生了沉淀,该盐可能是(可多选)。A.BaCl2 B.CuSO4 C.AgNO3 D.KNO3
29. 硝酸钠与氯化钙互相交换成分没有沉淀、气体或水生成,某化学小组同学从微观角度进一步理解复分解反应的实质。(1)、复分解反应的实质是某些阴、阳离子结合生成沉淀、气体或的过程。
(2)、A、B、C、D四种可溶性盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是NO3-、SO42-、Cl-、CO32-中的某一种。若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色。若向四支试管中分别加盐酸,B盐溶液有沉淀产生,D盐溶液有无色无味的气体逸出。推断它们的化学式为:A. , B. , C. , D.。
30. A、B、C、D四种离子化合物,由以下两组离子构成(每种离子只能选用一次)。阳离子
Ba2+
Na+
Fe3+
Mg2+
阴离子
Cl-
NO3-
SO42-
OH-
四种化合物之间的反应有如下现象:①A+B→白色沉淀,不溶于硝酸;②B+D→红褐色沉淀;③C+B→白色沉淀,再加硝酸沉淀则转化为C。
(1)、试确定A、B、C、D四种物质的名称:A为;B为;C为 ;D为 。
(2)、完成上述③中的两个反应的化学方程式 , 。三、实验探究题
-
31. 某无色溶液中可能含有Na+、H+、Cl-、SO42- , 现在想要检测两种阴离子是否存在,请你帮助完成实验:(1)、取适量溶液,先向其中滴加足量的溶液,再滴加足量的稀硝酸,若有白色沉淀生成,则证明有SO42-存在。(2)、再取上层清液滴加溶液,又出现白色沉淀,则可证明有Cl-存在。(3)、如何检验溶液中存在氢离子?。32. 在老师的指导下,小敏开展如下实验探究活动:(1)、A、B、C、D分别是碳酸钠、氢氧化钠、氢氧化钙、硫酸钠中的一种,它们之间的转化关系如图一所示(“→”表示物质之间的转化关系,“—”表示物质之间可以发生化学反应).


四种物质中,属于盐类的物质是(填化学式,下同).物质D是.
(2)、设计一个优化的实验方案,验证某氯化钠溶液中混有碳酸钠、硫酸钠和氢氧化钠并提纯氯化钠,其实验流程及部分实验现象如图二所示.药品溶液的pH7,试剂甲是溶液.33. 下图是初中科学中常见物质间的转化关系,其中C是光合作用的气态产物,D为一种理想的新能源,G为紫红色金属,它们均为单质,其余为化合物.其中F与H的组成元素相同;J不溶于水,是常见的重要的建筑材料(反应条件、部分反应物和生成物均已略去).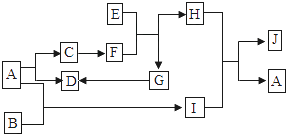 (1)、B的化学式为;(2)、D→G反应的基本类型是 .
(1)、B的化学式为;(2)、D→G反应的基本类型是 .
(3)、写出反应H+I→J+A的化学方程式 .
34. 现有含NaCl、Na2SO4、NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、NO3-的相互分离。相应的实验过程可用下列流程图表示: (1)、写出上述实验过程中所用试剂、沉淀的化学式:试剂1:试剂3:沉淀C:(2)、写出溶液a中所含有的阳离子(3)、恰当地控制试剂4的加入量的方法是35. 化工厂排放的污水中可能含有对人体有害的物质,某科学兴趣小组就收集了甲、乙、丙三家化工厂排放的污水.取得的三家化工厂的污水均为无色、透明、均一的状态.(1)、已知甲工厂排放的污水中可能含有Fe3+、Ba2+、Na+、OH﹣、Cl﹣、CO32﹣、SO42﹣;为了进一步确认,进行实验检测:
(1)、写出上述实验过程中所用试剂、沉淀的化学式:试剂1:试剂3:沉淀C:(2)、写出溶液a中所含有的阳离子(3)、恰当地控制试剂4的加入量的方法是35. 化工厂排放的污水中可能含有对人体有害的物质,某科学兴趣小组就收集了甲、乙、丙三家化工厂排放的污水.取得的三家化工厂的污水均为无色、透明、均一的状态.(1)、已知甲工厂排放的污水中可能含有Fe3+、Ba2+、Na+、OH﹣、Cl﹣、CO32﹣、SO42﹣;为了进一步确认,进行实验检测:a.向取样的污水中,滴入稀硫酸,有大量白色沉淀产生,再加稀硝酸,白色沉淀不消失.
b.用pH试纸测定污水的pH值,试纸显深蓝色.由此可知,该污水中,肯定含有离子是 . 肯定没有的离子是 .
(2)、乙、丙两工厂排放的废水中共含有H+、Ag+、K+、Ba2+、OH﹣、Cl﹣、NO3﹣、CO32﹣8种离子,两种废水里所含离子各不相同,已知向乙工厂废水里滴入石蕊试液,石蕊试液变成蓝色,则丙工厂废水里含有的4种离子应该是 .四、解答题
-
36. 现有 HCl 与 CaCl2 的混合溶液,为了分析混合溶液中 HCl 和 CaCl2 的质量分数,设计了如图 1 所示实验方案:
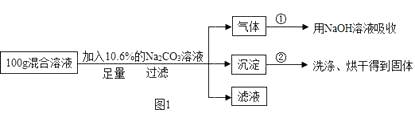
【实验数据】实验共记录了两组数据:
第①组,气体吸收完全后,NaOH 溶液质量增加 4.4g;
第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为 10g. 根据实验设计及有关数据进行分析与计算:
(1)、生成气体的质量为 .(2)、混合溶液中 CaCl2 的质量分数为多少?(写出计算过程)(3)、若在 100g 混合溶液中不断加入 10.6%的 Na2CO3 的溶液,请在图 2 中画出加入 Na2CO3溶液的质量与产生沉淀的质量的关系图。
 37. 镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取.主要步骤如下:
37. 镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取.主要步骤如下: (1)、为了使MgCl2转化为Mg(OH)2 , 试剂①可以选用 , 要使
(1)、为了使MgCl2转化为Mg(OH)2 , 试剂①可以选用 , 要使MgCl2完全转化为沉淀,加入试剂①的量应足量.
(2)、加入试剂①后,从溶液中能够分离得到Mg(OH)2沉淀的方法是.(3)、试剂②可以选用 .(4)、无水MgCl2在熔融状态下,通电后会产生Mg和Cl2 , 其化学方程式.38. 兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液。他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:
小杨、小陈同学在步骤I中提出X能否改用锌的问题上产生了分歧。请你也参与他们的讨论,表明论点,并说明理由。