备战2022 浙教版科学 中考高频考点 加强练 第65讲 有关化学式的计算和推断
试卷更新日期:2021-07-29 类型:一轮复习
一、单选题
-
1. 据报道,科学家已在实验室利用催化剂,实现常温常压下将甲酸分解制出氢气。其变化前后的微观示意图如图所示。下列说法正确的是( )
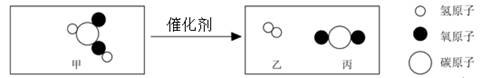 A、甲酸由碳、氢、氧三种原子组成 B、甲酸相对分子质量为46克 C、丙分子中碳、氧原子个数比为2 : 1 D、由乙分子构成的物质是单质2. 5月22日10时40分,“祝融号”火星车己安全驶离着陆平台(如图),到达火星表面,开始巡视探测。它将利用三结砷化镓太阳能电池作为其动力,制取砷化镓(GaAs)的化学原理为:(CH3)3Ga+AsH3 GaAs+3X,则X的化学式为( )
A、甲酸由碳、氢、氧三种原子组成 B、甲酸相对分子质量为46克 C、丙分子中碳、氧原子个数比为2 : 1 D、由乙分子构成的物质是单质2. 5月22日10时40分,“祝融号”火星车己安全驶离着陆平台(如图),到达火星表面,开始巡视探测。它将利用三结砷化镓太阳能电池作为其动力,制取砷化镓(GaAs)的化学原理为:(CH3)3Ga+AsH3 GaAs+3X,则X的化学式为( ) A、C2H2 B、C2H4 C、CH4 D、H23. 一定条件下,在一密闭容器内发生某化学反应,并测得反应前后各物质的质量如图所示。下列说法正确的是( )
A、C2H2 B、C2H4 C、CH4 D、H23. 一定条件下,在一密闭容器内发生某化学反应,并测得反应前后各物质的质量如图所示。下列说法正确的是( )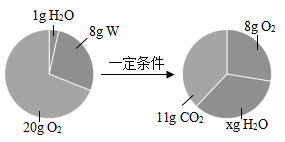 A、x的值为9 B、该反应中氧气与水的质量变化之比为6:5 C、W由碳、氢两种元素组成 D、W中碳、氢元素质量比为3:14. 2020年2月4日,中国工程院院士李兰娟的研究团队发现:达芦那韦(化学式:C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列说法错误的是( )A、 达芦那韦由五种元素组成 B、达芦那韦由分子构成 C、一个达芦那韦分子由75个原子构成 D、达芦那韦中C,H两种元素的质量比为27:375. 化合物A和B均由元素X、Y组成,X元素化合价均为正价,在A中X的质量分数为40%,在B中X的质量分数为50%,已知A中X、Y原子个数比为1:3,则B的化学式为( )A、Y2X B、Y3X C、XY2 D、XY36. 连花清瘟胶囊具有清瘟解毒,宣肺泄热的功效。其成分中含有一种名为绿原酸的物质,下列有关绿原酸(C16H18O9)的说法正确的是( )A、绿原酸是由3种元素组成的化合物 B、绿原酸的相对分子质量是354g C、绿原酸中氢元素的质量分数最大 D、绿原酸由16个碳原子、18个氢原子和9个氧原子构成7. PLA是一种新型可降解塑料,以乳酸(C3H6O3)为主要原料聚合而成,下列有关乳酸的说法错误的是( )A、乳酸是由碳、氢、氧三种元素组成 B、乳酸中含有12个原子 C、乳酸的相对分子质量是90 D、乳酸中氧元素的质量分数最大8. 《我不是药神》是一部关于白血病和印度药的电影作品。药品“甲磺酸伊马替尼片”用于治疗慢性髓性白血病和恶性胃肠道间质肿瘤,原理是融合基因,使BCR-ABL蛋白得不到磷酸,不能活化,就发不出指令,细胞的增殖态势便会得到抑制。甲磺酸伊马替尼的化学式为C29H31N7O·CH4SO3 , 关于甲磺酸伊马替尼的说法正确的是( )A、甲磺酸伊马替尼是由八种元素组成的化合物 B、甲磺酸伊马替尼由77个原子构成 C、甲磺酸伊马替尼中碳、氢、氧元素的质量比为30∶35∶4 D、甲磺酸伊马替尼的相对分子质量是5899. 现有一种由FeSO4和Fe2(SO4)3组成的固体混合物,已知该混合物中硫元素的质量分数为23%,则该混合物中铁元素的质量分数为( )A、31% B、40% C、30% D、46%10. 瑞德西韦一度被认为是治疗新冠肺炎较为有效的药物,其主要成分的化学式是C27H35N6O8P,对此分析可得出的信息是( )A、相对分子质量为602g B、1个C27H35N6O8P分子中有35个氢原子 C、该分子由五种元素组成 D、该物质中氢元素的质量分数最大11. 2013年5月,国内外各大媒体曝光;山东潍坊霞山区生姜种植户,在种植内销的生姜时使用了一种叫“神农丹”的剧毒农药.“神农丹”所含物质的化学式为C7H14N2O2S,下列关于该物质的说法,不正确的是( )A、该物质由五种元素组成 B、该物质的一个分子中含碳、氢原子的个数比为1:2 C、该物质燃烧时可能会产生形成酸雨的物质 D、该物质中硫元素质量分数最小12. 在CO、HCOOH、OHC—COOH的混合物中,H%=y,则C%为( )A、 B、 C、 D、13. 目前农村正在推广“测土配方施肥”技术,农技员对某土地检测后给出了施肥配方,该土壤施加NH4NO3 , K2CO3;若测定该混合化肥中氮元素的质量分数为28%,则固体混合物中K2CO3的质量分数为( )A、85% B、20% C、25% D、80%14. 某钢铁厂用800吨(Fe%=75%)FeO、Fe2O3、Fe3O4的混合铁矿石炼铁,炼得生铁(生铁中非铁元素含量<8%、C%为2%-4.3%)的质量可能是( )A、600吨 B、608吨 C、625吨 D、676.5吨15. 由碳、氧两种元素组成的气体中,碳与氧的质量比为3:5,则该气体可能是( )A、只由CO组成的纯净物 B、由CO和CO2共同组成的混合物 C、只由CO2组成的纯净物 D、由CO2和O2共同组成的混合物16. 硫化镉是“纹身彩贴”的主要成分,可经皮肤进入体内,干扰人体正常的新陈代谢。已知硫化镉中镉(Cd)元素的化合价为+2、硫(S)元素的化合价为-2,其化学式是( )A、Cd2S B、CdS2 C、Cd2S3 D、CdS17. 燃放烟花爆竹时,产生一种具有刺激性气味的气体,会造成大气污染。这种气体由两种元素组成且两种元素的质量分数相等,它是( )A、H2S B、SO2 C、NO2 D、CO18. 某混合物中只含Na2SO4 、Na2S和Na2SO3 , 已知硫元素的质量分数为16%,则氧元素的质量分数为( )A、16% B、32% C、39% D、61%19. X、Y两元素的相对原子质量之比为7∶2 ,X与Y形成的化合物中,X、Y两元素的质量之比为21∶8 ,则该化合物的化学式可表示为( )A、X3Y2 B、X3Y4 C、X2Y3 D、XY20. 某NH4Cl样品中含有92%的NH4Cl,此样品中所含氮元素的质量分数是( )A、46% B、34% C、28% D、24%
A、x的值为9 B、该反应中氧气与水的质量变化之比为6:5 C、W由碳、氢两种元素组成 D、W中碳、氢元素质量比为3:14. 2020年2月4日,中国工程院院士李兰娟的研究团队发现:达芦那韦(化学式:C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列说法错误的是( )A、 达芦那韦由五种元素组成 B、达芦那韦由分子构成 C、一个达芦那韦分子由75个原子构成 D、达芦那韦中C,H两种元素的质量比为27:375. 化合物A和B均由元素X、Y组成,X元素化合价均为正价,在A中X的质量分数为40%,在B中X的质量分数为50%,已知A中X、Y原子个数比为1:3,则B的化学式为( )A、Y2X B、Y3X C、XY2 D、XY36. 连花清瘟胶囊具有清瘟解毒,宣肺泄热的功效。其成分中含有一种名为绿原酸的物质,下列有关绿原酸(C16H18O9)的说法正确的是( )A、绿原酸是由3种元素组成的化合物 B、绿原酸的相对分子质量是354g C、绿原酸中氢元素的质量分数最大 D、绿原酸由16个碳原子、18个氢原子和9个氧原子构成7. PLA是一种新型可降解塑料,以乳酸(C3H6O3)为主要原料聚合而成,下列有关乳酸的说法错误的是( )A、乳酸是由碳、氢、氧三种元素组成 B、乳酸中含有12个原子 C、乳酸的相对分子质量是90 D、乳酸中氧元素的质量分数最大8. 《我不是药神》是一部关于白血病和印度药的电影作品。药品“甲磺酸伊马替尼片”用于治疗慢性髓性白血病和恶性胃肠道间质肿瘤,原理是融合基因,使BCR-ABL蛋白得不到磷酸,不能活化,就发不出指令,细胞的增殖态势便会得到抑制。甲磺酸伊马替尼的化学式为C29H31N7O·CH4SO3 , 关于甲磺酸伊马替尼的说法正确的是( )A、甲磺酸伊马替尼是由八种元素组成的化合物 B、甲磺酸伊马替尼由77个原子构成 C、甲磺酸伊马替尼中碳、氢、氧元素的质量比为30∶35∶4 D、甲磺酸伊马替尼的相对分子质量是5899. 现有一种由FeSO4和Fe2(SO4)3组成的固体混合物,已知该混合物中硫元素的质量分数为23%,则该混合物中铁元素的质量分数为( )A、31% B、40% C、30% D、46%10. 瑞德西韦一度被认为是治疗新冠肺炎较为有效的药物,其主要成分的化学式是C27H35N6O8P,对此分析可得出的信息是( )A、相对分子质量为602g B、1个C27H35N6O8P分子中有35个氢原子 C、该分子由五种元素组成 D、该物质中氢元素的质量分数最大11. 2013年5月,国内外各大媒体曝光;山东潍坊霞山区生姜种植户,在种植内销的生姜时使用了一种叫“神农丹”的剧毒农药.“神农丹”所含物质的化学式为C7H14N2O2S,下列关于该物质的说法,不正确的是( )A、该物质由五种元素组成 B、该物质的一个分子中含碳、氢原子的个数比为1:2 C、该物质燃烧时可能会产生形成酸雨的物质 D、该物质中硫元素质量分数最小12. 在CO、HCOOH、OHC—COOH的混合物中,H%=y,则C%为( )A、 B、 C、 D、13. 目前农村正在推广“测土配方施肥”技术,农技员对某土地检测后给出了施肥配方,该土壤施加NH4NO3 , K2CO3;若测定该混合化肥中氮元素的质量分数为28%,则固体混合物中K2CO3的质量分数为( )A、85% B、20% C、25% D、80%14. 某钢铁厂用800吨(Fe%=75%)FeO、Fe2O3、Fe3O4的混合铁矿石炼铁,炼得生铁(生铁中非铁元素含量<8%、C%为2%-4.3%)的质量可能是( )A、600吨 B、608吨 C、625吨 D、676.5吨15. 由碳、氧两种元素组成的气体中,碳与氧的质量比为3:5,则该气体可能是( )A、只由CO组成的纯净物 B、由CO和CO2共同组成的混合物 C、只由CO2组成的纯净物 D、由CO2和O2共同组成的混合物16. 硫化镉是“纹身彩贴”的主要成分,可经皮肤进入体内,干扰人体正常的新陈代谢。已知硫化镉中镉(Cd)元素的化合价为+2、硫(S)元素的化合价为-2,其化学式是( )A、Cd2S B、CdS2 C、Cd2S3 D、CdS17. 燃放烟花爆竹时,产生一种具有刺激性气味的气体,会造成大气污染。这种气体由两种元素组成且两种元素的质量分数相等,它是( )A、H2S B、SO2 C、NO2 D、CO18. 某混合物中只含Na2SO4 、Na2S和Na2SO3 , 已知硫元素的质量分数为16%,则氧元素的质量分数为( )A、16% B、32% C、39% D、61%19. X、Y两元素的相对原子质量之比为7∶2 ,X与Y形成的化合物中,X、Y两元素的质量之比为21∶8 ,则该化合物的化学式可表示为( )A、X3Y2 B、X3Y4 C、X2Y3 D、XY20. 某NH4Cl样品中含有92%的NH4Cl,此样品中所含氮元素的质量分数是( )A、46% B、34% C、28% D、24%二、填空题
-
21. 2020年12月,贴满“暖宝宝”的嫦娥五号返回器图片(如图1)火遍全网。给返回器贴“暖宝宝”是为了防止它携带的推进剂无水肼(N2H4)凝固。
 (1)、无水肼中各元素的质量分数模型如图2所示,图中甲表示的元素是。(2)、下列关于无水肼说法正确的有 。A、无水肼的相对分子质量是32 B、无水肼中氮元素的化合价为-2价 C、无水肼分子由氮元素和氢元素组成 D、无水肼由2个氮原子和4个氢原子构成22. 调味剂的主要作用是补充、增强或增加食品的味道。食醋是一种能增强食品酸味的调味剂,主要成分为醋酸(CH3COOH) 。根据所学知识回答:(1)、食醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CH3COO-和(填离子符号)。(2)、醋酸中C:H:O元素的质量比为。23. 尿素是一种常见的化肥,它的化学式是CO(NH2)2 。(1)、从化肥种类的角度判断,尿素属于。(2)、尿素中氮元素和氧元素的质量比为。(填最简比)24. 在K2R2O7中(R代表某元素)含钾元素26.5%,氧元素38.1%,推算出R的相对原子质量是;甲、乙两种化合物都只含有X、Y两种元素.甲、乙两种化合物中X元素的质量分数分别为30.4%和25.9%.若已知甲的化学式为XY2 , 则乙的化学式为 。25.(1)、X、Y两种元素组成的化合物甲和乙,甲的化学式为X2Y3 , 其中Y元素的质量分数为50%,乙中X元素的质量分数为60%,则乙的化学式为;(2)、元素X的原子失去1个电子,元素Y的原子得到2个电子后,所形成的离子所带电子数均与氖原子相同,由X、Y两元素的离子形成的化合物的相对分子质量为;(3)、相同质量的H2O2和D2O(D即2H)中氢元素的质量比为。(4)、某样品可能由铁、氧化亚铁、氧化铁和四氧化三铁中的一种或几种组成,现测得该样品中铁元素与氧元素的质量比是21:8;若该样品由两种物质混合而成,则一定不含;若该样品由三种物质混合而成,则一定含有。26.(1)、地壳中含量最多的金属元素与非金属元素形成的物质的化学式为;(2)、元素X的原子获得2个电子,元素Y的原子失去1个电子后,所形成离子的所带电子数均与氖原子相同,由X、Y两元素的离子形成的化合物(具体物质)的化学式为;(3)、相同质量的H2O2和H2O中氢元素的质量比为。(4)、某样品可能由氧化亚铁、氧化铁和四氧化三铁中的一种或几种组成,现测得该样品中铁元素与氧元素的质量比是21:8,则该样品的成分有种可能;若该样品由两种物质混合而成,则一定不含。27. 美国食品与药品管理局为美国吉利德科学公司的瑞德西韦开绿灯,批准该药物用于住院的新冠肺炎患者。瑞德西韦也成为美国首个获准用于新冠患者的药物。瑞德西韦的化学式为[C27H35N6O8P],请根据信息回答:(1)、瑞德西韦由种元素组成;一个瑞德西韦分子中共含有个原子;(2)、瑞德西韦中氢、氮元素质量比为;(3)、301g瑞德西韦中含有g碳元素。28.(1)、某三价金属与氧元素形成的化合物中氧元素质量分数为30%,则该金属的相对原子质量为。(2)、A、B两元素相对原子质量之比为2∶1,仅由这两种元素组成的化合物里,A、B两元素质量比为2∶3,若其中B为-n价,则此化合物中A元素的化合价为。(3)、元素R可与氧形成多种化合物,其中RO中含氧53.33%,那么相对分子质量为76,含氧量为63.16%的R与氧元素形成的化合物的化学式是。(4)、要使CO2和CO中含有相同质量的氧元素,则CO2和CO的质量比是。29. 可乐是一种碳酸饮料,由水、二氧化碳、蔗糖等物质组成。经常过量饮用可乐易导致肥胖。(1)、蔗糖的化学式是C12H22O11 , 蔗糖中碳元素和氢元素的质量比为 。(2)、成人每天摄入的糖分超过25克就容易导致肥胖。可乐中糖分的质量分数约为10%,则饮用克可乐就相当于摄入了25克糖分。30. 使H2O2和H2O中含有相同质量的氧元素,则H2O2和H2O的质量比是;若使H2O2和H2O中含有相同质量的氢元素,则H2O2和H2O的分子个数比为。
(1)、无水肼中各元素的质量分数模型如图2所示,图中甲表示的元素是。(2)、下列关于无水肼说法正确的有 。A、无水肼的相对分子质量是32 B、无水肼中氮元素的化合价为-2价 C、无水肼分子由氮元素和氢元素组成 D、无水肼由2个氮原子和4个氢原子构成22. 调味剂的主要作用是补充、增强或增加食品的味道。食醋是一种能增强食品酸味的调味剂,主要成分为醋酸(CH3COOH) 。根据所学知识回答:(1)、食醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CH3COO-和(填离子符号)。(2)、醋酸中C:H:O元素的质量比为。23. 尿素是一种常见的化肥,它的化学式是CO(NH2)2 。(1)、从化肥种类的角度判断,尿素属于。(2)、尿素中氮元素和氧元素的质量比为。(填最简比)24. 在K2R2O7中(R代表某元素)含钾元素26.5%,氧元素38.1%,推算出R的相对原子质量是;甲、乙两种化合物都只含有X、Y两种元素.甲、乙两种化合物中X元素的质量分数分别为30.4%和25.9%.若已知甲的化学式为XY2 , 则乙的化学式为 。25.(1)、X、Y两种元素组成的化合物甲和乙,甲的化学式为X2Y3 , 其中Y元素的质量分数为50%,乙中X元素的质量分数为60%,则乙的化学式为;(2)、元素X的原子失去1个电子,元素Y的原子得到2个电子后,所形成的离子所带电子数均与氖原子相同,由X、Y两元素的离子形成的化合物的相对分子质量为;(3)、相同质量的H2O2和D2O(D即2H)中氢元素的质量比为。(4)、某样品可能由铁、氧化亚铁、氧化铁和四氧化三铁中的一种或几种组成,现测得该样品中铁元素与氧元素的质量比是21:8;若该样品由两种物质混合而成,则一定不含;若该样品由三种物质混合而成,则一定含有。26.(1)、地壳中含量最多的金属元素与非金属元素形成的物质的化学式为;(2)、元素X的原子获得2个电子,元素Y的原子失去1个电子后,所形成离子的所带电子数均与氖原子相同,由X、Y两元素的离子形成的化合物(具体物质)的化学式为;(3)、相同质量的H2O2和H2O中氢元素的质量比为。(4)、某样品可能由氧化亚铁、氧化铁和四氧化三铁中的一种或几种组成,现测得该样品中铁元素与氧元素的质量比是21:8,则该样品的成分有种可能;若该样品由两种物质混合而成,则一定不含。27. 美国食品与药品管理局为美国吉利德科学公司的瑞德西韦开绿灯,批准该药物用于住院的新冠肺炎患者。瑞德西韦也成为美国首个获准用于新冠患者的药物。瑞德西韦的化学式为[C27H35N6O8P],请根据信息回答:(1)、瑞德西韦由种元素组成;一个瑞德西韦分子中共含有个原子;(2)、瑞德西韦中氢、氮元素质量比为;(3)、301g瑞德西韦中含有g碳元素。28.(1)、某三价金属与氧元素形成的化合物中氧元素质量分数为30%,则该金属的相对原子质量为。(2)、A、B两元素相对原子质量之比为2∶1,仅由这两种元素组成的化合物里,A、B两元素质量比为2∶3,若其中B为-n价,则此化合物中A元素的化合价为。(3)、元素R可与氧形成多种化合物,其中RO中含氧53.33%,那么相对分子质量为76,含氧量为63.16%的R与氧元素形成的化合物的化学式是。(4)、要使CO2和CO中含有相同质量的氧元素,则CO2和CO的质量比是。29. 可乐是一种碳酸饮料,由水、二氧化碳、蔗糖等物质组成。经常过量饮用可乐易导致肥胖。(1)、蔗糖的化学式是C12H22O11 , 蔗糖中碳元素和氢元素的质量比为 。(2)、成人每天摄入的糖分超过25克就容易导致肥胖。可乐中糖分的质量分数约为10%,则饮用克可乐就相当于摄入了25克糖分。30. 使H2O2和H2O中含有相同质量的氧元素,则H2O2和H2O的质量比是;若使H2O2和H2O中含有相同质量的氢元素,则H2O2和H2O的分子个数比为。三、实验探究题
-
31. 科学兴趣小组利用如图装置对FeSO4·nH2O晶体中的结晶水的含量进行测定(铁架台等己省略)。已知:①FeSO4和FeSO4·nH2O加热时易被空气氧化;②FeSO4·nH2O FeSO4+nH2O。实验步骤如下:

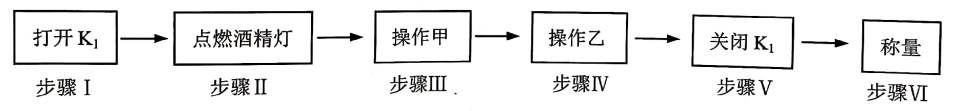
请回答:
(1)、步骤Ⅰ打开K1导入二氧化碳气体,排尽装置中的空气,其目的是 。(2)、步骤Ⅳ中的操作乙是通二氧化碳直至C装置冷却至室温,则操作甲指的是。(3)、有同学建议,为加快产生CO2的速率,可将A中装置中盐酸浓度增大、石灰石磨成粉状。制取气体时反应速度是否越快越好?其理由是。(4)、步骤Ⅵ称量,若晶体FeSO4·nH2O质量为m,反应前后C装置质量减少了m1 , D装置质量增加了m2 , 则此晶体中的结晶水的百分含量为。(用字母表示)
32. 实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子构成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按图所示装置进行实验,每步均充分反应。回答下列问题: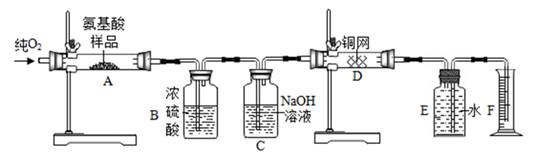 (1)、实验开始时,首先通入一段时间的氧气,其理由是。(2)、以上装置中需要加热的仪器有A和D两处,操作时应先点燃处的酒精灯。(3)、实验测得B、C装置分别增重4.5克和8.8克,则该物质化学式中x、y之比为。(4)、将B和C装置互换,则测得的氢元素的含量会(选填“偏大”、“偏小”“不变”)。33. 只含铜和氧两种元素的固体样品18g,测得铜元素的质量为16g。已知铜的氧化物有CuO和Cu2O。请通过分析或计算回答下列问题:(1)、该样品的组成情况有。(写出所有可能的组成);(2)、若固体样品由两种物质组成,则质量偏少的那种物质在样品中的质量分数为。(用分数表示)34. 用含有二氧化碳和水蒸气杂质的某种还原性气体测定一种铁的氧化物(FexOy)的组成,实验装置如图所示。根据下图,试回答:
(1)、实验开始时,首先通入一段时间的氧气,其理由是。(2)、以上装置中需要加热的仪器有A和D两处,操作时应先点燃处的酒精灯。(3)、实验测得B、C装置分别增重4.5克和8.8克,则该物质化学式中x、y之比为。(4)、将B和C装置互换,则测得的氢元素的含量会(选填“偏大”、“偏小”“不变”)。33. 只含铜和氧两种元素的固体样品18g,测得铜元素的质量为16g。已知铜的氧化物有CuO和Cu2O。请通过分析或计算回答下列问题:(1)、该样品的组成情况有。(写出所有可能的组成);(2)、若固体样品由两种物质组成,则质量偏少的那种物质在样品中的质量分数为。(用分数表示)34. 用含有二氧化碳和水蒸气杂质的某种还原性气体测定一种铁的氧化物(FexOy)的组成,实验装置如图所示。根据下图,试回答: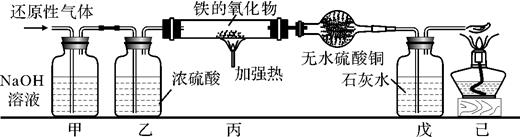 (1)、实验过程中丁装置白色粉末变蓝色,而戊装置中溶液没有明显变化,则该还原性气体是.(2)、当丙装置中的FexOy,全部被还原后,称量剩余固体的质量为11.2克,同时测得丁装置的质量增加了5.4克。则该铁的氧化物的化学式为。(3)、上述实验装置中,如果没有乙装置,将使测定结果中铁元素与氧元素的质量的比值。(填“偏大”、“偏小”或“无影响”)35. 为了了测定某品牌食用纯碱中碳酸钠的质量分数,小明取10克食用纯碱样品和足量的稀硫酸,进行如图甲实验,实验前后,均需往装置中缓慢通一会儿氮气.(样品中其他成分不与稀硫酸反应)
(1)、实验过程中丁装置白色粉末变蓝色,而戊装置中溶液没有明显变化,则该还原性气体是.(2)、当丙装置中的FexOy,全部被还原后,称量剩余固体的质量为11.2克,同时测得丁装置的质量增加了5.4克。则该铁的氧化物的化学式为。(3)、上述实验装置中,如果没有乙装置,将使测定结果中铁元素与氧元素的质量的比值。(填“偏大”、“偏小”或“无影响”)35. 为了了测定某品牌食用纯碱中碳酸钠的质量分数,小明取10克食用纯碱样品和足量的稀硫酸,进行如图甲实验,实验前后,均需往装置中缓慢通一会儿氮气.(样品中其他成分不与稀硫酸反应) (1)、实验前,先往A装置通入一会儿氮气的目的是;(2)、小金想用碱石灰(氢氧化钠固体和生石灰的混合物)来代替B装置中浓硫酸的吸水作用,小科认为不可以,其理由是;(3)、根据乙图分析,判断反应生成的二氧化碳已被完全吸收的依据是;(4)、下列情况会造成碳酸钠的质量分数偏大的是A、稀硫酸换为浓盐酸 B、反应结束后忘记通氮气 C、样品中的碳酸钠没有反应完 D、外界空气通过导管进入C 装置
(1)、实验前,先往A装置通入一会儿氮气的目的是;(2)、小金想用碱石灰(氢氧化钠固体和生石灰的混合物)来代替B装置中浓硫酸的吸水作用,小科认为不可以,其理由是;(3)、根据乙图分析,判断反应生成的二氧化碳已被完全吸收的依据是;(4)、下列情况会造成碳酸钠的质量分数偏大的是A、稀硫酸换为浓盐酸 B、反应结束后忘记通氮气 C、样品中的碳酸钠没有反应完 D、外界空气通过导管进入C 装置四、解答题
-
36. 嘌呤是合成DNA的主要物质,广泛存在于细胞核中,嘌呤的化学式为C5H4N4 , 在人体内会被氧化成尿酸,血液中尿酸含量过高容易引起痛风。(1)、嘌呤的相对分子质量为。(2)、嘌呤中碳元素和氢元素的质量比为。(3)、尿酸主要通过(器官)形成的尿液排出体外。(4)、对于以上材料。以下观点或者推论正确的有 。A、尿酸过高的人,应该控制高嘌呤食物的摄入 B、嘌呤是合成DNA的主要物质,动物性食物和植物性食物中都含嘌呤 C、嘌呤是合成DNA的主要物质,摄入嘌呤会引起人体遗传物质的改变37. “青团”是宁波的一种传统食物。在“青团”制作过程中,需要往糯米粉中添加艾草(或艾草汁)。艾草含有侧柏莲酮芳香油(C10H10O),侧柏莲酮芳香油是一种淡黄色液体,具有香脂香气,所以“青团”具有独特风味。(1)、侧柏莲酮芳香油由种元素组成。(2)、7.3g侧柏莲桐芳香油中碳元素的质量为g。(3)、侧柏莲桐芳香油在氧气中完全燃烧的产物是。38. 磁铁矿石(含Fe3O4)是常用的炼铁原料,工业上可通过如下反应:4CO+Fe3O4 3Fe+4CO2 , 将其中的Fe3O4转化为Fe。(1)、Fe3O4中铁元素和氧元素的质量比为。(2)、假设冶炼过程中铁没有损耗,用含有464吨Fe3O4的磁铁矿石可提炼出含铁质量分数为96%的生铁多少吨?39. 尿素(化学式为CO(NH2)2)是一种常用的氮肥。(1)、尿素的相对分子质量为;(2)、尿素中氮元素的质量分数为(用百分数表示,保留一位小数);(3)、氮元素是合成植物叶绿素、蛋白质的原料之一,能促进植物枝叶生长。计算与300元尿素所含氮元素质量相等的碳酸氢铵(NH4HCO3 , 相对分子质量79)质量是多少?(已知尿素的价格为5元/kg)40. 按我国政府要求2021年1月1日起餐饮行业已禁用不可降解的一次性塑料吸管,取而代之的是一些可降解的环保吸管,环保纸吸管的主要成分是纤维素,化学式为(C6H10O5)n,而原来塑料吸管的主要成分是聚丙烯,化学式为(C3H6)n。(1)、纤维素是一种(选填“有机物”或“无机物”)。(2)、纤维素分子中,氢、氧原子的个数比为 。(3)、计算32.4克纤维素中所含碳元素质量与多少克聚丙烯中所含碳元素质量相同?