备战2022 浙教版科学 中考高频考点 加强练 第61讲 元素
试卷更新日期:2021-07-28 类型:一轮复习
一、单选题
-
1. 钪在元素周期表中的信息如图,其单质在工业上常用来制耐高温合金等。则( )
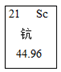 A、钪原子的原子核中有21个中子 B、钪元素的元素符号为Sc C、钪元素的相对原子质量为44.96g D、钪单质稍微加热就会熔化2. 2020年12月17日,嫦娥五号返回器携带月壤样品回到地球。月壤中蕴含He-3,它被认为是解决未来能源问题的重要物质之一。He-3原子核内有2个质子和1个中子。地球上的氦元素主要以He-4(信息如图所示)形式存在。下列说法不正确的是( )
A、钪原子的原子核中有21个中子 B、钪元素的元素符号为Sc C、钪元素的相对原子质量为44.96g D、钪单质稍微加热就会熔化2. 2020年12月17日,嫦娥五号返回器携带月壤样品回到地球。月壤中蕴含He-3,它被认为是解决未来能源问题的重要物质之一。He-3原子核内有2个质子和1个中子。地球上的氦元素主要以He-4(信息如图所示)形式存在。下列说法不正确的是( ) A、 He-3、He-4属于同种元素 B、 He-3、He-4互为同位素 C、 He-3和He-4的相对原子质量相同 D、 He-3原子和He-4原子的电子数相同3. 2021年4月13日,日本政府决定将福岛核污水排入大海。核污水中含大量对人体有害的放射性物质,如锶的同位素。如图是元素周期表中锶的有关信息,下列说法错误的是( )
A、 He-3、He-4属于同种元素 B、 He-3、He-4互为同位素 C、 He-3和He-4的相对原子质量相同 D、 He-3原子和He-4原子的电子数相同3. 2021年4月13日,日本政府决定将福岛核污水排入大海。核污水中含大量对人体有害的放射性物质,如锶的同位素。如图是元素周期表中锶的有关信息,下列说法错误的是( )
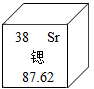 A、锶原子的质量为87.62克 B、锶原子的核外电子数为38 C、锶原子的核内质子数为38 D、锶原子的相对原子质量为87.624. 2019年是元素周期表诞生第150周年。下表是元素周期表的一部分,从表中不能获取的信息是( )
A、锶原子的质量为87.62克 B、锶原子的核外电子数为38 C、锶原子的核内质子数为38 D、锶原子的相对原子质量为87.624. 2019年是元素周期表诞生第150周年。下表是元素周期表的一部分,从表中不能获取的信息是( ) A、 元素在周期表中的位置 B、原子的质子数 C、元素的相对原子质量 D、原子的中子数5. 用
A、 元素在周期表中的位置 B、原子的质子数 C、元素的相对原子质量 D、原子的中子数5. 用 分别表示质子、中子和电子,如图表示四种原子结构模型,下列有关说法正确的是( )
分别表示质子、中子和电子,如图表示四种原子结构模型,下列有关说法正确的是( ) 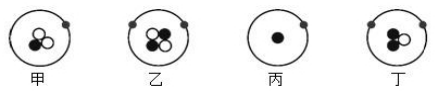 A、甲、乙互为同位素 B、乙、丁为同一种元素 C、甲、丙的核电荷数不同 D、丙、丁为同一种原子6. 含氧的微粒有O2、O3、O2-、O22- , 下列说法中正确的是( )A、相同的分子数的O2和O3具有相同的质子数 B、等质量的O2和O3具有相同的原子数 C、O2和O3是氧元素的两种同位素 D、H2O2、O2-、O22-三种微粒中所含的电子数多少排列为H2O2>O22->O2-7. 如图是元素周期表中的部分信息。下列叙述错误的是( )
A、甲、乙互为同位素 B、乙、丁为同一种元素 C、甲、丙的核电荷数不同 D、丙、丁为同一种原子6. 含氧的微粒有O2、O3、O2-、O22- , 下列说法中正确的是( )A、相同的分子数的O2和O3具有相同的质子数 B、等质量的O2和O3具有相同的原子数 C、O2和O3是氧元素的两种同位素 D、H2O2、O2-、O22-三种微粒中所含的电子数多少排列为H2O2>O22->O2-7. 如图是元素周期表中的部分信息。下列叙述错误的是( ) A、硼元素为非金属元素 B、碳元素原子的质子数为6 C、金刚石是由碳元素组成的单质 D、氮元素的相对原子质量为14.01g8. 我国的北斗导航卫星系统采用铷原子钟,授时精度达到百亿分之三秒。铷元素的部分信息如图所示,下列有关铷的说法不正确的是( )
A、硼元素为非金属元素 B、碳元素原子的质子数为6 C、金刚石是由碳元素组成的单质 D、氮元素的相对原子质量为14.01g8. 我国的北斗导航卫星系统采用铷原子钟,授时精度达到百亿分之三秒。铷元素的部分信息如图所示,下列有关铷的说法不正确的是( )
 A、属于金属元素 B、铷原子核外有37个电子 C、相对原子质量为85.47g D、元素符号为Rb9. 铱﹣192是一种放射性物质,对人体有严重辐射伤害。如图所示是元素周期表中铱元素的有关信息,下列说法错误的是( )
A、属于金属元素 B、铷原子核外有37个电子 C、相对原子质量为85.47g D、元素符号为Rb9. 铱﹣192是一种放射性物质,对人体有严重辐射伤害。如图所示是元素周期表中铱元素的有关信息,下列说法错误的是( )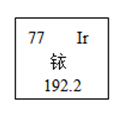 A、铱元素原子的原子核内有77个质子 B、铱元素是金属元素 C、铱元素原子的核外有77个电子 D、铱元素的相对原子质量为192.2g10. 下列元素分类正确的是( )A、金属元素:钙、镁、钡、铜、铁、汞 B、非金属元素:碳、氢、氧、氮、磷、金 C、稀有元素:氦、氖、氩、氪、氯、氡 D、人体必需的微量元素:铁、碘、氟、硒、钙、铅11. 下列关于符号“K”所表示的意义,正确的是( )
A、铱元素原子的原子核内有77个质子 B、铱元素是金属元素 C、铱元素原子的核外有77个电子 D、铱元素的相对原子质量为192.2g10. 下列元素分类正确的是( )A、金属元素:钙、镁、钡、铜、铁、汞 B、非金属元素:碳、氢、氧、氮、磷、金 C、稀有元素:氦、氖、氩、氪、氯、氡 D、人体必需的微量元素:铁、碘、氟、硒、钙、铅11. 下列关于符号“K”所表示的意义,正确的是( )①钾元素②钾的原子核③一个钾元素④一个钾原子⑤金属钾
A、①②⑤ B、②③④⑤ C、①④⑤ D、①③④⑤12. 如图是金元素在元素周期表中的信息示意图,从图中获取的信息正确的是( ) A、金元素属于非金属元素 B、一个金原子的中子数为197.0 C、一个金原子的核外电子数为118 D、一个金原子核带有79个单位的正电荷13. 溴元素的原子结构示意图及其在周期表中的信息如图所示,下列说法正确的是( )
A、金元素属于非金属元素 B、一个金原子的中子数为197.0 C、一个金原子的核外电子数为118 D、一个金原子核带有79个单位的正电荷13. 溴元素的原子结构示意图及其在周期表中的信息如图所示,下列说法正确的是( )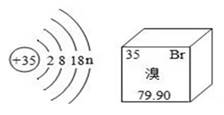 A、n=7 B、该元素为金属元素 C、相对原子质量和中子数均为35g D、原子序数、核电荷数、质子数均为79.9014. 人类用于制造触屏材料的铟,相关信息如图,下列说法中正确的是( )
A、n=7 B、该元素为金属元素 C、相对原子质量和中子数均为35g D、原子序数、核电荷数、质子数均为79.9014. 人类用于制造触屏材料的铟,相关信息如图,下列说法中正确的是( ) A、铟是一种非金属元素 B、原子的核电荷数为49 C、与其他元素根本区别是中子数不同 D、相对原子质量是114.8g15. 下列符号既可表示一个原子,又可表示一种元素,还能表示一种物质的是( )A、N B、Mg C、O2 D、H16. 国际通用的元素符号是用1个或2个拉丁文字母表示的,其中第一个字母大写,第二个字母小写。镍元素的拉丁文名称为Niccolum,则镍的元素符号为( )A、Ni B、NI C、n D、Na17. 下列元素名称与元素符号书写都正确的是( )A、锌Zn B、硅SI C、氯cl D、贡Hg18. 生活中常会见到“加碘盐”、“含氟牙膏”、“加铁酱油”,其中的“碘”、“氟”、“铁”指的是( )A、原子 B、离子 C、元素 D、分子19. 2019年诺贝尔化学奖授予给了三位科学家,以表彰他们在发明锂电池过程中做出的贡献。锂的元素符号是( )A、 La B、Li C、Al D、Be20. 用数轴表示某些化学知识直观、简明、易记,下列数轴表示错误的是( )
A、铟是一种非金属元素 B、原子的核电荷数为49 C、与其他元素根本区别是中子数不同 D、相对原子质量是114.8g15. 下列符号既可表示一个原子,又可表示一种元素,还能表示一种物质的是( )A、N B、Mg C、O2 D、H16. 国际通用的元素符号是用1个或2个拉丁文字母表示的,其中第一个字母大写,第二个字母小写。镍元素的拉丁文名称为Niccolum,则镍的元素符号为( )A、Ni B、NI C、n D、Na17. 下列元素名称与元素符号书写都正确的是( )A、锌Zn B、硅SI C、氯cl D、贡Hg18. 生活中常会见到“加碘盐”、“含氟牙膏”、“加铁酱油”,其中的“碘”、“氟”、“铁”指的是( )A、原子 B、离子 C、元素 D、分子19. 2019年诺贝尔化学奖授予给了三位科学家,以表彰他们在发明锂电池过程中做出的贡献。锂的元素符号是( )A、 La B、Li C、Al D、Be20. 用数轴表示某些化学知识直观、简明、易记,下列数轴表示错误的是( ) A、地壳中元素含量由高到低 B、不同种原子的原子序数依次递增 C、空气中气体体积分数由大到小 D、含氮物质中氮元素的化合价从低到高
A、地壳中元素含量由高到低 B、不同种原子的原子序数依次递增 C、空气中气体体积分数由大到小 D、含氮物质中氮元素的化合价从低到高二、填空题
-
21. A是相对原子量最小的元素,B元素组成的一种单质可供人体呼吸,C元素是地壳中含量最多的金属元素,请写出相应的化学式:A元素和B元素组成的一种化合物 , C元素组成的单质。22. 2021年3月,四川三星堆遗址进行了新一轮考古发掘。至今三星堆已出土了黄金面具、青铜纵目面具等一批珍贵文物,如图。
 (1)、出土的黄金面具仍金光灿灿,而青铜纵目面具已锈迹斑斑,这说明金的活动性比铜(选填“强”或“弱”)。(2)、古代制作青铜器的铜来源于铜矿,如黄铜矿。黄铜矿的主要成分为二硫化亚铁铜 (CuFeS2),其中铁元素和铜元素均为+2价,硫元素的化合价为 。(3)、应用碳-14测出三星堆遗址距今3000年左右,碳-12和碳-14是碳元素的两种同位素原子,它们的主要区别是原子核中 数不同。23. 如图为钟表式元素周期表,该钟表的整点时间小时数与该元素的质子数相等。“时针”和“分针”指向对应的两种元素,1:00对应的两种元素各自形成的单质、 , 8:00对应的两种元素形成的化合物为。
(1)、出土的黄金面具仍金光灿灿,而青铜纵目面具已锈迹斑斑,这说明金的活动性比铜(选填“强”或“弱”)。(2)、古代制作青铜器的铜来源于铜矿,如黄铜矿。黄铜矿的主要成分为二硫化亚铁铜 (CuFeS2),其中铁元素和铜元素均为+2价,硫元素的化合价为 。(3)、应用碳-14测出三星堆遗址距今3000年左右,碳-12和碳-14是碳元素的两种同位素原子,它们的主要区别是原子核中 数不同。23. 如图为钟表式元素周期表,该钟表的整点时间小时数与该元素的质子数相等。“时针”和“分针”指向对应的两种元素,1:00对应的两种元素各自形成的单质、 , 8:00对应的两种元素形成的化合物为。 24. 元素周期表是学习和研究科学的重要工具。下表是元素周期表的一部分,据表回答问题:
24. 元素周期表是学习和研究科学的重要工具。下表是元素周期表的一部分,据表回答问题: (1)、原子序数为11和17的两种元素组成的物质是生活中一种必不可少的物质,该物质是由(选填“分子”“原子”或“离子”)构成。(2)、核磁共振(NMR)技术已广泛应用于医学领域,已知只有质子数为奇数的原子才有NMR现象,表中标号为①~⑤的五种元素的原子,能产生NMR现象的是(填写元素符号)。25. 如图为某牙膏的部分标签,活性成分单氟磷酸钠的化学式为Na2PO3F(相对分子质量为144),请回答下列问题。
(1)、原子序数为11和17的两种元素组成的物质是生活中一种必不可少的物质,该物质是由(选填“分子”“原子”或“离子”)构成。(2)、核磁共振(NMR)技术已广泛应用于医学领域,已知只有质子数为奇数的原子才有NMR现象,表中标号为①~⑤的五种元素的原子,能产生NMR现象的是(填写元素符号)。25. 如图为某牙膏的部分标签,活性成分单氟磷酸钠的化学式为Na2PO3F(相对分子质量为144),请回答下列问题。 (1)、人体中氟元素属于(填“微量”或“常量”)元素。(2)、Na2PO3F中金属元素与氧元素的质量比为。(3)、若牙膏中其他成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为g。(结果保留小数点后一位)26. 信息:化学中我们可以用原子结构示意图来表示原子核电荷数和核外电子排布。如:氧原子的原子结构示意图为
(1)、人体中氟元素属于(填“微量”或“常量”)元素。(2)、Na2PO3F中金属元素与氧元素的质量比为。(3)、若牙膏中其他成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为g。(结果保留小数点后一位)26. 信息:化学中我们可以用原子结构示意图来表示原子核电荷数和核外电子排布。如:氧原子的原子结构示意图为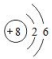 ,其中
,其中 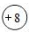 表示核电荷数,
表示核电荷数, 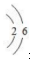 表示核外电子排布。
表示核外电子排布。 图中的①是元素周期表中的某种元素的信息,②中A、B、C、D是四种粒子的原子结构示意图。请你回答:
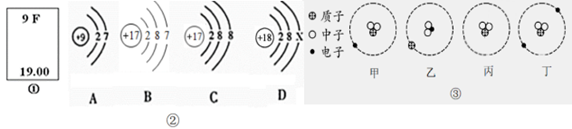 (1)、图①所代表的元素名称是 , 该元素的原子19F的中子数为;(2)、A,B,C,D属于同种元素的粒子是(填序号);(3)、图C所表示的粒子的化学符号是。(4)、图D所表示的元素所组成的单质化学式是。(5)、氚是氢的一种同位素,氚原子含有1个质子和2个中子。图③中能正确表示氚离子(3H+)结构的是(填序号)。27. 右表微粒中,属于同种元素的是。互为同位素原子的是。
(1)、图①所代表的元素名称是 , 该元素的原子19F的中子数为;(2)、A,B,C,D属于同种元素的粒子是(填序号);(3)、图C所表示的粒子的化学符号是。(4)、图D所表示的元素所组成的单质化学式是。(5)、氚是氢的一种同位素,氚原子含有1个质子和2个中子。图③中能正确表示氚离子(3H+)结构的是(填序号)。27. 右表微粒中,属于同种元素的是。互为同位素原子的是。组别
质子
中子
电子
A
14
14
14
B
17
18
17
C
17
20
17
D
17
18
18
28. 下列元素符号书写上都有错误,请改正。(1)、钙CA:(2)、氯CL:(3)、镁Ma:(4)、钠Ne:(5)、汞HG:(6)、氦Hi:29. 根据所给的元素名称填写元素符号①镁 ②铝 ③锂 ④氧 ⑤钙
⑥氩 ⑦氟 ⑧碳 ⑨氯 ⑩磷
30. 核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列问题。(注圆圈表示原子核,圈内数字表示核内带电微粒数目,弧线上数字表示电子数) (1)、2017年5月9日,中国科学院等单位联合发布了115号元素的中文名为“镆”。此元素原子的核电荷数为 , 核外电子数为。(2)、在第三周期中,随着原子序数的递增,元素原子核外电子数目的变化规律是。(3)、利用上表中给出的元素,写出含有氢元素的常见单质、化合物的化学式各一个:单质;化合物。(4)、钠和氯元素构成的化合物是由构成的。
(1)、2017年5月9日,中国科学院等单位联合发布了115号元素的中文名为“镆”。此元素原子的核电荷数为 , 核外电子数为。(2)、在第三周期中,随着原子序数的递增,元素原子核外电子数目的变化规律是。(3)、利用上表中给出的元素,写出含有氢元素的常见单质、化合物的化学式各一个:单质;化合物。(4)、钠和氯元素构成的化合物是由构成的。三、实验探究题
-
31. 20世纪30年代,美国科学家鲁宾和卡门利用18O分别标记H2O和CO2 , 将C18O2和CO2分别通入含小球藻的H2O和H218O中(如右图所示),迅速收集产生的氧气
 (1)、18O和16O互为原子,H218O和H2O以及CO2和C18O2具有相同的化学性质,因此可以用来示踪物质变化情况。(2)、该实验是为了研究。(3)、该实验必须在条件下进行。(4)、制备含有较多小球藻的液体时,需在盛有小球藻的液体中加入(选填“无机盐”或“无机盐和有机物”),并置于适宜环境下培养。32. 小林同学收集了一些微粒的资料,请你和他一起根据表格数据回答下列问题。
(1)、18O和16O互为原子,H218O和H2O以及CO2和C18O2具有相同的化学性质,因此可以用来示踪物质变化情况。(2)、该实验是为了研究。(3)、该实验必须在条件下进行。(4)、制备含有较多小球藻的液体时,需在盛有小球藻的液体中加入(选填“无机盐”或“无机盐和有机物”),并置于适宜环境下培养。32. 小林同学收集了一些微粒的资料,请你和他一起根据表格数据回答下列问题。微粒名称
质子数
中子数
电子数
带电性
A
14
14
14
不带电
B
26
30
24
带2个单位正电荷
C
14
14
16
D
14
16
14
不带电
(1)、表格中属于互为同位素的是。(2)、根据表格信息写出微粒C的符号。(3)、比较C与D两种微粒,其中质量较大的是。33. 元素周期表是化学学习和研究的重要工具。如图所示为元素周期表的一部分: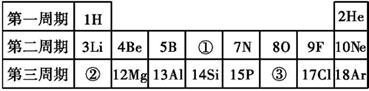 (1)、②所示元素与③所示元素的元素符号分别是和。它们在元素周期表里属于同一(选填“周期”或“族”),写出②所示元素与氧元素组成的化合物的化学式。(2)、③所示元素原子的核外电子数是 , 它在发生化学反应时容易(选填“得到”或“失去”)电子,形成的离子符号是。
(1)、②所示元素与③所示元素的元素符号分别是和。它们在元素周期表里属于同一(选填“周期”或“族”),写出②所示元素与氧元素组成的化合物的化学式。(2)、③所示元素原子的核外电子数是 , 它在发生化学反应时容易(选填“得到”或“失去”)电子,形成的离子符号是。四、解答题
-
34. 氕、氘、氚是氢的三种同位素原子,它们的原子结构模型如图所示,相关信息如下表。试回答:
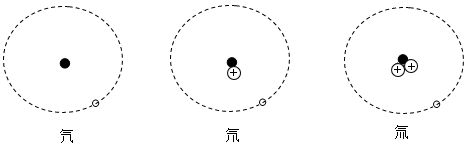
名称
符号
相对原子质量
氕 H
1
氘 D
2
氚 T
3
(1)、超重水有一定的放射性。一个超重水分子由两个氚原子和一个氧原子构成,其化学式可表示为T2O。T2O中T的化合价为。(2)、重水是由氘和氧组成的化合物,化学式可表示为D2O,重水和普通水化学性质相似。在海水中重水的质量约占0.02%,则100吨海水中所含氘的质量是多少?(3)、原子结构模型中的“ ”表示的粒子是。 35. 当前正是“水果之王”西瓜俏销的季节。西瓜味道甘甜多汁,清爽解渴,含有水、蛋白质、葡萄糖、维生素C、铁等多种营养成分,是最富有营养、最纯净、食用最安全的食品之一。(1)、人体需要七大营养素,上面没有涉及到的营养素是。(2)、上面提到的“铁”指的是铁(选填“原子”、“单质”或“元素”);(3)、维生素C也叫抗坏血酸,其化学式为:C6H8O6。则17.6克维生素C完全燃烧后放出的二氧化碳的质量为克。36. 在“宏观﹣微观﹣符号”之间建立联系,是学习化学的一种重要思维方式。如图是元素周期表中部分元素的原子结构模型图,根据所学知识回答下列问题.
”表示的粒子是。 35. 当前正是“水果之王”西瓜俏销的季节。西瓜味道甘甜多汁,清爽解渴,含有水、蛋白质、葡萄糖、维生素C、铁等多种营养成分,是最富有营养、最纯净、食用最安全的食品之一。(1)、人体需要七大营养素,上面没有涉及到的营养素是。(2)、上面提到的“铁”指的是铁(选填“原子”、“单质”或“元素”);(3)、维生素C也叫抗坏血酸,其化学式为:C6H8O6。则17.6克维生素C完全燃烧后放出的二氧化碳的质量为克。36. 在“宏观﹣微观﹣符号”之间建立联系,是学习化学的一种重要思维方式。如图是元素周期表中部分元素的原子结构模型图,根据所学知识回答下列问题. (1)、A属于元素(填元素种类);(2)、D原子与钠发生化学反应时易(填“得到”或“失去”)电子;(3)、由B元素和D元素组成的化合物的化学式为;(4)、E粒子带1个单位正电荷,则该粒子的符号为;(5)、F为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是 .A、原子序数Z>Y B、核外电子数:X=Y C、Y和Z的化学性质相似37. 元素周期表中,核电荷数从 1 到 18 的元素的原子结构示意图如下图。根据已有的结 构理论回答下列问题:
(1)、A属于元素(填元素种类);(2)、D原子与钠发生化学反应时易(填“得到”或“失去”)电子;(3)、由B元素和D元素组成的化合物的化学式为;(4)、E粒子带1个单位正电荷,则该粒子的符号为;(5)、F为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是 .A、原子序数Z>Y B、核外电子数:X=Y C、Y和Z的化学性质相似37. 元素周期表中,核电荷数从 1 到 18 的元素的原子结构示意图如下图。根据已有的结 构理论回答下列问题: (1)、已知 M2-核外有 x 个电子,其中相对原子质量为 a,则该粒子含有的中子数为 ;(2)、1-18 号元素中,A 原子的核电荷数为 m,已知 A2-和 B3+具有相同的电子层结构,则 B 原子核中 的质子数为 ;(3)、具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有一些相似的结构和性质。 下列各组粒子中属于等电子体的是 (填字母序号);A、NO 和 O2 B、CO 和 N2 C、SO2 和 CO2 D、PO4和SO4(4)、某粒子的结构示意图
(1)、已知 M2-核外有 x 个电子,其中相对原子质量为 a,则该粒子含有的中子数为 ;(2)、1-18 号元素中,A 原子的核电荷数为 m,已知 A2-和 B3+具有相同的电子层结构,则 B 原子核中 的质子数为 ;(3)、具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有一些相似的结构和性质。 下列各组粒子中属于等电子体的是 (填字母序号);A、NO 和 O2 B、CO 和 N2 C、SO2 和 CO2 D、PO4和SO4(4)、某粒子的结构示意图 ,当 x-y=8 时,该粒子的符号为 。
,当 x-y=8 时,该粒子的符号为 。