山西省晋中市祁县、灵石县2021年中考化学模拟试卷
试卷更新日期:2021-07-28 类型:中考模拟
一、单选题
-
1. 下列物质的用途体现了物质的物理性质的是( )A、用高梁酿造高梁酒 B、干冰用于食品冷藏保鲜 C、一定条件下,石墨转化为金刚石 D、一氧化碳用于冶炼金属2. 硫元素形成的化合物种类较多,下列化合物中硫元素化合价为+4 的是( )A、SO3 B、H2S C、Na2SO3 D、H2SO43. 下列微粒结构示意图中,表示阳离子的是( )A、
 B、
B、 C、
C、 D、
D、 4. 下图中四位同学正在讨论某一化学方程式表示的意义,他们所描述的化学方程式是( )
4. 下图中四位同学正在讨论某一化学方程式表示的意义,他们所描述的化学方程式是( ) A、 B、 2 C、 D、5. 建造北京大兴国际机场使用了大量钒钢,下图是钒在元素周期表中的信息及原子结构示意图,由此获得的信息错误的是( )
A、 B、 2 C、 D、5. 建造北京大兴国际机场使用了大量钒钢,下图是钒在元素周期表中的信息及原子结构示意图,由此获得的信息错误的是( ) A、图中x=23 B、钒属于金属元素 C、钒的中子数为50.94 D、钒原子核外有4个电子层6. 每个人都要有安全意识。下列做法中,正确的是( )A、乘坐地铁时,携带易燃易爆物 B、家用电器着火时,立即用水进行灭火 C、少量浓硫酸沾到皮肤上,立即用大量水冲洗 D、厨房里天然气大量泄漏时,立刻打开抽油烟机排气7. 过氧化氢常用于实验室制取氧气,其水溶液适用于医用伤口消毒及环境消毒和食品消毒。下列关于过氧化氢的叙述正确的是( )A、过氧化氢中氧元素的质量分数约为 94.1% B、过氧化氢的相对分子质量为34 g C、1 个过氧化氢分子由1个氢分子和1个氧分子构成 D、过氧化氢是由2个氧原子和2个氢原子构成的8. 推理是化学学习中常见的思维方法。下列推理正确的是( )A、碱性溶液能使酚酞溶液变红,滴入酚酞溶液后变红的溶液一定呈碱性 B、锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气 C、酸能使石蕊溶液变红,CO2也能使紫色的石蕊溶液变红,所以 CO2是酸 D、酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应9. 实验是学习化学的一条重要途径。下列实验能达到目的的是( )
A、图中x=23 B、钒属于金属元素 C、钒的中子数为50.94 D、钒原子核外有4个电子层6. 每个人都要有安全意识。下列做法中,正确的是( )A、乘坐地铁时,携带易燃易爆物 B、家用电器着火时,立即用水进行灭火 C、少量浓硫酸沾到皮肤上,立即用大量水冲洗 D、厨房里天然气大量泄漏时,立刻打开抽油烟机排气7. 过氧化氢常用于实验室制取氧气,其水溶液适用于医用伤口消毒及环境消毒和食品消毒。下列关于过氧化氢的叙述正确的是( )A、过氧化氢中氧元素的质量分数约为 94.1% B、过氧化氢的相对分子质量为34 g C、1 个过氧化氢分子由1个氢分子和1个氧分子构成 D、过氧化氢是由2个氧原子和2个氢原子构成的8. 推理是化学学习中常见的思维方法。下列推理正确的是( )A、碱性溶液能使酚酞溶液变红,滴入酚酞溶液后变红的溶液一定呈碱性 B、锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气 C、酸能使石蕊溶液变红,CO2也能使紫色的石蕊溶液变红,所以 CO2是酸 D、酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应9. 实验是学习化学的一条重要途径。下列实验能达到目的的是( )选项
实验目的
实验方案
A
验证质量守恒定律

B
除去O2中混有的CO2

C
证明某固体中含有碳酸盐

D
验证铁、铜、银三种金属的活动性顺序
 A、A B、B C、C D、D10. 小龙同学在工具书中查到NaOH在水和酒精中的溶解度(见下表)。通过分析她得出以下结论,其中错误的是( )
A、A B、B C、C D、D10. 小龙同学在工具书中查到NaOH在水和酒精中的溶解度(见下表)。通过分析她得出以下结论,其中错误的是( )20 ℃
40 ℃
水
109 g
129 g
酒精
17.3 g
40 g
A、温度和溶剂种类对NaOH的溶解度都有影响 B、NaOH易溶于水,也易溶于酒精 C、40 ℃,40 g NaOH溶解在100 g酒精中达到饱和 D、将等质量40 ℃的饱和NaOH水溶液和饱和NaOH酒精溶液降温至20 ℃,析出的晶体前者比后者多二、填空题
-
11. 生活中处处有化学。请回答下列问题:(1)、“真金不怕火炼”说明金。(2)、铝比铁抗腐蚀性能好的原因是 。(3)、用稀盐酸给铁除锈时,不能浸泡时间过长,其原因是(用化学方程式表示)。(4)、洗衣凝珠是一种创新性洗涤产品,该产品是由一层薄膜包裹的浓缩洗涤剂,外形透明似珠,遇水即溶。薄膜是一种用聚乙烯醇制成的新型塑料,它属于材料。该产品能有效去除油污,是因为洗涤剂具有作用。(5)、小明在饮用碳酸饮料时,发现打开瓶盖时有大量气泡冒出,从化学变化的角度解释为:(用化学方程式表示)。12. 化学辩论组的同学们在参加了有关“碳氧水循环”的辩论赛后,构建了“水循环”“氧循环”和“碳循环”的循环示意图。
 (1)、从物质变化及分子角度看,三种循环中有一种与另外两种在变化上有本质的区别,这种循环主要是由 (填“物理变化”或“化学变化”)引起的。(2)、从学科观点分析碳循环和氧循环,其中正确的是。
(1)、从物质变化及分子角度看,三种循环中有一种与另外两种在变化上有本质的区别,这种循环主要是由 (填“物理变化”或“化学变化”)引起的。(2)、从学科观点分析碳循环和氧循环,其中正确的是。A变化观:我们每个人都在参与碳、氧循环
B守恒观:碳、氧循环过程中各元素守恒,其化合价不变
C微粒观:绿色植物的作用是使自然界中的氧原子总数增加
13. 《本草纲目》记载,杨桃具有去风热、生津止渴等功效。(1)、杨桃的主要成分是水,还含有糖类和蛋白质等。葡萄糖和蛋白质中属于有机高分子化合物的是 , 能在人体内分解生成氨基酸的是。葡萄糖由 三种元素组成。(2)、经测定,酸杨桃的 pH 为 1.35,甜杨桃的 pH 为 1.81,其中酸性较强的是(填“酸杨桃”或“甜杨桃”)。(3)、酸杨桃中矿质元素含量如表。人体缺少元素易得佝偻病。表中所列元素中属于微量元素的是 。每克酸杨桃中矿质元素的含量
矿质元素
K
Ca
Zn
Fe
含量/mg
0.389
0.587
0.049
0.070
三、综合题
-
14. 我国有许多盐碱湖,湖中溶有大量的碳酸钠和氯化钠,它们的溶解度曲线如图1所示。碳酸钠是一种重要的化工原料,可用于制取氢氧化钠,工业上制取氢氧化钠的一种方法,如图2所示。 请据图回答:
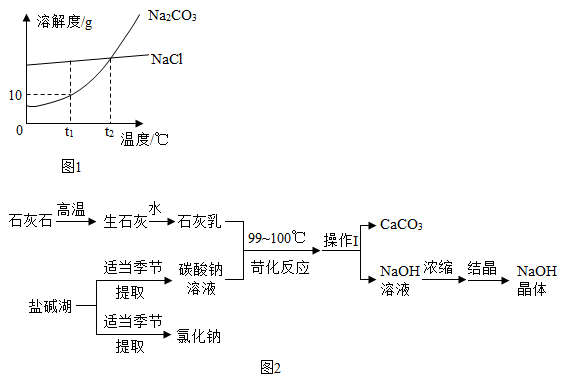 (1)、由石灰石制取石灰乳的过程中,发生反应的一个化学方程式是。(2)、根据图1分析,提取碳酸钠的季节最好是。(3)、苛化反应时将温度升高至99~100℃的原因是 , 操作1中需要用到的一种玻璃仪器是。(4)、配制等浓度的碳酸钠和氯化钠的饱和溶液,需要将温度控制在℃。15. “碳达峰”和“碳中和”
(1)、由石灰石制取石灰乳的过程中,发生反应的一个化学方程式是。(2)、根据图1分析,提取碳酸钠的季节最好是。(3)、苛化反应时将温度升高至99~100℃的原因是 , 操作1中需要用到的一种玻璃仪器是。(4)、配制等浓度的碳酸钠和氯化钠的饱和溶液,需要将温度控制在℃。15. “碳达峰”和“碳中和”中央经济工作会议2020年12月16日至18日在北京举行。会议确定,2021年要抓好的重点任务之一就是做好“碳达峰”和“碳中和”工作。气候变化是人类面临的全球性问题,随着各国二氧化碳排放,温室气体猛增,对生命系统形成威胁。在这一背景下,世界各国以全球协约的方式减排温室气体,我国由此提出“碳达峰”和“碳中和”目标。什么是“碳达峰”和“碳中和”呢?“碳达峰”就是我们国家承诺在2030年前,二氧化碳的排放不再增长,达到峰值之后再慢慢减下去;而到2060年,针对排放的二氧化碳,要采取植树、节能减排等各种方式全部抵消掉,这就是“碳中和”。大气能使太阳短波辐射到地面,而地表受热后向外放出的大量长波热辐射线,却被大气吸收,这样的作用形成了类似于栽培农作物的温室,故名温室效应。形成温室效应的气体,除二氧化碳外还有甲烷、臭氧、氟氯代烷等30多种。如果二氧化碳含量比现在增加一倍,气候将明显变暖,全球气温将升高3~5℃,两极地区可能升高10℃。气温升高将导致某些地区雨量增加,某些地区出现干旱巨分力量增强,出现频率也将提高,自然灾害加剧。更令人担忧的是,由于气温升高将使两极地区冰川融化,海平面升高,许多沿海城市、岛屿或低洼地区将面临海水上涨的威胁,甚至被海水吞没。为减少大气中过多的二氧化碳,一方面需要人们尽量减少不可再生的化石燃料的燃烧,使用清洁能源。另一方面要保护好森林和海洋,使他们多吸收二氧化碳,来帮助减缓温室效应。让我们一起来保护我们的地球吧!
依据短文内容,回答下列问题:
(1)、“碳达峰”和“碳中和”中的“碳”是指______。A、碳元素 B、碳单质 C、碳原子 D、二氧化碳(2)、空气中二氧化碳含量增多的主要原因是。(3)、除二氧化碳外,再写出一种能够形成温室效应的气体(填化学式)。(4)、解释“碳达峰”。(5)、海洋帮助减缓温室效应后,海水的 pH 会(填“增大”“减小”或“不变”)。16. A~E 是初中化学常见的5种不同物质,D的溶液呈蓝色,工业上A→B 是一个复杂的过程,B→A的探究需要一周的时间。图中“—”表示物质间可相互反应,“→”表示一种物质可生成另一种物质(部分反应物、生成物和反应条件已略去)。 (1)、D 的化学式是 , B 与 D 反应的现象。反应发生的原因。(2)、A→B 的化学方程式为。(3)、C 与 E 反应的微观实质是。17. 根据下列实验装置图填空:
(1)、D 的化学式是 , B 与 D 反应的现象。反应发生的原因。(2)、A→B 的化学方程式为。(3)、C 与 E 反应的微观实质是。17. 根据下列实验装置图填空: (1)、选用 A 装置制取氧气的化学方程式是。(2)、若用过氧化氢溶液制取一瓶干燥的氧气,需要用到装置 F,则装置 F 中应放入的物质是(填“浓盐酸”或“浓硫酸”),气体应从端通入(填“a”或“b”)。(3)、实验室制取二氧化碳选择的收集装置是(填选项字母),选择该收集装置是因为该气体应具有的性质是。若用 F 装置检验制得的气体是否为二氧化碳,则 F 装置内发生反应的化学方程式为。(4)、氨气极易溶于水,且密度比空气小,实验室用加热氯化铵和熟石灰固体混合物的方法制取氨气,应选用的发生装置和收集装置是(填字母)。18. 实验室有一瓶敞口放置且标签受损的无色溶液。已知原溶液中的溶质可能是 NaCl、NaNO3、NaOH、Na2SO4或Na2CO3中的一种,化学兴趣小组的同学们为确定该无色溶液的成分展开了探究。
(1)、选用 A 装置制取氧气的化学方程式是。(2)、若用过氧化氢溶液制取一瓶干燥的氧气,需要用到装置 F,则装置 F 中应放入的物质是(填“浓盐酸”或“浓硫酸”),气体应从端通入(填“a”或“b”)。(3)、实验室制取二氧化碳选择的收集装置是(填选项字母),选择该收集装置是因为该气体应具有的性质是。若用 F 装置检验制得的气体是否为二氧化碳,则 F 装置内发生反应的化学方程式为。(4)、氨气极易溶于水,且密度比空气小,实验室用加热氯化铵和熟石灰固体混合物的方法制取氨气,应选用的发生装置和收集装置是(填字母)。18. 实验室有一瓶敞口放置且标签受损的无色溶液。已知原溶液中的溶质可能是 NaCl、NaNO3、NaOH、Na2SO4或Na2CO3中的一种,化学兴趣小组的同学们为确定该无色溶液的成分展开了探究。(查阅资料)CaCl2溶液呈中性
(1)、(实验探究)实验步骤
实验现象
实验结论
①
测得 pH=11
② 取少量待测液于一支洁净的试管中,向试管中逐滴加入
开始时无明显现象,一段时间后产生气泡
原溶液是 Na2CO3
(2)、(反思评价)小陈同学对实验结论提出质疑,她的理由是。小陈继续进行了实验:另取少量待测溶液于一支洁净的试管中,向其中加入过量CaCl2溶液,产生白色沉淀,静置一会儿,过滤,向滤液中滴加少量溶液,溶液变红,证明她的猜想正确。小陈检验过程中有关反应的化学方程式是。
(3)、将步骤②及小陈实验后的废液倒入洁净的废液缸中,观察到有气泡产生且溶液呈无色,该烧杯中的液体能否直接倒入下水道?同学们对其中的溶质成分继续进行探究。猜想一:溶质为 NaCl、CaCl2
猜想二:溶质为
猜想三:溶质为 NaCl、CaCl2、Na2CO3
你认为上述哪个猜想不合理?说出你的理由。 经过实验,最终确定猜想二正确。
(4)、(表达与交流)应向废液中加入适量的后再排放。
四、计算题
-
19. 鸡蛋壳的主要成分是碳酸钙,小李为检测鸡蛋壳中碳酸钙的含量,进行的实验如下:向盛有 15g 碎鸡蛋壳的烧杯中加入 100g 稀盐酸,恰好完全反应后,烧杯内物质的总质量 110.6g。(温馨提示:鸡蛋壳中其他成分与稀盐酸接触不产生气体)(1)、根据质量守恒定律,完全反应生成气体的质量为。(2)、计算鸡蛋壳中碳酸钙的质量分数(请写出计算过程,精确到 0.1%)。