辽宁省沈阳市苏家屯区2021年中考化学二模试卷
试卷更新日期:2021-07-28 类型:中考模拟
一、单选题
-
1. 下列变化没有新物质生成的是( )A、葡萄酿成红酒 B、白雪缓慢消融 C、石蕊遇碱变蓝 D、铜器锈蚀变绿2. 下列食物中富含维生素C的是( )A、油菜 B、牛奶 C、豆腐 D、米饭3. 下列物质属于纯净物的是( )A、蔗糖溶液 B、生铁 C、空气 D、氧化镁4. 元素符号“N”除表示氮元素外,还能表示( )A、氮气 B、一个氮原子 C、一个氮分子 D、一个氮离子5. 如果人体内缺少钙元素,有可能引起的疾病是( )A、贫血症 B、夜盲症 C、佝偻病 D、甲状腺肿大6. 下列物质在氧气中燃烧,火星四射的是( )A、木炭 B、镁条 C、铁丝 D、红磷7. 下列实验中玻璃棒不是用来搅拌的是( )A、稀释浓硫酸 B、测定溶液pH C、蒸发食盐水 D、溶解蔗糖8. 在太空舱里常用NiFe2O4作催化剂将宇航员呼出的CO2转化为O2。已知NiFe2O4中铁元素为+3价,则Ni元素的化合价为( )A、+1价 B、+2价 C、+3价 D、+4价9. 如下图所示,水中的白磷能否燃烧与鼓入的气体和水温有关,表中能使白磷燃烧的选项是( )
选项
气体X
水温/℃
A
氧气
5
B
氮气
40
C
二氧化碳
80
D
空气
80
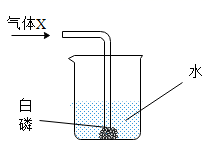 A、A B、B C、C D、D10. 下列常见的材料中,属于金属材料的是( )A、青铜 B、陶瓷 C、钢筋混凝土 D、聚乙烯塑料11. 现有Al、Cu、Ag三种金属,限用一种试剂一次性就可以验证它们的金属活动性强弱,则该试剂是( )A、CuSO4溶液 B、稀H2SO4 C、AgNO3溶液 D、AlCl3溶液12. 在“绿色化学工艺”中,最好是反应物中原子全部转化为欲制得的产物,即原子的利用率为100%。在用C3H4(丙炔)合成C5H8O2(2-甲基丙烯酸甲酯)的过程中,欲使原子的利用率到最高,在催化剂作用下还需要其他的反应物是( )A、CH4和CH3OH B、CO2和H2O C、H2和CO D、CH3OH和H213. 某工厂排出的废水pH小于7,并含有较多的Cu2+ , 对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入( )A、烧碱和熟石灰 B、盐酸和铁粉 C、生石灰和金属汞 D、生石灰和铁粉
A、A B、B C、C D、D10. 下列常见的材料中,属于金属材料的是( )A、青铜 B、陶瓷 C、钢筋混凝土 D、聚乙烯塑料11. 现有Al、Cu、Ag三种金属,限用一种试剂一次性就可以验证它们的金属活动性强弱,则该试剂是( )A、CuSO4溶液 B、稀H2SO4 C、AgNO3溶液 D、AlCl3溶液12. 在“绿色化学工艺”中,最好是反应物中原子全部转化为欲制得的产物,即原子的利用率为100%。在用C3H4(丙炔)合成C5H8O2(2-甲基丙烯酸甲酯)的过程中,欲使原子的利用率到最高,在催化剂作用下还需要其他的反应物是( )A、CH4和CH3OH B、CO2和H2O C、H2和CO D、CH3OH和H213. 某工厂排出的废水pH小于7,并含有较多的Cu2+ , 对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入( )A、烧碱和熟石灰 B、盐酸和铁粉 C、生石灰和金属汞 D、生石灰和铁粉二、填空题
-
14. 人类生产、生活离不开化学。(1)、人的胃液pH7,我们把pH的降雨称为酸雨,属于大气污染物,且能形成硫酸型酸雨的气体是(2)、净化水的操作有①过滤②蒸馏③静置沉淀④吸附⑤消毒等多种,其中净化程度最高的操作是(填序号)。(3)、用洗涤剂洗去餐具上的油污,利用的是原理。(4)、NO是大气污染物之一,目前有一种治理方法是在400℃左右、有催化剂存在的条件下,用氨气把NO还原为氮气和水,化学方程式为。(5)、聚乙烯和聚氯乙烯都是常见的塑料,鉴别它们的方法是。15. 如图1,A、B、C是三种粒子的结构示意图,D是钛元素在元素周期表中的信息。
 (1)、若B表示离子,则x=。离子符号是(2)、A、C表示的微粒化学性质(填“相似”或“不相似”)。(3)、钛广泛应用于航空、宇航以及医学上、钛的核电荷数是 , 相对原子质量是。下列图2中科学家对于测定相对原子质量作出卓越贡献的是(填字母)。
(1)、若B表示离子,则x=。离子符号是(2)、A、C表示的微粒化学性质(填“相似”或“不相似”)。(3)、钛广泛应用于航空、宇航以及医学上、钛的核电荷数是 , 相对原子质量是。下列图2中科学家对于测定相对原子质量作出卓越贡献的是(填字母)。 16. 将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得0℃、t1℃、t2℃、t3℃时烧杯中溶液的质量分别如图中A、B、C、D点所示。
16. 将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得0℃、t1℃、t2℃、t3℃时烧杯中溶液的质量分别如图中A、B、C、D点所示。
回答下列问题:
(1)、A、B两点对应的溶液中溶质的质量分数较大的是(填字母编号)。(2)、0℃时,物质X的溶解度是。(3)、A、B、C、D四点对应的溶液中,一定属于饱和溶液的是(填字母编号)。(4)、下列说法正确的是(填序号)。①t1℃时,若向B点对应的烧杯中再加入30g水,搅拌,所得溶液为不饱和溶液
②若要从D点对应的溶液中得到全部固体X,可采用蒸发结晶的方法
③t2℃时,将物质X的饱和溶液变为不饱和溶液,溶质的质量可能增大
三、综合题
-
17. FeSO4·7H2O是一种重要的食品和饲料添加剂。某工业废渣主要成分是Fe2O3 , 还含有CaCO3和SiO2(既不溶于水也不溶于稀硫酸),实验室用此废渣制备FeSO4·7H2O的流程如图l:

请根据流程图回答下列问题:
(1)、稀硫酸与粉末中的氧化铁反应的化学方程式为。(2)、操作②所需要的玻璃仪器是:烧杯、玻璃棒和。(3)、经测定,滤渣中只含有CaSO4和SiO2 , 你认为实验室(填“能”或者“不能”)用粉末状的石灰石与稀硫酸反应制二氧化碳。(4)、Fe与Fe2(SO4)3反应的化学方程式为 , 该反应的基本类型是。(5)、硫酸亚铁的溶解度曲线如图2。待结晶完毕后,过滤出晶体,用少量冰水洗涤2—3次,用冰水洗涤的目的是:Ⅰ除去晶体表面的杂质;Ⅱ。18.(1)、小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%。现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁96%的生铁的质量是(结果保留整数)?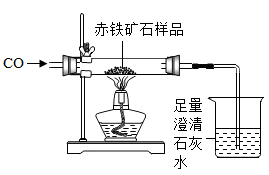 (2)、在利用上图装置进行实验时,小强得到如下两组数据(杂质不参加反应):
(2)、在利用上图装置进行实验时,小强得到如下两组数据(杂质不参加反应):反应前
氧化铁完全反应后
A组
玻璃管和赤铁矿石样品的质量m1g
玻璃管和固体物质的质量m2g
B组
烧杯和澄清石灰水的质量m3g
烧杯和烧杯中物质的质量m4g
①m1-m2表示的质量
②你认为他应该选用(填“A”或“B”)组数据来计算赤铁矿石中氧化铁的质量分数。结合装置图回答他不能选用另一组数据计算的原因为。
19. 如图所示是实验室制取并检验气体性质的常用装置。请回答下列问题。 (1)、装置A中仪器a的名称是 , 试管口略向下倾斜的原因是。(2)、装置B中仪器b的名称是 , 该仪器的主要作用是。(3)、实验室用锌粒与稀硫酸反应制取H2 , 应该选择的发生装置是(填序号)。反应的化学方程式为 , 收集氢气的装置是。(4)、装置C中,若X为澄清石灰水,则C中可以观察到的现象是。若X是水,D中能观察到紫色石蕊试纸变红,若D中紫色石蕊试纸没有变红,则X可能是(填序号)。
(1)、装置A中仪器a的名称是 , 试管口略向下倾斜的原因是。(2)、装置B中仪器b的名称是 , 该仪器的主要作用是。(3)、实验室用锌粒与稀硫酸反应制取H2 , 应该选择的发生装置是(填序号)。反应的化学方程式为 , 收集氢气的装置是。(4)、装置C中,若X为澄清石灰水,则C中可以观察到的现象是。若X是水,D中能观察到紫色石蕊试纸变红,若D中紫色石蕊试纸没有变红,则X可能是(填序号)。A.NaOH溶液 B.CaCl2溶液 C.浓硫酸 D.食盐水
20. 实验探究是重要的核心素养。(1)、探究一:碳酸钠俗称纯碱或苏打,在生活、生产和实验研究中均有广泛应用。Na2CO3属于(填“酸”、“碱”、“盐”)
(2)、若配制50g溶质质量分数为4%的Na2CO3溶液,下列操作正确的是(填字母)。a.用托盘天平称取2gNa2CO3固体
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(3)、25℃时,分别测定溶质质量分数分别为1%、2%和4%的Na2CO3溶液的pH,记录数据如下:实验编号
I
II
III
溶质质量分数
1%
2%
4%
溶液pH
11.62
11.76
11.90
分析Ⅰ、Ⅱ、Ⅲ三组数据可得出的结论是。
(4)、用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3[已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀]在烧杯中制备FeCO3沉淀时,应选用的加料方式是(填字母)。a.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
b.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
c.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
d.将FeSO4溶液迅速加入到盛有Na2CO3溶液的烧杯中
(5)、潮湿的FeCO3固体置于空气中易变质,生成一种红褐色的碱,同时生成二氧化碳该反应的化学方程式为。(6)、探究二:小伟利用下图所示装置进行系列探究活动。从分液漏斗依次向集气瓶中加入①适量滴有酚酞的氢氧化钠溶液;②过量的氢氧化钙溶液;③一定量的稀盐酸。回答下列问题:
实验①发生反应的化学方程式为。
(7)、实验②的探究目的是。(8)、整个实验过程中,酚酞起到的作用是。(9)、实验③结束时,集气瓶内溶液澄清,则溶液中溶质的组成可能是(写其中的一种)