备战2022 浙教版科学 中考高频考点 加强练 第59讲 物质的分离
试卷更新日期:2021-07-28 类型:一轮复习
一、单选题
-
1. 北宋沈括在《梦溪笔谈》中记载了用“苦泉水”制取铜的方法,其主要生产流程如图所示。下列解释合理的是( )
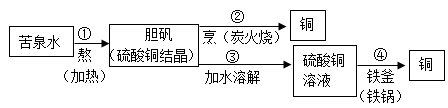 A、①通过蒸发溶剂可获得晶体 B、②是通过复分解反应获得铜 C、③所得硫酸铜溶液一定是饱和的 D、④说明铁元素变成了铜元素2. 测定粗盐纯度,需经过称量、溶解、过滤、蒸发结晶……下列操作规范的是( )A、称量
A、①通过蒸发溶剂可获得晶体 B、②是通过复分解反应获得铜 C、③所得硫酸铜溶液一定是饱和的 D、④说明铁元素变成了铜元素2. 测定粗盐纯度,需经过称量、溶解、过滤、蒸发结晶……下列操作规范的是( )A、称量 B、溶解
B、溶解  C、过滤
C、过滤 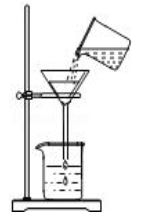 D、蒸发结晶
D、蒸发结晶  3. 科学兴趣小组先将粗盐提纯,并用制得的氯化钠配制100g溶质质量分数为8%的氯化钠溶液,下列说法正确的是( )A、蒸发滤液时,待蒸发皿中的滤液蒸干后再停止加热 B、配制该溶液需要氯化钠固体8g,加水100g C、粗盐溶解和蒸发操作中都要用到玻璃棒,其作用相同 D、配制溶液需要经过计算、称量和量取、溶解等步骤4. 自制简易净水器如图所示,可将浑浊的河水变成清水。其中石英砂的作用是( )
3. 科学兴趣小组先将粗盐提纯,并用制得的氯化钠配制100g溶质质量分数为8%的氯化钠溶液,下列说法正确的是( )A、蒸发滤液时,待蒸发皿中的滤液蒸干后再停止加热 B、配制该溶液需要氯化钠固体8g,加水100g C、粗盐溶解和蒸发操作中都要用到玻璃棒,其作用相同 D、配制溶液需要经过计算、称量和量取、溶解等步骤4. 自制简易净水器如图所示,可将浑浊的河水变成清水。其中石英砂的作用是( ) A、沉淀 B、吸附 C、过滤 D、消毒5. 中医药在治疗新冠肺炎中,为全球抗击疫情贡献了中国智慧。下列中药煎制步骤与实验室过滤操作原理相同的是( )A、浸泡热水
A、沉淀 B、吸附 C、过滤 D、消毒5. 中医药在治疗新冠肺炎中,为全球抗击疫情贡献了中国智慧。下列中药煎制步骤与实验室过滤操作原理相同的是( )A、浸泡热水 
B、加热煎制
B、加热煎制 
C、液渣分离
C、液渣分离 
D、装袋保存
D、装袋保存 
6. “五水共治”是浙江省政府推出的环保举措,为了清理河道,某区河道管理人员使用铁圈和塑料网做成的网兜(如图)来打捞河道漂浮物,这种方法最接近( )
6. “五水共治”是浙江省政府推出的环保举措,为了清理河道,某区河道管理人员使用铁圈和塑料网做成的网兜(如图)来打捞河道漂浮物,这种方法最接近( ) A、溶解 B、过滤 C、蒸馏 D、结晶7. 如图是同学们开展精制粗盐实验的主要步骤,下列有关说法错误的是( )
A、溶解 B、过滤 C、蒸馏 D、结晶7. 如图是同学们开展精制粗盐实验的主要步骤,下列有关说法错误的是( ) A、该实验的操作顺序应为乙、甲、丙 B、乙实验中,玻璃棒搅拌能加速食盐溶解 C、甲实验中,所得的滤液为混合物 D、丙实验中,所得的精盐为纯净物8. 粗盐提纯实验的部分操作如图所示,其中正确的是( )A、取粗盐
A、该实验的操作顺序应为乙、甲、丙 B、乙实验中,玻璃棒搅拌能加速食盐溶解 C、甲实验中,所得的滤液为混合物 D、丙实验中,所得的精盐为纯净物8. 粗盐提纯实验的部分操作如图所示,其中正确的是( )A、取粗盐 B、溶解
B、溶解  C、过滤
C、过滤  D、移走蒸发皿,
D、移走蒸发皿,  9. 将KNO3和K2SO4混合物进行分离,有如下操作:①将混合物溶解制成浓溶液;②加热蒸发浓溶液;③冷却溶液;④过滤,移出KNO3晶体;⑤过滤,移出K2SO4晶体。试据图分析,判断出正确的操作顺序是( )
9. 将KNO3和K2SO4混合物进行分离,有如下操作:①将混合物溶解制成浓溶液;②加热蒸发浓溶液;③冷却溶液;④过滤,移出KNO3晶体;⑤过滤,移出K2SO4晶体。试据图分析,判断出正确的操作顺序是( ) A、①②③④⑤ B、①②⑤③④ C、①③⑤②④ D、①③④②⑤10. 如图是茶水分离保温杯示意图,按压茶杯按钮,泡好的茶水便会从隔离层缝隙间流出,茶叶留在茶仓从而实现茶水分离,得到一杯香醇的清茶。这种功能类似于物质分离方法中的( )
A、①②③④⑤ B、①②⑤③④ C、①③⑤②④ D、①③④②⑤10. 如图是茶水分离保温杯示意图,按压茶杯按钮,泡好的茶水便会从隔离层缝隙间流出,茶叶留在茶仓从而实现茶水分离,得到一杯香醇的清茶。这种功能类似于物质分离方法中的( ) A、沉淀法 B、过滤法 C、蒸馏法 D、结晶法11. 下列图示的净水方法中,净化程度最高的是( )A、过滤
A、沉淀法 B、过滤法 C、蒸馏法 D、结晶法11. 下列图示的净水方法中,净化程度最高的是( )A、过滤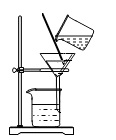 B、沉淀
B、沉淀  C、蒸馏
C、蒸馏 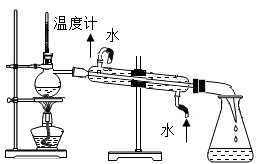 D、吸附
D、吸附  12. 科学实验课上,同学们要对20g纯度约为90%的粗盐进行初步提纯(已知:20℃时氯化钠的溶解度为36g)。以下实验操作可能导致精盐质量偏低的是( )
12. 科学实验课上,同学们要对20g纯度约为90%的粗盐进行初步提纯(已知:20℃时氯化钠的溶解度为36g)。以下实验操作可能导致精盐质量偏低的是( )①量取40mL水溶解粗盐;②过滤时,滤纸有破损;③蒸发结束转移精盐时,精盐有撒漏;④称量精盐时,左盘放了砝码,右盘放了精盐,而后移动游码至平衡;
A、①③ B、①④ C、②④ D、②③13. 小科是一个科学迷,在观看了野外求生的电视节目后,自己也试着自制净水装置,在较大容器内装有天然水,中间放置另一相对小一些的容器,在大容器上方用保鲜膜封上,并将一枚硬币置于保鲜膜上恰好停留在小容器的正上方,然后将装置置于烈日底下,一段时间以后,小容器内获得了纯净的水。小科利用这个装置获得纯水的过程中,运用的主要方法是( ) A、结晶 B、过滤 C、沉淀 D、蒸馏14. 下列是某同学对水的一些认识:①水是由氢气和氧气组成的;②“南水北调;工程主要改变水循环环节中的蒸发;③我国水资源分布不均衡,夏季丰富,冬季欠缺;④分别运用沉淀法、过滤法、蒸馏法得到的水,蒸馏法得到的水最为纯净;⑤陆地淡水约占地球总水量的96.53%;⑥多种物质可以在水中溶解。其中正确的是( )A、①③⑤ B、③④⑥ C、①②④ D、③⑤⑥15. 河水净化的主要流程如图所示,下列说法不正确的是( )
A、结晶 B、过滤 C、沉淀 D、蒸馏14. 下列是某同学对水的一些认识:①水是由氢气和氧气组成的;②“南水北调;工程主要改变水循环环节中的蒸发;③我国水资源分布不均衡,夏季丰富,冬季欠缺;④分别运用沉淀法、过滤法、蒸馏法得到的水,蒸馏法得到的水最为纯净;⑤陆地淡水约占地球总水量的96.53%;⑥多种物质可以在水中溶解。其中正确的是( )A、①③⑤ B、③④⑥ C、①②④ D、③⑤⑥15. 河水净化的主要流程如图所示,下列说法不正确的是( ) A、X可以是明矾 B、Y可以是活性炭 C、步骤I的目的是除去不溶性杂质 D、河水经该流程净化后变为纯水
A、X可以是明矾 B、Y可以是活性炭 C、步骤I的目的是除去不溶性杂质 D、河水经该流程净化后变为纯水二、填空题
-
16. 瑞安陶山甘蔗制糖有着悠久的历史。甘蔗制糖的部分环节为: 清洗甘蔗→压榨甘蔗→分离渣汁→蒸发浓缩→……,制糖的部分环节与下图的实验原理相同。
 (1)、在制蔗糖过程中发生的主要变化属于变化。(2)、上述制糖环节中与下图实验原理相同的是。17. 某小组通过如下四组实验对稀硫酸部分化学性质进行验证:①Mg和稀硫酸:②MgO和稀硫酸;③Ba(NO3)2溶液和稀硫酸;④NaOH溶液和稀硫酸。实验结束后将所有反应后的溶液混合进行了以下操作,请分析并回答下列问题:
(1)、在制蔗糖过程中发生的主要变化属于变化。(2)、上述制糖环节中与下图实验原理相同的是。17. 某小组通过如下四组实验对稀硫酸部分化学性质进行验证:①Mg和稀硫酸:②MgO和稀硫酸;③Ba(NO3)2溶液和稀硫酸;④NaOH溶液和稀硫酸。实验结束后将所有反应后的溶液混合进行了以下操作,请分析并回答下列问题: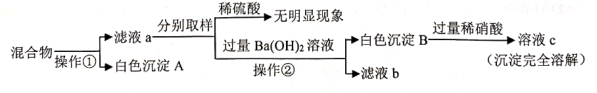 (1)、操作①的名称为。(2)、实验④无明显现象,再将打磨过的铁丝浸入该实验后的溶液中,仍无明显现象,据此(填“能”或“不能”)验证NaOH溶液和H2SO4发生反应。(3)、滤液b的成分中一定含有。(用化学式表示)18. 豆腐富含蛋白质,深受人们欢迎,其制作的主要工艺流程如图甲。
(1)、操作①的名称为。(2)、实验④无明显现象,再将打磨过的铁丝浸入该实验后的溶液中,仍无明显现象,据此(填“能”或“不能”)验证NaOH溶液和H2SO4发生反应。(3)、滤液b的成分中一定含有。(用化学式表示)18. 豆腐富含蛋白质,深受人们欢迎,其制作的主要工艺流程如图甲。 (1)、图甲的工艺流程中,磨浆属于变化。(2)、大豆的营养物质主要储存在图乙种子结构中的(填序号)
(1)、图甲的工艺流程中,磨浆属于变化。(2)、大豆的营养物质主要储存在图乙种子结构中的(填序号)
 (3)、将豆腐花压制成豆腐的过程就是将豆腐与其中的水分离,该过程与图丙中哪一个实验相同? (填序号)
(3)、将豆腐花压制成豆腐的过程就是将豆腐与其中的水分离,该过程与图丙中哪一个实验相同? (填序号)
 19. 实验室里有一包白色固体,可能由氯化钠,碳酸钠,氢氧化钠中的一种或几种组成,为了检测其成分,按以下流程进行操作:
19. 实验室里有一包白色固体,可能由氯化钠,碳酸钠,氢氧化钠中的一种或几种组成,为了检测其成分,按以下流程进行操作: (1)、上述中“操作Ⅰ”的名称是。(2)、加少量硝酸钡溶液,产生白色沉淀,可以推出白色粉末中一定有。(3)、滴加酚酞试剂后,溶液呈红色,能否说明白色粉末中是否一定含有氢氧化钠,并说明理由。20. 为了比较活性炭和石英砂对泥水的过滤效果,小东选用的实验器材有:两个相同的下端带有漏水小孔的透明圆柱形容器甲和乙,活性炭、锰砂、石英砂、鹅卵石四种过滤材料。在甲容器里依次装入活性炭、石英砂、锰砂、鹅卵石四种过滤材料,每种材料的厚度均为3cm,如图甲所示。在乙容器里依次装入石英砂、锰砂、鹅卵石三种过滤材料,每种材料的厚度均为3cm,如图乙所示。把摇晃均匀的一瓶泥水分成相等的两份,分别缓慢全部倒入甲、乙两容器中,发现经甲容器过滤后的泥水比经乙容器过滤后的泥水透明程度高。于是小东得出了结论:活性炭对泥水的过滤效果比石英砂对泥水的过滤效果好。
(1)、上述中“操作Ⅰ”的名称是。(2)、加少量硝酸钡溶液,产生白色沉淀,可以推出白色粉末中一定有。(3)、滴加酚酞试剂后,溶液呈红色,能否说明白色粉末中是否一定含有氢氧化钠,并说明理由。20. 为了比较活性炭和石英砂对泥水的过滤效果,小东选用的实验器材有:两个相同的下端带有漏水小孔的透明圆柱形容器甲和乙,活性炭、锰砂、石英砂、鹅卵石四种过滤材料。在甲容器里依次装入活性炭、石英砂、锰砂、鹅卵石四种过滤材料,每种材料的厚度均为3cm,如图甲所示。在乙容器里依次装入石英砂、锰砂、鹅卵石三种过滤材料,每种材料的厚度均为3cm,如图乙所示。把摇晃均匀的一瓶泥水分成相等的两份,分别缓慢全部倒入甲、乙两容器中,发现经甲容器过滤后的泥水比经乙容器过滤后的泥水透明程度高。于是小东得出了结论:活性炭对泥水的过滤效果比石英砂对泥水的过滤效果好。 (1)、请写出小东实验过程中存在的问题:。(2)、请你针对小东实验过程中存在的问题,写出改正的步骤:。21. 目前许多学校安装了直饮水机,其主要工作流程如图:
(1)、请写出小东实验过程中存在的问题:。(2)、请你针对小东实验过程中存在的问题,写出改正的步骤:。21. 目前许多学校安装了直饮水机,其主要工作流程如图: (1)、①的作用是___;A、杀菌消毒 B、吸附杂质 C、蒸馏 D、过滤(2)、直饮水机使用方便:只要 将它与自来水管网对接,截 留清除水中的有害物质(如 细菌等),便得到直饮水。 直饮水属于(选填 “混合物”或“纯净物”)。22. 某校进行了学生科学实验操作竞赛,其中一竞赛题为:“用粗盐配制 100g10%的氯化钠(NaCl)溶液”。该实验的部分操作如下图所示。请回答下列问题:
(1)、①的作用是___;A、杀菌消毒 B、吸附杂质 C、蒸馏 D、过滤(2)、直饮水机使用方便:只要 将它与自来水管网对接,截 留清除水中的有害物质(如 细菌等),便得到直饮水。 直饮水属于(选填 “混合物”或“纯净物”)。22. 某校进行了学生科学实验操作竞赛,其中一竞赛题为:“用粗盐配制 100g10%的氯化钠(NaCl)溶液”。该实验的部分操作如下图所示。请回答下列问题:
 (1)、操作①、②、③依次为图中的(填字母);(2)、用上述实验所得氯化钠(NaCl)晶体配制溶液 ,以下操作会使所配制的氯化钠溶液溶质质量分数偏小的是_________。A、氯化钠固体中含有不溶性杂质 B、称量氯化钠时,用了生锈的砝码 C、量取水时,仰视量筒读数 D、一开始搅拌时,有部分液体溅出 E、将配好的溶液倒入用蒸馏水洗过的细口瓶中23. 某化学兴趣小组同学去佛子岭水库游玩时,用瓶装了一些水库中的水。他们在老师的指导下,按如图流程进行水的净化实验。
(1)、操作①、②、③依次为图中的(填字母);(2)、用上述实验所得氯化钠(NaCl)晶体配制溶液 ,以下操作会使所配制的氯化钠溶液溶质质量分数偏小的是_________。A、氯化钠固体中含有不溶性杂质 B、称量氯化钠时,用了生锈的砝码 C、量取水时,仰视量筒读数 D、一开始搅拌时,有部分液体溅出 E、将配好的溶液倒入用蒸馏水洗过的细口瓶中23. 某化学兴趣小组同学去佛子岭水库游玩时,用瓶装了一些水库中的水。他们在老师的指导下,按如图流程进行水的净化实验。请回答下列问题:
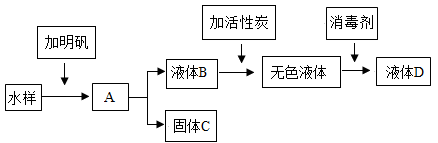
水样中加入明矾后的A操作是;若A操作后的液体依然浑浊可能的原因是 , 经过净化实验后的液体D同学们觉得还不够洁净,可以通过来进一步净化。
24. 某化工厂流程会产生澄清废水,其中可能含有的离子是Ag+、Cu2+、Cl−、NO3− , 已知:白色的沉淀Fe(OH)2在空气中会迅速转化为红褐色的Fe(OH)3.①取少量废水,加入过量稀盐酸,产生白色沉淀;再加入过量氢氧化钠溶液,产生蓝色沉淀。该废水中含有的金属离子是.
②兴趣小组设计了一个除去该废水中原有金属离子的实验方案,部分流程如图所示。操作I的名称是 , 单质A是.
 25. 下图为粗盐精制实验的一个步骤,回答:(1)、写出仪器名称②;下图中此时玻璃棒的作用是。
25. 下图为粗盐精制实验的一个步骤,回答:(1)、写出仪器名称②;下图中此时玻璃棒的作用是。 (2)、漏斗中的液面应 (填“高”或“低”)于滤纸边缘。粗盐提纯时正确顺序是_。
(2)、漏斗中的液面应 (填“高”或“低”)于滤纸边缘。粗盐提纯时正确顺序是_。A、溶解、蒸发、过滤 B、过滤、蒸发、冷却 C、溶解、过滤、蒸发
三、实验探究题
-
26. 某炉渣中主要含氧化亚铁、氧化铁,还含少量杂质(不溶于水,也不与酸反应);现按如图所示流程制备绿矾(FeSO4•7H2O),已知氧化亚铁与稀硫酸、铁与硫酸铁反应均可生成硫酸亚铁。
 (1)、为了提高“浸取”过程中的反应速率,可采取的措施有(选填序号:①加水稀释;②升高温度;③粉碎炉渣)。(2)、“过滤”操作需要使用的玻璃仪器有烧杯、玻璃棒和
(1)、为了提高“浸取”过程中的反应速率,可采取的措施有(选填序号:①加水稀释;②升高温度;③粉碎炉渣)。(2)、“过滤”操作需要使用的玻璃仪器有烧杯、玻璃棒和
。实验测得,滤液II的pH比滤液I的大,其原因是。杂质
(3)、将滤液II蒸发浓缩、降温结晶、过滤、冰水洗涤、低温干燥后得到绿矾,其中采用“冰水洗涤”的好处是。27. 如图是粗盐提纯实验的部分操作,请回答相关问题 (1)、图所示操作中,有错误的是(填字母)。(2)、粗盐提纯的正确操作顺序为(填字母)。(3)、操作B中,玻璃棒的作用是。(4)、步骤D中称取10.0g粗盐,将该粗盐逐渐加入盛有10mL水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称得剩余粗盐为2.0g,最终得到食盐晶体3.2g,该实验精盐的产率是。28. 某科学兴趣小组的同学做粗盐(含有杂质,且杂质难溶于水)提纯实验,并用所得的精盐配制50克10%的氯化钠溶液。请回答下列有关问题:
(1)、图所示操作中,有错误的是(填字母)。(2)、粗盐提纯的正确操作顺序为(填字母)。(3)、操作B中,玻璃棒的作用是。(4)、步骤D中称取10.0g粗盐,将该粗盐逐渐加入盛有10mL水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称得剩余粗盐为2.0g,最终得到食盐晶体3.2g,该实验精盐的产率是。28. 某科学兴趣小组的同学做粗盐(含有杂质,且杂质难溶于水)提纯实验,并用所得的精盐配制50克10%的氯化钠溶液。请回答下列有关问题:实验一:按下列实验步骤和要求回答粗盐提纯的有关问题。
第一步:溶解。①称量:称量前先把天平调平,准确称取5.0g粗盐。
②量取10mL 水倒入烧杯,加粗盐于水中,用玻璃棒搅拌,直到粗盐不再溶解为止。
第二步:过滤。①待过滤的混合液在引流之前先静置一会儿再过滤。
②引流时与玻璃棒下端接触的部分是。
第三步:蒸发。①如果蒸发皿中有液滴飞溅,原因是。
②当蒸发皿出现时,应停止加热。
第四步:转移。此粗盐精制过程中,玻璃棒在过滤时的作用是。
实验二:用粗盐提纯后得到的精盐(氯化钠)配制了氯化钠溶液,经检测溶质质量分数偏小,其原因可能有(填字母序号,多选)。
①氯化钠固体仍然不纯②称量时砝码和氯化钠放错盘
③称量时只在天平左盘垫上滤纸④用量筒量取水时俯视读数
⑤ 配制好的氯化钠溶液装瓶时,有少量溶液洒出
29. 某科学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50克20%的氯化钠溶液。请回答下列有关问题:(1)、实验一:下图是同学们做粗盐提纯实验的操作示意图。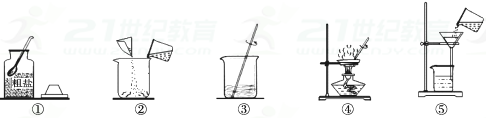
a.实验操作有错误的步骤是;
b.步骤③中玻璃棒的作用是;
(2)、实验二:用粗盐提纯后得到的精盐配制了氯化钠溶液,经检测,溶质质量分数偏小。其原因可能有 (填字母序号)。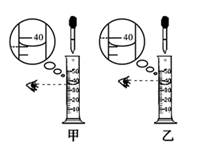 A、氯化钠固体仍然不纯 B、称量时只在天平左盘垫上滤纸 C、配制好的氯化钠溶液装瓶时,有少量溶液洒出 D、称量时使用了生锈的砝码 E、用量筒量取水时,仰视读数(3)、实验三:在溶液配制过程中,若要用量筒量取40毫升的水,当液面接近刻度线时,要改用胶头滴管,在用滴管滴加水的过程中,眼睛视线应同时按图进行观察。
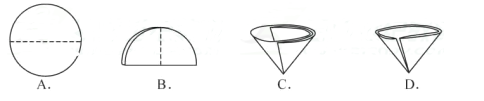
A、氯化钠固体仍然不纯 B、称量时只在天平左盘垫上滤纸 C、配制好的氯化钠溶液装瓶时,有少量溶液洒出 D、称量时使用了生锈的砝码 E、用量筒量取水时,仰视读数(3)、实验三:在溶液配制过程中,若要用量筒量取40毫升的水,当液面接近刻度线时,要改用胶头滴管,在用滴管滴加水的过程中,眼睛视线应同时按图进行观察。实验四:操作⑤中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是(填序号)。
 30. 以下是小华同学先将粗盐提纯,然后用精盐配制一定溶质质量分数溶液的实验过程。(1)、粗盐提纯。
30. 以下是小华同学先将粗盐提纯,然后用精盐配制一定溶质质量分数溶液的实验过程。(1)、粗盐提纯。
如图是同学们做粗盐提纯实验的操作示意图,请回答下列问题:
a.操作③中用玻璃棒搅拌的作用是
b.所有操作中,步骤是多余的(填序号),并指出其余步骤中的一处错误
c.实验最后称量精盐并计算产率。若此实验精盐的产率偏高,则可能的原因是(填字母)
A.过滤时滤纸有破损 B.蒸发时有固体溅出
C.溶解含泥沙的粗食盐时,加入的水量不足 D.所得的氯化钠晶体没有烘干,带有水分
E.过滤后滤纸是湿的,纸上含有溶液中的食盐
(2)、用精盐配制一定溶质质量分数溶液

①称量时C出现了右盘低的现象,则接下来小华的操作是。
②以上步骤在实验过程中的正确顺序为(用字母表示)。
③小华量取蒸馏水的体积如图2所示,则小华配制的碳酸钠溶液中溶质的质量分数为(答案精确到小数点后一位)。
四、解答题
-
31. 实验室有一瓶敞口放置的氢氧化钠固体样品,为探究样品中的成分,小科进行如下实验:
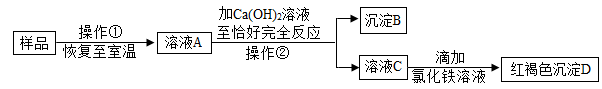 (1)、操作①是加水充分溶解,操作②的名称是。(2)、沉淀B的化学式是。(3)、小科根据实验现象认为样品中一定含有氢氧化钠,请你评价小科的判断是否正确,并说明理由。。32. 根据下面的实验过程和提供的数据,请回答:
(1)、操作①是加水充分溶解,操作②的名称是。(2)、沉淀B的化学式是。(3)、小科根据实验现象认为样品中一定含有氢氧化钠,请你评价小科的判断是否正确,并说明理由。。32. 根据下面的实验过程和提供的数据,请回答: (1)、操作①的名称为。(2)、求原混合物中炭粉的质量。(3)、求反应后所得溶液A的溶质质量分数。(4)、请分析溶液A与溶液B的溶质质量分数的大小关系。33. 科学家尝试通过多种途径减少CO2的排放,或将CO2转化为有用的物质。其中一种途径是利用NaOH溶液来“捕捉”CO2 , 并将CO2储存或利用,反应流程如图所示。
(1)、操作①的名称为。(2)、求原混合物中炭粉的质量。(3)、求反应后所得溶液A的溶质质量分数。(4)、请分析溶液A与溶液B的溶质质量分数的大小关系。33. 科学家尝试通过多种途径减少CO2的排放,或将CO2转化为有用的物质。其中一种途径是利用NaOH溶液来“捕捉”CO2 , 并将CO2储存或利用,反应流程如图所示。
反应流程图
(1)、反应分离室中分离物质的操作是。(2)、上述反应流程中,可循环利用的物质是。(3)、若反应分离室中有溶质质量分数为10.6%的Na2CO3溶液100kg,求完全反应后,理论上可生成CaCO3的质量(要求根据化学方程式计算)。34. 某白色粉末,可能含有硫酸钠、硫酸铜、氯化钠、硝酸钡、碳酸钙中的一种或几种。某科学兴趣小组为探究其成分,设计了如下实验流程(所加试剂均足量)。 (1)、操作Ⅰ、Ⅱ的名称是。(2)、无色气体的质量是g。(3)、固体甲的成分是。(4)、这种白色粉末中一定不含有。(5)、求白色粉末中肯定含有的物质总质量。35. 某兴趣小组提纯含少量泥沙的粗盐,一般经过如图所示操作流程:
(1)、操作Ⅰ、Ⅱ的名称是。(2)、无色气体的质量是g。(3)、固体甲的成分是。(4)、这种白色粉末中一定不含有。(5)、求白色粉末中肯定含有的物质总质量。35. 某兴趣小组提纯含少量泥沙的粗盐,一般经过如图所示操作流程: (1)、操作①中玻璃棒的作用。(2)、操作②中需要将圆形滤纸折叠处理,如图所示不该出现的情形是。
(1)、操作①中玻璃棒的作用。(2)、操作②中需要将圆形滤纸折叠处理,如图所示不该出现的情形是。 (3)、实验结束后称量获得的精盐,计算发现精盐的质量明显偏小,其原因可能有(填数字序号)。
(3)、实验结束后称量获得的精盐,计算发现精盐的质量明显偏小,其原因可能有(填数字序号)。①溶解时,溶解不够充分 ②过滤时,滤渣没有清洗
③蒸发时,液滴飞溅 ④蒸发后所得的食盐很潮湿
⑤转移后,蒸发皿上还沾有食盐