备战2022 浙教版科学 中考高频考点 加强练 第56讲 饱和溶液和不饱和溶液
试卷更新日期:2021-07-28 类型:一轮复习
一、单选题
-
1. 20℃时,取一定质量的固体硝酸钾于烧杯中,把100克水平均分成四份依次加入烧杯,不断搅拌,使之充分到溶解,实验过程如图所示。下列分析正确的是( )
 A、甲烧杯中,硝酸钾溶液是不饱和溶液 B、丁烧杯中,硝酸钾溶液是不饱和溶液 C、乙→丙过程中,硝酸钾溶液的溶质质量分数变大 D、丙→丁过程中,硝酸钾溶液的溶质质量分数变大2. 常温下,对100mL氯化钠的饱和溶液进行图示的2个小实验。下列分析错误的是( )
A、甲烧杯中,硝酸钾溶液是不饱和溶液 B、丁烧杯中,硝酸钾溶液是不饱和溶液 C、乙→丙过程中,硝酸钾溶液的溶质质量分数变大 D、丙→丁过程中,硝酸钾溶液的溶质质量分数变大2. 常温下,对100mL氯化钠的饱和溶液进行图示的2个小实验。下列分析错误的是( ) A、实验2后,甲中溶液为氯化钠的不饱和溶液 B、实验2后,乙中比甲中氯化钠的溶解度大 C、实验2后,甲、乙中溶液的溶质质量分数不相等 D、实验1后的甲和实验2后的乙中溶液所含溶质质量相等3. 20℃时,KCl和KNO3的溶解度分别为34g和31.6g。小金在20℃时进行了如图所示的操作,得到溶液①②③④。下列有关溶液①~④的分析错误的是( )
A、实验2后,甲中溶液为氯化钠的不饱和溶液 B、实验2后,乙中比甲中氯化钠的溶解度大 C、实验2后,甲、乙中溶液的溶质质量分数不相等 D、实验1后的甲和实验2后的乙中溶液所含溶质质量相等3. 20℃时,KCl和KNO3的溶解度分别为34g和31.6g。小金在20℃时进行了如图所示的操作,得到溶液①②③④。下列有关溶液①~④的分析错误的是( ) A、 属于20℃时的饱和溶液的是②和④ B、溶质的质量相等的是②和④ C、溶液的溶质质量分数相等的是①和③ D、溶液的质量②>④>③=①4. 如图所示为蒸发氯化钠溶液的过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态,分析实验过程,下列说法错误的是( )
A、 属于20℃时的饱和溶液的是②和④ B、溶质的质量相等的是②和④ C、溶液的溶质质量分数相等的是①和③ D、溶液的质量②>④>③=①4. 如图所示为蒸发氯化钠溶液的过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态,分析实验过程,下列说法错误的是( ) A、①溶液肯定是不饱和溶液 B、溶液中溶质质量的关系为:①=②>③>④ C、在②→④过程中,氯化钠的质量分数始终不变 D、将④烧杯中的混合物过滤后所得的滤液为饱和溶液5. 甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是( )
A、①溶液肯定是不饱和溶液 B、溶液中溶质质量的关系为:①=②>③>④ C、在②→④过程中,氯化钠的质量分数始终不变 D、将④烧杯中的混合物过滤后所得的滤液为饱和溶液5. 甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是( ) A、甲一定是不饱和溶液 B、乙、丙、丁一定是饱和溶液 C、乙的溶质质量分数一定比甲大 D、甲、乙溶液中蔗糖的溶解度相等6. 20℃时,KCl 和 KNO3 的溶解度分别为 34g 和 31.6g。小金在 20℃时进行了如图所示的操作,得到溶液①②③④。下列有关溶液①~④的分析错误的是( )
A、甲一定是不饱和溶液 B、乙、丙、丁一定是饱和溶液 C、乙的溶质质量分数一定比甲大 D、甲、乙溶液中蔗糖的溶解度相等6. 20℃时,KCl 和 KNO3 的溶解度分别为 34g 和 31.6g。小金在 20℃时进行了如图所示的操作,得到溶液①②③④。下列有关溶液①~④的分析错误的是( )
 A、属于 20℃时的饱和溶液的是②和④ B、溶质的质量相等的是②和④ C、溶液的溶质质量分数相等的是①和③ D、溶液的质量②﹥④﹥③=①7. 烧杯①中溶液是60℃时含有120g水的NH4Cl溶液,经过下图操作后得到18.0gNH4Cl固体,已知60℃和20℃时,NH4Cl的溶解度分别为55.2g和37.2g,下列说法正确的是( )
A、属于 20℃时的饱和溶液的是②和④ B、溶质的质量相等的是②和④ C、溶液的溶质质量分数相等的是①和③ D、溶液的质量②﹥④﹥③=①7. 烧杯①中溶液是60℃时含有120g水的NH4Cl溶液,经过下图操作后得到18.0gNH4Cl固体,已知60℃和20℃时,NH4Cl的溶解度分别为55.2g和37.2g,下列说法正确的是( ) A、②中溶液和③中溶液分别为60℃和20℃时NH4Cl的饱和溶液 B、①中溶液和②中溶液均为60℃时NH4Cl的不饱和溶液 C、①中溶液的溶质质量大于②中溶液的溶质质量 D、②中溶液和③中溶液的溶质质量分数相等8. 如图是恒温下模拟海水晒盐过程的示意图,从甲到丙可以肯定是饱和溶液的是( )
A、②中溶液和③中溶液分别为60℃和20℃时NH4Cl的饱和溶液 B、①中溶液和②中溶液均为60℃时NH4Cl的不饱和溶液 C、①中溶液的溶质质量大于②中溶液的溶质质量 D、②中溶液和③中溶液的溶质质量分数相等8. 如图是恒温下模拟海水晒盐过程的示意图,从甲到丙可以肯定是饱和溶液的是( )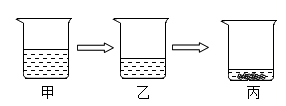 A、甲 B、乙 C、丙 D、无法判断9. 温州苍南有“世界矾都”之称,迄今有600多年的炼矾历史。制取的明矾可用于净水,也可用于制备发酵粉、油漆等,其制作流程为:煅烧明矾石→加水溶解→蒸发浓缩→析出结晶物→……如图是明矾制作过程中的结晶环节,能作为判断结晶池中液体为饱和溶液的依据是( )
A、甲 B、乙 C、丙 D、无法判断9. 温州苍南有“世界矾都”之称,迄今有600多年的炼矾历史。制取的明矾可用于净水,也可用于制备发酵粉、油漆等,其制作流程为:煅烧明矾石→加水溶解→蒸发浓缩→析出结晶物→……如图是明矾制作过程中的结晶环节,能作为判断结晶池中液体为饱和溶液的依据是( ) A、溶液澄清透明 B、溶液均一稳定 C、溶液浓度较大 D、池底晶体析出10. 某次蔗糖溶解实验过程如图所示,不计水分蒸发,下列判断错误的是( )
A、溶液澄清透明 B、溶液均一稳定 C、溶液浓度较大 D、池底晶体析出10. 某次蔗糖溶解实验过程如图所示,不计水分蒸发,下列判断错误的是( ) A、②中溶液是饱和溶液 B、③中溶液一定是不饱和溶液 C、②③中溶液的溶质质量分数不相同 D、③中溶液的溶质质量大于②中溶液的溶质质量11. 某温度下,一只烧杯中盛有20g水,放入2g熟石灰并搅拌,有白色固体沉淀到烧杯底部,则对于烧杯中的上层清液,说法正确的是( )A、是白色溶液 B、是水 C、是不饱和溶液 D、是饱和溶液12. 在一定温度下,某物质的饱和溶液一定是( )A、非常浓的溶液 B、很稀的溶液 C、增加该溶质,溶质还能继续溶解的溶液 D、增加该溶质,溶质不能继续溶解的溶液13. 许多科学知识在逻辑上存在如图所示关系.其中并列关系是由于分类依据的相同而把事物截然分开并列,而交叉关系是对事物分类时,由于釆用不同的分类依据,则必然出现交叉关系,下列说法正确的是( )
A、②中溶液是饱和溶液 B、③中溶液一定是不饱和溶液 C、②③中溶液的溶质质量分数不相同 D、③中溶液的溶质质量大于②中溶液的溶质质量11. 某温度下,一只烧杯中盛有20g水,放入2g熟石灰并搅拌,有白色固体沉淀到烧杯底部,则对于烧杯中的上层清液,说法正确的是( )A、是白色溶液 B、是水 C、是不饱和溶液 D、是饱和溶液12. 在一定温度下,某物质的饱和溶液一定是( )A、非常浓的溶液 B、很稀的溶液 C、增加该溶质,溶质还能继续溶解的溶液 D、增加该溶质,溶质不能继续溶解的溶液13. 许多科学知识在逻辑上存在如图所示关系.其中并列关系是由于分类依据的相同而把事物截然分开并列,而交叉关系是对事物分类时,由于釆用不同的分类依据,则必然出现交叉关系,下列说法正确的是( ) A、饱和溶液包含浓溶液 B、饱和溶液与稀溶液属于并列关系 C、饱和溶液与不饱和溶液属于交叉关系 D、不饱和溶液与稀溶液属于交叉关系14. 某物质A的溶解度曲线如图所示,现有20℃的100克物质A的饱和溶液样品若干份,下列说法或措施正确的有( )
A、饱和溶液包含浓溶液 B、饱和溶液与稀溶液属于并列关系 C、饱和溶液与不饱和溶液属于交叉关系 D、不饱和溶液与稀溶液属于交叉关系14. 某物质A的溶解度曲线如图所示,现有20℃的100克物质A的饱和溶液样品若干份,下列说法或措施正确的有( )
①取样品升高温度至60℃将变为不饱和溶液
②取样品降温度至10℃仍是饱和溶液
③取样品升温至60℃,加入80克物质A,固体恰好全部溶解
④加入20克水降温度至0℃仍是饱和溶液
⑤蒸发掉20克水,再恢复到20℃仍是饱和溶液
⑥配置图中C状态下的此溶液100g,需要的水比100g样品中含有的水要少
A、三种 B、四种 C、五种 D、六种15. 20℃时氯化钾的溶解度为34g。如图是四位同学在20℃时配制的氯化钾溶液,其中定达到饱和的是( )A、 B、
B、 C、
C、 D、
D、
二、填空题
-
16. 科学发现往往源于对实验现象的观察与研究。
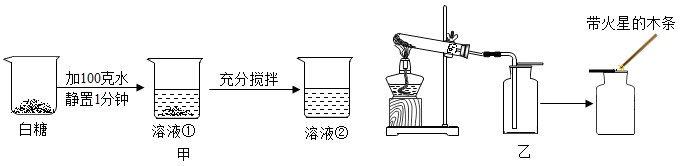 (1)、如图甲进行白糖溶解实验,根据图中现象判断:溶液②(填“是”“不是”或“可能是")白糖的饱和溶液。(2)、如图乙所示,小科利用集气瓶收集从导管导出的氧气时,每隔一段时间,他就取出导管,再用带火星的木条放在瓶口验满。可是他始终没有观察到带火星木条复燃,小科实验操作中出现的错误是。17. 图为甲、乙(均不含结晶水)两种固体物质在水中的溶解度曲线。
(1)、如图甲进行白糖溶解实验,根据图中现象判断:溶液②(填“是”“不是”或“可能是")白糖的饱和溶液。(2)、如图乙所示,小科利用集气瓶收集从导管导出的氧气时,每隔一段时间,他就取出导管,再用带火星的木条放在瓶口验满。可是他始终没有观察到带火星木条复燃,小科实验操作中出现的错误是。17. 图为甲、乙(均不含结晶水)两种固体物质在水中的溶解度曲线。 (1)、t1℃时,甲的溶解度乙的溶解度(填“大于”或“小于”或“等于”)。(2)、t2℃时,100g水中溶解g乙物质恰好达到饱和。(3)、某同学在t1℃时开始如下实验,得到相应的溶液A、B、C。在溶液A、B、C中,属于饱和溶液的是;在溶液C中再加入25g甲后,充分搅拌,恢复到t2℃,所得溶液的质量为g。18. 甲烧杯中盛有30℃、溶质质量分数为20%的饱和硫酸铜溶液100克,进行如图所示实验(不考虑水分蒸发)。
(1)、t1℃时,甲的溶解度乙的溶解度(填“大于”或“小于”或“等于”)。(2)、t2℃时,100g水中溶解g乙物质恰好达到饱和。(3)、某同学在t1℃时开始如下实验,得到相应的溶液A、B、C。在溶液A、B、C中,属于饱和溶液的是;在溶液C中再加入25g甲后,充分搅拌,恢复到t2℃,所得溶液的质量为g。18. 甲烧杯中盛有30℃、溶质质量分数为20%的饱和硫酸铜溶液100克,进行如图所示实验(不考虑水分蒸发)。 (1)、乙中溶液(填“是”、“不是”或“可能是”)饱和溶液。(2)、丙中溶液的溶质质量分数为%(结果保留一位小数)。19. 结合如图中硝酸钾和氯化钠的溶解度曲线,回答下列问题。
(1)、乙中溶液(填“是”、“不是”或“可能是”)饱和溶液。(2)、丙中溶液的溶质质量分数为%(结果保留一位小数)。19. 结合如图中硝酸钾和氯化钠的溶解度曲线,回答下列问题。 (1)、10℃时,溶解度较大的物质是。(2)、20℃时,将20g氯化钠加到100g水中,充分溶解后,得到(选填“饱和”或“不饱和”)溶液。(3)、将50℃的硝酸钾饱和溶液降温至10℃,下列分析正确的是____。A、溶液中溶质质量不变 B、降温后的溶液仍是饱和溶液 C、溶液中溶质的质量分数变大20. 如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图回答下列问题:
(1)、10℃时,溶解度较大的物质是。(2)、20℃时,将20g氯化钠加到100g水中,充分溶解后,得到(选填“饱和”或“不饱和”)溶液。(3)、将50℃的硝酸钾饱和溶液降温至10℃,下列分析正确的是____。A、溶液中溶质质量不变 B、降温后的溶液仍是饱和溶液 C、溶液中溶质的质量分数变大20. 如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图回答下列问题: (1)、t1℃时,溶解度最大的物质是。(2)、若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是(填序号)。
(1)、t1℃时,溶解度最大的物质是。(2)、若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是(填序号)。①降低温度 ②增加溶质 ③蒸发溶剂
三、实验探究题
-
21. 向100克水中不断加入固体A或改变温度,该过程如图所示,得到相应的溶液①~~~⑤

温度/℃
20
30
40
50
60
溶解度/克
37.2
41.4
45.8
50.4
55.2
(1)、这五种溶液中,溶质质量分数最大的是(填序号,下同)。(2)、这五种溶液中,属于饱和溶液为。22. 某实验小组对不同条件下的硝酸钾的溶解情况进行了以下实验:在甲乙丙三个烧杯中放入20g硝酸钾晶体,再分别加入50g冷水、热水与酒精,充分搅拌后(保持各自的温度不变),结果如下图所示。 (1)、甲烧杯中溶液是(填“饱和”或“不饱和”)溶液。(2)、由以上实验可得出结论:影响固体物质溶解度的因素有、。23. 如图是小丽对 20℃一定质量的甲的溶液进行恒温蒸发的结晶实验过程,请回答:
(1)、甲烧杯中溶液是(填“饱和”或“不饱和”)溶液。(2)、由以上实验可得出结论:影响固体物质溶解度的因素有、。23. 如图是小丽对 20℃一定质量的甲的溶液进行恒温蒸发的结晶实验过程,请回答: (1)、蒸发前原溶液是(填“饱和”或“不饱和”)溶液,n 的数值是 , 该温度下,甲的溶解度是。(2)、依据上述实验,你认为甲的溶解度随温度变化的趋势是( )(填字母)的。A、随温度升高而增大 B、随温度升高而减小 C、无法判断(3)、溶液中溶质质量分数的比较:第 2 个烧杯第 3 个烧杯(填“>”、“=”或“<”)
(1)、蒸发前原溶液是(填“饱和”或“不饱和”)溶液,n 的数值是 , 该温度下,甲的溶解度是。(2)、依据上述实验,你认为甲的溶解度随温度变化的趋势是( )(填字母)的。A、随温度升高而增大 B、随温度升高而减小 C、无法判断(3)、溶液中溶质质量分数的比较:第 2 个烧杯第 3 个烧杯(填“>”、“=”或“<”)四、解答题
-
24. 下表为氯化钾在不同温度下的溶解度。
温度/℃
0
10
20
30
40
50
60
溶解度/g
27.6
31.6
34
37
40
42.6
45.5
(1)、40℃时,在45g水中加入5g氯化钾而得到的溶液中溶质的质量分数为多少?(2)、40℃时,氯化钾溶液饱和时,其质量分数为多少?(3)、将40℃氯化钾饱和溶液变成不饱和溶液时,可采用的方法有。25. 20℃时,向甲烧杯中加入100g水和25g固体固体A,向乙烧杯中加入100g水和25g固体B(A、B两种物质均不与水反应),充分搅拌后,甲烧杯中固体剩余,乙烧杯中固体全部溶解。请回答下列问题:(1)、20℃时,甲烧杯中溶液是(填“饱和”或“不饱和”溶液);一定能使甲烧杯中的固体A继续溶解的方法是。(2)、求乙烧杯中B溶液的溶质质量分数(请列式计算)26. 已知20℃时100克水中溶解36克氯化钠恰好达到饱和,20℃时将54克氯化钠配制成400克的溶液.通过计算:(1)、溶液是否饱和?(2)、若不饱和,为了使其饱和可用下面的方法:①蒸发溶剂法:需蒸发多少克水才能成为饱和溶液?
②加溶质法:需再加入多少克氯化钠溶液才能成为饱和溶液?
五、综合说理题
-
27.
60℃时,某同学在盛有硝酸钾饱和溶液的烧杯中,漂浮一个木块(如图),然后将溶液冷却到室温(20℃).请你说出观察到的两个现象,并运用你学过的化学知识和物理知识分别解释这些现象产生的原因.
