浙教版科学九上第二章 第2节 金属的化学性质同步练习(基础巩固)
试卷更新日期:2021-07-21 类型:同步测试
一、单选题
-
1. 电脑芯片的制作需要硅,可用石英砂来制取,其中反应有SiO2+2C Si+2CO↑。该反应属于( )A、化合反应 B、置换反应 C、复分解反应 D、分解反应2. “中国高铁,世界第一”,高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是:C+2NiO 2Ni+CO2↑,该反应属于基本反应类型中的( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应3. 高纯度的硅是制作电脑芯片的重要原料,目前广泛采用石英砂(主要成分是SiO2)为原料制取,其中一步反应为:SiO2+2C Si+2CO↑,该反应的类型是( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应.4. 如图是包含物质a、b、c、d和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生化学反应。单质a不可能是( )
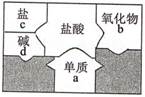 A、Mg B、Fe C、Ag D、Zn5. 铁在海水中容易被锈蚀,通常在轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳。该金属块的材料可以是( )A、金 B、锌 C、铜 D、银6. 工业冶炼金属钛的反应原理是TiCl4+2Mg Ti+2MgCl2 , 该反应类型属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应7. 某学生将沾有清水的细铁丝放在如图的装置中,经过几天后能观察到的现象是( )
A、Mg B、Fe C、Ag D、Zn5. 铁在海水中容易被锈蚀,通常在轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳。该金属块的材料可以是( )A、金 B、锌 C、铜 D、银6. 工业冶炼金属钛的反应原理是TiCl4+2Mg Ti+2MgCl2 , 该反应类型属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应7. 某学生将沾有清水的细铁丝放在如图的装置中,经过几天后能观察到的现象是( )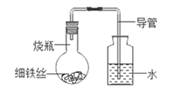 A、铁丝不变,导管中水面上升 B、铁丝不变,导管中水面不变 C、铁丝生锈,导管中水面上升 D、铁丝生锈,导管中水面不变8. 光亮的铁钉在下列几种情况下(如图所示),最不容易生锈的是( )A、
A、铁丝不变,导管中水面上升 B、铁丝不变,导管中水面不变 C、铁丝生锈,导管中水面上升 D、铁丝生锈,导管中水面不变8. 光亮的铁钉在下列几种情况下(如图所示),最不容易生锈的是( )A、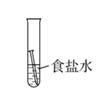 B、
B、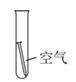 C、
C、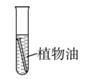 D、
D、 9. 芯片是智能家电的核心部件,它是用高纯度硅制成的,工业上通过以下反应将自然界的二氧化硅(SiO2)转化为硅:SiO2+2C=Si+2CO↑,该反应的类型属于( )A、分解反应 B、化合反应 C、置换反应 D、复分解反应10. 铁制菜刀在生产时要通过“粹火”处理来增加刀的硬度,其原理为:3Fe+4H2O Fe3O4+4H2↑,该反应属于基本反应类型中的( )A、分解反应 B、化合反应 C、复分解反应 D、置换反应11. 下列物质能通过金属和稀盐酸一步反应制得的是( )A、氯化铝 B、氯化铁 C、氯化铜 D、氯化银12. 下列现象和事实,可用金属活动性顺序作出合理解释的是( )
9. 芯片是智能家电的核心部件,它是用高纯度硅制成的,工业上通过以下反应将自然界的二氧化硅(SiO2)转化为硅:SiO2+2C=Si+2CO↑,该反应的类型属于( )A、分解反应 B、化合反应 C、置换反应 D、复分解反应10. 铁制菜刀在生产时要通过“粹火”处理来增加刀的硬度,其原理为:3Fe+4H2O Fe3O4+4H2↑,该反应属于基本反应类型中的( )A、分解反应 B、化合反应 C、复分解反应 D、置换反应11. 下列物质能通过金属和稀盐酸一步反应制得的是( )A、氯化铝 B、氯化铁 C、氯化铜 D、氯化银12. 下列现象和事实,可用金属活动性顺序作出合理解释的是( )①金属镁在空气中比铝更易点燃,说明镁比铝活动性强;
②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强;
③硫酸铜、石灰乳配制农药波尔多液,不宜用铁制容器;
④金属锌与稀硫酸反应速率适中,更适于实验室制取氢气。
A、①② B、③④ C、①③④ D、①②③④13. 世界每年因锈蚀而损失的金属数量巨大,防止金属锈蚀已成为科学研究中的重大问题。下列有关金属锈蚀与保护措施中,不正确的是( )A、在铁表面刷油漆可以防止铁锈蚀 B、及时擦干被雨水淋湿的自行车可以防止自行车生锈 C、铝的抗锈蚀件能比铁强,生活中可用钢丝球洗刷铝锅 D、铁锈蚀的实质是铁与空气中的氧气、水蒸气等发生了化学变化14. 下列属于置换反应的是( )A、H2+CuO Cu+H2O B、2KMnO4 K2MnO4+MnO2+O2↑ C、HCl+NaOH=NaCl+H2O D、2Mg+O2 2MgO15. 地球上的金属资源广泛存在于地壳和海洋中,它们的存在形式为( )A、都是单质 B、都是化合物 C、都是混合物 D、少数是单质,其余为化合物16. 为了防止食品氧化变质,延长食品的保质期,在包装袋中可放入的化学物质是( )A、氧气 B、铁粉 C、硫 D、生石灰17. 下列环境中,铁钉表面最容易产生铁锈的是( )A、在稀盐酸中 B、在潮湿的空气中 C、在干燥的空气中 D、浸没在植物油中18. 下列金属活动性最强的是( )A、Cu B、Zn C、Fe D、Mg19. 钛(Ti)是一种广泛应用于航空、航天等领域的重要金属。工业上制钛的化学方程式为:TiCl4+2Mg=Ti+2MgCl2 ,该反应属于( )
A、化合反应 B、分解反应 C、置换反应 D、复分解反应20. 收藏家收藏清末铝制品,至今保存十分完好,该艺术品不易锈蚀的主要原因是( )A、铝不易发生化学反应 B、铝的氧化物容易发生化学反应 C、铝不易被氧化 D、铝易被氧化,但氧化铝具有保护内部铝的作用二、填空题
-
21. 为了提高原料的利用率,现从含有金属镁、铁、铜的粉末中分离和提取出重要化工原料MgSO4和有关金属, 实验过程如下:
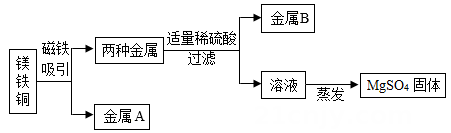 (1)、金属B是。(2)、写出上述实验过程中发生反应的化学方程式。22. 铁、镁、铜三种金属的活动性由强到弱的顺序为;将铜投入稀硫酸中反应(选填“会”或“不会”)。23. 金属冶炼是把金属化合物转变成金属单质,如炼铜的方法有:(1)、湿法炼铜:Fe+CuSO4=Cu+FeSO4 , 该反应属于(填基本反应类型);(2)、干法炼铜:CO+CuO Cu+CO2 , 这是利用CO的 性。24. 金属是一类重要的材料,在日常生活和工农业生产中有广泛的应用。(1)、高层建筑的楼顶常装有用钢铁做的避雷针,其作用是将雷电引导到地下,这说明钢铁具 有良好的性(填一物理性质);(2)、小王家厨房里的菜刀生锈了,铁生锈需要有(填名称)的参与。除锈可以用砂纸打磨,也可以通过化学方法用厨房中的除锈。为了防止除锈后的菜刀再生锈,可以采取的措施有(任写一种)。25. 把铜粉和铁粉的混合物放入硝酸银溶液中,理论上会发生 个化学反应.反应结束后有固体剩余.如果固体的成分就一种,固体是 (填化学式,下同),溶液中溶质最多有 种.26. 金属和金属材料在生活、生产中应用广泛.
(1)、金属B是。(2)、写出上述实验过程中发生反应的化学方程式。22. 铁、镁、铜三种金属的活动性由强到弱的顺序为;将铜投入稀硫酸中反应(选填“会”或“不会”)。23. 金属冶炼是把金属化合物转变成金属单质,如炼铜的方法有:(1)、湿法炼铜:Fe+CuSO4=Cu+FeSO4 , 该反应属于(填基本反应类型);(2)、干法炼铜:CO+CuO Cu+CO2 , 这是利用CO的 性。24. 金属是一类重要的材料,在日常生活和工农业生产中有广泛的应用。(1)、高层建筑的楼顶常装有用钢铁做的避雷针,其作用是将雷电引导到地下,这说明钢铁具 有良好的性(填一物理性质);(2)、小王家厨房里的菜刀生锈了,铁生锈需要有(填名称)的参与。除锈可以用砂纸打磨,也可以通过化学方法用厨房中的除锈。为了防止除锈后的菜刀再生锈,可以采取的措施有(任写一种)。25. 把铜粉和铁粉的混合物放入硝酸银溶液中,理论上会发生 个化学反应.反应结束后有固体剩余.如果固体的成分就一种,固体是 (填化学式,下同),溶液中溶质最多有 种.26. 金属和金属材料在生活、生产中应用广泛.(1)铁在潮湿的空气中容易生锈,实际上是铁与空气中的、等发生了化学反应.
(2)在实验室中探究铁、铜的金属活动性顺序,除铁、铜外,还需要一种试剂,你选择的试剂是 (填序号),写出有关反应的化学方程式 .
①AgNO3溶液 ②CuSO4溶液 ③Al2(SO4)3溶液.
27.- “沙里淘金”说明黄金在自然界中能够以 (填“单质”或“化合物”)形式存在。
28.神奇的化学变化﹣﹣光合作用与燃烧反应,如图为光合作用和木柴燃烧过程中,部分物质参与循环的示意图.

请据图并结合你学过的知识,回答下列问题:
(1)从物质组成的角度看,葡萄糖和纤维素均属于(填“无机物”或“有机物”).
(2)从物质转化的角度看,光合作用及葡萄糖转化为纤维素属于(填“物理”或“化学”)的变化.光合作用的化学方程式为 ,碳不完全燃烧的化学方程式为 .
(3)从能量转化的角度看,绿色植物光合作用时能量转化的方式是 , 而木炭燃烧时能量转化的方程式是 .
(4)在图中光合作用与燃烧反应过程中参与循环的元素有 .
29.21世纪的能源金属﹣锂(Li)
金属锂,被誉“21世纪的能源金属”,当前手机中广泛使用的电池,主要是高能锂电池.请回答下列问题:
(1)锂原子的原子结构示意图如图所示;锂原子在化学反应中容易(填“得到”或“失去”)电子变成离子,其离子符号为 .
(2)研究表明,锂的金属活动性比较活泼.写出金属锂与稀硫酸反应的化学方程式 .
(3)金属锂除了制造锂电池外,还可以用于储存氢气,其原理是金属锂与氢气化合生成白色粉末状的氢化锂(LiH),氢化锂与水反应生成氢氧化锂和氢气.写出上述过程中发生反应的化学方程式 .
 30. 金属与酸的置换反应:
30. 金属与酸的置换反应:Fe+2HCl=
Zn+H2SO4= (实验室制H2)
只有排在金属活动性顺序 的金属才能和酸发生置换反应。
31. 在金属活动性顺序里,金属的位置越靠前,它的活动性就越。32. 金属活动性顺序由强逐渐减弱:K Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au。
三、解答题
-
33. 某初中科技活动举行了一次有趣的比赛:“谁的小车一次运行的距离最远”。九年级二班的科学兴趣小组制作了如图所示的一辆小车,他们往试管中加入两种试剂,塞紧塞子,通过产生的。气体喷出时的反冲力,使小车向前运动。(可选择的试剂:①锌粉,②铜粉,③10%的稀盐酸,④10%的稀硫酸)
 (1)、要想实验能成功,二班科学兴趣小组选择的固体药品是。(填序号)(2)、理论上,在加入的两种试剂总质量相同的条件下,二班科学兴趣小组选择的最符合比赛要求的试剂应是(填序号)。(3)、三班科学兴趣小组根据同样的推进原理,但不进行化学反应,也能使小车运动。他们向盛有水的试管中加入的物质可以是(填物质名称)。
(1)、要想实验能成功,二班科学兴趣小组选择的固体药品是。(填序号)(2)、理论上,在加入的两种试剂总质量相同的条件下,二班科学兴趣小组选择的最符合比赛要求的试剂应是(填序号)。(3)、三班科学兴趣小组根据同样的推进原理,但不进行化学反应,也能使小车运动。他们向盛有水的试管中加入的物质可以是(填物质名称)。四、实验探究题
-
34.
根据下列图示的探究过程,回答下列问题:
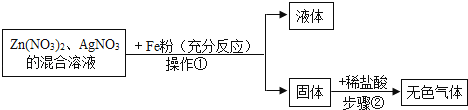 (1)、操作①的名称 .(2)、图中固体中含有的物质(化学式) .(3)、写出步骤②发生反应的化学方程式 .35.
(1)、操作①的名称 .(2)、图中固体中含有的物质(化学式) .(3)、写出步骤②发生反应的化学方程式 .35.某化学兴趣小组进行铁生锈的实验探究活动.
 (1)、【探究一】铁生锈的条件
(1)、【探究一】铁生锈的条件(1)该兴趣小组将洁净无锈的铁钉分别置于如图所示装置中,经过一段时间观察 ,(填装置序号)装置中出现了明显的锈迹.
他们的结论:铁生锈是因为铁与空气中的等发生了化学反应.
(2)甲同学提出了疑问:空气中的氮气、二氧化碳没有参与铁的生锈过程吗?请设计实验为甲同学释疑. ,观察并记录现象即可证明.
(2)、【探究二】影响铁生锈速率快慢的因素乙同学说:妈妈常说菜刀沾有盐水生锈更快.这种说法对吗?同学广泛查阅资料.
资料一:导电性强的溶液都可加速铁的生锈.
资料二:海上航行的轮船在与海水接触的部分镶嵌一锌块,能有效降低钢材被腐蚀的速率.
(3)将上述A装置中的蒸馏水改为下列液体中的 ,可使铁生锈的速率加快.
a、硫酸钠溶液 b、无水乙醇 C、蔗糖溶液
(4)一些铁制品表面覆盖了某些涂层.不同的涂层被破坏后,铁生锈的速率不同.你认为下列 涂层破坏后,铁生锈的速率较快.
a、镀锌铁 b、镀锡铁
(5)一些建筑的大门刷上了一层银白色的金属,你认为该金属可能是 .
a、银粉 b、铜粉 c、镁粉
(3)、【交流与思考】(6)写出一种防止铁生锈的方法 .
36.铁生锈探秘

为探究铁生锈的原因,化学兴趣小组的同学进行了如图所示的四个实验,实验结果显示:B、D实验中铁生了锈,而A、C实验中没有明显的现象,仔细分析这4 个实验,回答下列问题:
(1)、评价方案:对照实验指除了一个变量外,其他的量都保持不变的实验.该实验方案中采用了对照实验方法.请指出其中的对照实验(填ABCD实验代号)和变量.第①组对照实验 ,变量 .
第②组对照实验 ,变量 .
第③组对照实验 ,变量 .
(2)、解释数据:实验时,每隔一段时间测量导管内水面上升的高度,结果如下表所示(表中所列数据为导管中水面上升的高度/cm )时间/小时
编号
0
0.5
1.0
1.5
2.0
2.5
3.0
A
0
0
0
0
0
0
0
B
0
0
0
0.3
0.8
2.0
3.5
C
0
0
0
0
0
0
0
D
0
0.4
1.2
3.4
7.6
9.5
9.8
导致B、D实验装置中导管内水面上升的原因是 .
(3)、获得结论:根据本实验,你认为导致铁生锈的物质有 ;能加快铁生锈的物质是 .
-