辽宁省营口市2021年中考化学试卷
试卷更新日期:2021-07-21 类型:中考真卷
一、单选题
-
1. 下列变化属于化学变化的是( )A、合成新药 B、铁水铸锅 C、酒精挥发 D、矿石粉碎2. 下列图示的“不符合题意操作”与选项中“可能引起的后果”不匹配的是( )A、
 读数偏大
B、
读数偏大
B、 腐蚀胶帽
C、
腐蚀胶帽
C、 标签受损
D、
标签受损
D、 测量不准
3. 要提高全民的环境意识,保护我们的空气。下列不属于空气污染物的是( )A、CO B、O3 C、CO2 D、PM2.54. 下列物质中氯元素的化合价最低的是( )A、NaClO3 B、Cl2 C、NaCl D、HClO5. 合成材料的应用,大大方便了人类的生活。下列生活用品由合成材料制成的是( )A、纯棉毛巾 B、不锈钢餐具 C、真丝睡衣 D、塑料水管6. 下列灭火方法,主要是利用隔绝氧气原理的是( )A、吹灭蜡烛 B、用灯帽盖灭酒精灯 C、关闭炉具阀门 D、用高压水枪灭火7. 下列物质能溶于水形成溶液的是( )A、蔗糖 B、面粉 C、植物油 D、泥沙8. 化肥对提高农作物产量具有重要作用。下列属于复合肥料的是( )A、K2SO4 B、CO(NH2)2 C、(NH4)2HPO4 D、Ca3(PO4)29. 某同学用pH试纸测定了生活中一些物质的pH如下,其中能使酚酞试液变红的是( )
测量不准
3. 要提高全民的环境意识,保护我们的空气。下列不属于空气污染物的是( )A、CO B、O3 C、CO2 D、PM2.54. 下列物质中氯元素的化合价最低的是( )A、NaClO3 B、Cl2 C、NaCl D、HClO5. 合成材料的应用,大大方便了人类的生活。下列生活用品由合成材料制成的是( )A、纯棉毛巾 B、不锈钢餐具 C、真丝睡衣 D、塑料水管6. 下列灭火方法,主要是利用隔绝氧气原理的是( )A、吹灭蜡烛 B、用灯帽盖灭酒精灯 C、关闭炉具阀门 D、用高压水枪灭火7. 下列物质能溶于水形成溶液的是( )A、蔗糖 B、面粉 C、植物油 D、泥沙8. 化肥对提高农作物产量具有重要作用。下列属于复合肥料的是( )A、K2SO4 B、CO(NH2)2 C、(NH4)2HPO4 D、Ca3(PO4)29. 某同学用pH试纸测定了生活中一些物质的pH如下,其中能使酚酞试液变红的是( )物质
苹果汁
酱油
食盐水
炉具清洁剂
pH
3
5
7
12
A、食盐水 B、炉具清洁剂 C、苹果汁 D、酱油10. 防控新冠肺炎期间,很多医院使用来苏水进行杀菌消毒,来苏水的主要成分之一是对甲基苯酚(化学式为:C7H8O)下列有关对甲基苯酚的叙述正确的是( )A、对甲基苯酚的相对分子质量为108g B、对甲基苯酚中碳元素的质量分数最大 C、对甲基苯酚由16个原子构成 D、对甲基苯酚中碳、氢、氧元素的质量比为7:8:111. 下列金属不能与 溶液反应的是( )A、 B、 C、 D、12. 某反应的微观示意图如下,有关说法正确的是( ) A、参加反应的两种物质的质量比为17:24 B、反应前后各元素的化合价不变 C、化学方程式为: D、该反应类型为置换反应13. 下列关于二氧化碳与一氧化碳用途的说法,错误的是( )A、CO2可用于灭火 B、CO2可用作气体肥料 C、CO可用于人工降雨 D、CO可用作燃料14. 除去下列物质中混有的少量杂质(括号内为杂质),所选试剂和操作方法均正确的是( )
A、参加反应的两种物质的质量比为17:24 B、反应前后各元素的化合价不变 C、化学方程式为: D、该反应类型为置换反应13. 下列关于二氧化碳与一氧化碳用途的说法,错误的是( )A、CO2可用于灭火 B、CO2可用作气体肥料 C、CO可用于人工降雨 D、CO可用作燃料14. 除去下列物质中混有的少量杂质(括号内为杂质),所选试剂和操作方法均正确的是( )选项
物质
试剂和操作方法
A
CuO(Cu)
加入适量的盐酸充分反应后,过滤、洗涤、烘干
B
C(MnO2)
加入H2O2溶液,待无气泡产生后,过滤、洗涤、干燥
C
KCl(AlCl3)
加入适量的KOH溶液,蒸发
D
BaCl2溶液(NaCl)
加过量Na2CO3溶液,过滤,向洗涤后的滤渣中加入适量稀盐酸
A、A B、B C、C D、D15. 只用水这一种试剂不能将下列各组固体物质鉴别出来的是( )A、KNO3和NH4NO3 B、CaCO3和Ca(NO3)2 C、NaOH和NaCl D、K2SO4和NaNO3二、填空题
-
16. 请用化学用语回答:(1)、两个汞原子。(2)、天然气的主要成分。(3)、亚铁离子。(4)、人体胃液中含有的酸。17. 根据下图所示回答问题:
 (1)、A,B,C,D中,表示钙离子结构示意图的是(填字母,下同),与钙原子化学性质相似的是 , 表示同一种元素的是。(2)、具有相对稳定结构的原子是(填字母)图E中“20”表示。18. 化学就在我们身边,人类的生活离不开化学。请回答下列问题:(1)、饮用水硬度过大会影响人体健康。生活中降低水硬度常用的方法是。(2)、人们每天需要从食物中摄取充足的营养素。下列食物中富含蛋白质的是。
(1)、A,B,C,D中,表示钙离子结构示意图的是(填字母,下同),与钙原子化学性质相似的是 , 表示同一种元素的是。(2)、具有相对稳定结构的原子是(填字母)图E中“20”表示。18. 化学就在我们身边,人类的生活离不开化学。请回答下列问题:(1)、饮用水硬度过大会影响人体健康。生活中降低水硬度常用的方法是。(2)、人们每天需要从食物中摄取充足的营养素。下列食物中富含蛋白质的是。A.馒头 B.西红柿 C.牛肉 D.黄花鱼
(3)、下列物质可用作食品干燥剂的是。A.生石灰 B.熟石灰 C.火碱 D.纯碱
(4)、未经处理的煤燃烧产生的(写化学式)排放到空气中,会形成酸雨;(5)、甲醛(CH2O)为室内装修产生的有害物质之一。为去除污染,科学家研制出一种新型的催化剂,在其催化作用下,甲醛与空气中的氧气反应生成两种最常见的氧化物,该反应的化学方程式为。19. 下图所示是初中化学常见的四个实验,请依图回答: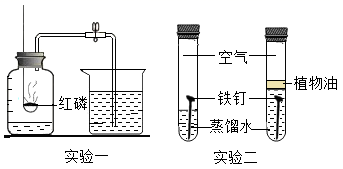
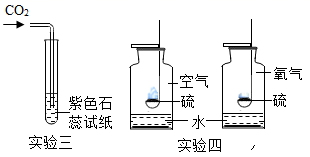 (1)、实验一:红磷需过量的目的是。(2)、实验二:通过对比实验得出结论:铁生锈需要和接触;(3)、实验三:证明二氧化碳具有的化学性质是。(4)、实验四:由于不同造成硫燃烧的现象不同。20. 数据处理是对数据进行加工的过程,列表法和作图法是常用的数据处理方法。已知KNO3和KCl在不同温度时的溶解度如下表所示,请回答下列问题:
(1)、实验一:红磷需过量的目的是。(2)、实验二:通过对比实验得出结论:铁生锈需要和接触;(3)、实验三:证明二氧化碳具有的化学性质是。(4)、实验四:由于不同造成硫燃烧的现象不同。20. 数据处理是对数据进行加工的过程,列表法和作图法是常用的数据处理方法。已知KNO3和KCl在不同温度时的溶解度如下表所示,请回答下列问题:温度/℃
0
10
20
30
40
50
60
70
溶解度/g
KNO3
13.3
20.9
31.6
45.8
63.9
85.5
110
138
KCl
27.6
31.0
34.0
37.0
40.0
42.6
45.5
48.3
(1)、依据上表数据,绘制KNO3和KCl的溶解度曲线,下图中能表示KNO3溶解度曲线的是(填“A”或“B”); (2)、分析表中数据可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x取值范围是。(3)、40℃时,将140gKCl的饱和溶液恒温蒸发10g水后,析出KCl晶体的质量为g。(4)、要使A物质的不饱和溶液转化为饱和溶液,方法是。(5)、将60℃时KNO3和KCl的饱和溶液降温至20℃,析出晶体质量关系为。
(2)、分析表中数据可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x取值范围是。(3)、40℃时,将140gKCl的饱和溶液恒温蒸发10g水后,析出KCl晶体的质量为g。(4)、要使A物质的不饱和溶液转化为饱和溶液,方法是。(5)、将60℃时KNO3和KCl的饱和溶液降温至20℃,析出晶体质量关系为。A KNO3> KCl B KNO3< KCl C KNO3=KCl D无法确定
三、综合题
-
21. 阅读下列材料文字。
材料一:绿色化学的理念是使污染消除在产生的源头,不再使用有毒、有害的物质,不再产生废物,这是从根本上消除污染的对策,过程和终端均为零排放或零污染。世界上很多国家己把“化学的绿色化”作为新世纪化学发展的主要方向之一。原子经济性和“5R”原则是绿色化学的核心内容。“5R”原则,即Reduce(减量);Reuse(循环使用);Recycling(回收);Regeneration(再生);:Rejection(拒用)。
材料二:垃圾分类一般是指按一定规定或标准将垃圾分类储存,分类投放和分类搬运,从而变成公共资源的一系列活动的总称。分类的目的是提高垃圾的资源价值和经济价值,力争物尽其用。进行垃圾分类回收可以降低垃圾处理成本,减少土地资源的消耗,具有社会、经济、环保等多方面的好处。垃圾分类从我做起。
绿水青山就是金山银山,保护环境,人人有责。
根据材料内容和所学化学知识,回答下列问题:
(1)、“绿色化学”的理念是。(2)、今年起国家提倡用纸质吸管代替塑料吸管,你认为这一做法最能体现“5R”原则中的 , 请简单阐述理由;(3)、下列属于可回收垃圾的是。A.废旧报纸 B.生锈铁管 C.矿泉水瓶 D.腐烂水果
(4)、垃圾分类回收的好处是。22. 下面为“去除粗盐中难溶性杂质并计算产率”的实验操作示意图: (1)、请将上述操作进行合理排序:(填序号)、计算;请改正操作④中的不正确。(2)、操作②中,用玻璃棒不断搅拌的目的是。(3)、过滤后,如果滤液仍然浑浊,其原因可能是。(4)、通过以上操作只能除去粗盐中难溶性杂质,欲除去可溶性杂质如MgCl2、CaCl2 , 得到纯净的NaCl,还需依次用到NaOH溶液、Na2CO3溶液和稀盐酸(三种药品均过量);
(1)、请将上述操作进行合理排序:(填序号)、计算;请改正操作④中的不正确。(2)、操作②中,用玻璃棒不断搅拌的目的是。(3)、过滤后,如果滤液仍然浑浊,其原因可能是。(4)、通过以上操作只能除去粗盐中难溶性杂质,欲除去可溶性杂质如MgCl2、CaCl2 , 得到纯净的NaCl,还需依次用到NaOH溶液、Na2CO3溶液和稀盐酸(三种药品均过量);①碳酸钠溶液要过量的原因是;②稀盐酸的作用是。
23. 下图为初中化学中关于酸、碱、盐化学性质的知识框架图,X、Y是除酸、碱、盐之外的不同类别的物质,据图回答问题: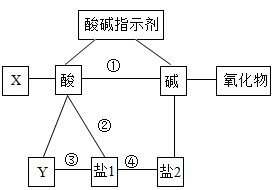 (1)、X的物质类别是。(2)、若“盐1”为 ,则反应③的化学方程式为(任写一个);(3)、反应④能够发生应该满足的条件是。(4)、在反应①②③④中,属于中和反应的是。24. 实验室制取气体时需要的一些装置如下图所示,请回答下列问题:
(1)、X的物质类别是。(2)、若“盐1”为 ,则反应③的化学方程式为(任写一个);(3)、反应④能够发生应该满足的条件是。(4)、在反应①②③④中,属于中和反应的是。24. 实验室制取气体时需要的一些装置如下图所示,请回答下列问题: (1)、写出标有序号的仪器名称:②。(2)、写出用A装置制取氧气的化学方程式。(3)、实验室制取CO2时,收集装置通常只选择E的原因是 , 若要收集一瓶干燥的二氧化碳,应在E之前连接装置(填字母);(4)、实验室常用高锰酸钾固体和浓盐酸在常温下反应制取氯气(Cl2),用该方法制取氯气时选用的发生装置是(填字母);如果用G装置收集氯气,气体应从(填“a”或“b”)口进;氯气有毒,可与水反应生成酸,为防止其污染空气,应选择性溶液吸收尾气。25. 在学习了单质碳的化学性质后,某化学兴趣小组的同学对含碳化合物燃烧后的产物进行了探究。
(1)、写出标有序号的仪器名称:②。(2)、写出用A装置制取氧气的化学方程式。(3)、实验室制取CO2时,收集装置通常只选择E的原因是 , 若要收集一瓶干燥的二氧化碳,应在E之前连接装置(填字母);(4)、实验室常用高锰酸钾固体和浓盐酸在常温下反应制取氯气(Cl2),用该方法制取氯气时选用的发生装置是(填字母);如果用G装置收集氯气,气体应从(填“a”或“b”)口进;氯气有毒,可与水反应生成酸,为防止其污染空气,应选择性溶液吸收尾气。25. 在学习了单质碳的化学性质后,某化学兴趣小组的同学对含碳化合物燃烧后的产物进行了探究。(提出问题)乙醇燃烧后的产物是什么?
(查阅资料)①无水硫酸铜为白色粉末,遇水会变蓝;②氯化钙有吸水性,可做干燥剂。
(1)、(做出猜想)猜想一:产物中含有CO、H2O;
猜想二:产物中含有CO2、H2O;
猜想三:产物中含有。
(2)、(进行实验)同学们设计了如下图的实验:检查装置气密性后,将乙醇燃烧的产物依次通过如图所示的装置进行验证;(部分夹持、固定装置省略;B、D、G装置中均为澄清的石灰水)。
①装置B的作用是。
②F装置中若发生反应,则化学方程式是。
(解释与结论)经过实验,同学们认为猜想三成立。
(3)、实验中能观察到的现象是;装置C中发生反应的化学方程式为。(反思与评价)实验结束后,由于小丽同学的操作不当造成了仪器损坏,小组内同学针对这个事故,进行了分析和讨论。
(4)、为了避免此事故再次发生,同学们对该装置进行了创新和改进,你认为他们的改进是(文字说明或画图都可)。四、计算题
-
26. 小明用含碳酸钠的氢氧化钠样品进行了如图所示的实验。请回答:
 (1)、此实验中发生反应的化学方程式是。(2)、过滤后滤液中溶质为 , 其质量分数是。
(1)、此实验中发生反应的化学方程式是。(2)、过滤后滤液中溶质为 , 其质量分数是。